文档内容
专题三 离子反应和离子方程式 专题检验
一、选择题(16×3=48分)
1.(2022·吉林长春·二模)下列对应离子方程式书写错误的是
A.向BaCl 溶液中通入CO 气体: Ba2++CO + H O= BaCO ↓+2H+
2 2 2 2 3
B.向FeCl 溶液中通入Cl : 2Fe2+ Cl = 2Fe3+ +2Cl-
2 2 2
2-
C.向NaClO溶液中通入过量SO : ClO- +SO +H O = Cl-+SO4 +2H+
2 2 2
2-
D.向NH Al(SO ) 溶液中加入同体积同浓度的Ba(OH) 溶液:2A13++3SO4 +3Ba2++6OH-
4 4 2 2
=3BaSO ↓+2Al(OH) ↓
4 3
2.(2022·安徽马鞍山·三模)下列指定反应的离子方程式正确的是
NH+ SO2-
A.用氨水吸收足量的SO 气体: 2NH ·H O + SO = 2 4+ 3 + H O
2 3 2 2 2
B.将Cl 通入石灰乳中制漂白粉: Cl + 2OH- = ClO- + Cl-+ H O
2 2 2
CO2-
C.ZnCO 溶于稀盐酸: 3 + 2H+= H O + CO ↑
3 2 2
D.向AgBr悬浊液中滴加足量Na S溶液,出现黑色沉淀: 2AgBr(s)+S2- (aq)=Ag S(s) +2Br-
2 2
(aq)
3.(2022·新高考广东卷)下列关于 的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:
B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
4.(2022·安徽芜湖·三模)下列离子能大量共存,且加入相应试剂后发生反应的离子方程
式书写正确的是
选项 离子 加入试剂 加入试剂后发生反应的离子方程式A Fe3+、Cl-、SO 2 4 、K+ 铜粉 2Fe3++Cu=2Fe2++Cu2+
B K+、HCO3 、AlO2 、Cl- 盐酸 H++ AlO2 +H O=Al(OH) ↓
2 3
C Na+、Fe2+、Br-、Mg2+ 氯气 2 Br-+Cl =Br +2Cl-
2 2
2
D NH4、Na+、SO4 、HCO3 NaOH NH4+OH-=NH ·H O
3 2
5.(2022·安徽马鞍山·一模)下列指定反应的离子方程式正确的是
A.向Ca(ClO) 溶液中通入过量CO :Ca2++2ClO-+CO +H O=2HClO+CaCO
2 2 2 2 3
SO2
B.向Na SO 溶液中滴加稀HNO 溶液: 3 +2H+=SO ↑+H O
2 3 3 2 2
C.向FeI 溶液中通入等物质的量的Cl :2Fe2++2I-+2Cl =2Fe3++I +4Cl-
2 2 2 2
SO2
D.向NH HSO 溶液中滴加少量的Ba(OH) 溶液:Ba2++2OH-+2H++ 4 =BaSO ↓+2H O
4 4 2 4 2
6.(2022·宁夏吴忠·二模)下列各组离子在指定溶液中能大量共存的是
SO2- NO-
A.中性溶液中:Fe3+、Na+、 4 、 3
c
H+
B.lg
c
OH-=10的溶液中:Na+、K+、CH
3
COO-、Cl-
NH+
C.明矾溶液中: 4、K+、I-、Br-
NO-
D.加入铝粉会产生H 的溶液中:Cu2+、Mg2+、 3、ClO-
2
7.(2022·河南开封·二模)下列过程中的化学反应,相应的离子方程式错误的是
A.将稀H SO 加入NaIO 和NaI的混合溶液中:5I-+IO3+6H+=3I +3H O
2 4 3 2 2
2 2
B.向稀HNO 中滴加Na SO 溶液:3SO3 +2H++2NO3=3SO4 +2NO↑+H O
3 2 3 2
C.将Na O 加入CuSO 溶液中:2Na O +2Cu2++2H O=4Na++2Cu(OH) ↓+O ↑
2 2 4 2 2 2 2 2
2
D.向NaHCO 溶液中加入足量Ba(OH) 溶液:2HCO3+Ba2++2OH-=BaCO ↓+2H O+CO3
3 2 3 28.(2022·河南许昌·二模)下列反应对应的离子方程式书写正确的是
A.将H S通入Hg(NO ) 溶液中:Hg2++S2-=HgS↓
2 3 2
B.向FeBr 溶液中通入过量Cl :3Cl +2Fe2++4Br-=2Fe3++2Br +6Cl-
2 2 2 2
NH+
C.向NH Al(SO ) 溶液中滴入少量NaOH溶液: 4+OH-=NH ·H O
4 4 2 3 2
MnO-
D.向KMnO 酸性溶液中滴入H O 溶液:2 4+3H O +6H+=2Mn2++4O ↑+6H O
4 2 2 2 2 2 2
9.(2022·河南郑州·一模)下列相关原理或化学用语错误的是
通电
A.电解MgCl 水溶液制取Mg:MgCl Mg+Cl ↑
2 2 2
B.海水提溴的过程中用Cl 氧化Br-:Cl +2Br-=Br +2Cl-
2 2 2
2
C.食盐水精制的过程中用Na CO 除去Ba2+:Ba2++CO3 =BaCO ↓
2 3 3
2 2
D.锅炉除垢的过程中把CaSO 转化为CaCO :CaSO (s)+CO3 (aq)=CaCO (s)+SO4 (aq)
4 3 4 3
10.(2022·甘肃·二模)下列过程中的化学反应,相应的离子方程式书写不正确的是
A.向稀盐酸中加入少量钠粒:2Na+2H O=Na++2OH-+H ↑
2 2
B.硫酸酸化的淀粉碘化钾溶液久置后变蓝:4I-+O +4H+=2I +2H O
2 2 2
S O2-
C.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠: 2 3 +2H+=SO ↑+S↓+H O
2 2
D.向含氯化铁的氯化镁溶液中加入氧化镁:2Fe3++3MgO+3H O=2Fe(OH) ↓+3Mg2+
2 3
11.(2022·山西临汾·三模)下列关于离子反应或离子共存表达正确的是
CO2- AlO-
A.以下离子在0.1mol·L-1NaOH溶液中能大量共存:Na+、K+、 3 、 2
B.以下离子在0.1mol·L-1K CO 溶液中能大量共存:Na+、Ba2+、Cl-、OH-
2 3
AlO- NH+
C.向氯化铝溶液中滴加过量氨水:4NH ·H O+Al3+= 2+4 4+2H O
3 2 2
D.漂白粉漂白原理:Ca(ClO) +2CO +2H O=Ca(HCO ) +2HClO
2 2 2 3 2
12.(2022·山西太原·二模)宏观辨识和微观探析是化学学科的核心素养之一。下列描述物质制备和应用的离子方程式正确的是
2
A.泡沫灭火器的反应原理:2Al3++3CO3 +3H O=2Al(OH) ↓+3CO ↑
2 3 2
B.海水提溴工艺中,用纯碱溶液富集Br :Br +2OH-=Br-+BrO-+H O
2 2 2
2
2
C.锅炉除垢过程中将CaSO 转化为CaCO :CaSO (s)+CO3 (aq) CaCO (s)+SO4 (aq)
4 3 4 3
通电
D.用惰性电极电解饱和MgCl 溶液:2Cl-+2H O Cl ↑+H ↑+2OH-
2 2 2 2
13.(2022·山西吕梁·一模)下列离子方程式正确的是
0.1molL1MgCl Mg2++Ca(OH) =Mg(OH) +Ca2+
A. 2溶液中加入足量石灰乳: 2 2
AlO-+CO +2H O=Al(OH) +HCO-
B.在偏铝酸钠溶液中通入少量二氧化碳: 2 2 2 3 3
4H++2Fe2++SO2-=2Fe3++SO 2H O
C.酸化的硫酸亚铁溶液长时间存放溶液变黄: 4 2 2
2MnO-+5C O2-+16H+=2Mn2++10CO +8H O
D.用高锰酸钾标准溶液滴定草酸: 4 2 4 2 2
14.(2022·山西吕梁·一模)常温下,下列各组离子在指定溶液中可能大量共存的是
c
OH-
=11012
A.在 c H+ 的溶液中: HCO、K、Na、SO2
3 4
Na、OH、Br、K
B.含有大量Fe3+的溶液中:
pH0 Na+、K+、SO2-、S O2-
C. 的溶液中: 4 2 3
K
w 11012molL1
D.在c
OH-
的溶液中:Na、Ba2、Cl、Br
15.(2022·吉林延边·一模)下列过程中的化学反应对应的离子方程式正确的是
A.用KSCN试剂检验Fe3+:Fe3++3SCN-=Fe(SCN) ↓
3
2 2
B.向Na S O 溶液中加入足量稀硫酸:2S O3 +4H+=SO4 +3S↓+2H O
2 2 3 2 22
C.向Na CO 溶液中通入过量SO :CO3 +2SO +H O=CO +2HSO3
2 3 2 2 2 2
D.将洗净的鸡蛋壳浸泡在米醋中获得溶解液:2H++CaCO =Ca2++H O+CO ↑
3 2 2
16.(2022·新高考湖南三模)下列离子方程式正确的是
A. 通入冷水中:
B.用醋酸和淀粉 溶液检验加碘盐中的 :
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合:
二、主观题(4×13=42分)
17.(13分)(2022·山西太原·二模)某工业生产上用铜镍矿石(主要成分为CuS、NiS、
FeS、SiO 及不溶于酸的杂质)制备胆矾CuSO •5H O的流程如图。
2 4 2
已知:有机萃取剂HR可以萃取Cu2+,其萃取原理(org为有机相)Cu2+(aq)+2HR(org)
反
萃
萃
取
取
CuR (org)+2H+(aq)。
2
回答下列问题:
(1)为了提高焙烧的速度,可采取的措施是____。
(2)“调节pH时,生成氢氧化铁沉淀的离子方程式为____,
(3)25℃时,“调节pH”后,测得滤液中各离子浓度及相关数据如表所示。(lg2=0.3)
离子 Fe3+ Cu2+ Ni2+ Fe2+浓度/(mol·L-1) 1.0×10-6 5.0 1.2 0
对应氢氧化物的K 6.4×10-38 2.2×10-20 2.0×10-15 8.0×10-16
sp
该滤液的pH为___;加入的Cu(OH) ____(填“已经”或“没有”)完全溶解。
2
(4)向“萃取”后的水相中加入一定量的NaClO和NaOH,能制得黑色不溶物NiOOH,该反
应的离子方程式为___。
(5)“操作Ⅱ”包括洗涤,洗涤该沉淀的操作为___。
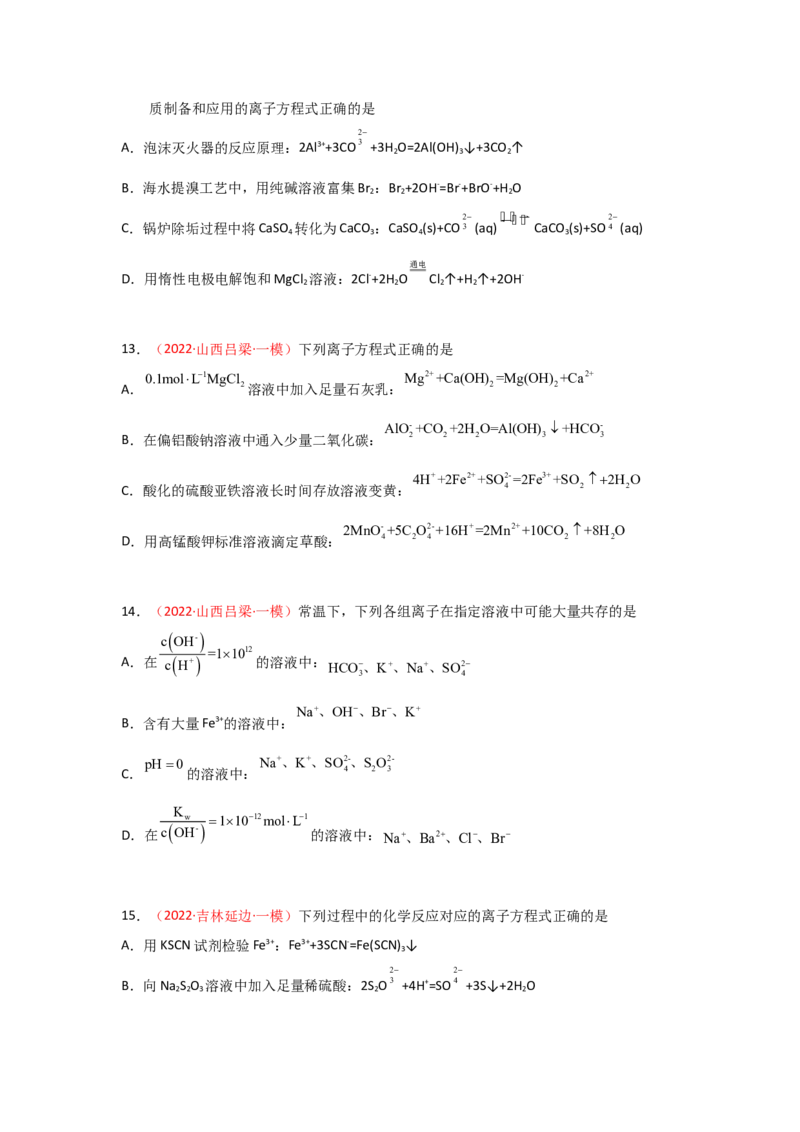
(6)将得到的胆矾产品做热重分析,测得的数据如图所示。
已知:杂质不分解,250℃时,胆矾失去所有结晶水。则A点胆矾分解得到的物质为___(填
化学式)。
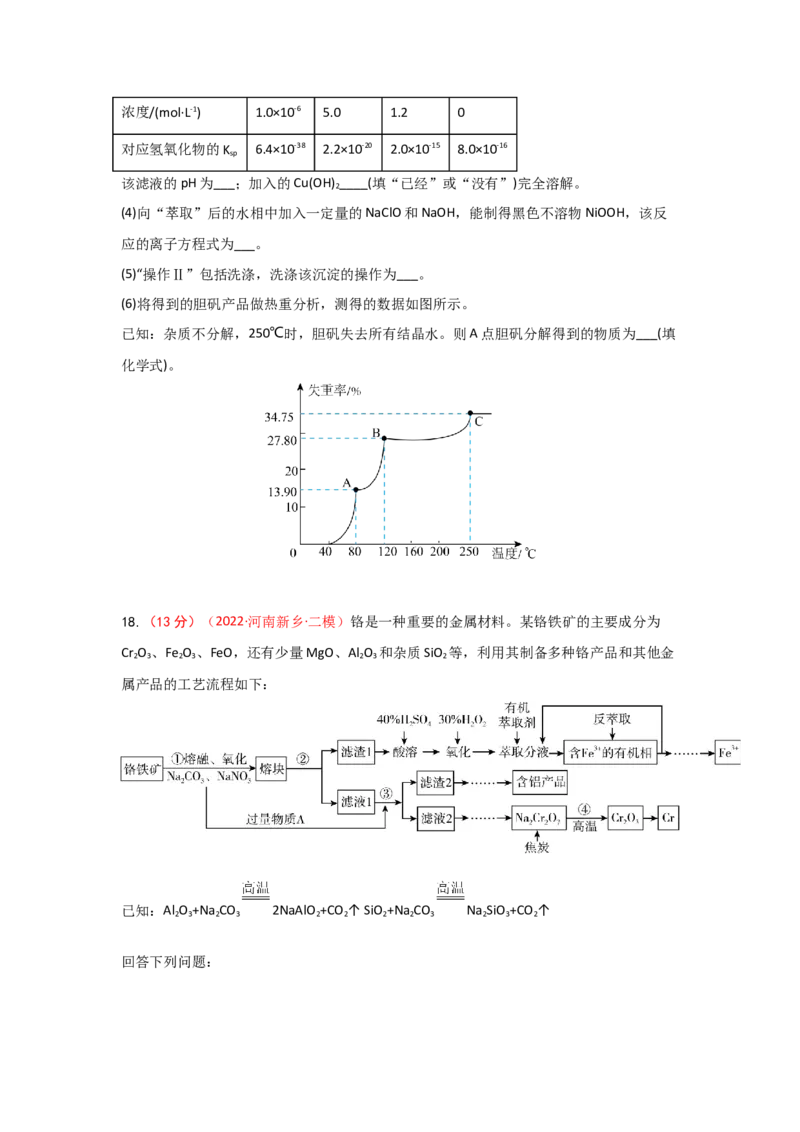
18.(13分)(2022·河南新乡·二模)铬是一种重要的金属材料。某铬铁矿的主要成分为
Cr O 、Fe O 、FeO,还有少量MgO、Al O 和杂质SiO 等,利用其制备多种铬产品和其他金
2 3 2 3 2 3 2
属产品的工艺流程如下:
已知:Al O +Na CO 2NaAlO +CO ↑ SiO +Na CO Na SiO +CO ↑
2 3 2 3 2 2 2 2 3 2 3 2
回答下列问题:(1)步骤①发生的主要反应为FeO+Cr O +Na CO +NaNO Na CrO +Fe O +NaNO +A↑,反应
2 3 2 3 3 2 4 2 3 2
时应选用何种材质的容器?_______(填字母)。
A.塑料 B.刚玉 C.铁 D.石英
(2)“滤渣 2”是Al(OH) 和_______。 写出过量物质A与“滤液1"中溶质生成Al(OH) 的离子
3 3
方程式:_______。
(3)“滤液2”中的Na CrO 需要用H SO 酸化,用离子方程式表示该反应:_______。
2 4 2 4
(4)步骤④是在隔绝空气条件下,除生成Cr O 外,还生成了Na CO 和CO,若该反应中有3
2 3 2 3
mol Na Cr O 参加反应,则转移的电子为_______mol。
2 2 7
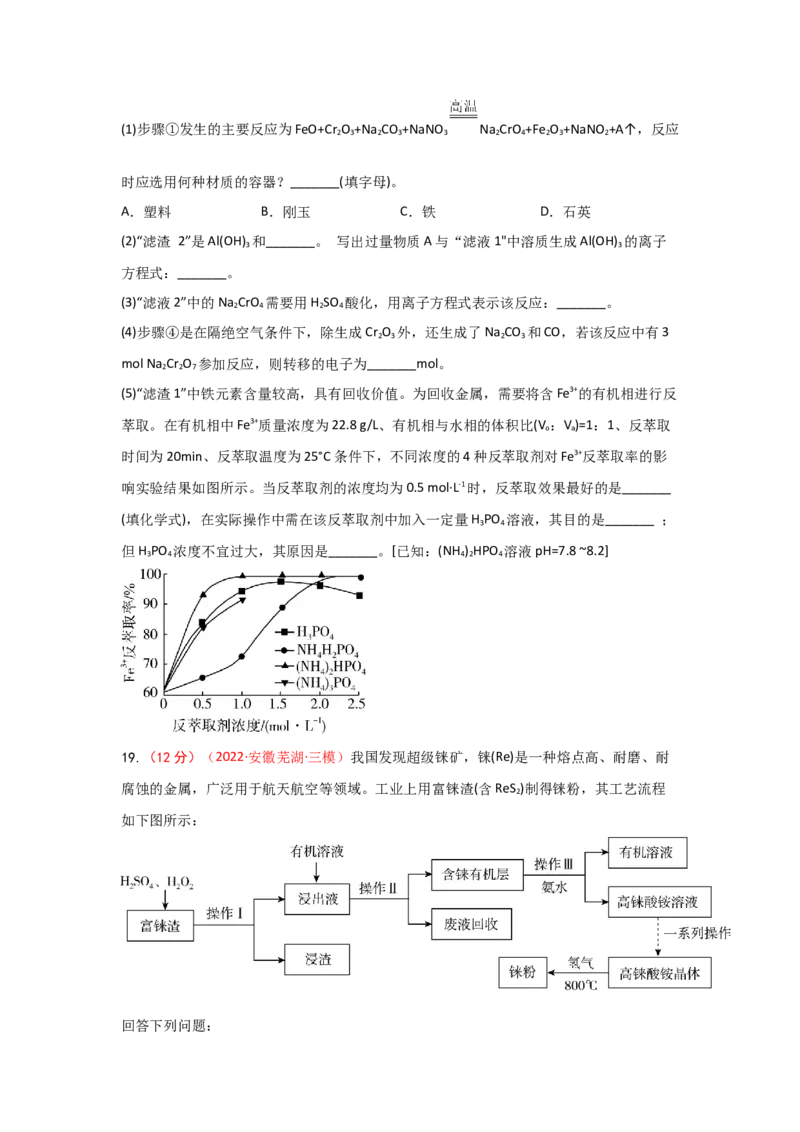
(5)“滤渣1”中铁元素含量较高,具有回收价值。为回收金属,需要将含Fe3+的有机相进行反
萃取。在有机相中Fe3+质量浓度为22.8 g/L、有机相与水相的体积比(V:V)=1:1、反萃取
o a
时间为20min、反萃取温度为25°C条件下,不同浓度的4种反萃取剂对Fe3+反萃取率的影
响实验结果如图所示。当反萃取剂的浓度均为0.5 mol·L-1时,反萃取效果最好的是_______
(填化学式),在实际操作中需在该反萃取剂中加入一定量H PO 溶液,其目的是_______ ;
3 4
但H PO 浓度不宜过大,其原因是_______。[已知:(NH ) HPO 溶液pH=7.8 ~8.2]
3 4 4 2 4
19.(12分)(2022·安徽芜湖·三模)我国发现超级铼矿,铼(Re)是一种熔点高、耐磨、耐
腐蚀的金属,广泛用于航天航空等领域。工业上用富铼渣(含ReS )制得铼粉,其工艺流程
2
如下图所示:
回答下列问题:(1)铼不溶于盐酸,可溶于稀硝酸生成强酸高铼酸(HReO ),请写出反应的离子方程式
4
_______。
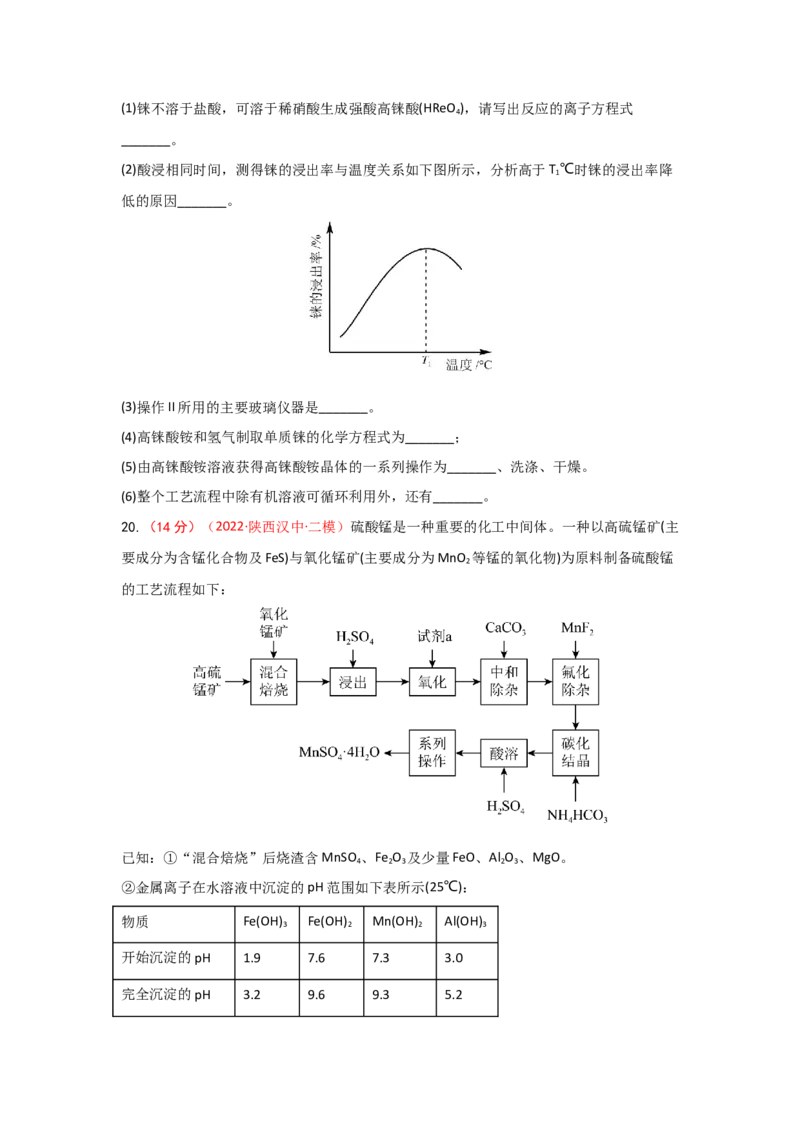
(2)酸浸相同时间,测得铼的浸出率与温度关系如下图所示,分析高于T ℃时铼的浸出率降
1
低的原因_______。
(3)操作II所用的主要玻璃仪器是_______。
(4)高铼酸铵和氢气制取单质铼的化学方程式为_______;
(5)由高铼酸铵溶液获得高铼酸铵晶体的一系列操作为_______、洗涤、干燥。
(6)整个工艺流程中除有机溶液可循环利用外,还有_______。
20.(14分)(2022·陕西汉中·二模)硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主
要成分为含锰化合物及FeS)与氧化锰矿(主要成分为MnO 等锰的氧化物)为原料制备硫酸锰
2
的工艺流程如下:
已知:①“混合焙烧”后烧渣含MnSO 、Fe O 及少量FeO、Al O 、MgO。
4 2 3 2 3
②金属离子在水溶液中沉淀的pH范围如下表所示(25℃):
物质 Fe(OH) Fe(OH) Mn(OH) Al(OH)
3 2 2 3
开始沉淀的pH 1.9 7.6 7.3 3.0
完全沉淀的pH 3.2 9.6 9.3 5.2③离子浓度≤10-5mol·L-1时,离子沉淀完全。
(1)“混合焙烧”的主要目的是_______
(2)若试剂a为MnO ,则氧化步骤发生反应的离子方程式为_______,若省略“氧化”步骤,
2
造成的影响是_______。
(3)“中和除杂”时,应控制溶液的pH范围是_______。
(4)“氟化除杂”后,溶液中c(F-)浓度为0.05mol·L-1。则溶液中c(Mg2+)和c(Ca2+)的比值
=_______(已知:K (MgF )=6.4×10-10;K (CaF )=3.6×10-12)
sp 2 sp 2
(5)“碳化结晶”时发生反应的离子方程式为_______,选择NH HCO 而不选择Na CO 溶液的
4 3 2 3
原因是_______。