文档内容
平衡体系中的有关计算
1.(6分)对于反应CO (g)+H (g) CO(g)+H O(g) ΔH>0,反应速率v=v -v =k p(CO )·p(H )-k
2 2 2 正 逆 正 2 2 逆
p(CO)·p(H O),其中k 、k 分别为正、逆反应速率常数,p为气体的分压(分压=总压×物质的量分数)。
2 正 逆
(1)降低温度,k -k (填“增大”“减小”或“不变”)。
正 逆
v 4
(2)在T K、101 kPa下,按照n(CO )∶n(H )=1∶1投料,CO 转化率为50%时, 正 = ,用气体分压表示的
2 2 2 v 5
逆
平衡常数K = (保留小数点后一位)。
p
2.(9分)某化学兴趣小组模拟SO 催化氧化制备SO ,在2 L刚性容器中进行下列三组实验,数据如下:
2 3
第1组
第2组
第3组
温度/℃
T
1
T
2
T
3
投料n(SO )/mol
2
1
2
4
投料n(O )/mol
2
2
2
2
SO 平衡
2
转化率(α)/%
40
50
α
(1)T ℃时平衡常数K= (保留两位有效数字)。
1(2)若T =T ,则α (填“>”“<”或“=”)40%,结合相关数据计算,写出推理过程: 。
1 3
3.(15分)在5.0 MPa下,将5 mol CO 和16 mol H 在Cu/ZrO 催化剂作用下进行主反应:CO (g) +3H (g)
2 2 2 2 2
CH OH(g) + H O(g) ΔH =-49.3 kJ·mol-1。该合成过程还存在一个副反应:CO (g) + H (g) CO(g) +
3 2 1 2 2
CH OH或CO的量
H O(g) ΔH =+41 kJ·mol-1。平衡时CH OH和CO 选择性S[S(CH OH或CO)= 3 ×100%]
2 2 3 3 已转化CO 的总量
2
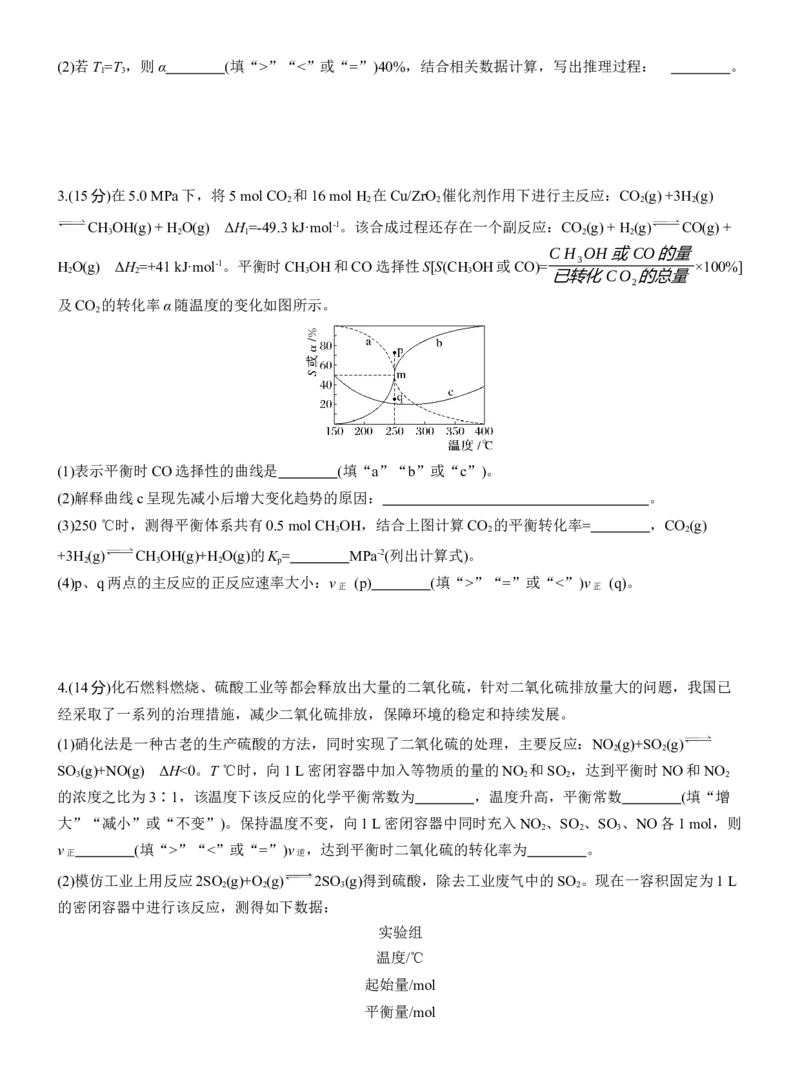
及CO 的转化率α随温度的变化如图所示。
2
(1)表示平衡时CO选择性的曲线是 (填“a”“b”或“c”)。
(2)解释曲线c呈现先减小后增大变化趋势的原因: 。
(3)250 ℃时,测得平衡体系共有0.5 mol CH OH,结合上图计算CO 的平衡转化率= ,CO (g)
3 2 2
+3H (g) CH OH(g)+H O(g)的K = MPa-2(列出计算式)。
2 3 2 p
(4)p、q两点的主反应的正反应速率大小:v (p) (填“>”“=”或“<”)v (q)。
正 正
4.(14分)化石燃料燃烧、硫酸工业等都会释放出大量的二氧化硫,针对二氧化硫排放量大的问题,我国已
经采取了一系列的治理措施,减少二氧化硫排放,保障环境的稳定和持续发展。
(1)硝化法是一种古老的生产硫酸的方法,同时实现了二氧化硫的处理,主要反应:NO (g)+SO (g)
2 2
SO (g)+NO(g) ΔH<0。T ℃时,向1 L密闭容器中加入等物质的量的NO 和SO ,达到平衡时NO和NO
3 2 2 2
的浓度之比为3∶1,该温度下该反应的化学平衡常数为 ,温度升高,平衡常数 (填“增
大”“减小”或“不变”)。保持温度不变,向1 L密闭容器中同时充入NO 、SO 、SO 、NO各1 mol,则
2 2 3
v (填“>”“<”或“=”)v ,达到平衡时二氧化硫的转化率为 。
正 逆
(2)模仿工业上用反应2SO (g)+O (g) 2SO (g)得到硫酸,除去工业废气中的SO 。现在一容积固定为1 L
2 2 3 2
的密闭容器中进行该反应,测得如下数据:
实验组
温度/℃
起始量/mol
平衡量/mol达平衡
所需时
间/min
SO
2
O
2
SO
3
1
550
2
1
0.5
10
2
650
1
0.5
0.4
4
①分析第1组和第2组实验数据,可以得出有关反应速率的结论是 。
②已知,反应中v =k c2(SO )·c(O ),v =k c2(SO ),k 、k 为速率常数。若实验组2,1 min时n(SO )=0.2
正 1 2 2 逆 2 3 1 2 3
k v
mol,则 1 = , 正 = 。
k v
2 逆
5.(18分)合成氨原料气高纯氢可以由天然气、水蒸气催化重整制取,所涉及的主要反应如下:
相关反应
ΔH
物质的量分数平衡常数
反应ⅰ
CH (g)+H O(g) CO(g)+3H (g)
4 2 2
ΔH =+206 kJ·mol-1
1K
x1
反应ⅱ
CO(g)+H O(g) CO (g)+H (g)
2 2 2
ΔH =-41 kJ·mol-1
2
K
x2
反应ⅲ
CH (g)+2H O(g) CO (g)+4H (g)
4 2 2 2
ΔH =+165 kJ·mol-1
3
K
x3
xc (C)·xd (D)
已知:反应aA(g)+bB(g) cC(g)+dD(g)的物质的量分数平衡常数K= ,其中x(A)、x(B)、
x xa (A)·xb (B)
x(C)、x(D)为各组分的物质的量分数。
K
(1)相同条件下,随着反应温度的升高,化学平衡常数K 、K 的比值( x1 ) (填“增大”“减小”
x1 x3 K
x3
或“不变”),其原因为 。
(2)T ℃时,向2 L恒容密闭容器中充入1 mol CH 和2 mol H O(g),发生上述反应ⅰ和ⅲ。测得反应达到平
4 2
衡时,容器中n(CH )=0.4 mol,n(H )=2 mol。
4 2
①T ℃时,反应中H O的平衡转化率为 。
2
②T ℃时,反应ⅰ的平衡常数K = (列出表达式,无需化简)。
x1
③若将容器的体积压缩为1 L,甲烷的平衡转化率 (填“增大”“减小”或“不变”,下同),反应
ⅲ的逆反应速率 。
6.(15分)CO 催化加氢可合成乙烯,反应为2CO (g)+6H (g) C H (g)+4H O(g) ΔH<0,在恒压密闭容器
2 2 2 2 4 2
中,起始充入2 mol CO (g)和6 mol H (g)发生反应,不同温度下达到平衡时各组分的体积分数随温度的变
2 2
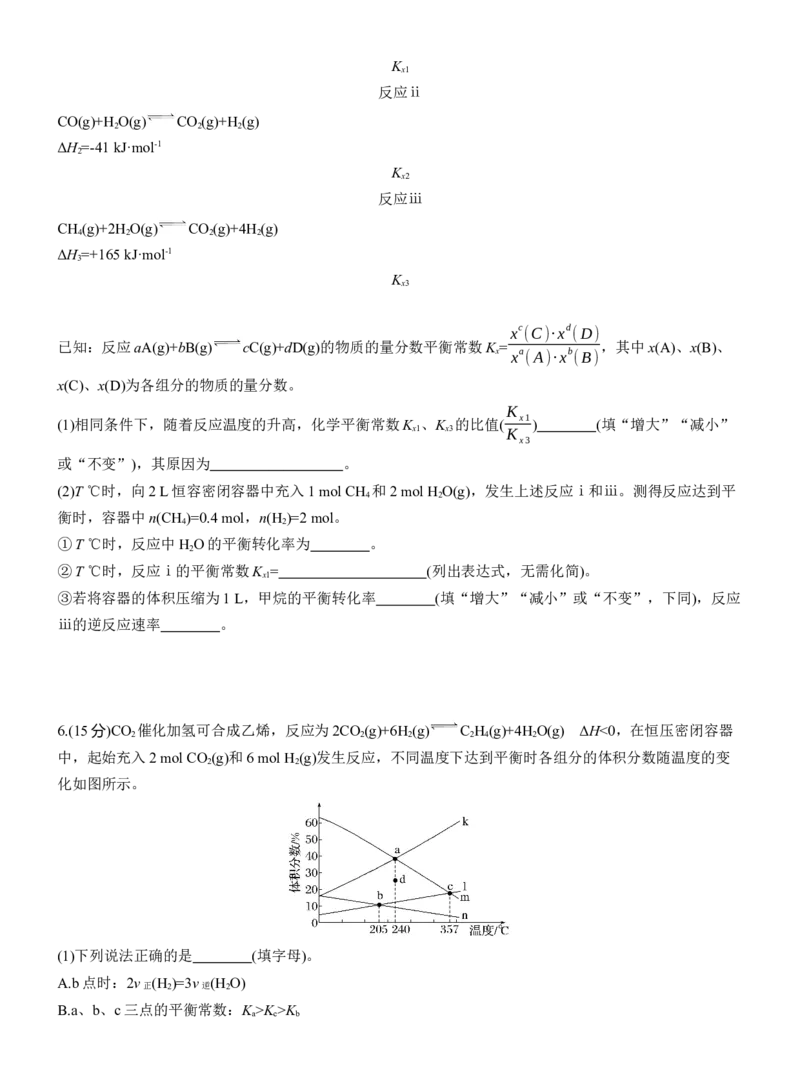
化如图所示。
(1)下列说法正确的是 (填字母)。
A.b点时:2v (H )=3v (H O)
正 2 逆 2
B.a、b、c三点的平衡常数:K>K>K
a c bC.将H O(g)液化分离可提高C H 的产率
2 2 4
D.活性更高的催化剂可提高CO 的平衡转化率
2
(2)表示C H 体积分数随温度变化的曲线是 (填“k”“l”“m”或“n”)。
2 4
(3)若d点表示240 ℃某时刻H 的体积分数,保持温度不变,则反应向 (填“正”或“逆”)反应方
2
向进行。
(4)205 ℃,反应达b点所用时间为t min,则此过程中用CO 表示的反应速率是 mol·min-1。若平
2
衡时b点总压为p,则平衡常数K = (列出计算式,以分压表示,分压=总压×物质的量分数)。
p
7.(6分)我国科学家成功开发Pd⁃Fe/Fe
2
O
3
催化剂在低温条件下高选择性合成高纯度的乙烯,化学原理为
主反应:C H (g)+H (g) C H (g) ΔH
2 2 2 2 4 1
副反应:C H (g)+2H (g) C H (g) ΔH
2 2 2 2 6 2
在密闭容器中充入1 mol C H 和2 mol H ,发生上述两个反应,测得C H 平衡转化率与温度、压强的关系
2 2 2 2 2
8 n(C H )
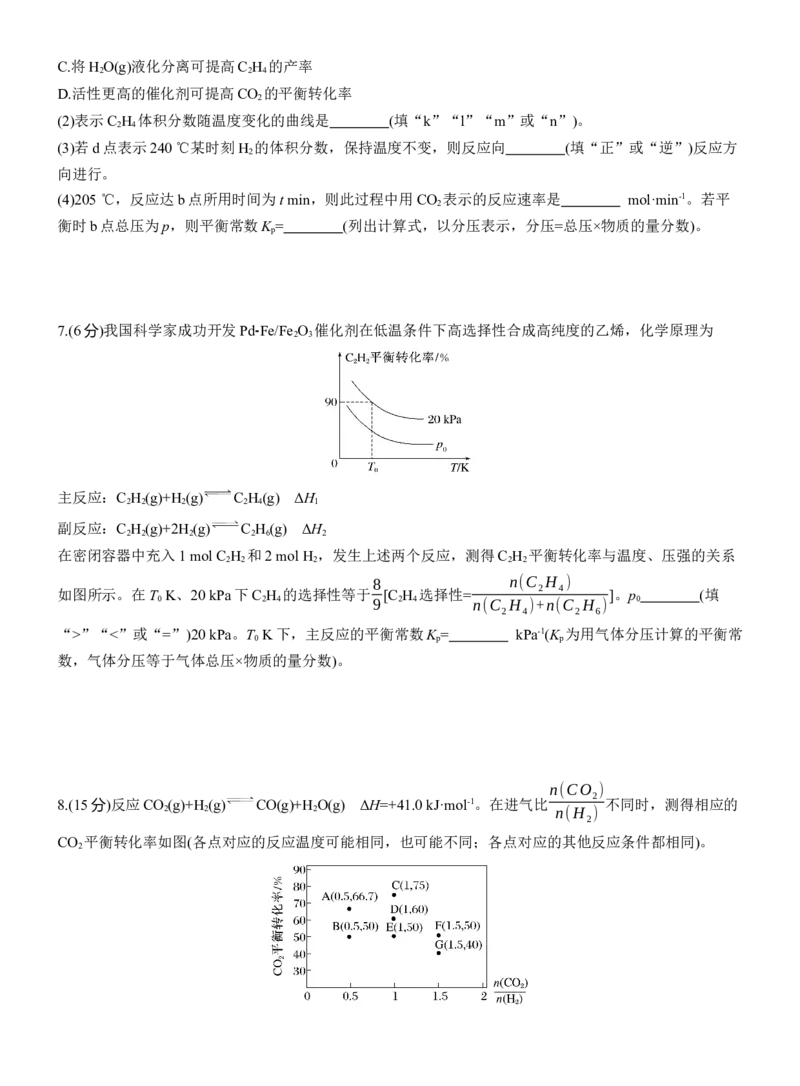
如图所示。在T K、20 kPa下C H 的选择性等于 [C H 选择性= 2 4 ]。p (填
0 2 4 9 2 4 n(C H )+n(C H ) 0
2 4 2 6
“>”“<”或“=”)20 kPa。T K下,主反应的平衡常数K = kPa-1(K 为用气体分压计算的平衡常
0 p p
数,气体分压等于气体总压×物质的量分数)。
n(CO )
2
8.(15分)反应CO (g)+H (g) CO(g)+H O(g) ΔH=+41.0 kJ·mol-1。在进气比 不同时,测得相应的
2 2 2 n(H )
2
CO 平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。
2(1)反应中CO 的平衡转化率与进气比、反应温度之间的关系是 。
2
(2)图中E和G两点对应的反应温度T 、T 的关系是 ,其原因是 。
E G
(3)A、B两点对应的反应速率v (填“<”“=”或“>”)v 。已知反应速率v =k
A B 正 正
x(CO )·x(H ),v =k x(CO)·x(H O),k为反应速率常数,x为物质的量分数,在达到平衡状态为C点的反应
2 2 逆 逆 2
v
过程(此过程为恒温)中,当CO 的转化率刚好达到60%时, 正 = 。
2 v
逆答案精析
1.(1)减小 (2)0.8
解析 (1)降低温度,反应逆向进行,所以k -k 减小。
正 逆
(2)设初始n(CO )=2 mol,
2
CO (g)+H (g) CO(g)+H O(g)
2 2 2
起始/mol 2 2 0 0
转化/mol 1 1 1 1
平衡/mol 1 1 1 1
v k p(CO )·p(H ) 4 1 v k 4
正= 正× 2 2 = ,其中p(CO )=p(H )=p(CO)=p(H O)= p ,即 正 = 正 = ,平衡时v =v
v k p(CO)·p(H O) 5 2 2 2 4 总 v k 5 正
逆 逆 2 逆 逆
p(CO)·p(H O) k 4
,有k p(CO )·p(H )=k p(CO)·p(H O),则K= 2 = 正= =0.8。
逆 正 2 2 逆 2 p p(CO )·p(H ) k 5
2 2 逆
2.(1)0.49
(2)< T =T 时,假设反应达到平衡时,SO 的转化率也为40%,则转化的c(SO )=0.8 mol·L-1。
3 1 2 2
2SO (g)+O (g) 2SO (g)
2 2 3
起始浓度/(mol·L-1) 2 1 0
转化浓度/(mol·L-1) 0.8 0.4 0.8
α=40%时浓度/(mol·L-1) 1.2 0.6 0.8
c2 (SO ) 0.82 20
Q= 3 = = >K,平衡逆向移动,所以SO 的平衡转化率小于40%
c2 (SO )·c(O ) 1.22×0.6 27 2
2 2
解析 (1)T ℃时SO 的平衡转化率为40%,则转化的c(SO )=0.2 mol·L-1。
1 2 2
2SO (g)+O (g) 2SO (g)
2 2 3
起始浓度/(mol·L-1) 0.5 1 0
转化浓度/(mol·L-1) 0.2 0.1 0.2
平衡浓度/(mol·L-1) 0.3 0.9 0.2
c2 (SO ) 0.22
3
K= = ≈0.49。
c2 (SO )·c(O ) 0.32×0.9
2 2
3.(1)b (2)250 ℃以前,体系以主反应为主,温度升高,主反应平衡逆向移动,CO 的转化率降低;250 ℃
2
以后,体系以副反应为主,温度升高,副反应平衡正向移动,CO 的转化率升高 (3)20%
2
(0.5 ) ( 1 )
×5 × ×5
20 20
(4)<
( 4 ) (14 ) 3
×5 × ×5
20 20解析 (1)主反应为放热反应,副反应为吸热反应,升温主反应平衡逆向移动,副反应平衡正向移动,故表
示平衡时CO选择性的曲线是b。(3)250 ℃时,测得平衡体系共有0.5 mol CH OH,结合题图可知,
3
0.5mol 1
S(CH OH)=50%,S(CH OH)= ×100%=50%,所以Δn(CO )=1 mol,CO 的平衡转化率=
3 3 Δn(CO ) 2 2 5
2
×100%=20%,对于主反应:
CO (g)+3H (g) CH OH(g)+H O(g)
2 2 3 2
变化/mol 0.5 1.5 0.5 0.5
对于副反应,变化的CO 为0.5 mol ,则
2
CO (g)+H (g) CO(g)+H O(g)
2 2 2
变化/mol 0.5 0.5 0.5 0.5
平衡时n(CO )=(5-1) mol=4 mol,n(H )=(16-1.5-0.5) mol=14 mol,n(CH OH)=0.5 mol,n(H O)=(0.5+0.5)
2 2 3 2
mol=1 mol,n(CO)=0.5 mol,总物质的量为(4+14+0.5+1+0.5) mol=20 mol,对于主反应,K =
p
(0.5 ) ( 1 )
×5 × ×5
20 20
MPa-2。(4)根据图像,p位于曲线a之上,q位于曲线a之下,p、q两点的主反应的正
( 4 ) (14 ) 3
×5 × ×5
20 20
反应速率大小:v (p) 50% (2)①温度升高,反应速率增大 ②1.48 9.472
5.(1)增大 根据盖斯定律可知反应ⅰ-反应ⅲ可得:CO (g)+H (g) CO(g)+H O(g),该反应ΔH=+41
2 2 2
K
kJ·mol-1,温度升高,平衡正向移动,该反应的物质的量分数平衡常数K= x1增大 (2)①40%
x K
x3
( 2 ) 3 0.4
×
4.2 4.2
② ③减小 增大
0.4 1.2
×
4.2 4.2
4+2×2-0.4×4-2×2
解析 (2)①根据H原子守恒,平衡时H O的物质的量为 mol=1.2 mol,H O的平衡
2 2 2
2-1.2
转化率为 ×100%=40%。②设平衡时反应ⅰ消耗x mol甲烷,反应ⅲ消耗y mol甲烷,则:
2
CH (g)+H O(g) CO(g)+3H (g)
4 2 2
变化/mol x x x 3x
CH (g)+2H O(g) CO (g)+4H (g)
4 2 2 2
变化/mol y 2y y 4y由题意得:x+y=1-0.4=0.6,3x+4y=2,解得:x=0.4,y=0.2;则平衡时n(CH )=0.4 mol,n(H )=2 mol,
4 2
( 2 ) 3 0.4
×
4.2 4.2
n(CO)=0.4 mol,n(CO )=0.2 mol,n(H O)=1.2 mol,n(总)=4.2 mol,反应ⅰ的平衡常数K = 。
2 2 x1
0.4 1.2
×
4.2 4.2
③反应ⅰ和ⅲ正向气体分子数均增大,压缩体积,平衡均逆向移动,甲烷的平衡转化率减小;压缩体积各
物质的浓度均增大,则正、逆反应速率均增大。
1 4
( p)×( p) 4
4 9 9
6.(1)AC (2)n (3)逆 (4)
3t 1 1
( p) 2×( p) 6
9 3
解析 (1)由化学方程式体现的关系可知,b点时达到平衡状态,正、逆反应速率相等,则有2v (H )=3v
正 2 逆
(H O),A正确;反应为放热反应,随着温度升高,平衡逆向移动,平衡常数减小,故a、b、c三点的平衡
2
常数:K >K>K,B错误;将H O(g)液化分离,平衡正向移动,可提高C H 的产率,C正确;活性更高的
b a c 2 2 4
催化剂可提高反应速率,但是不改变CO 的平衡转化率,D错误。(2)随着温度升高,平衡逆向移动,乙烯、
2
水的体积分数减小,结合化学方程式中化学计量数可知,乙烯减小的程度小于水,故表示水体积分数随温
度变化的曲线是m,表示C H 体积分数随温度变化的曲线是n。(3)随着温度升高,平衡逆向移动,二氧化
2 4
碳、氢气的体积分数增大,结合化学方程式中化学计量数可知,二氧化碳增大的程度小于氢气,则l为二
氧化碳体积分数随温度变化曲线,k为氢气体积分数随温度变化曲线;若d点表示240 ℃某时刻H 的体积
2
分数,此时氢气的体积分数小于平衡时氢气的体积分数,保持温度不变,反应向逆反应方向进行。(4)205
℃,反应达b点所用时间为t min,设CO 转化了2a mol,可得
2
2CO (g)+6H (g) C H (g)+4H O(g)
2 2 2 4 2
起始/mol 2 6 0 0
转化/mol 2a 6a a 4a
平衡/mol 2-2a 6-6a a 4a
2
2 ×2
此时二氧化碳和乙烯体积分数相同,则2-2a=a,a= ,则此过程中用CO 表示的反应速率是3
3 2
t
4 2 2 8
mol·min-1= mol·min-1;平衡时二氧化碳、氢气、乙烯、水分别为 mol、2 mol、 mol、 mol,总的物
3t 3 3 3
1 4
( p)×( p) 4
9 9
质的量为6 mol,若平衡时b点总压为p,则平衡常数K = 。
p 1 1
( p) 2×( p) 6
9 3
7.< 0.8
解析 主反应和副反应均为气体分子数减小的反应,增大压强,平衡正向移动,C H 的转化率升高,结合
2 2
图像可知,p <20 kPa;T K时,设平衡时C H (g)、C H (g)的物质的量分别为x mol、y mol;
0 0 2 4 2 6C H (g)+ H (g) C H (g)
2 2 2 2 4
起始/mol 1 2 0
转化/mol x x x
平衡/mol 1-x-y 2-x-2y x
C H (g)+ 2H (g) C H (g)
2 2 2 2 6
起始/mol 1-x 2-x 0
转化/mol y 2y y
平衡/mol 1-x-y 2-x-2y y
x+ y 8
由图可知,在T K、20 kPa下C H 的平衡转化率为90%,则 ×100%=90%;C H 的选择性等于 ,则
0 2 2 1 2 4 9
x 8
= ;解得x=0.8,y=0.1;平衡时C H (g)、C H (g)、C H (g)、H (g)的物质的量分别为0.1 mol、0.1
x+ y 9 2 2 2 6 2 4 2
0.8
20×
2.0
mol、0.8 mol、1.0 mol,总物质的量为2.0 mol,则T K下,主反应的平衡常数K =
0 p 0.1 1.0
(20× )×(20× )
2.0 2.0
kPa-1=0.8 kPa-1。
8.(1)反应温度相同,进气比越大,CO 的平衡转化率越小;进气比相同,反应温度越高,CO 的平衡转化
2 2
率越大(或进气比越大,反应温度越低,CO 的平衡转化率越小) (2)T =T K =K =1 (3)> 4
2 E G E G
n(CO )
解析 (2)在E点时
2
=1,CO 的平衡转化率为50%,根据三段式得
n(H ) 2
2
CO (g)+H (g) CO(g)+H O(g)
2 2 2
始/(mol·L-1) 1 1 0 0
转/(mol·L-1) 0.5 0.5 0.5 0.5
平/(mol·L-1) 0.5 0.5 0.5 0.5
c(CO)·c(H O) 0.5×0.5
2
K = = =1;
E c(CO )·c(H ) 0.5×0.5
2 2
n(CO )
2
在G点时 =1.5,CO 的平衡转化率为40%,根据三段式得
n(H ) 2
2
CO (g)+H (g) CO(g)+H O(g)
2 2 2
始/(mol·L-1) 1.5 1 0 0
转/(mol·L-1) 0.6 0.6 0.6 0.6
平/(mol·L-1) 0.9 0.4 0.6 0.6
c(CO)·c(H O) 0.6×0.6
2
K = = =1。
G c(CO )·c(H ) 0.9×0.4
2 2平衡常数只与温度有关,平衡常数相等,温度相等,故T =T 。(3)反应CO (g)+H (g) CO(g)+H O(g)
E G 2 2 2
n(CO )
2
ΔH=+41.0 kJ·mol-1,该反应为吸热反应,当 相同时,温度高CO 转化率大,A点的转化率大于B
n(H ) 2
2
n(CO )
2
点,说明A点的温度高,故反应速率:v >v ;在C点时 =1,CO 的平衡转化率为75%,根据三段
A B n(H ) 2
2
式得
CO (g)+H (g) CO(g)+H O(g)
2 2 2
始/(mol·L-1) 1 1 0 0
转/(mol·L-1) 0.75 0.75 0.75 0.75
平/(mol·L-1) 0.25 0.25 0.75 0.75
c(CO)·c(H O) 0.75×0.75
2
K= = =9,
c(CO )·c(H ) 0.25×0.25
2 2
k x(CO)·x(H O)
正 2
平衡状态时v =v ,得 = =K=9。当CO 的转化率刚好达到60%时,
正 逆 k x(CO )·x(H ) 2
逆 2 2
CO (g)+H (g) CO(g)+H O(g)
2 2 2
始/(mol·L-1) 1 1 0 0
转/(mol·L-1) 0.6 0.6 0.6 0.6
CO 转化率为60%时/(mol·L-1) 0.4 0.4 0.6 0.6
2
v k x(CO )·x(H ) 0.4×0.4
正 正 2 2
= =9× =4。
v k x(CO)·x(H O) 0.6×0.6
逆 逆 2