文档内容
2025新教材化学高考第一轮
专题十 化学反应与电能
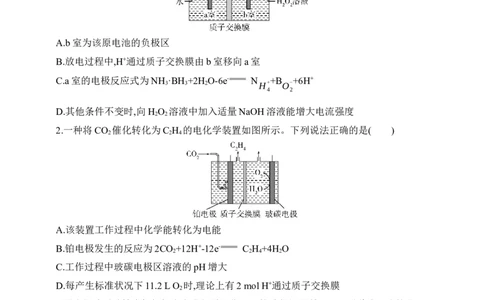
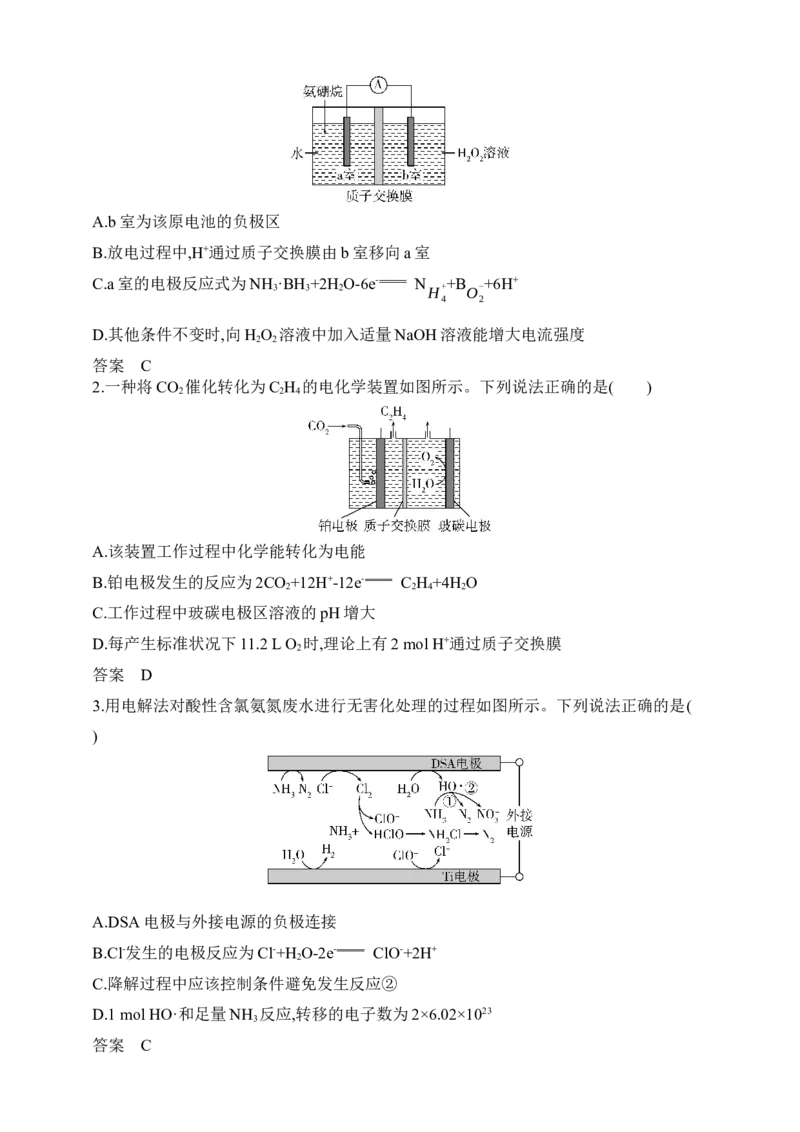
1.科学家利用氨硼烷设计成原电池装置如图所示,常温下该电池总反应为NH ·BH +3H O
3 3 2 2
NH BO +4H O。下列说法正确的是( )
4 2 2
A.b室为该原电池的负极区
B.放电过程中,H+通过质子交换膜由b室移向a室
C.a室的电极反应式为NH ·BH +2H O-6e- N +B +6H+
3 3 2 H+ O-
4 2
D.其他条件不变时,向H O 溶液中加入适量NaOH溶液能增大电流强度
2 2
2.一种将CO 催化转化为C H 的电化学装置如图所示。下列说法正确的是( )
2 2 4
A.该装置工作过程中化学能转化为电能
B.铂电极发生的反应为2CO +12H+-12e- C H +4H O
2 2 4 2
C.工作过程中玻碳电极区溶液的pH增大
D.每产生标准状况下11.2 L O 时,理论上有2 mol H+通过质子交换膜
2
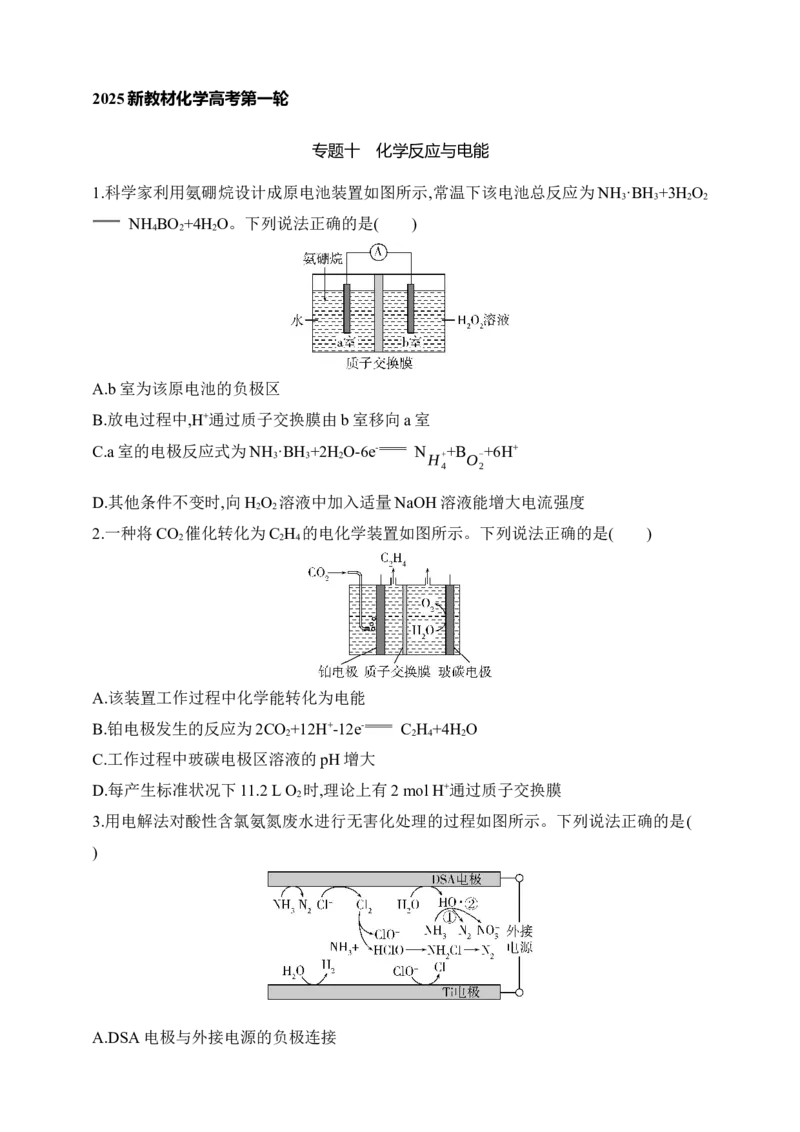
3.用电解法对酸性含氯氨氮废水进行无害化处理的过程如图所示。下列说法正确的是(
)
A.DSA电极与外接电源的负极连接B.Cl-发生的电极反应为Cl-+H O-2e- ClO-+2H+
2
C.降解过程中应该控制条件避免发生反应②
D.1 mol HO·和足量NH 反应,转移的电子数为2×6.02×1023
3
i
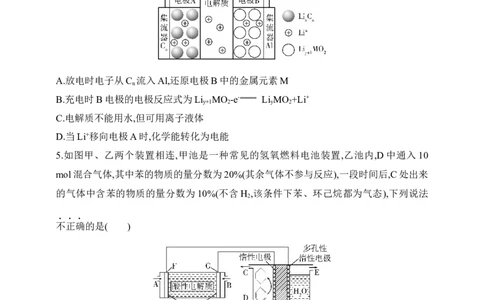
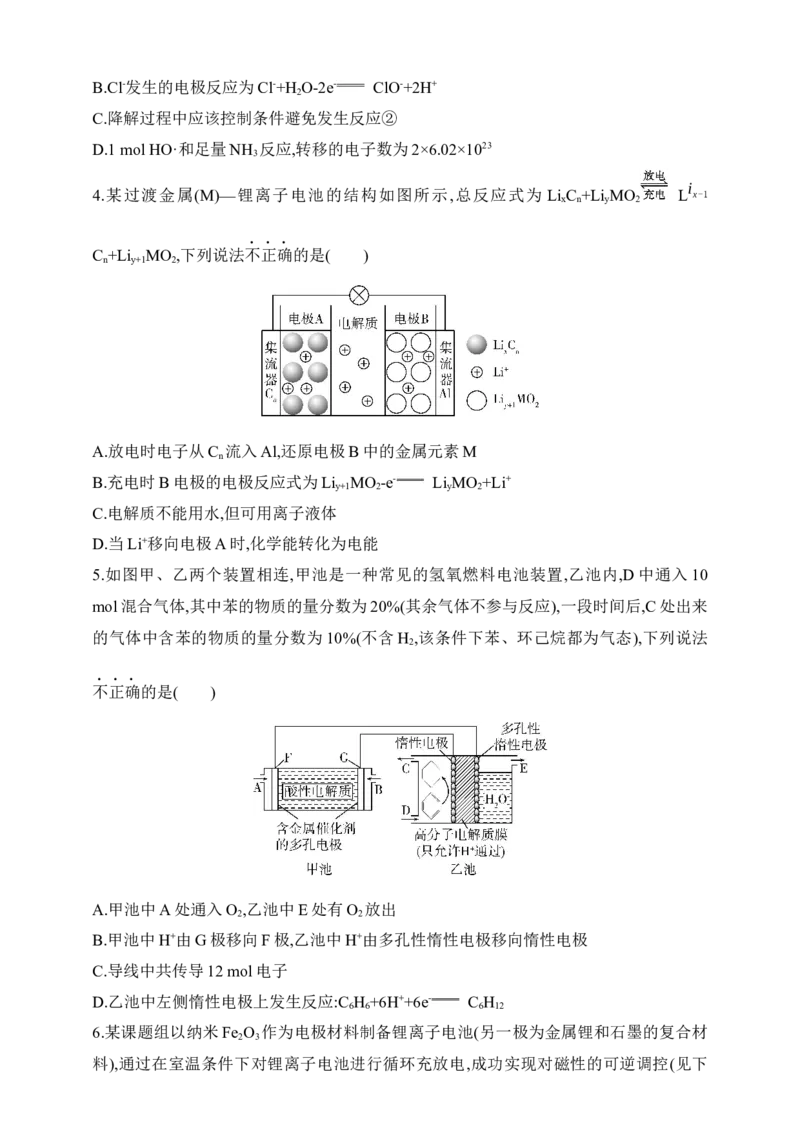
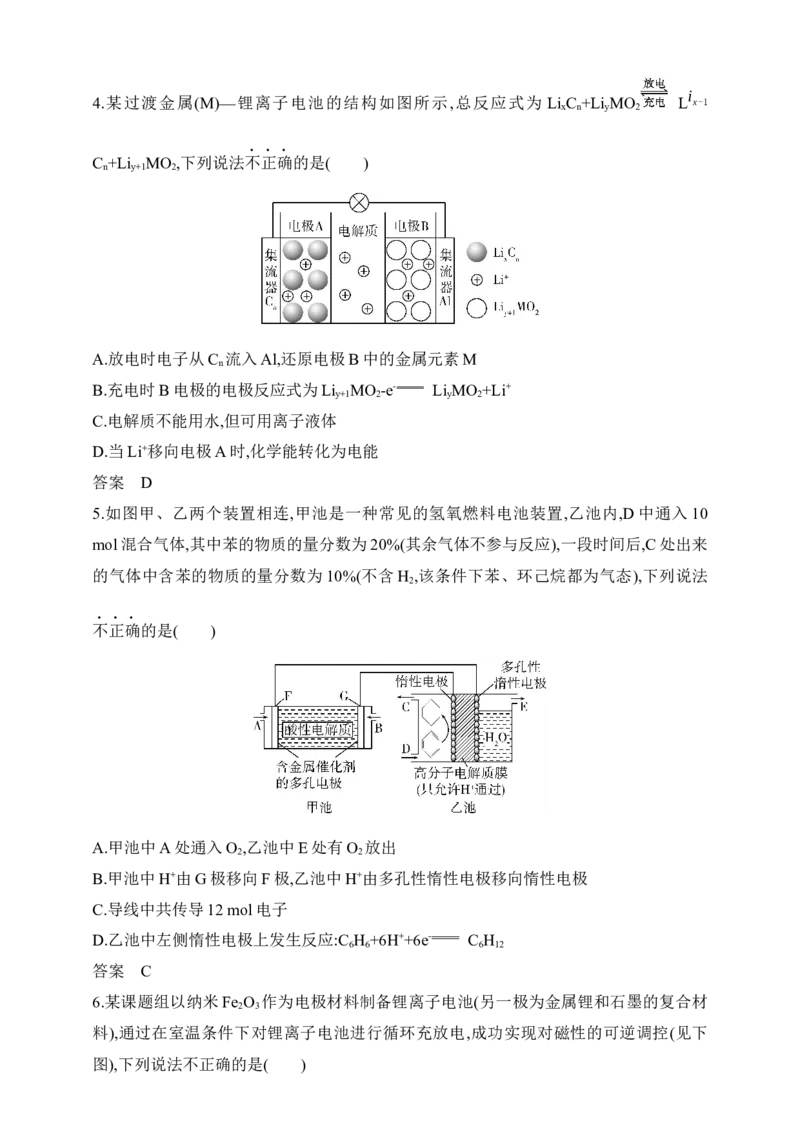
4.某过渡金属(M)—锂离子电池的结构如图所示,总反应式为 Li C +Li MO L x-1
x n y 2
C +Li MO ,下列说法不正确的是( )
n y+1 2
A.放电时电子从C 流入Al,还原电极B中的金属元素M
n
B.充电时B电极的电极反应式为Li MO -e- Li MO +Li+
y+1 2 y 2
C.电解质不能用水,但可用离子液体
D.当Li+移向电极A时,化学能转化为电能
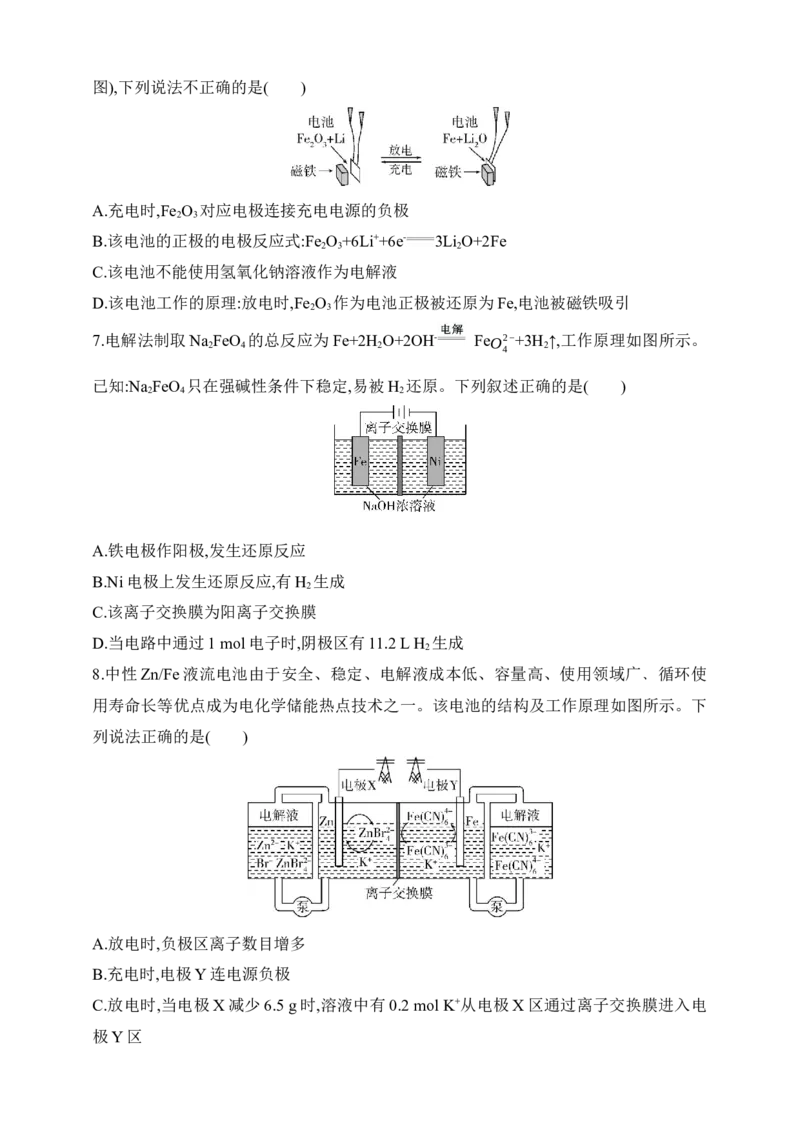
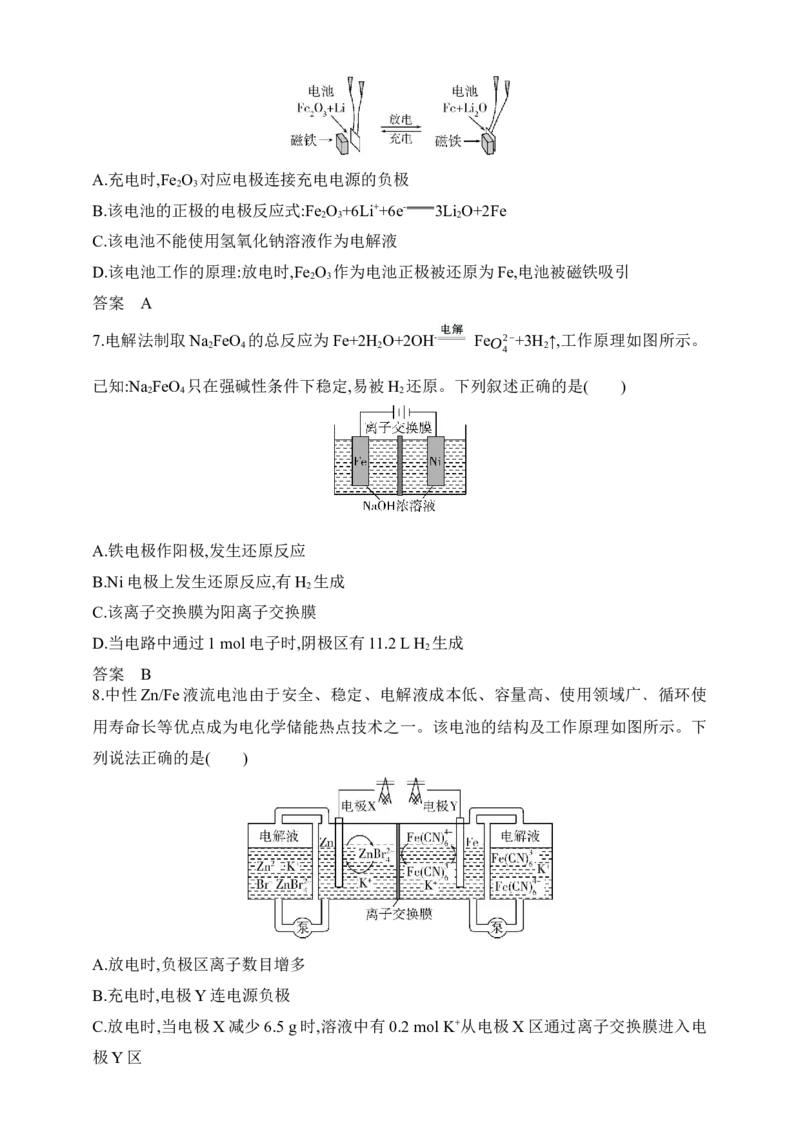
5.如图甲、乙两个装置相连,甲池是一种常见的氢氧燃料电池装置,乙池内,D中通入10
mol混合气体,其中苯的物质的量分数为20%(其余气体不参与反应),一段时间后,C处出来
的气体中含苯的物质的量分数为10%(不含H ,该条件下苯、环己烷都为气态),下列说法
2
不正确的是( )
A.甲池中A处通入O ,乙池中E处有O 放出
2 2
B.甲池中H+由G极移向F极,乙池中H+由多孔性惰性电极移向惰性电极
C.导线中共传导12 mol电子
D.乙池中左侧惰性电极上发生反应:C H +6H++6e- C H
6 6 6 12
6.某课题组以纳米Fe O 作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材
2 3
料),通过在室温条件下对锂离子电池进行循环充放电,成功实现对磁性的可逆调控(见下图),下列说法不正确的是( )
A.充电时,Fe O 对应电极连接充电电源的负极
2 3
B.该电池的正极的电极反应式:Fe O +6Li++6e- 3Li O+2Fe
2 3 2
C.该电池不能使用氢氧化钠溶液作为电解液
D.该电池工作的原理:放电时,Fe O 作为电池正极被还原为Fe,电池被磁铁吸引
2 3
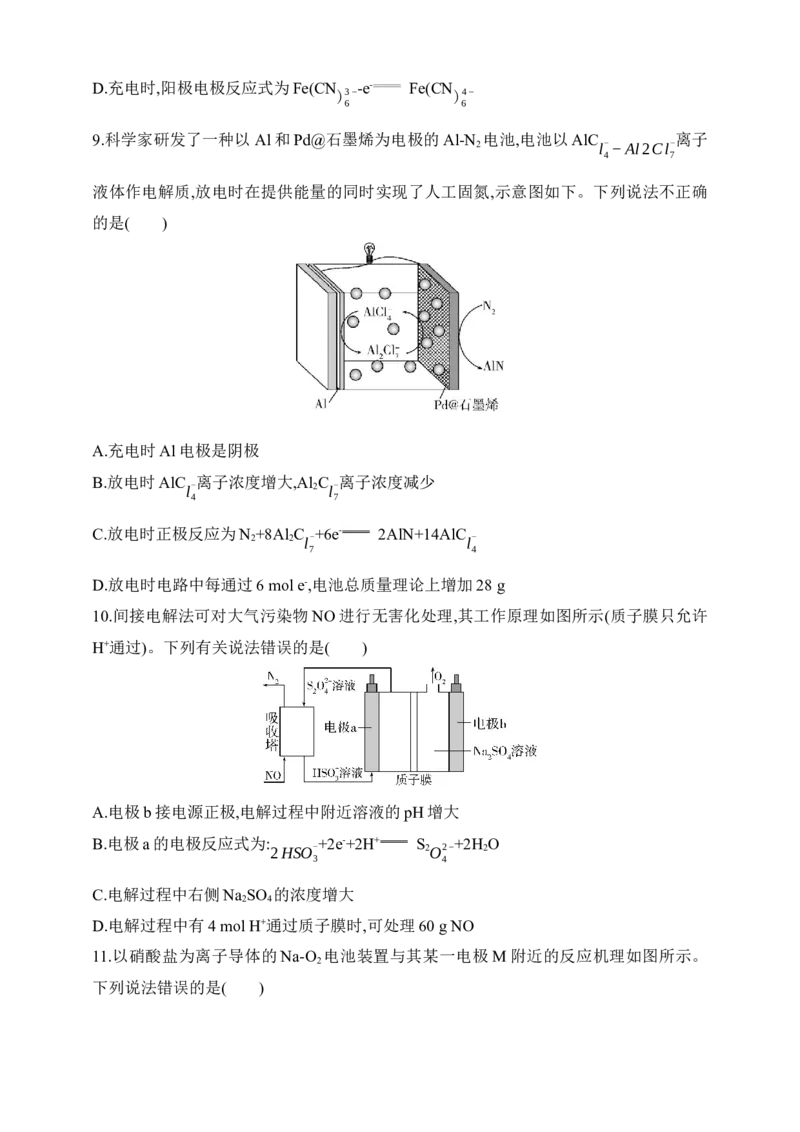
7.电解法制取Na FeO 的总反应为Fe+2H O+2OH- FeO2−+3H ↑,工作原理如图所示。
2 4 2 2
4
已知:Na FeO 只在强碱性条件下稳定,易被H 还原。下列叙述正确的是( )
2 4 2
A.铁电极作阳极,发生还原反应
B.Ni电极上发生还原反应,有H 生成
2
C.该离子交换膜为阳离子交换膜
D.当电路中通过1 mol电子时,阴极区有11.2 L H 生成
2
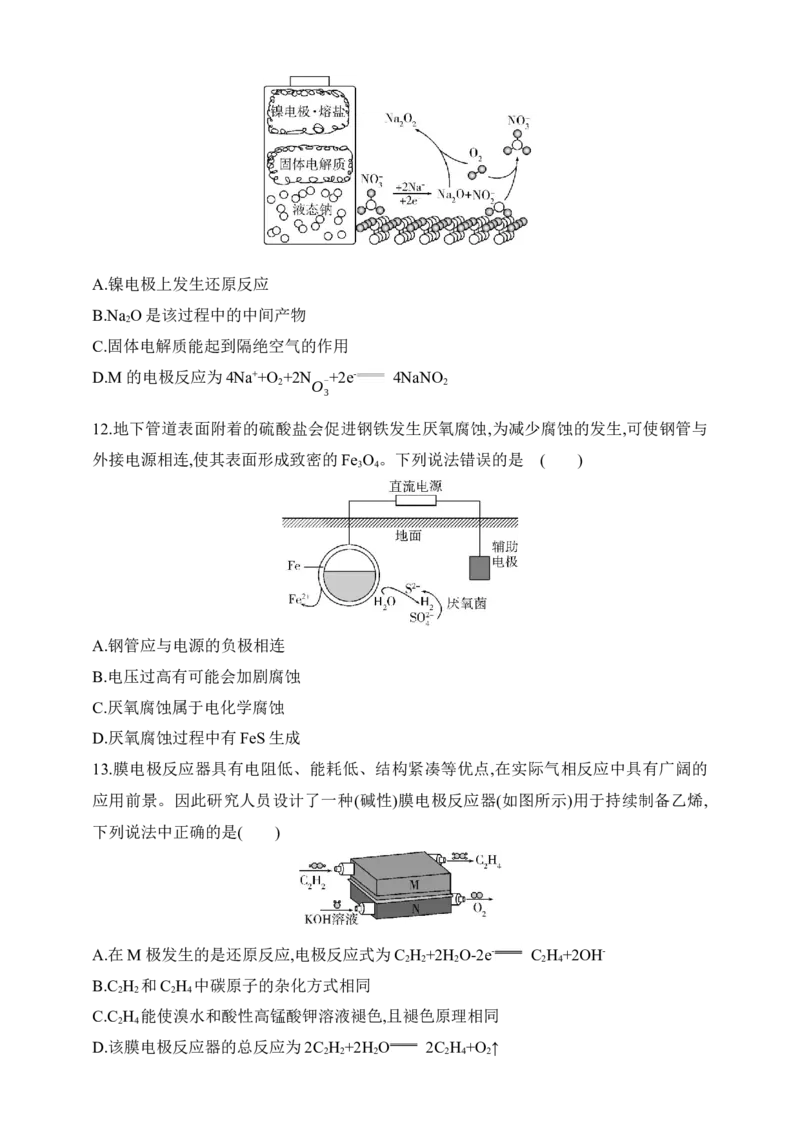
8.中性Zn/Fe液流电池由于安全、稳定、电解液成本低、容量高、使用领域广﹑循环使
用寿命长等优点成为电化学储能热点技术之一。该电池的结构及工作原理如图所示。下
列说法正确的是( )
A.放电时,负极区离子数目增多
B.充电时,电极Y连电源负极
C.放电时,当电极X减少6.5 g时,溶液中有0.2 mol K+从电极X区通过离子交换膜进入电
极Y区D.充电时,阳极电极反应式为Fe(CN -e- Fe(CN
)3− )4−
6 6
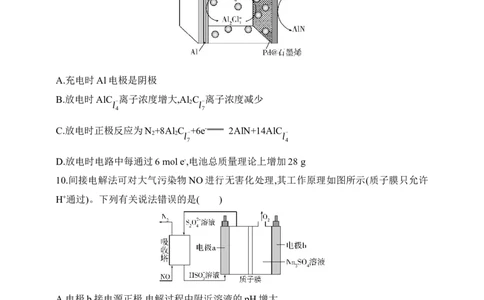
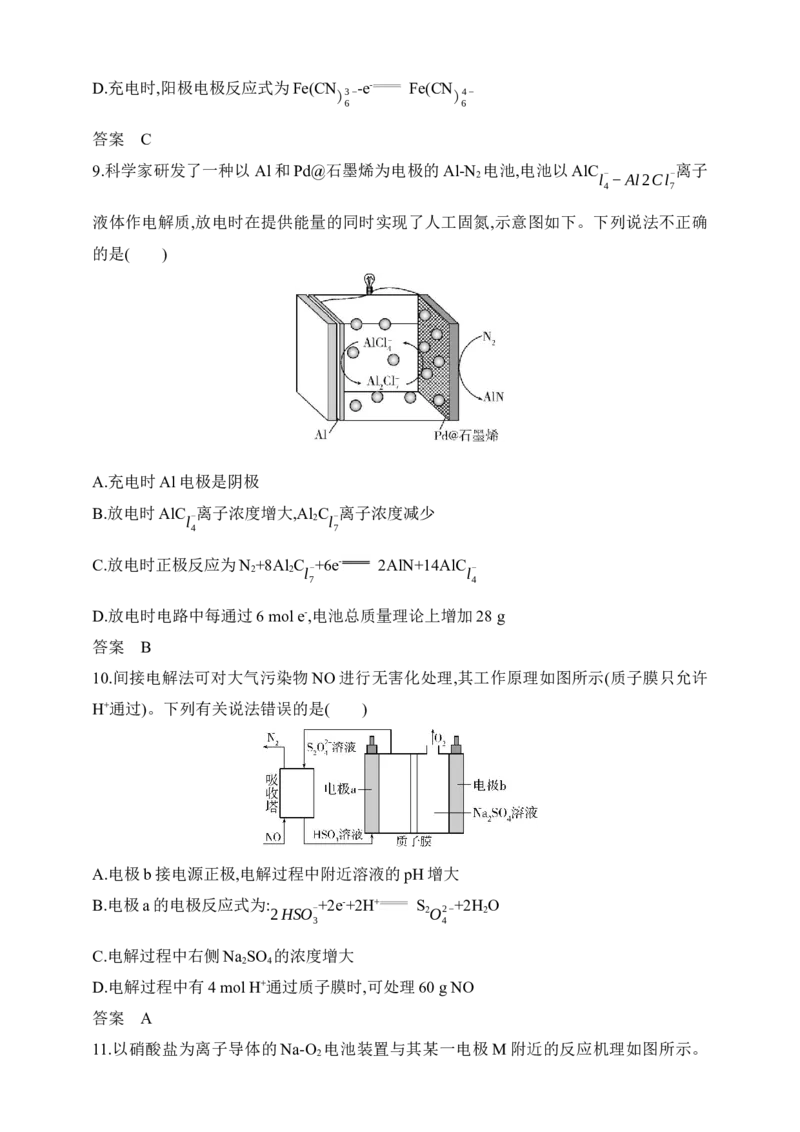
9.科学家研发了一种以 Al和Pd@石墨烯为电极的Al-N 电池,电池以AlC 离子
2 l-−Al2Cl-
4 7
液体作电解质,放电时在提供能量的同时实现了人工固氮,示意图如下。下列说法不正确
的是( )
A.充电时Al电极是阴极
B.放电时AlC 离子浓度增大,Al C 离子浓度减少
l- 2 l-
4 7
C.放电时正极反应为N +8Al C +6e- 2AlN+14AlC
2 2 l- l-
7 4
D.放电时电路中每通过6 mol e-,电池总质量理论上增加28 g
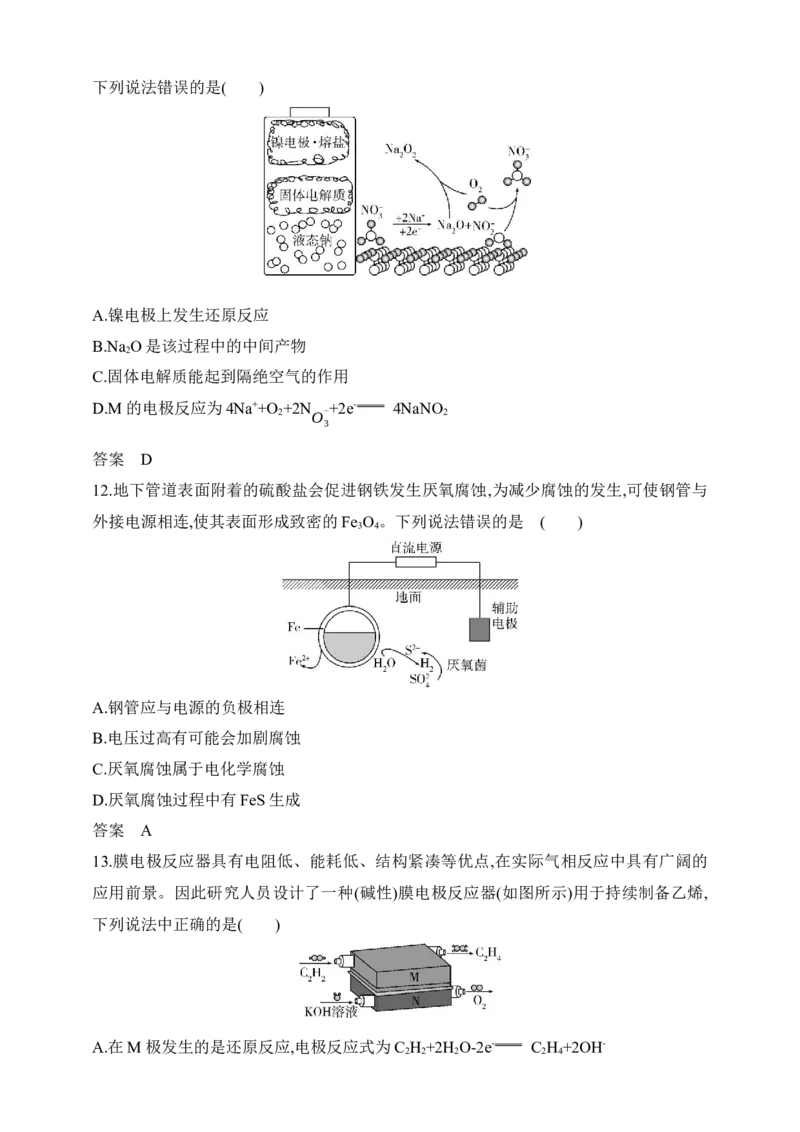
10.间接电解法可对大气污染物NO进行无害化处理,其工作原理如图所示(质子膜只允许
H+通过)。下列有关说法错误的是( )
A.电极b接电源正极,电解过程中附近溶液的pH增大
B.电极a的电极反应式为: +2e-+2H+ S +2H O
2HSO- 2O2− 2
3 4
C.电解过程中右侧Na SO 的浓度增大
2 4
D.电解过程中有4 mol H+通过质子膜时,可处理60 g NO
11.以硝酸盐为离子导体的Na-O 电池装置与其某一电极M附近的反应机理如图所示。
2
下列说法错误的是( )A.镍电极上发生还原反应
B.Na O是该过程中的中间产物
2
C.固体电解质能起到隔绝空气的作用
D.M的电极反应为4Na++O +2N +2e- 4NaNO
2 O- 2
3
12.地下管道表面附着的硫酸盐会促进钢铁发生厌氧腐蚀,为减少腐蚀的发生,可使钢管与
外接电源相连,使其表面形成致密的Fe O 。下列说法错误的是 ( )
3 4
A.钢管应与电源的负极相连
B.电压过高有可能会加剧腐蚀
C.厌氧腐蚀属于电化学腐蚀
D.厌氧腐蚀过程中有FeS生成
13.膜电极反应器具有电阻低、能耗低、结构紧凑等优点,在实际气相反应中具有广阔的
应用前景。因此研究人员设计了一种(碱性)膜电极反应器(如图所示)用于持续制备乙烯,
下列说法中正确的是( )
A.在M极发生的是还原反应,电极反应式为C H +2H O-2e- C H +2OH-
2 2 2 2 4
B.C H 和C H 中碳原子的杂化方式相同
2 2 2 4
C.C H 能使溴水和酸性高锰酸钾溶液褪色,且褪色原理相同
2 4
D.该膜电极反应器的总反应为2C H +2H O 2C H +O ↑
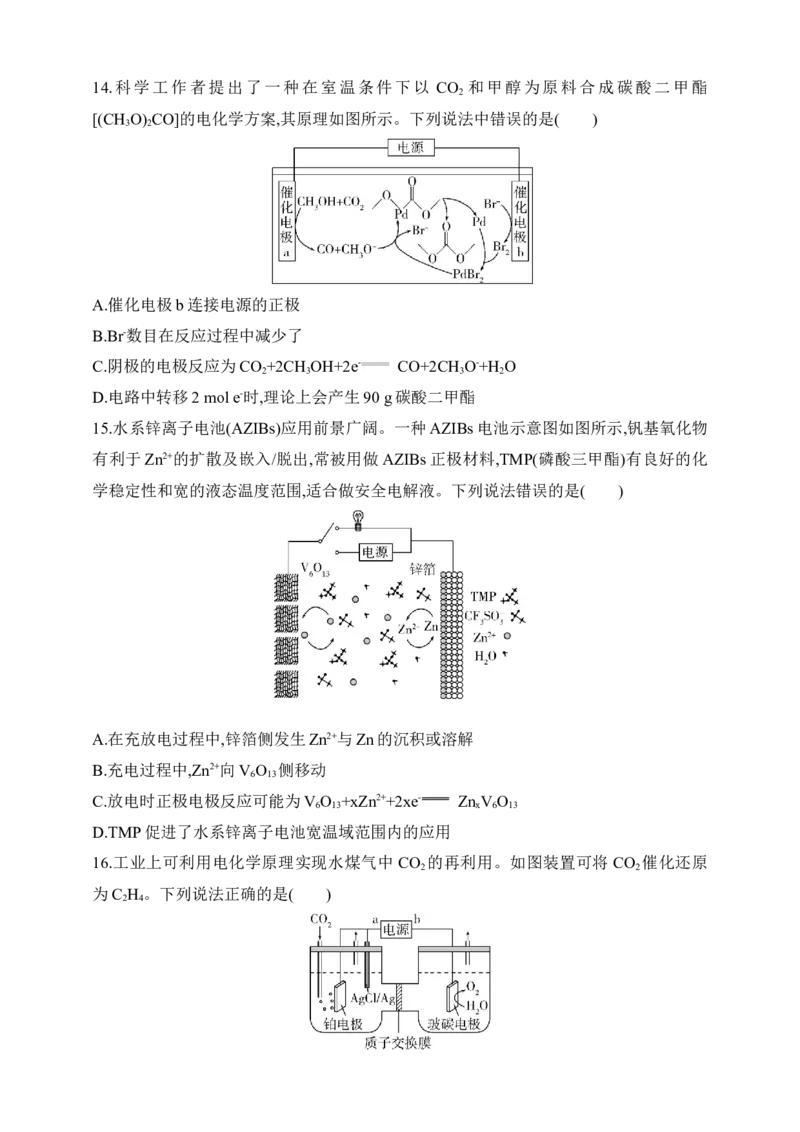
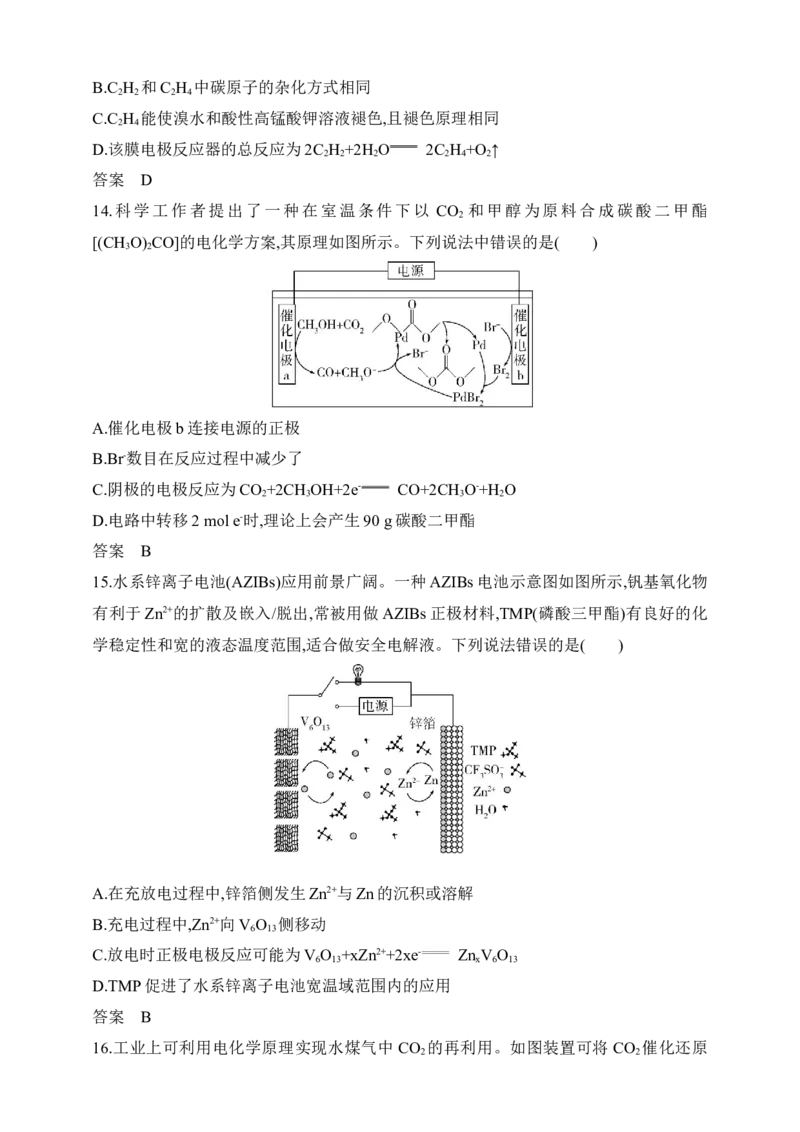
2 2 2 2 4 214.科学工作者提出了一种在室温条件下以 CO 和甲醇为原料合成碳酸二甲酯
2
[(CH O) CO]的电化学方案,其原理如图所示。下列说法中错误的是( )
3 2
A.催化电极b连接电源的正极
B.Br-数目在反应过程中减少了
C.阴极的电极反应为CO +2CH OH+2e- CO+2CH O-+H O
2 3 3 2
D.电路中转移2 mol e-时,理论上会产生90 g碳酸二甲酯
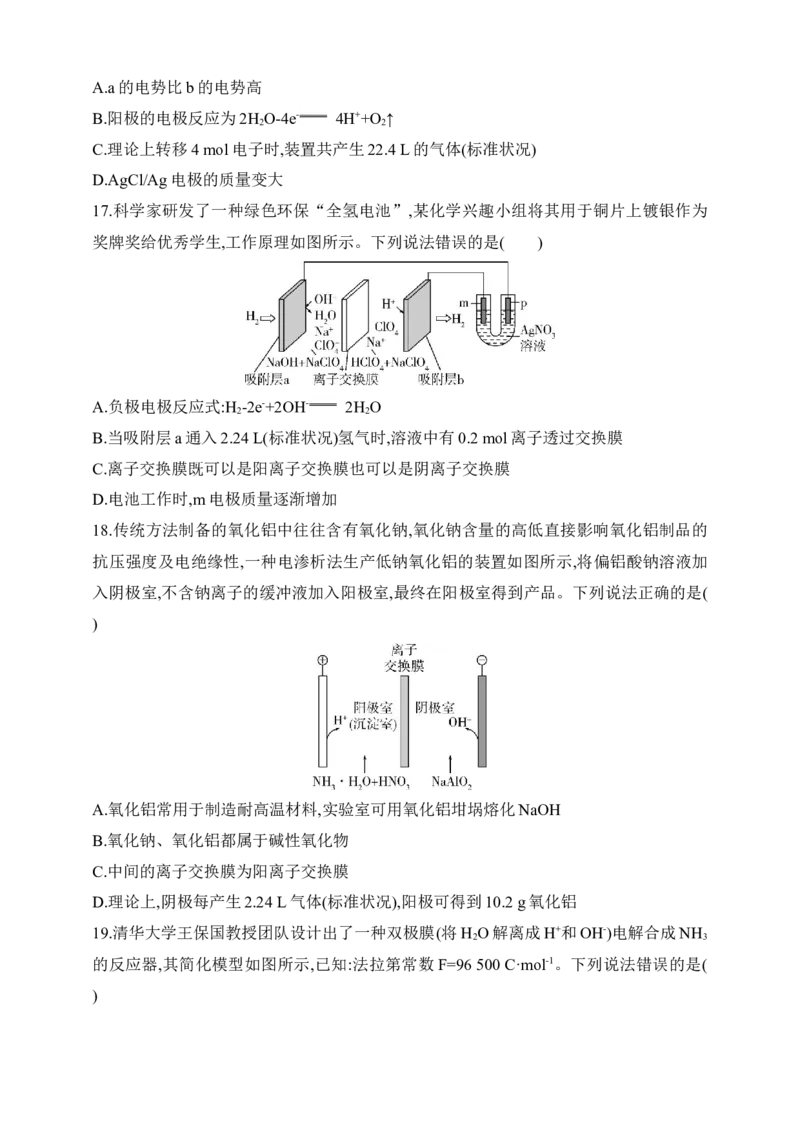
15.水系锌离子电池(AZIBs)应用前景广阔。一种AZIBs电池示意图如图所示,钒基氧化物
有利于Zn2+的扩散及嵌入/脱出,常被用做AZIBs正极材料,TMP(磷酸三甲酯)有良好的化
学稳定性和宽的液态温度范围,适合做安全电解液。下列说法错误的是( )
A.在充放电过程中,锌箔侧发生Zn2+与Zn的沉积或溶解
B.充电过程中,Zn2+向V O 侧移动
6 13
C.放电时正极电极反应可能为V O +xZn2++2xe- Zn V O
6 13 x 6 13
D.TMP促进了水系锌离子电池宽温域范围内的应用
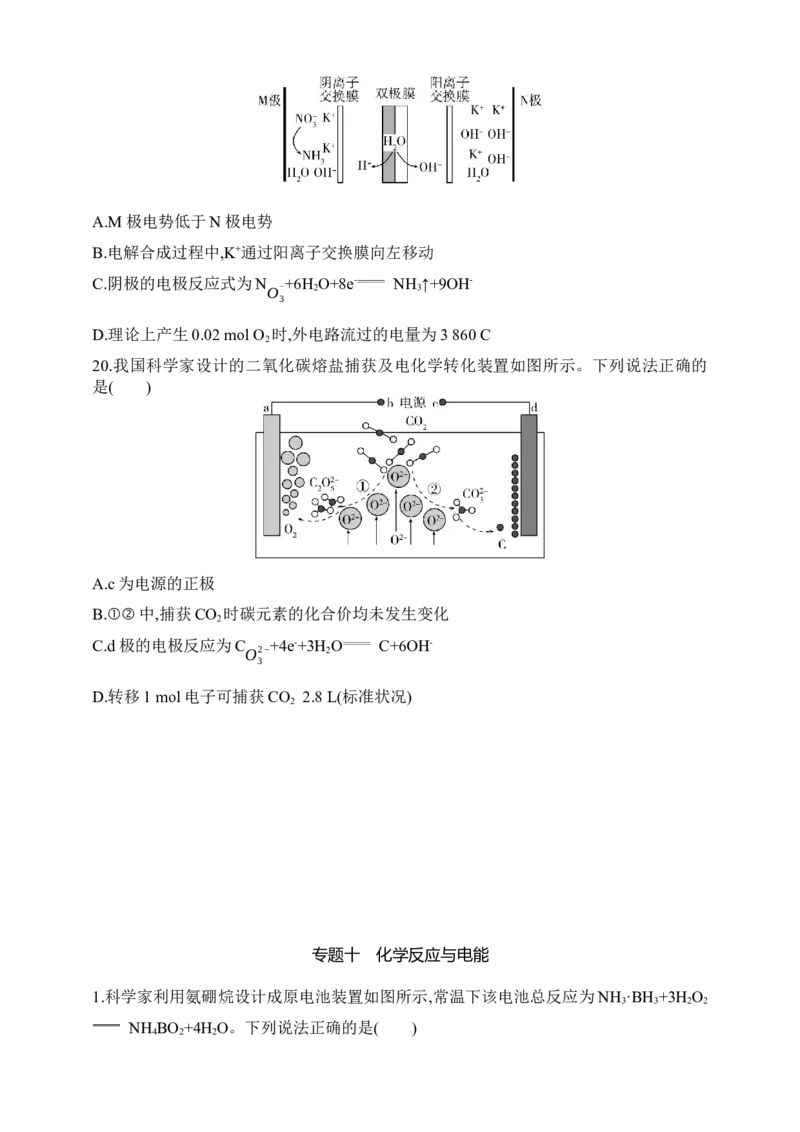
16.工业上可利用电化学原理实现水煤气中 CO 的再利用。如图装置可将 CO 催化还原
2 2
为C H 。下列说法正确的是( )
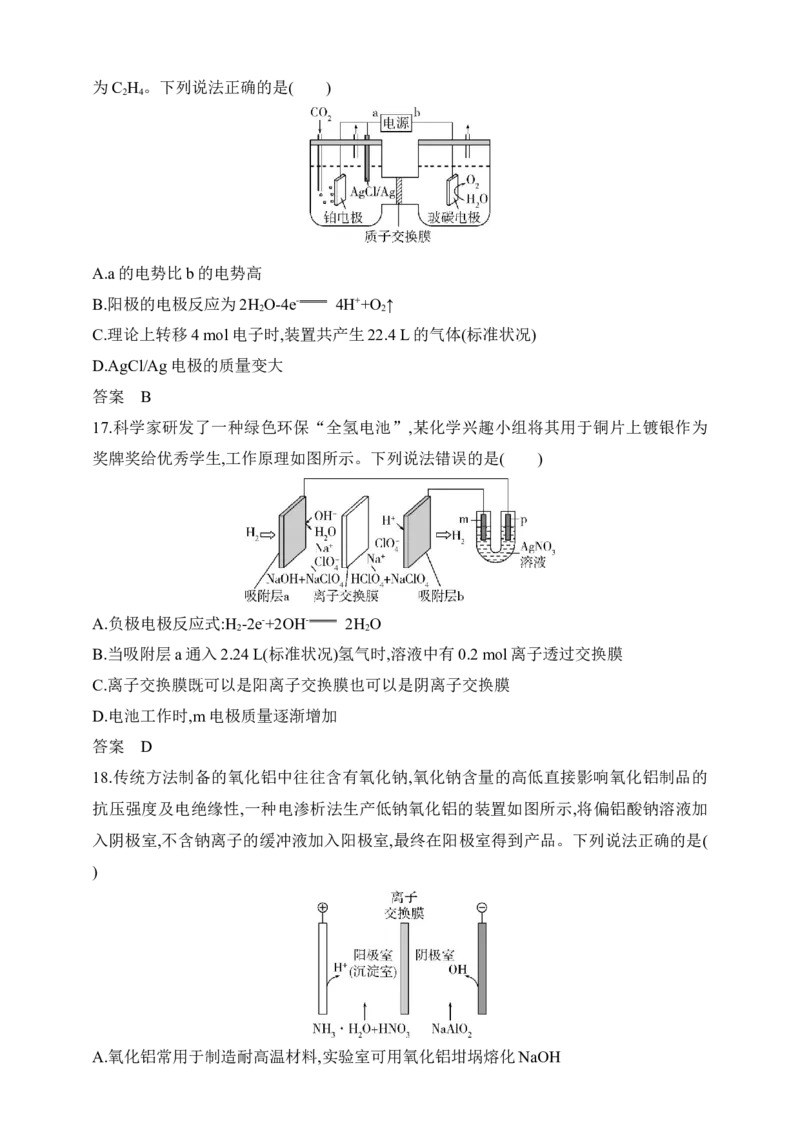
2 4A.a的电势比b的电势高
B.阳极的电极反应为2H O-4e- 4H++O ↑
2 2
C.理论上转移4 mol电子时,装置共产生22.4 L的气体(标准状况)
D.AgCl/Ag电极的质量变大
17.科学家研发了一种绿色环保“全氢电池”,某化学兴趣小组将其用于铜片上镀银作为
奖牌奖给优秀学生,工作原理如图所示。下列说法错误的是( )
A.负极电极反应式:H -2e-+2OH- 2H O
2 2
B.当吸附层a通入2.24 L(标准状况)氢气时,溶液中有0.2 mol离子透过交换膜
C.离子交换膜既可以是阳离子交换膜也可以是阴离子交换膜
D.电池工作时,m电极质量逐渐增加
18.传统方法制备的氧化铝中往往含有氧化钠,氧化钠含量的高低直接影响氧化铝制品的
抗压强度及电绝缘性,一种电渗析法生产低钠氧化铝的装置如图所示,将偏铝酸钠溶液加
入阴极室,不含钠离子的缓冲液加入阳极室,最终在阳极室得到产品。下列说法正确的是(
)
A.氧化铝常用于制造耐高温材料,实验室可用氧化铝坩埚熔化NaOH
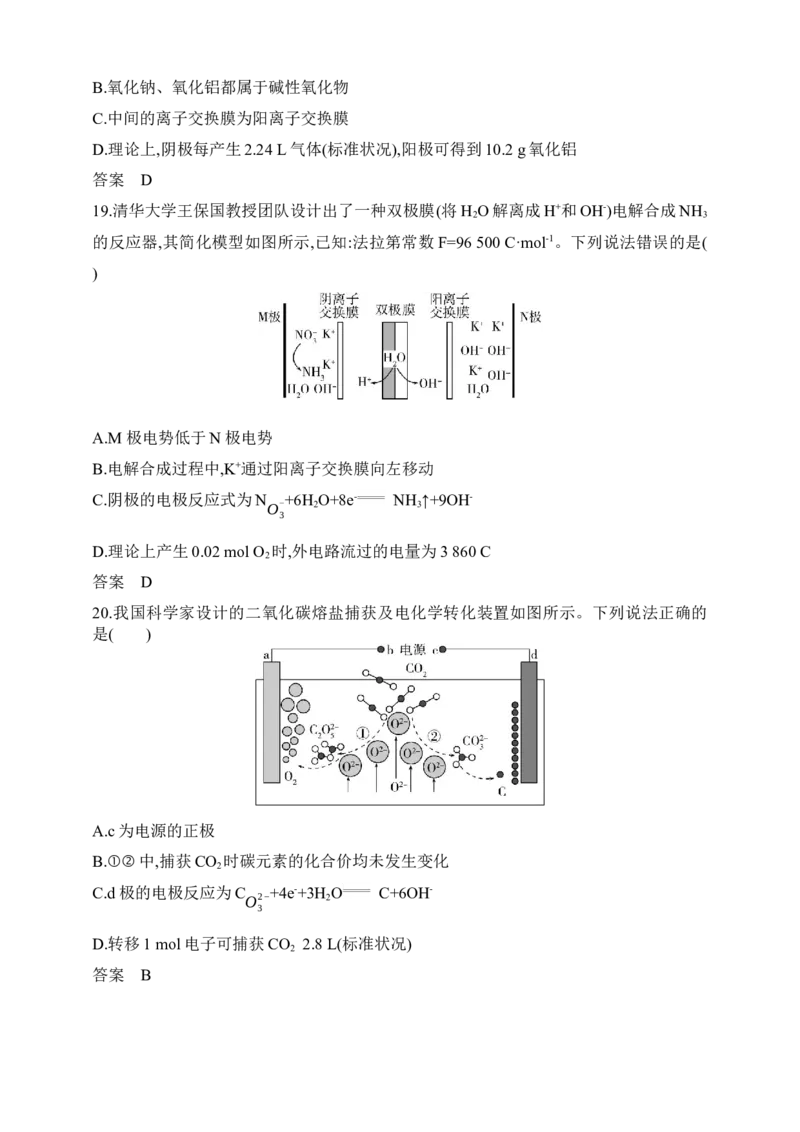
B.氧化钠、氧化铝都属于碱性氧化物
C.中间的离子交换膜为阳离子交换膜
D.理论上,阴极每产生2.24 L气体(标准状况),阳极可得到10.2 g氧化铝
19.清华大学王保国教授团队设计出了一种双极膜(将H O解离成H+和OH-)电解合成NH
2 3
的反应器,其简化模型如图所示,已知:法拉第常数F=96 500 C·mol-1。下列说法错误的是(
)A.M极电势低于N极电势
B.电解合成过程中,K+通过阳离子交换膜向左移动
C.阴极的电极反应式为N +6H O+8e- NH ↑+9OH-
O- 2 3
3
D.理论上产生0.02 mol O 时,外电路流过的电量为3 860 C
2
20.我国科学家设计的二氧化碳熔盐捕获及电化学转化装置如图所示。下列说法正确的
是( )
A.c为电源的正极
B.①②中,捕获CO 时碳元素的化合价均未发生变化
2
C.d极的电极反应为C +4e-+3H O C+6OH-
O2− 2
3
D.转移1 mol电子可捕获CO 2.8 L(标准状况)
2
专题十 化学反应与电能
1.科学家利用氨硼烷设计成原电池装置如图所示,常温下该电池总反应为NH ·BH +3H O
3 3 2 2
NH BO +4H O。下列说法正确的是( )
4 2 2A.b室为该原电池的负极区
B.放电过程中,H+通过质子交换膜由b室移向a室
C.a室的电极反应式为NH ·BH +2H O-6e- N +B +6H+
3 3 2 H+ O-
4 2
D.其他条件不变时,向H O 溶液中加入适量NaOH溶液能增大电流强度
2 2
答案 C
2.一种将CO 催化转化为C H 的电化学装置如图所示。下列说法正确的是( )
2 2 4
A.该装置工作过程中化学能转化为电能
B.铂电极发生的反应为2CO +12H+-12e- C H +4H O
2 2 4 2
C.工作过程中玻碳电极区溶液的pH增大
D.每产生标准状况下11.2 L O 时,理论上有2 mol H+通过质子交换膜
2
答案 D
3.用电解法对酸性含氯氨氮废水进行无害化处理的过程如图所示。下列说法正确的是(
)
A.DSA电极与外接电源的负极连接
B.Cl-发生的电极反应为Cl-+H O-2e- ClO-+2H+
2
C.降解过程中应该控制条件避免发生反应②
D.1 mol HO·和足量NH 反应,转移的电子数为2×6.02×1023
3
答案 Ci
4.某过渡金属(M)—锂离子电池的结构如图所示,总反应式为 Li C +Li MO L x-1
x n y 2
C +Li MO ,下列说法不正确的是( )
n y+1 2
A.放电时电子从C 流入Al,还原电极B中的金属元素M
n
B.充电时B电极的电极反应式为Li MO -e- Li MO +Li+
y+1 2 y 2
C.电解质不能用水,但可用离子液体
D.当Li+移向电极A时,化学能转化为电能
答案 D
5.如图甲、乙两个装置相连,甲池是一种常见的氢氧燃料电池装置,乙池内,D中通入10
mol混合气体,其中苯的物质的量分数为20%(其余气体不参与反应),一段时间后,C处出来
的气体中含苯的物质的量分数为10%(不含H ,该条件下苯、环己烷都为气态),下列说法
2
不正确的是( )
A.甲池中A处通入O ,乙池中E处有O 放出
2 2
B.甲池中H+由G极移向F极,乙池中H+由多孔性惰性电极移向惰性电极
C.导线中共传导12 mol电子
D.乙池中左侧惰性电极上发生反应:C H +6H++6e- C H
6 6 6 12
答案 C
6.某课题组以纳米Fe O 作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材
2 3
料),通过在室温条件下对锂离子电池进行循环充放电,成功实现对磁性的可逆调控(见下
图),下列说法不正确的是( )A.充电时,Fe O 对应电极连接充电电源的负极
2 3
B.该电池的正极的电极反应式:Fe O +6Li++6e- 3Li O+2Fe
2 3 2
C.该电池不能使用氢氧化钠溶液作为电解液
D.该电池工作的原理:放电时,Fe O 作为电池正极被还原为Fe,电池被磁铁吸引
2 3
答案 A
7.电解法制取Na FeO 的总反应为Fe+2H O+2OH- FeO2−+3H ↑,工作原理如图所示。
2 4 2 2
4
已知:Na FeO 只在强碱性条件下稳定,易被H 还原。下列叙述正确的是( )
2 4 2
A.铁电极作阳极,发生还原反应
B.Ni电极上发生还原反应,有H 生成
2
C.该离子交换膜为阳离子交换膜
D.当电路中通过1 mol电子时,阴极区有11.2 L H 生成
2
答案 B
8.中性Zn/Fe液流电池由于安全、稳定、电解液成本低、容量高、使用领域广﹑循环使
用寿命长等优点成为电化学储能热点技术之一。该电池的结构及工作原理如图所示。下
列说法正确的是( )
A.放电时,负极区离子数目增多
B.充电时,电极Y连电源负极
C.放电时,当电极X减少6.5 g时,溶液中有0.2 mol K+从电极X区通过离子交换膜进入电
极Y区D.充电时,阳极电极反应式为Fe(CN -e- Fe(CN
)3− )4−
6 6
答案 C
9.科学家研发了一种以 Al和Pd@石墨烯为电极的Al-N 电池,电池以AlC 离子
2 l-−Al2Cl-
4 7
液体作电解质,放电时在提供能量的同时实现了人工固氮,示意图如下。下列说法不正确
的是( )
A.充电时Al电极是阴极
B.放电时AlC 离子浓度增大,Al C 离子浓度减少
l- 2 l-
4 7
C.放电时正极反应为N +8Al C +6e- 2AlN+14AlC
2 2 l- l-
7 4
D.放电时电路中每通过6 mol e-,电池总质量理论上增加28 g
答案 B
10.间接电解法可对大气污染物NO进行无害化处理,其工作原理如图所示(质子膜只允许
H+通过)。下列有关说法错误的是( )
A.电极b接电源正极,电解过程中附近溶液的pH增大
B.电极a的电极反应式为: +2e-+2H+ S +2H O
2HSO- 2O2− 2
3 4
C.电解过程中右侧Na SO 的浓度增大
2 4
D.电解过程中有4 mol H+通过质子膜时,可处理60 g NO
答案 A
11.以硝酸盐为离子导体的Na-O 电池装置与其某一电极M附近的反应机理如图所示。
2下列说法错误的是( )
A.镍电极上发生还原反应
B.Na O是该过程中的中间产物
2
C.固体电解质能起到隔绝空气的作用
D.M的电极反应为4Na++O +2N +2e- 4NaNO
2 O- 2
3
答案 D
12.地下管道表面附着的硫酸盐会促进钢铁发生厌氧腐蚀,为减少腐蚀的发生,可使钢管与
外接电源相连,使其表面形成致密的Fe O 。下列说法错误的是 ( )
3 4
A.钢管应与电源的负极相连
B.电压过高有可能会加剧腐蚀
C.厌氧腐蚀属于电化学腐蚀
D.厌氧腐蚀过程中有FeS生成
答案 A
13.膜电极反应器具有电阻低、能耗低、结构紧凑等优点,在实际气相反应中具有广阔的
应用前景。因此研究人员设计了一种(碱性)膜电极反应器(如图所示)用于持续制备乙烯,
下列说法中正确的是( )
A.在M极发生的是还原反应,电极反应式为C H +2H O-2e- C H +2OH-
2 2 2 2 4B.C H 和C H 中碳原子的杂化方式相同
2 2 2 4
C.C H 能使溴水和酸性高锰酸钾溶液褪色,且褪色原理相同
2 4
D.该膜电极反应器的总反应为2C H +2H O 2C H +O ↑
2 2 2 2 4 2
答案 D
14.科学工作者提出了一种在室温条件下以 CO 和甲醇为原料合成碳酸二甲酯
2
[(CH O) CO]的电化学方案,其原理如图所示。下列说法中错误的是( )
3 2
A.催化电极b连接电源的正极
B.Br-数目在反应过程中减少了
C.阴极的电极反应为CO +2CH OH+2e- CO+2CH O-+H O
2 3 3 2
D.电路中转移2 mol e-时,理论上会产生90 g碳酸二甲酯
答案 B
15.水系锌离子电池(AZIBs)应用前景广阔。一种AZIBs电池示意图如图所示,钒基氧化物
有利于Zn2+的扩散及嵌入/脱出,常被用做AZIBs正极材料,TMP(磷酸三甲酯)有良好的化
学稳定性和宽的液态温度范围,适合做安全电解液。下列说法错误的是( )
A.在充放电过程中,锌箔侧发生Zn2+与Zn的沉积或溶解
B.充电过程中,Zn2+向V O 侧移动
6 13
C.放电时正极电极反应可能为V O +xZn2++2xe- Zn V O
6 13 x 6 13
D.TMP促进了水系锌离子电池宽温域范围内的应用
答案 B
16.工业上可利用电化学原理实现水煤气中 CO 的再利用。如图装置可将 CO 催化还原
2 2为C H 。下列说法正确的是( )
2 4
A.a的电势比b的电势高
B.阳极的电极反应为2H O-4e- 4H++O ↑
2 2
C.理论上转移4 mol电子时,装置共产生22.4 L的气体(标准状况)
D.AgCl/Ag电极的质量变大
答案 B
17.科学家研发了一种绿色环保“全氢电池”,某化学兴趣小组将其用于铜片上镀银作为
奖牌奖给优秀学生,工作原理如图所示。下列说法错误的是( )
A.负极电极反应式:H -2e-+2OH- 2H O
2 2
B.当吸附层a通入2.24 L(标准状况)氢气时,溶液中有0.2 mol离子透过交换膜
C.离子交换膜既可以是阳离子交换膜也可以是阴离子交换膜
D.电池工作时,m电极质量逐渐增加
答案 D
18.传统方法制备的氧化铝中往往含有氧化钠,氧化钠含量的高低直接影响氧化铝制品的
抗压强度及电绝缘性,一种电渗析法生产低钠氧化铝的装置如图所示,将偏铝酸钠溶液加
入阴极室,不含钠离子的缓冲液加入阳极室,最终在阳极室得到产品。下列说法正确的是(
)
A.氧化铝常用于制造耐高温材料,实验室可用氧化铝坩埚熔化NaOHB.氧化钠、氧化铝都属于碱性氧化物
C.中间的离子交换膜为阳离子交换膜
D.理论上,阴极每产生2.24 L气体(标准状况),阳极可得到10.2 g氧化铝
答案 D
19.清华大学王保国教授团队设计出了一种双极膜(将H O解离成H+和OH-)电解合成NH
2 3
的反应器,其简化模型如图所示,已知:法拉第常数F=96 500 C·mol-1。下列说法错误的是(
)
A.M极电势低于N极电势
B.电解合成过程中,K+通过阳离子交换膜向左移动
C.阴极的电极反应式为N +6H O+8e- NH ↑+9OH-
O- 2 3
3
D.理论上产生0.02 mol O 时,外电路流过的电量为3 860 C
2
答案 D
20.我国科学家设计的二氧化碳熔盐捕获及电化学转化装置如图所示。下列说法正确的
是( )
A.c为电源的正极
B.①②中,捕获CO 时碳元素的化合价均未发生变化
2
C.d极的电极反应为C +4e-+3H O C+6OH-
O2− 2
3
D.转移1 mol电子可捕获CO 2.8 L(标准状况)
2
答案 B