文档内容
专题突破(十五) 分子或离子的空间构型的判断
分子或离子的空间构型的判断是高考命题的重要角度,主要涉及价层电子对互斥理论
及应用(中心原子的价层电子对数、键角的比较、空间构型的判断等)、杂化轨道理论(中心原
子杂化方式的判断、空间构型的判断)等,考查考生进行新颖的推测和设想并周密论证的能力,
考查考生综合运用知识和能力应对复杂问题的水平,要求建立观点、结论和证据之间的逻辑
关系,建立认知模型,并能运用于解释化学现象,揭示现象的本质和规律。
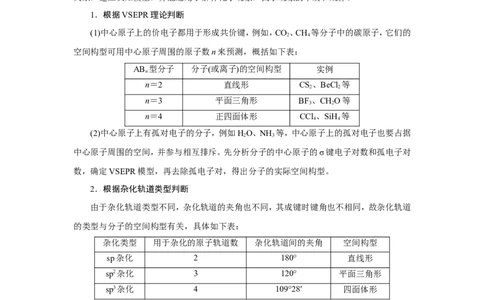
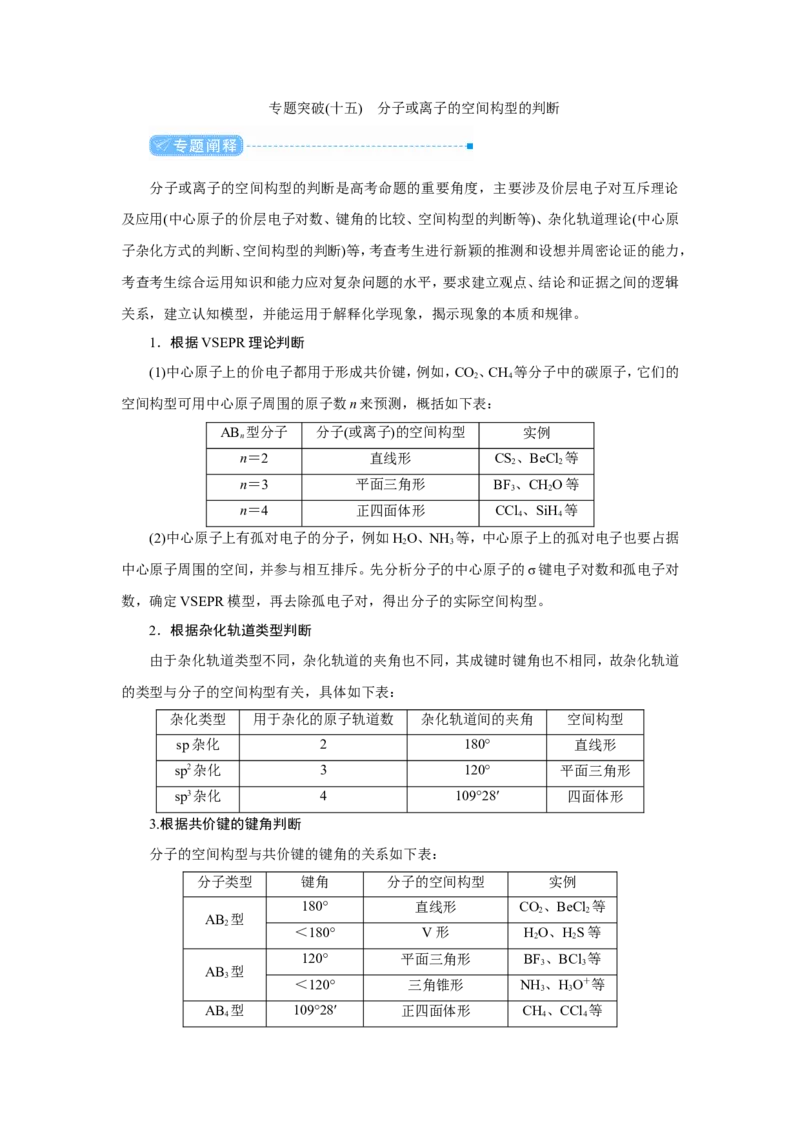
1.根据VSEPR理论判断
(1)中心原子上的价电子都用于形成共价键,例如,CO、CH 等分子中的碳原子,它们的
2 4
空间构型可用中心原子周围的原子数n来预测,概括如下表:
AB 型分子 分子(或离子)的空间构型 实例
n
n=2 直线形 CS、BeCl 等
2 2
n=3 平面三角形 BF、CHO等
3 2
n=4 正四面体形 CCl 、SiH 等
4 4
(2)中心原子上有孤对电子的分子,例如HO、NH 等,中心原子上的孤对电子也要占据
2 3
中心原子周围的空间,并参与相互排斥。先分析分子的中心原子的σ键电子对数和孤电子对
数,确定VSEPR模型,再去除孤电子对,得出分子的实际空间构型。
2.根据杂化轨道类型判断
由于杂化轨道类型不同,杂化轨道的夹角也不同,其成键时键角也不相同,故杂化轨道
的类型与分子的空间构型有关,具体如下表:
杂化类型 用于杂化的原子轨道数 杂化轨道间的夹角 空间构型
sp杂化 2 180° 直线形
sp2杂化 3 120° 平面三角形
sp3杂化 4 109°28′ 四面体形
3.根据共价键的键角判断
分子的空间构型与共价键的键角的关系如下表:
分子类型 键角 分子的空间构型 实例
180° 直线形 CO、BeCl 等
2 2
AB 型
2
<180° V形 HO、HS等
2 2
120° 平面三角形 BF、BCl 等
3 3
AB 型
3
<120° 三角锥形 NH 、HO+等
3 3
AB 型 109°28′ 正四面体形 CH、CCl 等
4 4 44.根据等电子体原理判断
通常情况下,等电子体的空间构型相同,例如,SO 与O 均为V形结构,CH 与NH均为
2 3 4
正四面体形结构。
(2019·海南卷,19Ⅱ题节选)锰单质及其化合物应用十分广泛。回答下列问题:
(1)Mn位于元素周期表中第四周期________族,基态Mn原子核外未成对电子有____个。
(2)MnCl 可与NH 反应生成[Mn(NH)]Cl ,新生成的化学键为______键。NH 分子的空
2 3 3 6 2 3
间构型为_____________________________________________________________,
其中N原子的杂化轨道类型为________。
解析 (1)基态Mn原子核外有25个电子,其电子排布式为[Ar]3d54s2,原子核外未成对
电子有5个,则Mn元素处于周期表的第四周期第ⅦB族。
(2)NH 分子中N原子形成3个σ键,且含有1对孤电子对,则N原子的杂化轨道类型为
3
sp3杂化,NH 的空间构型为三角锥形。
3
答案 (1)ⅦB 5 (2)配位 三角锥形 sp3
(2018·海南卷,19Ⅱ节选)黄铜矿是主要的炼铜原料,CuFeS 是其中铜的主要存在
2
形式。回答下列问题:
(1)在较低温度下CuFeS 与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
2
①X分子的立体构型是________,中心原子杂化类型为________,属于________(填
“极性”或“非极性”)分子。
②X的沸点比水低的主要原因是________________________。
(2)CuFeS 与氧气反应生成SO ,SO 中心原子的价层电子对数为______,共价键的类型
2 2 2
有________。
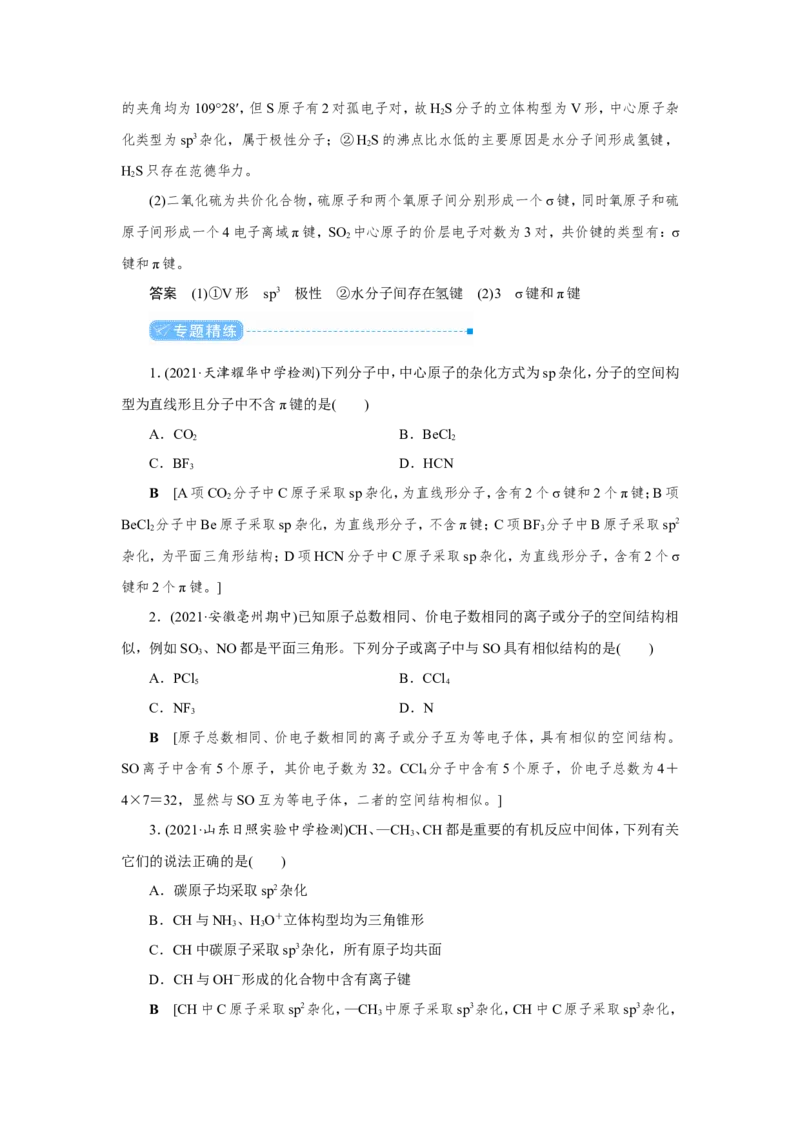
解析 (1)①HS分子中,价层电子对为4对,VSEPR模型为四面体形,价层电子对之间
2的夹角均为109°28′,但S原子有2对孤电子对,故HS分子的立体构型为V形,中心原子杂
2
化类型为sp3杂化,属于极性分子;②HS的沸点比水低的主要原因是水分子间形成氢键,
2
HS只存在范德华力。
2
(2)二氧化硫为共价化合物,硫原子和两个氧原子间分别形成一个σ键,同时氧原子和硫
原子间形成一个4电子离域π键,SO 中心原子的价层电子对数为3对,共价键的类型有:σ
2
键和π键。
答案 (1)①V形 sp3 极性 ②水分子间存在氢键 (2)3 σ键和π键
1.(2021·天津耀华中学检测)下列分子中,中心原子的杂化方式为sp杂化,分子的空间构
型为直线形且分子中不含π键的是( )
A.CO B.BeCl
2 2
C.BF D.HCN
3
B [A项CO 分子中C原子采取sp杂化,为直线形分子,含有2个σ键和2个π键;B项
2
BeCl 分子中Be原子采取sp杂化,为直线形分子,不含π键;C项BF 分子中B原子采取sp2
2 3
杂化,为平面三角形结构;D项HCN分子中C原子采取sp杂化,为直线形分子,含有2个σ
键和2个π键。]
2.(2021·安徽亳州期中)已知原子总数相同、价电子数相同的离子或分子的空间结构相
似,例如SO 、NO都是平面三角形。下列分子或离子中与SO具有相似结构的是( )
3
A.PCl B.CCl
5 4
C.NF D.N
3
B [原子总数相同、价电子数相同的离子或分子互为等电子体,具有相似的空间结构。
SO离子中含有5个原子,其价电子数为32。CCl 分子中含有5个原子,价电子总数为4+
4
4×7=32,显然与SO互为等电子体,二者的空间结构相似。]
3.(2021·山东日照实验中学检测)CH、—CH、CH都是重要的有机反应中间体,下列有关
3
它们的说法正确的是( )
A.碳原子均采取sp2杂化
B.CH与NH 、HO+立体构型均为三角锥形
3 3
C.CH中碳原子采取sp3杂化,所有原子均共面
D.CH与OH-形成的化合物中含有离子键
B [CH中C原子采取sp2杂化,—CH 中原子采取sp3杂化,CH中C原子采取sp3杂化,
3A错误;三者均为三角锥形结构,B正确;CH中C的价层电子对数为3,为sp2杂化,微粒立体
构型为平面三角形,C错误;CHOH中不含离子键,D错误。]
3
4.(2021·天津塘沽一中检测)芦笋中的天冬酰胺(结构如下图)和微量元素硒、铬、锰等,具
有提高身体免疫力的功效。
(1)天冬酰胺所含元素中,____________(填元素名称)元素基态原子核外未成对电子数最
多。
(2)天冬酰胺中碳原子的杂化轨道类型有________种。
(3)H S和HSe的参数对比见下表。
2 2
化学式 键长/nm 键角 沸点/℃
HS 1.34 92.3° -60.75
2
HSe 1.47 91.0° -41.50
2
①HSe的晶体类型为________,含有的共价键类型为______________。
2
②HS的键角大于HSe的原因可能为______________________________。
2 2
解析 (3)①HS和HSe的熔、沸点均较低,为分子晶体,不同种元素原子形成的为极性
2 2
键。②S的电负性强于Se,形成的共用电子对斥力大,故HS键角大。
2
答案 (1)氮 (2)2 (3)①分子晶体 极性键 ②S的电负性强于Se,形成的共用电子
对斥力大,键角大