文档内容
专题讲座(二) 整合有效信息书写陌生化学方程
式
第一部分:高考真题感悟
1.(2021·全国·高考真题(节选))碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回
答下列问题:
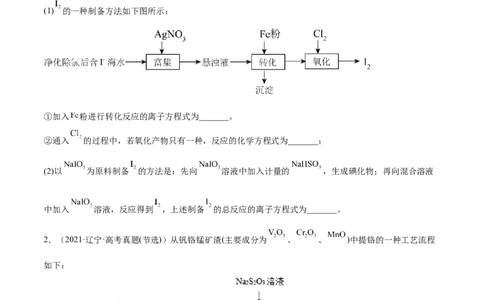
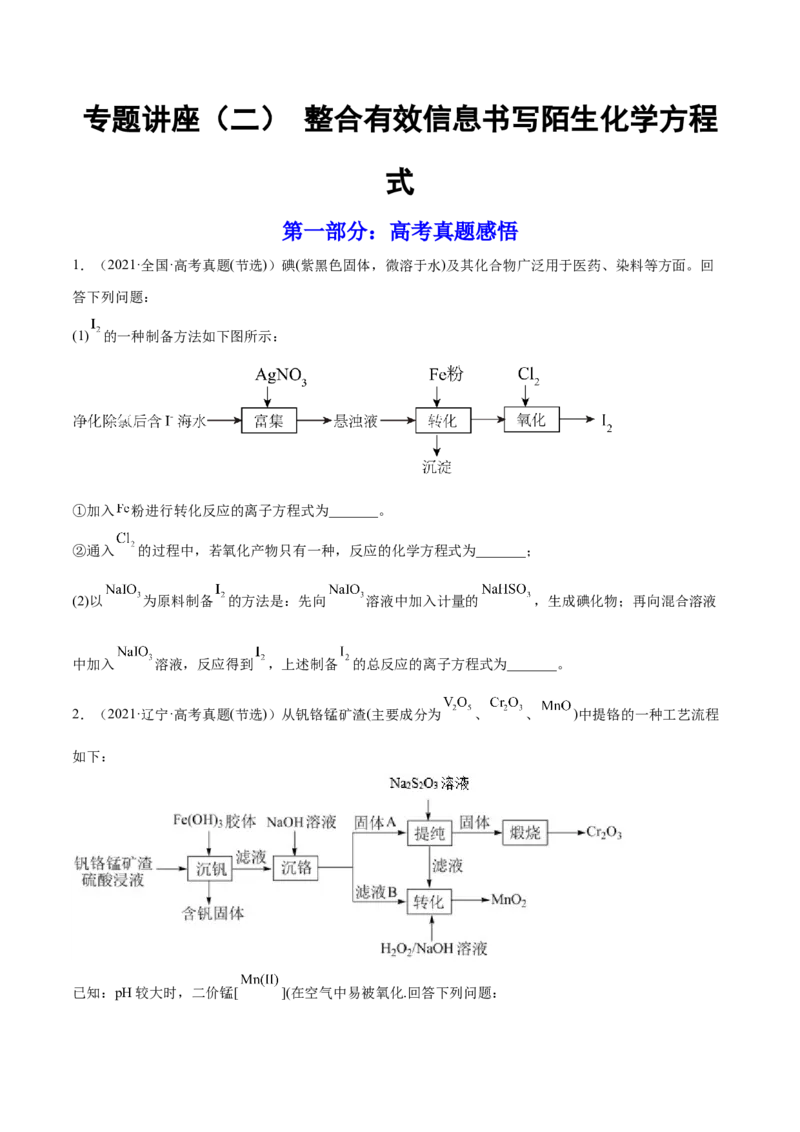
(1) 的一种制备方法如下图所示:
①加入 粉进行转化反应的离子方程式为_______。
②通入 的过程中,若氧化产物只有一种,反应的化学方程式为_______;
(2)以 为原料制备 的方法是:先向 溶液中加入计量的 ,生成碘化物;再向混合溶液
中加入 溶液,反应得到 ,上述制备 的总反应的离子方程式为_______。
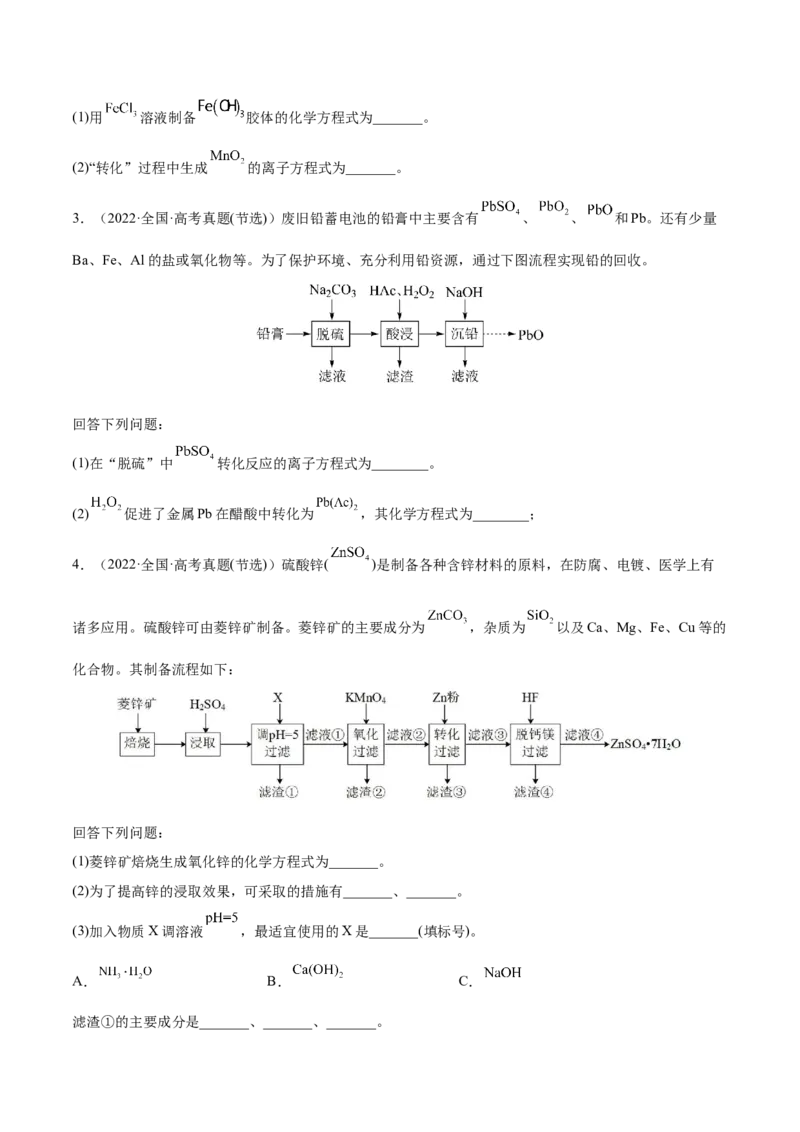
2.(2021·辽宁·高考真题(节选))从钒铬锰矿渣(主要成分为 、 、 )中提铬的一种工艺流程
如下:
已知:pH较大时,二价锰[ ](在空气中易被氧化.回答下列问题:(1)用 溶液制备 胶体的化学方程式为_______。
(2)“转化”过程中生成 的离子方程式为_______。
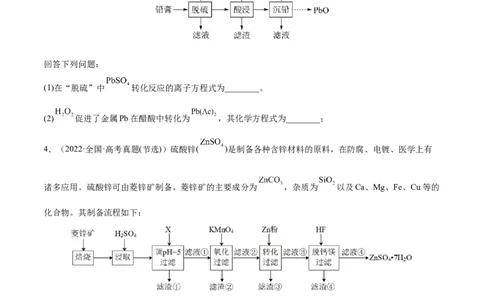
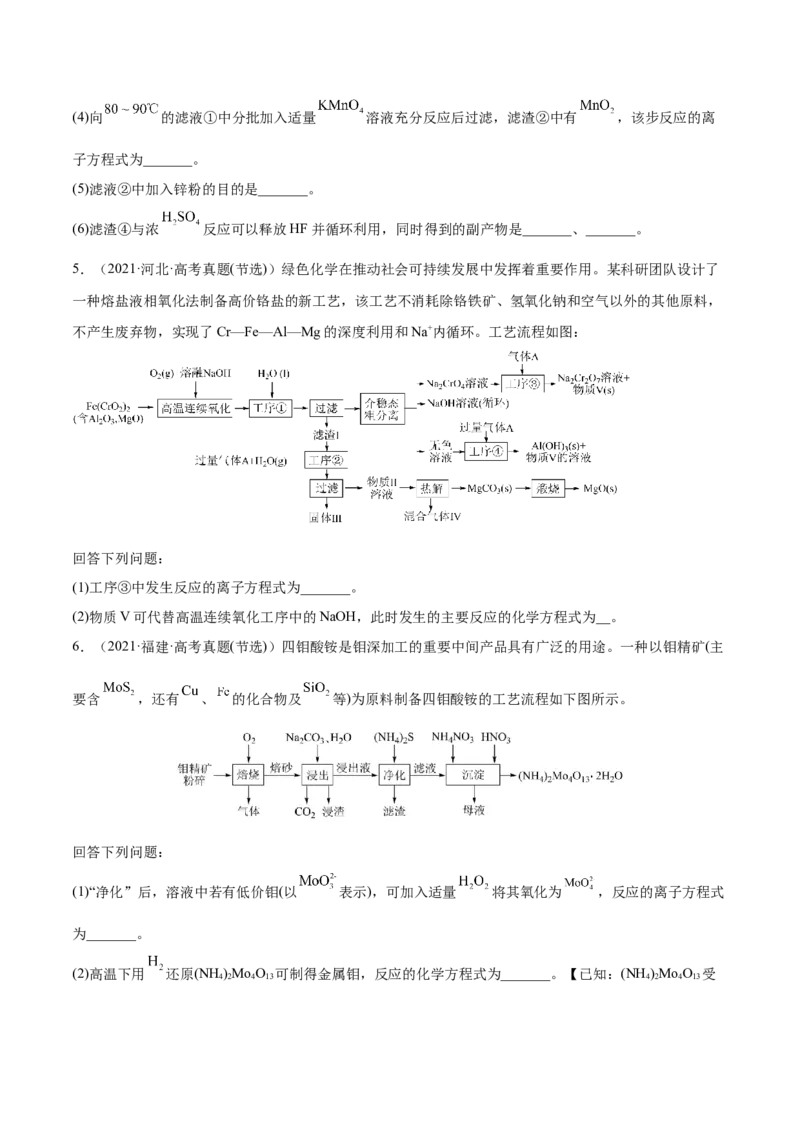
3.(2022·全国·高考真题(节选))废旧铅蓄电池的铅膏中主要含有 、 、 和Pb。还有少量
Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
回答下列问题:
(1)在“脱硫”中 转化反应的离子方程式为________。
(2) 促进了金属Pb在醋酸中转化为 ,其化学方程式为________;
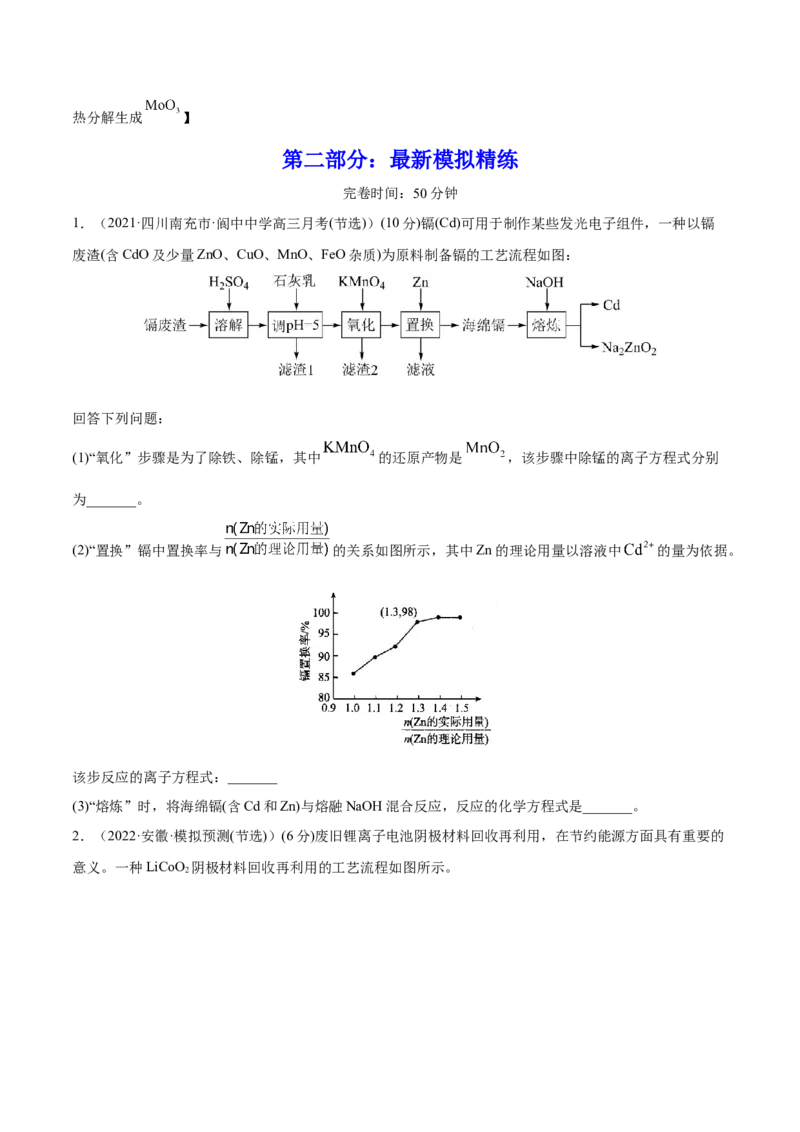
4.(2022·全国·高考真题(节选))硫酸锌( )是制备各种含锌材料的原料,在防腐、电镀、医学上有
诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为 ,杂质为 以及Ca、Mg、Fe、Cu等的
化合物。其制备流程如下:
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。
A. B. C.
滤渣①的主要成分是_______、_______、_______。(4)向 的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有 ,该步反应的离
子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓 反应可以释放HF并循环利用,同时得到的副产物是_______、_______。
5.(2021·河北·高考真题(节选))绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了
一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,
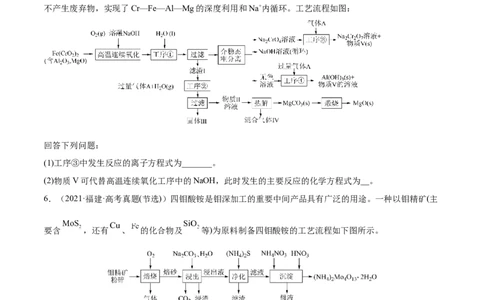
不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
回答下列问题:
(1)工序③中发生反应的离子方程式为_______。
(2)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为__。
6.(2021·福建·高考真题(节选))四钼酸铵是钼深加工的重要中间产品具有广泛的用途。一种以钼精矿(主
要含 ,还有 、 的化合物及 等)为原料制备四钼酸铵的工艺流程如下图所示。
回答下列问题:
(1)“净化”后,溶液中若有低价钼(以 表示),可加入适量 将其氧化为 ,反应的离子方程式
为_______。
(2)高温下用 还原(NH )MoO 可制得金属钼,反应的化学方程式为_______。【已知:(NH )MoO 受
4 2 4 13 4 2 4 13热分解生成 】
第二部分:最新模拟精练
完卷时间:50分钟
1.(2021·四川南充市·阆中中学高三月考(节选))(10分)镉(Cd)可用于制作某些发光电子组件,一种以镉
废渣(含CdO及少量ZnO、CuO、MnO、FeO杂质)为原料制备镉的工艺流程如图:
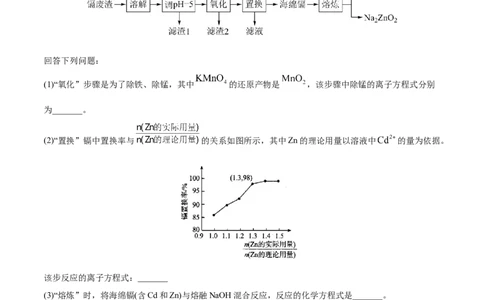
回答下列问题:
(1)“氧化”步骤是为了除铁、除锰,其中 的还原产物是 ,该步骤中除锰的离子方程式分别
为_______。
(2)“置换”镉中置换率与 的关系如图所示,其中Zn的理论用量以溶液中 的量为依据。
该步反应的离子方程式:_______
(3)“熔炼”时,将海绵镉(含Cd和Zn)与熔融NaOH混合反应,反应的化学方程式是_______。
2.(2022·安徽·模拟预测(节选))(6分)废旧锂离子电池阴极材料回收再利用,在节约能源方面具有重要的
意义。一种LiCoO 阴极材料回收再利用的工艺流程如图所示。
2回答下列问题:
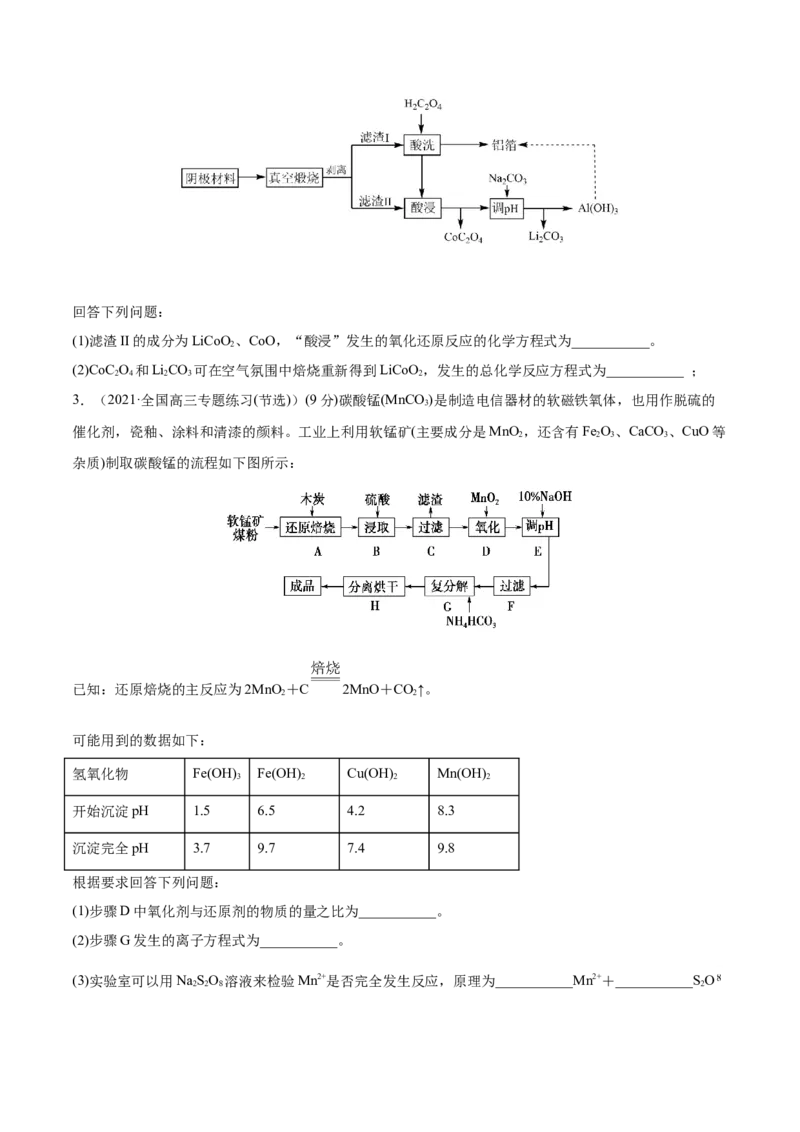
(1)滤渣II的成分为LiCoO 、CoO,“酸浸”发生的氧化还原反应的化学方程式为___________。
2
(2)CoC O 和LiCO 可在空气氛围中焙烧重新得到LiCoO ,发生的总化学反应方程式为___________ ;
2 4 2 3 2
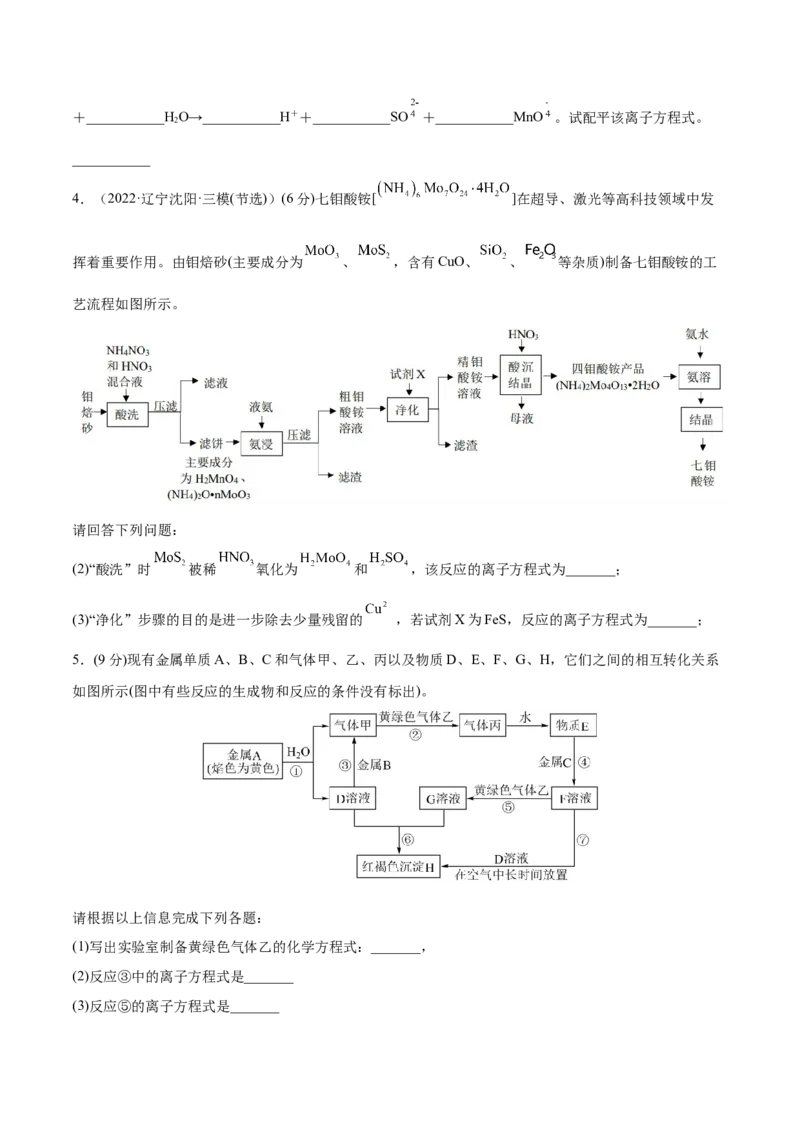
3.(2021·全国高三专题练习(节选))(9分)碳酸锰(MnCO )是制造电信器材的软磁铁氧体,也用作脱硫的
3
催化剂,瓷釉、涂料和清漆的颜料。工业上利用软锰矿(主要成分是MnO ,还含有Fe O、CaCO 、CuO等
2 2 3 3
杂质)制取碳酸锰的流程如下图所示:
已知:还原焙烧的主反应为2MnO +C 2MnO+CO↑。
2 2
可能用到的数据如下:
氢氧化物 Fe(OH) Fe(OH) Cu(OH) Mn(OH)
3 2 2 2
开始沉淀pH 1.5 6.5 4.2 8.3
沉淀完全pH 3.7 9.7 7.4 9.8
根据要求回答下列问题:
(1)步骤D中氧化剂与还原剂的物质的量之比为___________。
(2)步骤G发生的离子方程式为___________。
(3)实验室可以用NaSO 溶液来检验Mn2+是否完全发生反应,原理为___________Mn2++___________SO
2 2 8 2+___________HO→___________H++___________SO +___________MnO 。试配平该离子方程式。
2
___________
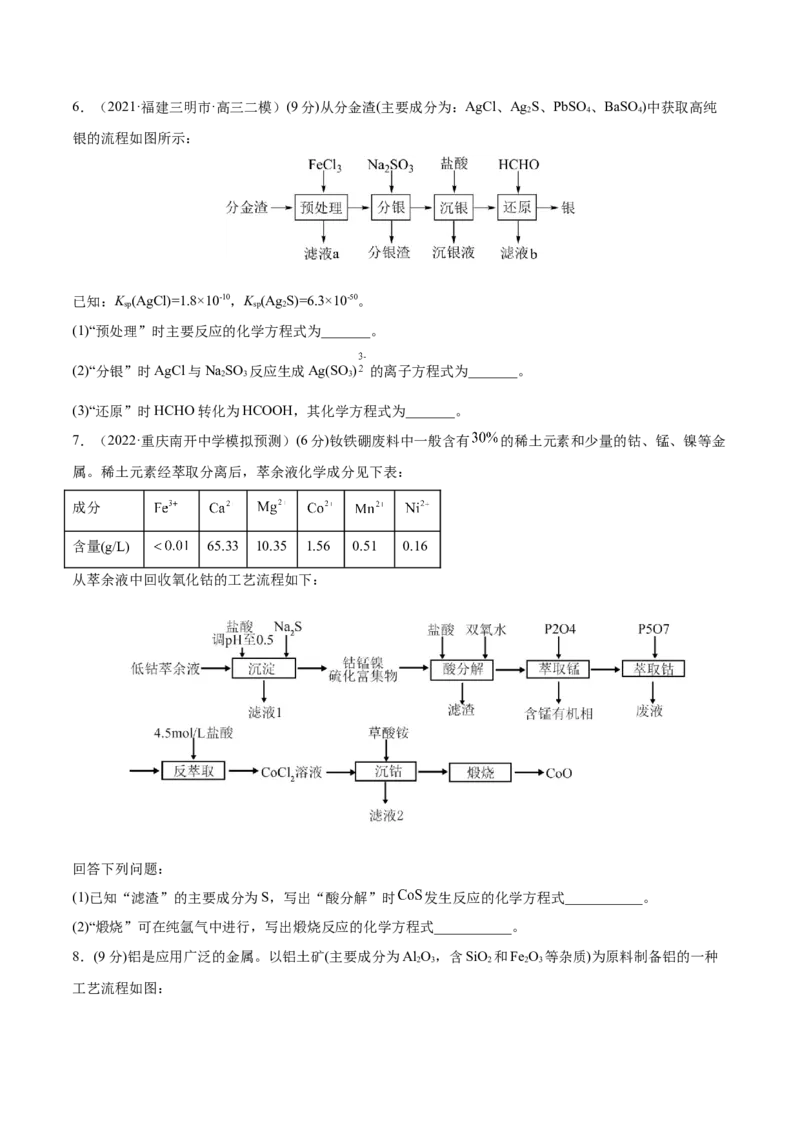
4.(2022·辽宁沈阳·三模(节选))(6分)七钼酸铵[ ]在超导、激光等高科技领域中发
挥着重要作用。由钼焙砂(主要成分为 、 ,含有CuO、 、 等杂质)制备七钼酸铵的工
艺流程如图所示。
请回答下列问题:
(2)“酸洗”时 被稀 氧化为 和 ,该反应的离子方程式为_______;
(3)“净化”步骤的目的是进一步除去少量残留的 ,若试剂X为FeS,反应的离子方程式为_______;
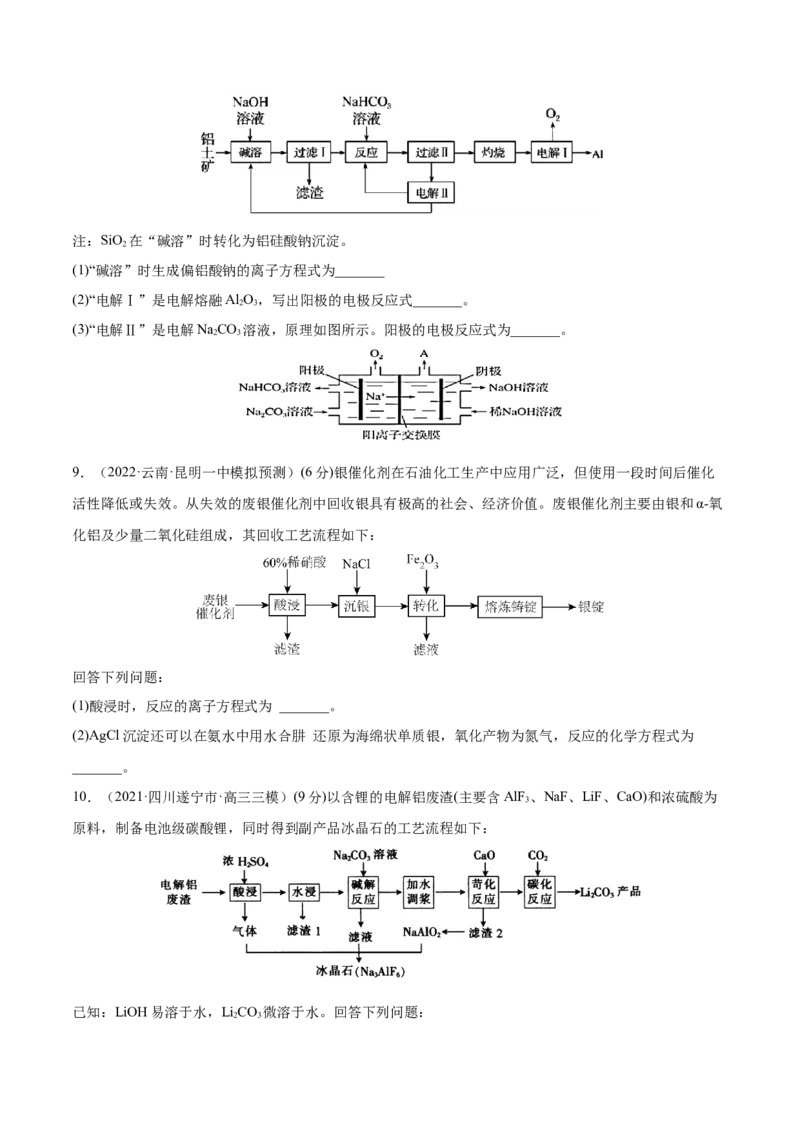
5.(9分)现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系
如图所示(图中有些反应的生成物和反应的条件没有标出)。
请根据以上信息完成下列各题:
(1)写出实验室制备黄绿色气体乙的化学方程式:_______,
(2)反应③中的离子方程式是_______
(3)反应⑤的离子方程式是_______6.(2021·福建三明市·高三二模)(9分)从分金渣(主要成分为:AgCl、Ag S、PbSO 、BaSO)中获取高纯
2 4 4
银的流程如图所示:
已知:K (AgCl)=1.8×10-10,K (Ag S)=6.3×10-50。
sp sp 2
(1)“预处理”时主要反应的化学方程式为_______。
(2)“分银”时AgCl与NaSO 反应生成Ag(SO ) 的离子方程式为_______。
2 3 3
(3)“还原”时HCHO转化为HCOOH,其化学方程式为_______。
7.(2022·重庆南开中学模拟预测)(6分)钕铁硼废料中一般含有 的稀土元素和少量的钴、锰、镍等金
属。稀土元素经萃取分离后,萃余液化学成分见下表:
成分
含量(g/L) 65.33 10.35 1.56 0.51 0.16
从萃余液中回收氧化钴的工艺流程如下:
回答下列问题:
(1)已知“滤渣”的主要成分为S,写出“酸分解”时 发生反应的化学方程式___________。
(2)“煅烧”可在纯氩气中进行,写出煅烧反应的化学方程式___________。
8.(9分)铝是应用广泛的金属。以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂质)为原料制备铝的一种
2 3 2 2 3
工艺流程如图:注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
2
(1)“碱溶”时生成偏铝酸钠的离子方程式为_______
(2)“电解Ⅰ”是电解熔融Al O,写出阳极的电极反应式_______。
2 3
(3)“电解Ⅱ”是电解NaCO 溶液,原理如图所示。阳极的电极反应式为_______。
2 3
9.(2022·云南·昆明一中模拟预测)(6分)银催化剂在石油化工生产中应用广泛,但使用一段时间后催化
活性降低或失效。从失效的废银催化剂中回收银具有极高的社会、经济价值。废银催化剂主要由银和α-氧
化铝及少量二氧化硅组成,其回收工艺流程如下:
回答下列问题:
(1)酸浸时,反应的离子方程式为 _______。
(2)AgCl沉淀还可以在氨水中用水合肼 还原为海绵状单质银,氧化产物为氮气,反应的化学方程式为
_______。
10.(2021·四川遂宁市·高三三模)(9分)以含锂的电解铝废渣(主要含AlF、NaF、LiF、CaO)和浓硫酸为
3
原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如下:
已知:LiOH易溶于水,LiCO 微溶于水。回答下列问题:
2 3(1)碱解反应中,同时得到气体和沉淀,反应的离子方程式为___________。
(2)上述流程得到的副产品冰晶石的化学方程式___________
(3)电池级LiCO 可由高纯度LiOH转化而来。将电池级LiCO 和C、FePO 高温下反应,生成LiFePO 和
2 3 2 3 4 4
一种可燃性气体,该反应的化学方程式为___________。
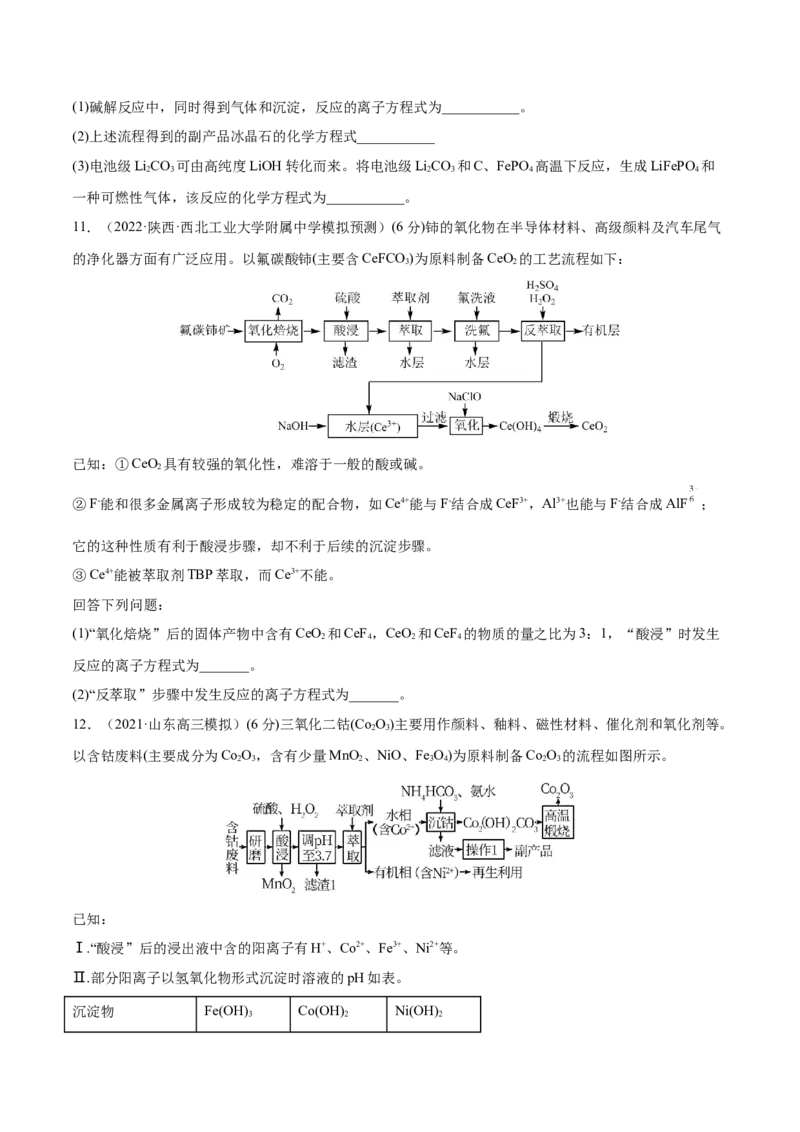
11.(2022·陕西·西北工业大学附属中学模拟预测)(6分)铈的氧化物在半导体材料、高级颜料及汽车尾气
的净化器方面有广泛应用。以氟碳酸铈(主要含CeFCO)为原料制备CeO 的工艺流程如下:
3 2
已知:①CeO 具有较强的氧化性,难溶于一般的酸或碱。
2
②F-能和很多金属离子形成较为稳定的配合物,如Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF ;
它的这种性质有利于酸浸步骤,却不利于后续的沉淀步骤。
③Ce4+能被萃取剂TBP萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”后的固体产物中含有CeO 和CeF ,CeO 和CeF 的物质的量之比为3:1,“酸浸”时发生
2 4 2 4
反应的离子方程式为_______。
(2)“反萃取”步骤中发生反应的离子方程式为_______。
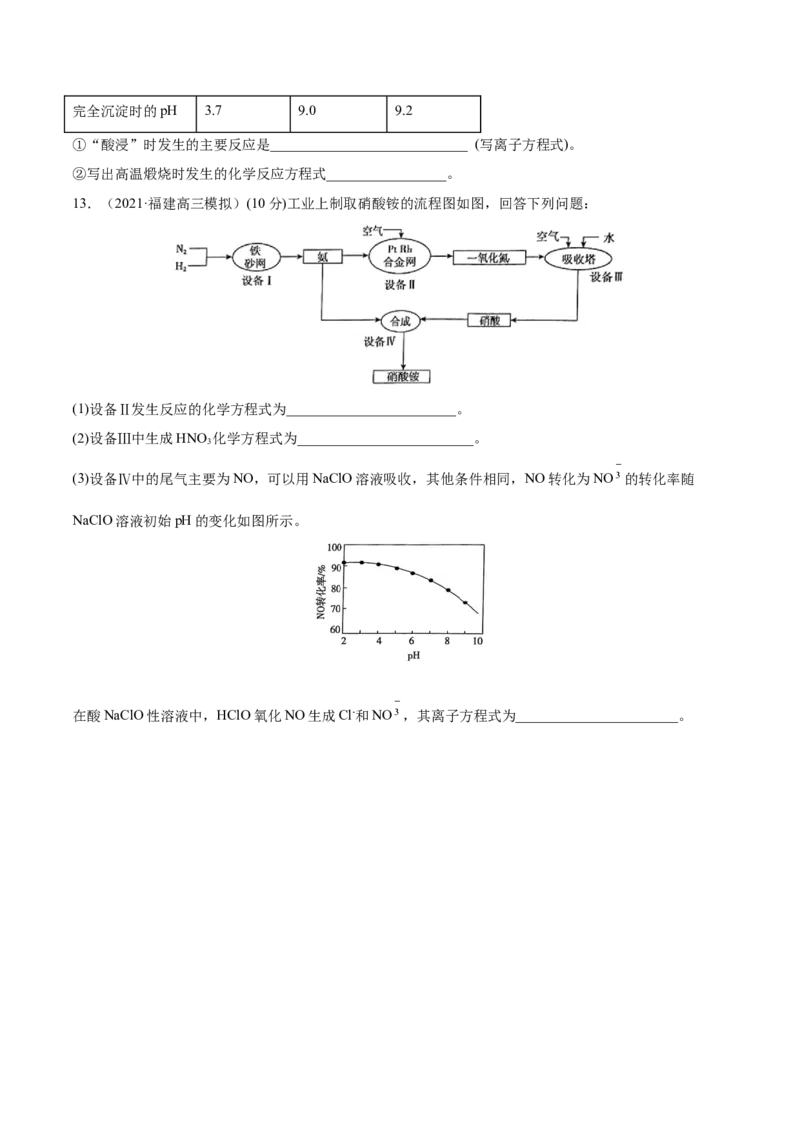
12.(2021·山东高三模拟)(6分)三氧化二钴(Co O)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。
2 3
以含钴废料(主要成分为Co O,含有少量MnO 、NiO、Fe O)为原料制备Co O 的流程如图所示。
2 3 2 3 4 2 3
已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+等。
Ⅱ.部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
沉淀物 Fe(OH) Co(OH) Ni(OH)
3 2 2完全沉淀时的pH 3.7 9.0 9.2
①“酸浸”时发生的主要反应是____________________________ (写离子方程式)。
②写出高温煅烧时发生的化学反应方程式_________________。
13.(2021·福建高三模拟)(10分)工业上制取硝酸铵的流程图如图,回答下列问题:
(1)设备Ⅱ发生反应的化学方程式为________________________。
(2)设备Ⅲ中生成HNO 化学方程式为_________________________。
3
(3)设备Ⅳ中的尾气主要为NO,可以用NaClO溶液吸收,其他条件相同,NO转化为NO 的转化率随
NaClO溶液初始pH的变化如图所示。
在酸NaClO性溶液中,HClO氧化NO生成Cl-和NO ,其离子方程式为_______________________。