文档内容
主题四 化学工艺流程测试(二)
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 K-39 Cr-52 Mn-55
第Ⅰ卷(选择题 共45分)
一、选择题(本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
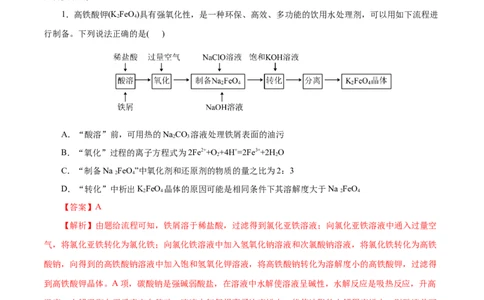
1.高铁酸钾(K FeO)具有强氧化性,是一种环保、高效、多功能的饮用水处理剂,可以用如下流程进
2 4
行制备。下列说法正确的是( )
A.“酸溶”前,可用热的NaCO 溶液处理铁屑表面的油污
2 3
B.“氧化”过程的离子方程式为2Fe2++O +4H+=2Fe3++2H O
2 2
C.“制备Na FeO”中氧化剂和还原剂的物质的量之比为2:3
2 4
D.“转化”中析出KFeO 晶体的原因可能是相同条件下其溶解度大于Na FeO
2 4 2 4
【答案】A
【解析】由题给流程可知,铁屑溶于稀盐酸,过滤得到氯化亚铁溶液;向氯化亚铁溶液中通入过量空
气,将氯化亚铁转化为氯化铁;向氯化铁溶液中加入氢氧化钠溶液和次氯酸钠溶液,将氯化铁转化为高铁
酸钠,向得到的高铁酸钠溶液中加入饱和氢氧化钾溶液,将高铁酸钠转化为溶解度小的高铁酸钾,过滤得
到高铁酸钾晶体。A项,碳酸钠是强碱弱酸盐,在溶液中水解使溶液呈碱性,水解反应是吸热反应,升高
温度,水解平衡向正反应方向移动,溶液中氢氧根离子浓度增大,能使油脂的水解程度增大,则酸溶前可
用热的碳酸钠溶液处理铁屑表面的油污,故A正确;B项,,氧化过程为过量空气将溶液中的氯化亚铁转
化为氯化铁,反应的离子方程式为2Fe2++O +4H+=2Fe3++2H O,故B错误;C项,制备高铁酸钠的反应中,
2 2
氯化铁是反应的还原剂,次氯酸钠是反应的氧化剂,由得失电子数目守恒可知,氧化剂次氯酸钠和还原剂
氯化铁的物质的量之比为3:2,故C错误;D项,转化中发生的反应为向得到的高铁酸钠溶液中加入饱和
氢氧化钾溶液,将高铁酸钠转化为溶解度小的高铁酸钾,故D错误;故选A。
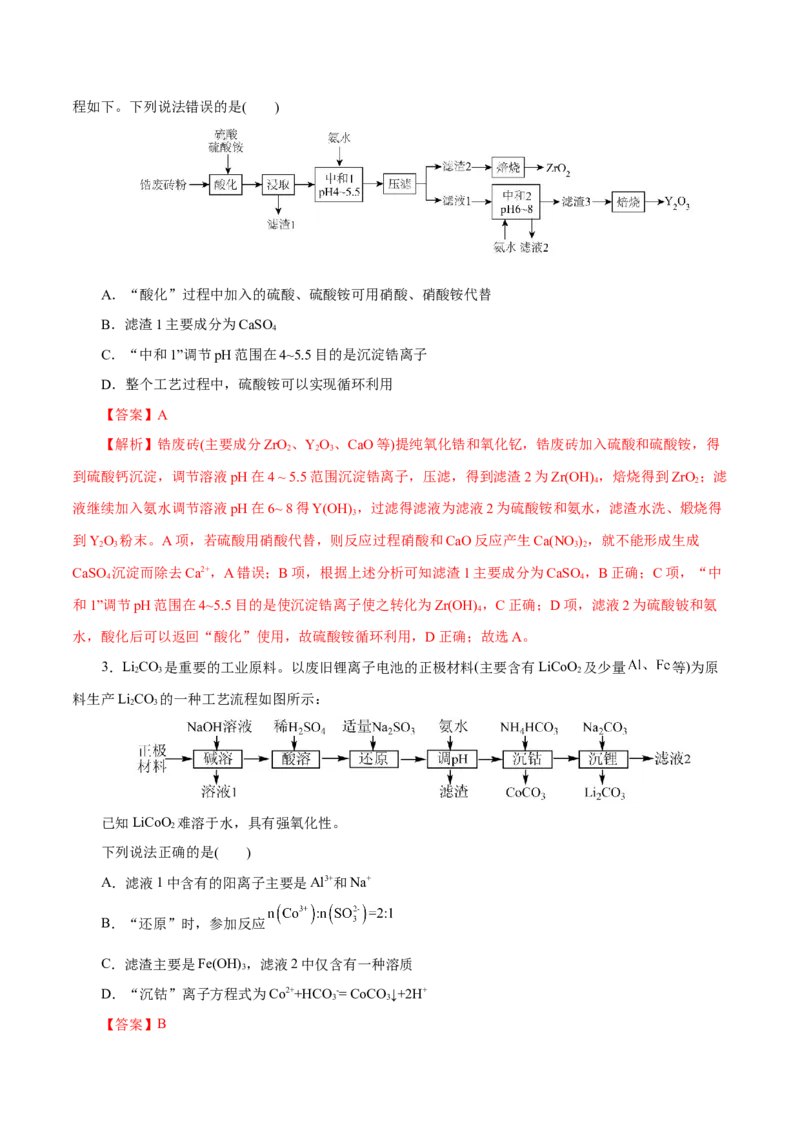
2.一种利用玻璃窑炉替换下的锆废砖(主要成分ZrO、YO、CaO等)提纯成分ZrO 和YO 的工艺流
2 2 3 2 2 3程如下。下列说法错误的是( )
A.“酸化”过程中加入的硫酸、硫酸铵可用硝酸、硝酸铵代替
B.滤渣1主要成分为CaSO
4
C.“中和1”调节pH范围在4~5.5目的是沉淀锆离子
D.整个工艺过程中,硫酸铵可以实现循环利用
【答案】A
【解析】锆废砖(主要成分ZrO、YO、CaO等)提纯氧化锆和氧化钇,锆废砖加入硫酸和硫酸铵,得
2 2 3
到硫酸钙沉淀,调节溶液pH在4 ~ 5.5范围沉淀锆离子,压滤,得到滤渣2为Zr(OH) ,焙烧得到ZrO;滤
4 2
液继续加入氨水调节溶液pH在6~ 8得Y(OH) ,过滤得滤液为滤液2为硫酸铵和氨水,滤渣水洗、煅烧得
3
到YO 粉末。A项,若硫酸用硝酸代替,则反应过程硝酸和CaO反应产生Ca(NO ),就不能形成生成
2 3 3 2
CaSO 沉淀而除去Ca2+,A错误;B项,根据上述分析可知滤渣1主要成分为CaSO,B正确;C项,“中
4 4
和1”调节pH范围在4~5.5目的是使沉淀锆离子使之转化为Zr(OH) ,C正确;D项,滤液2为硫酸铍和氨
4
水,酸化后可以返回“酸化”使用,故硫酸铵循环利用,D正确;故选A。
3.LiCO 是重要的工业原料。以废旧锂离子电池的正极材料(主要含有LiCoO 及少量 等)为原
2 3 2
料生产LiCO 的一种工艺流程如图所示:
2 3
已知LiCoO 难溶于水,具有强氧化性。
2
下列说法正确的是( )
A.滤液1中含有的阳离子主要是Al3+和Na+
B.“还原”时,参加反应
C.滤渣主要是Fe(OH) ,滤液2中仅含有一种溶质
3
D.“沉钴”离子方程式为Co2++HCO-= CoCO↓+2H+
3 3
【答案】B【解析】正极材料主要含LiCoO 、Al、Fe,加入NaOH 溶液,Al 与 NaOH 反应生成 NaAlO 溶液,
2 2
Fe不反应,剩余的Fe与 HSO 溶液反应生成Fe2+,LiCoO 与酸反应生成Co3+,Co3+具有氧化性,与
2 4 2
NaSO 反应CoSO 和LiSO ,加入氨水调节pH使Fe2+沉淀,Fe2+和氢氧根离子反应生成氢氧化亚铁沉淀,
2 3 4 2 4
但氢氧化亚铁不稳定易被氧气氧化生成氢氧化铁沉淀,所以废渣的成分是氢氧化铁,加入NH HCO 溶液沉
4 3
钴,得到滤液 Y为 LiSO 溶液,加入NaCO 得到LiCO 沉淀。A项,滤液1中含有的阳离子主要是
4 2 3 2 3
Na+,Al以AlO-的形式存在,A项错误;B项,“还原”时,Co3+具有氧化性,与NaSO 反应CoSO 和
2 2 3 4
LiSO ,反应离子方程式为 ,参加反应 ,B项
2 4
正确;C项,滤渣主要是Fe(OH) ,滤液2中含 ,C项错误;D项,“沉钴”离子方程
3
式为Co2++2HCO-= CoCO↓+H O+CO↑,D项错误;故选B。
3 3 2 2
4.亚铁氰化钾K[Fe(CN) ]是一种黄色颜料。以含铁废水[主要成分为Fe (SO ),含少量NiSO 、
4 6 2 4 3 4
CuSO 等]为原料合成亚铁氰化钾的工艺流程如下:
4
下列说法不正确的是( )
A.“调pH”时选用的试剂X可以是Fe O 或Fe(OH)
2 3 3
B.“还原”后可用KSCN溶液检验Fe3+是否被完全还原
C.“反应”时Fe2+提供孤电子对给予 形成配位健
D.“滤渣Ⅱ”的主要成分是CaCO
3
【答案】C
【解析】含铁废水中的铁为三价铁,加入试剂X调高pH生成氢氧化铁沉淀,过滤后,用硫酸溶解沉
淀,加入单质铁还原三价铁离子,加入氯化钙沉淀硫酸根离子,再用碳酸钠沉淀没有沉淀完的钙离子,过
滤后,加入氯化钾经过转化生成亚铁氰化钾,以此解题。A项,Fe O 或Fe(OH) 可以和氢离子反应从而使
2 3 3
pH升高,且不会引入杂质离子,A正确;B项,Fe3+遇到KSCN溶液会变红色,可以检验Fe3+,B正确;C
项,Fe2+是阳离子,和CN-形成配位键时,Fe2+提供空轨道,CN-提供孤电子对,C错误;D项,碳酸钠中的
碳酸根离子和没有完全沉淀的钙离子生成沉淀碳酸钙,D正确;故选C。
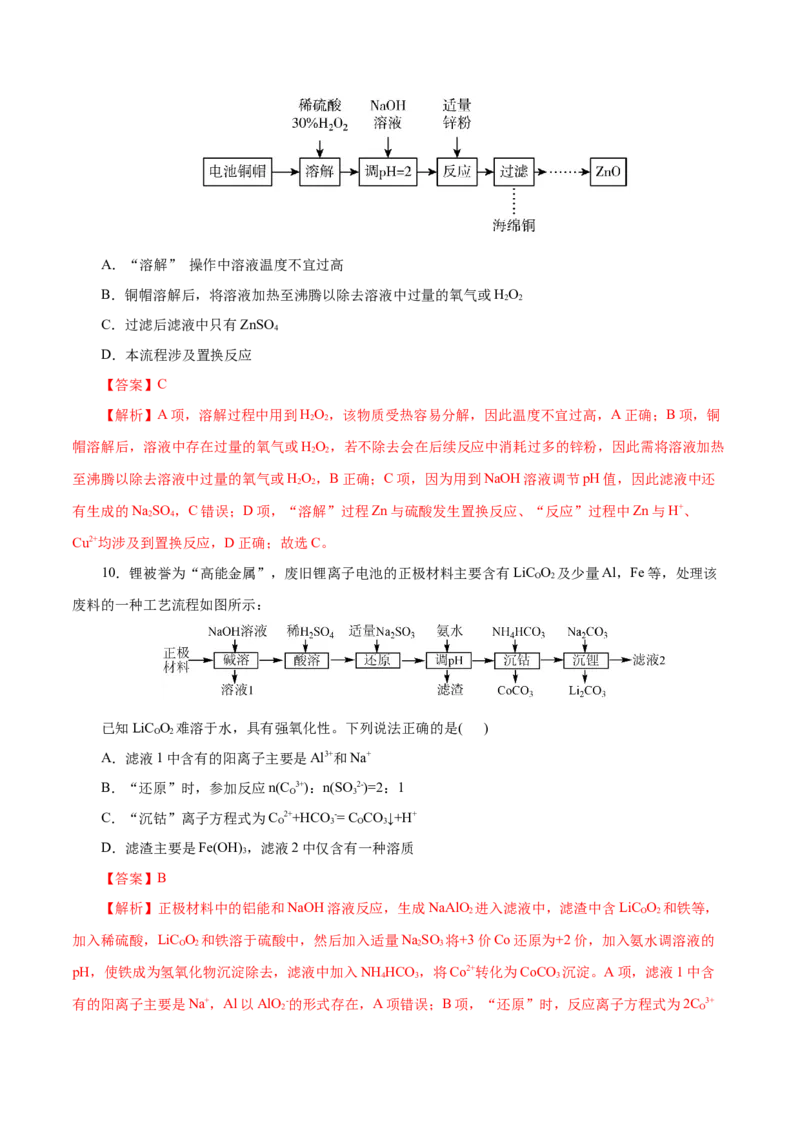
5.黄铜灰渣(含有Cu 、Zn、CuO、ZnO及少量FeO、Fe O)生产硝酸铜溶液的流程如图,下列说法不
2 3
正确的是( )A.“浸取”时适当提高硫酸浓度可加快反应速率
B.若反应中所加Zn过量,所得Cu(NO ) 溶液中含Zn(NO ) 杂质
3 2 3 2
C.滤液II含Zn2+、Fe2+、Fe3+、SO 2-等离子
4
D.由Cu(NO ) 溶液制备Cu(NO )·3H O,采用蒸发结晶的操作
3 2 3 2 2
【答案】C
【解析】黄铜灰渣加硫酸浸取,Zn、ZnO转化为ZnSO,CuO转化为CuSO ,FeO转化为FeSO ,
4 4 4
Fe O 转化为Fe (SO ),过滤得到Cu,向滤液中加入适量的Zn,Zn先和Fe3+反应生成Fe2+,再和Cu2+反应
2 3 2 4 3
生成Cu,向Cu中加入稀硝酸,得到Cu(NO ) 溶液。A项,适当增加反应物浓度可以加快反应速率,A项
3 2
正确;B项,加Zn过量,会导致过滤所得滤渣中含有Zn,硝酸溶解后会在硝酸铜中会有Zn(NO ) 杂质,
3 2
B项正确;C项,由分析可知,向滤液I中加入适量的Zn,Zn先和Fe3+反应生成Fe2+,再和Cu2+反应生成
Cu,故滤液II中不含Fe3+,C项错误;D项,将Cu(NO ) 溶液蒸发结晶,可得到Cu(NO )·3H O,D项正
3 2 3 2 2
确;故选C。
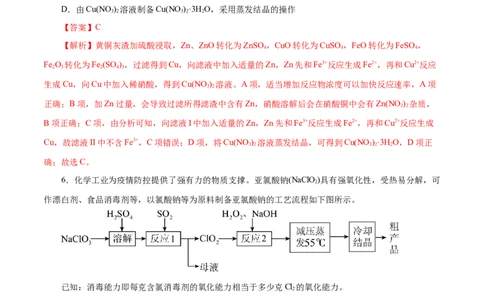
6.化学工业为疫情防控提供了强有力的物质支撑。亚氯酸钠(NaClO )具有强氧化性,受热易分解,可
2
作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如下图所示。
已知:消毒能力即每克含氯消毒剂的氧化能力相当于多少克Cl 的氧化能力。
2
下列说法错误的是( )
A.“母液”中溶质的主要成分是NaSO
2 4
B.相同质量ClO 的消毒能力是Cl 的2.5倍
2 2
C.“反应2”中氧化剂与还原剂的物质的量之比为2∶1
D.“减压蒸发”可以降低蒸发时的温度,提高产品产率
【答案】B
【解析】由题给流程可知,反应1为二氧化硫与稀硫酸、氯酸钠反应生成硫酸钠、二氧化氯和水,反应2为二氧化氯与过氧化氢、氢氧化钠混合溶液反应生成亚氯酸钠、氧气和水,反应得到的亚氯酸钠在
55℃条件下减压蒸发、冷却结晶、过滤得到亚氯酸钠粗产品。A项,根据元素转化分析可知“母液”中溶
质的主要成分是NaSO ,A项正确;B项,1 mol Cl 完全反应转化2 mol e-,1 mol ClO 完全反应转化5
2 4 2 2
mol e-,所以等物质的量ClO 的消毒能力是Cl 的2.5倍,B项错误;C项,“反应2”中发生反应的化学方
2 2
程式为HO+2ClO + 2NaOH=2NaClO +2H O+O↑,氧化剂与还原剂的物质的量之比为2∶1,C项正确;D项,
2 2 2 2 2 2
温度过高,NaClO 会分解,所以采用“减压蒸发”可以降低蒸发时的温度,提高产品产率,D项正确;故
2
选B。
7.生产软磁铁氧体的主要原料是α-FeOOH,以硫铁矿(主要成分是FeS,含少量Al O、SiO 和Fe O)
2 2 3 2 3 4
为原料制备α-FeOOH的工艺流程如下,相关数据见下表。下列说法错误的是 ( )
物质
开始沉淀pH(25℃) 1.9 7.6 4.0
沉淀完全pH(25℃) 3.2 9.7 5.2
A.“焙烧”的产物之一可用于工业制硫酸
B.“试剂a”可以为FeS,主要目的是除去过量硫酸
C.“试剂b”可以为氨水,调pH的范围为5.2~7.6
D.“沉淀”时,pH过高或者过低均不利于生成
【答案】B
【解析】硫铁矿焙烧主要发生的反应方程式为:4FeS+11O 2Fe O+8SO ,然后加入稀硫酸进行
2 2 2 3 2
酸 浸 , 反 应 原 理 有 : Fe O+3H SO =Fe (SO )+3H O 、 Al O+3H SO =Al(SO )+3H O 、
2 3 2 4 2 4 3 2 2 3 2 4 2 4 3 2
Fe O+4H SO =Fe (SO )+4H O+FeSO ,然后过滤得到滤渣A,主要成分为SiO ,试剂a为还原性铁粉,主
3 4 2 4 2 4 3 2 4 2
要目的为将Fe3+转化为Fe2+,便以后续步骤中除去Al3+,过滤得到滤渣B,主要成分为Fe,加入试剂b调节
溶液pH为5.2~7.6将Al3+完全沉淀,而除去过滤得到滤渣C,主要成分为Al(OH) ,向滤液中主要含有
3
Fe2+加入过氧化氢和氨水,产生沉淀FeOOH,过滤得到滤液D,主要成分为(NH )SO 。A项,由分析可知,
4 2 4“焙烧”的产物之一SO ,可以转化为SO ,然后SO +H O=HSO ,故可用于工业制硫酸,A正确;B项,
2 3 3 2 2 4
“试剂a”的主要目的是将Fe3+完全还原为Fe2+,可以为FeS,但主要目的不是除去过量硫酸,B错误;C项,
“试剂b” 的目的为调节溶液pH为5.2~7.6将Al3+完全沉淀,故可以为氨水,C正确;D项,“沉淀”时,
pH过高则溶液中的OH-浓度过大,将生成Fe(OH) 沉淀,pH过低即溶液中H+浓度过大,不利于生成α-
3
FeOOH,D正确;故选B。
8.某新型纳米材料氧缺位铁酸盐ZnFe O(3