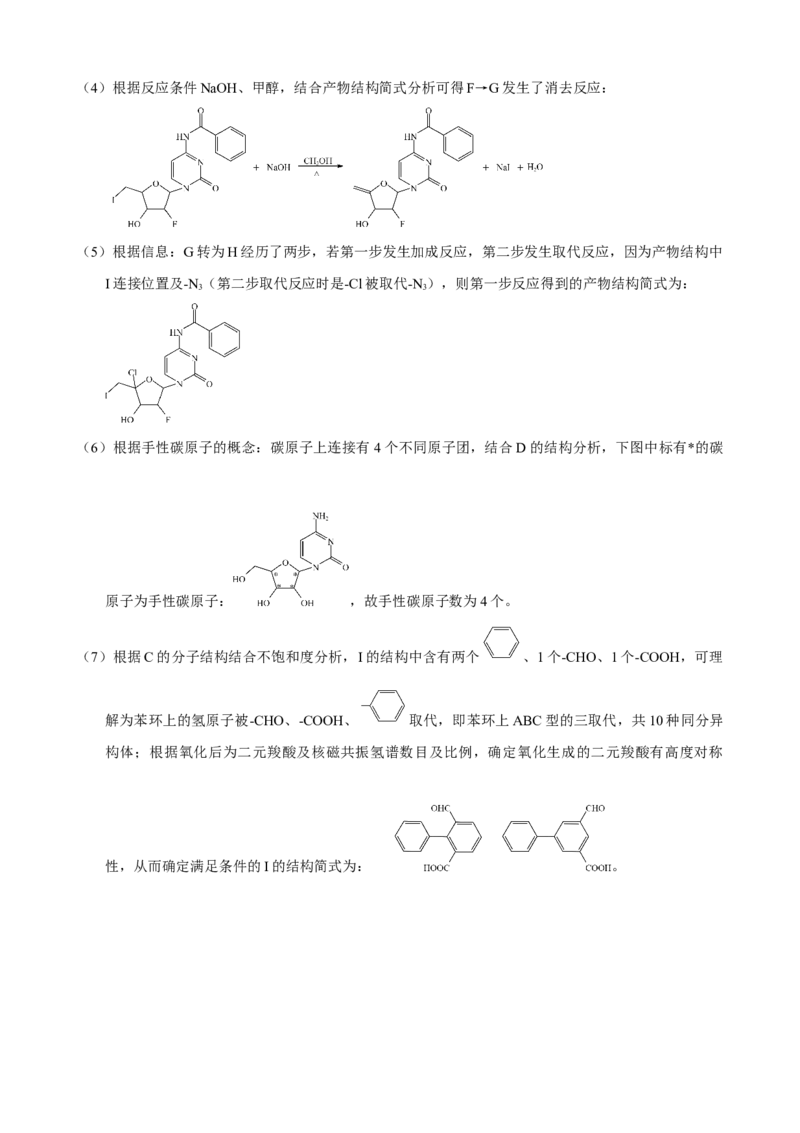文档内容
红河州第一中学 2023 届高三年级第二次联考
化学参考答案
题序 7 8 9 10 11 12 13
答案 A C D B C D C
7.【答案】A
【解析】
A项,现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析,A项正确。
B项,聚丙烯中无碳碳双键不能使溴水褪色,B项错误;
C项,生产计算机芯片使用高纯硅,C项错误;
D项,合金熔点低于成分金属,D项错误;
综上所述,答案为A。
8.【答案】C
【解析】
A项,根据有机物的结构简式可得分子式为C H O ,A项错误;
21 20 11
B项,有机分子结构含有酚羟基和碳碳双键能与Br 反应,1mol该有机物最多消耗5mol Br ,由于
2 2
没有指明该物质的量,故B项错误;
C项,碳原子杂化方式有sp2、sp3 2种,C项正确;
D项,2个苯环上的碳原子可共面,D项错误。
综上所述,答案为C。
9.【答案】D
【解析】
A项,因不知溶液体积,所以无法计算溶液中离子的数目,A项错误;
B项,在含0.1molNaClO的溶液中,无HCl存在,B项错误;
C项,1mol氢氧根所含电子数为10 N ,1mol羟基所含电子数为9 N ,C项错误;
A A
D项,每制得1mol高铁酸钠,转移电子数目为3N ,D项正确。
A
综上所述,答案为D。
10.【答案】B
【解析】
A项,向饱和NaCO 溶液中加入BaSO 固体,溶液中碳酸根离子远远大于硫酸根离子导致沉淀转
2 3 4
化,不能说明BaCO 溶解度大于BaSO,A项错误;
3 4
B项,醛基在碱性条件下可以和新制氢氧化铜悬浊液反应生成砖红色沉淀,若出现砖红色沉淀,则证明有机物含有醛基,B项正确;
C项,加热条件下挥发出的乙醇蒸汽也能使酸性高锰酸钾褪色,无法证明1-溴丁烷中发生消去反应生
成含不饱和键的化合物,应在气体通入酸性高锰酸钾前先通入水,C项错误;
D项,KCr O 具有强氧化性,浓盐酸具有还原性,将KCr O 固体溶于水后加入浓盐酸,两者发生氧
2 2 7 2 2 7
化还原反应生成氯化钾、三氯化铬、氯气和水,无法证明:KCr O 溶液中存在平衡Cr O2-+H O
2 2 7 2 7 2
2CrO2-+2H+,D项错误;
4
综上所述,答案为B。
11.【答案】C
【解析】
A项,碳酸酸性强于苯酚,苯酚钠溶液能够与二氧化碳反应生成苯酚和碳酸氢钠,A项正确;
B项,K (CuS)O>C,A项错误;
B项,NH 能形成分子间氢键,故沸点:NH >CH ,B项错误;
3 3 4
C项,CO 有2个σ键,2个п键,C项错误;
2
D项,最高价含氧酸的酸性:HCO>H SiO,D项正确;
2 3 2 3
综上所述,答案为D。
13.【答案】C
【解析】
A项,放电时,负极的电极反应式为Zn - 2e- = Zn2+,A项正确;
B项, 放电时,Zn2+向正极区移动,B项正确;
C项,充电时,阳极的电极反应式为3I- - 2e- = I-,C项错误;
3
D项,发生反应I+I-=I -,增大单质碘的溶解度,D项正确。
2 3
综上所述,答案为C。
27.(14分,除特殊标注外,每空2分)
(1)S乙>甲(1分) , 正反应为放热反应,升高温度,平衡逆向移动,氨气体积分数减小,
则甲、乙、丙中温度从高到低的顺序是丙>乙>甲(1分)
② b c
60
3.24 2
③57.0%
60 ( × 60 )
8.58
1.29 1.29 3
( × )∙( × )
8.58 8.58
【解析】
(1)①略
②净化干燥是为了防止混有杂质使催化剂“中毒 ”故a错;步骤中“加压”可使平衡正向移动,可提
高原料的转化率,增大压强,可以使反应物浓度增大,则可增大反应速率,故b正确;合成氨一般选择
在400~500℃是因为在此温度下铁触媒的活性最大,不是反应速率最快,故c错;液态NH 用作制冷剂是
3
因为其汽化时吸收大量的热而不是放热,故d错。
(2)化学反应速率快慢取决于慢反应的速率,能量越高反应速率越慢,根据图知,反应速率取决于
*N→*NH。故选B。
2 2
(3)①正反应放热,升高温度,平衡逆向移动,氨气体积分数减小,则甲、乙、丙中温度从高到低的顺
序是丙>乙>甲。
②a.v(NH )=2v(N) 没有同时描述正逆反应,不能判断该反应达到平衡; b.M= ,刚性密闭容器
3 2
内气体质量不变,而反应前后气体物质的量有变化,故M不变,则能判断该反应达到平衡,b正确;
c. 为浓度商不再变化则能判断该反应达到平衡,c正确; d.密闭刚性容器内气体质
量不变,体积不变,密度不会变化,不能判断该反应达到平衡。故选 b c
③ N(g ) + 3H(g) 2NH (g)
2 2 3
初始(mol) 3 9 0
转化(mol) x 3x 2x
平衡(mol) 3-x 9-3x 2x2x 1.71
d点氨气的体积分数为40%, =0.4,x=1.71,d点N 的转化率是 ×100%=57.0%。
12−2x 2 3
平衡常数大小只与温度有关,丙温度的平衡常数可用d点进行计算,d的压强为60Mpa
平衡时:n(总气体)=12mol-2×1.71mol=8.58mol n( N)=1.29mol n( H)= 3.87mol n(
2 2
NH )=3.42mol
3
60
p2 (N H 3 ) 3.24 2
60 ( × 60)
p(N )∙p3 (H ) 8.58
K p = 2 2 = 1.29 1.29 3
( × )∙( × )
8.58 8.58
30.(15分,除特殊标注外,每空2分)
(1)甲苯(1分)
(2)氧化反应(1分) 取代反应(1分)
(3)羟基 醚键 酰胺键(写对2个给2分,有错不给分)
(4) (其他合理答案均给分)
(5)
(6)4
(7)10
【解析】
(1)根据A的分子式C H,结合A→B反应条件及B的结构分析可得A的结构简式为 。即A
7 8
的名称为甲苯。
(2)A→B为甲苯在酸性条件下氧化为苯甲酸,C+D→E的反应结合反应物及生成物结构分析可得,此
反应产生了酰胺键,即发生了取代反应。
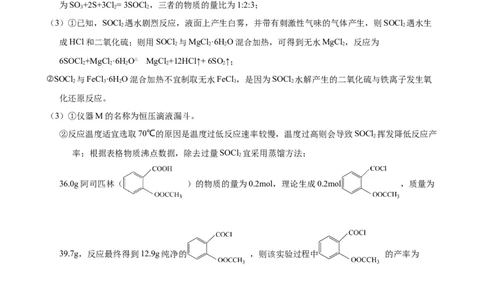
(3)根据E的结构简简式可得分子中的含氧官能团为羟基、醚键、酰胺键。(4)根据反应条件NaOH、甲醇,结合产物结构简式分析可得F→G发生了消去反应:
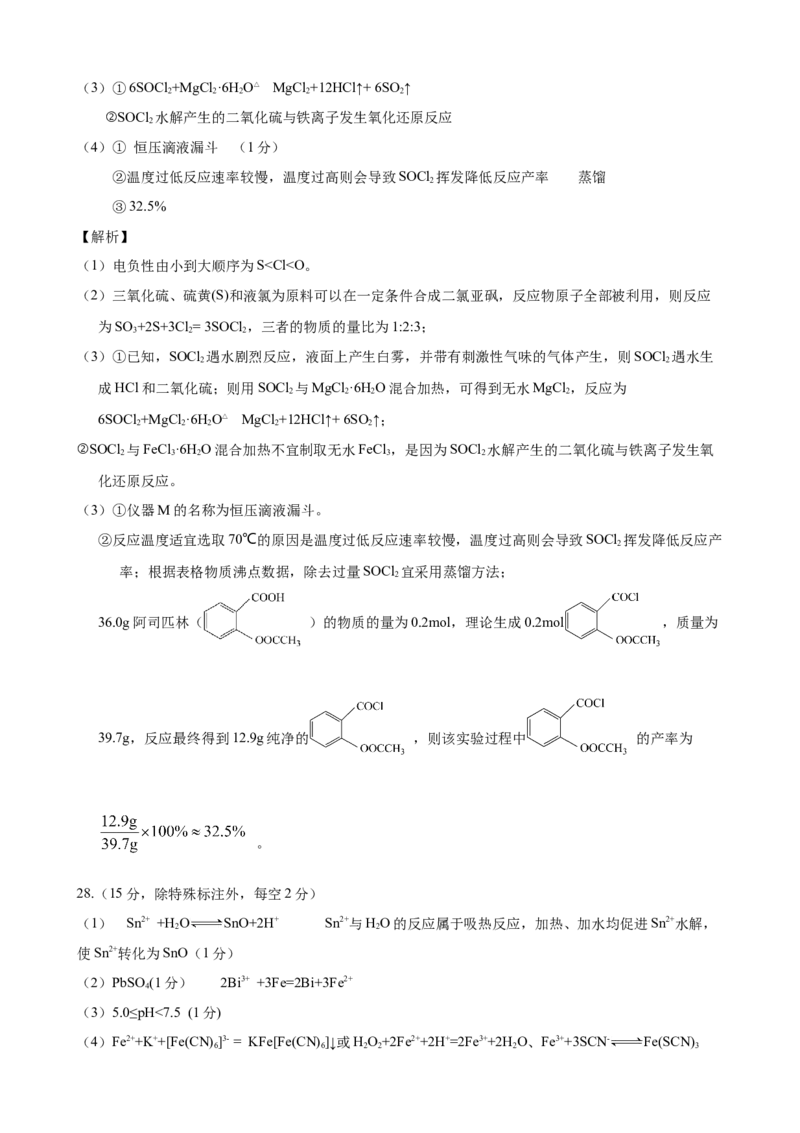
(5)根据信息:G转为H经历了两步,若第一步发生加成反应,第二步发生取代反应,因为产物结构中
I连接位置及-N (第二步取代反应时是-Cl被取代-N ),则第一步反应得到的产物结构简式为:
3 3
(6)根据手性碳原子的概念:碳原子上连接有4个不同原子团,结合D的结构分析,下图中标有*的碳
原子为手性碳原子: ,故手性碳原子数为4个。
(7)根据C的分子结构结合不饱和度分析,I的结构中含有两个 、1个-CHO、1个-COOH,可理
解为苯环上的氢原子被-CHO、-COOH、 取代,即苯环上ABC型的三取代,共10种同分异
构体;根据氧化后为二元羧酸及核磁共振氢谱数目及比例,确定氧化生成的二元羧酸有高度对称
性,从而确定满足条件的I的结构简式为: 。