文档内容
微专题23 金属与硝酸反应的规律与计算
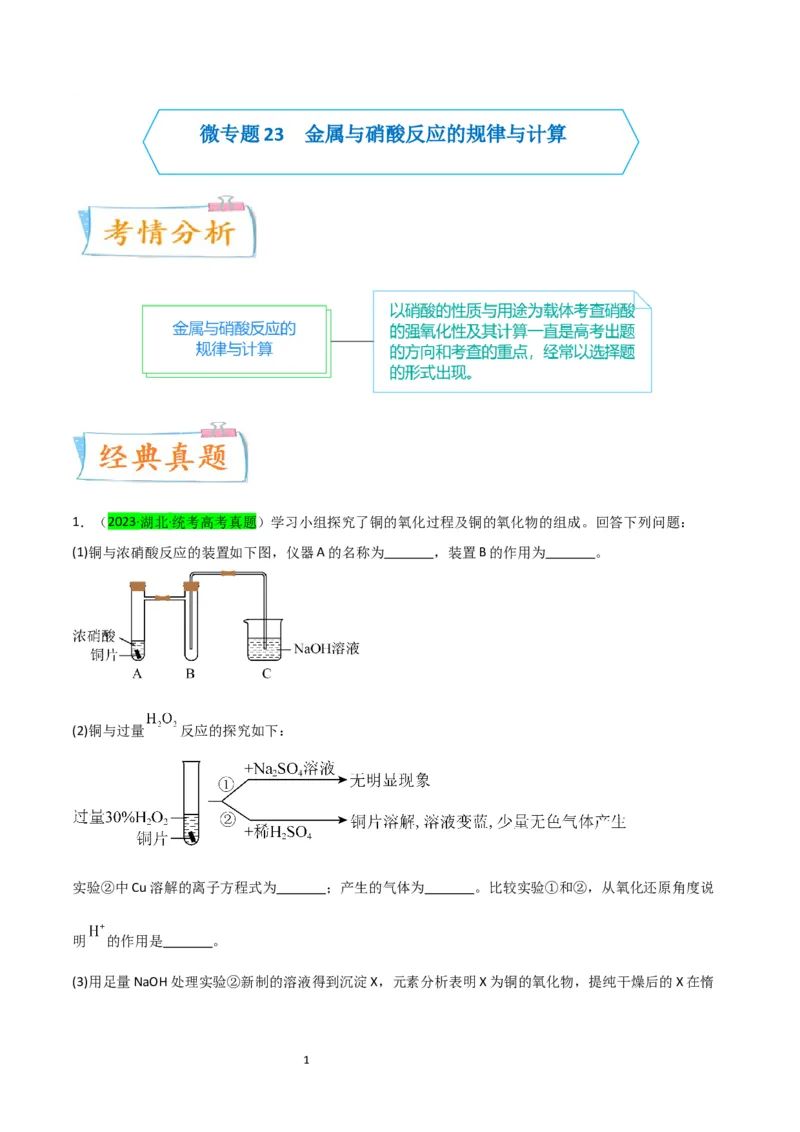
1.(2023·湖北·统考高考真题)学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为 ,装置B的作用为 。
(2)铜与过量 反应的探究如下:
实验②中Cu溶解的离子方程式为 ;产生的气体为 。比较实验①和②,从氧化还原角度说
明 的作用是 。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰
1性氛围下加热,mgX完全分解为ng黑色氧化物Y, 。X的化学式为 。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,
用 标准溶液滴定,滴定终点时消耗 标准溶液15.00mL。(已知:
, )标志滴定终点的现象是 ,粗品中X的相对含量
为 。
【答案】(1) 具支试管 防倒吸
(2) Cu+H O +2H+= Cu2++2H O O 既不是氧化剂,又不是还原剂
2 2 2 2
(3)CuO
2
(4) 溶液蓝色消失,且半分钟不恢复原来的颜色 96%
【解析】(1)由图可知,仪器A的名称为具支试管;铜和浓硝酸反应生成硝酸铜和二氧化氮,其中二氧
化氮易溶于水,需要防倒吸,则装置B的作用为防倒吸;
(2)根据实验现象,铜片溶解,溶液变蓝,可知在酸性条件下铜和过氧化氢发生反应,生成硫酸铜,离
子方程式为:Cu+H O +2H+= Cu2++2H O;硫酸铜可以催化过氧化氢分解生成氧气,则产生的气体为O ;在铜
2 2 2 2
和过氧化氢的反应过程中,氢元素的化合价没有发生变化,故从氧化还原角度说明 的作用是:既不是氧
化剂,又不是还原剂;
(3)在该反应中铜的质量m(Cu)=n× ,因为 ,则m(O)= ,则X的化学式中
铜原子和氧原子的物质的量之比为: ,则X为CuO ;
2
(4)滴定结束的时候,单质碘消耗完,则标志滴定终点的现象是:溶液蓝色消失,且半分钟不恢复原来
的颜色;在CuO 中铜为+2价,氧为-1价,根据 ,可以得到关系式:
2
2,则n(CuO )= ×0.1mol/L×0.015L=0.0005mol,粗品中X的相对含量为
2
。
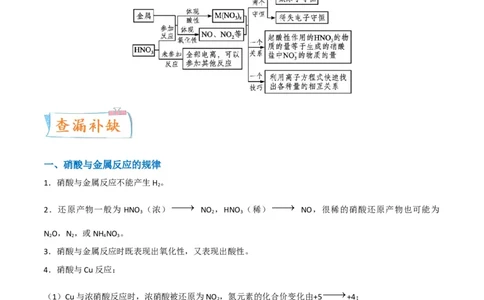
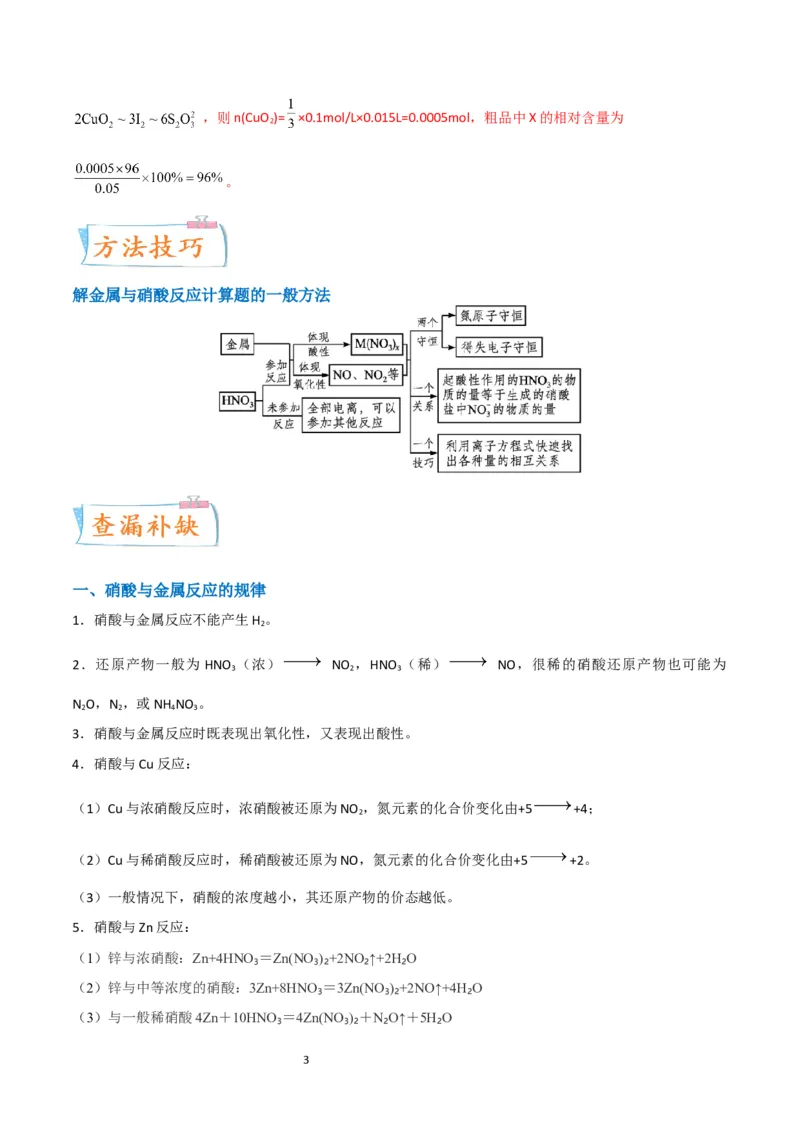
解金属与硝酸反应计算题的一般方法
一、硝酸与金属反应的规律
1.硝酸与金属反应不能产生H 。
2
2.还原产物一般为 HNO (浓) NO ,HNO (稀) NO,很稀的硝酸还原产物也可能为
3 2 3
N O,N ,或NH NO 。
2 2 4 3
3.硝酸与金属反应时既表现出氧化性,又表现出酸性。
4.硝酸与Cu反应:
(1)Cu与浓硝酸反应时,浓硝酸被还原为NO ,氮元素的化合价变化由+5 +4;
2
(2)Cu与稀硝酸反应时,稀硝酸被还原为NO,氮元素的化合价变化由+5 +2。
(3)一般情况下,硝酸的浓度越小,其还原产物的价态越低。
5.硝酸与Zn反应:
(1)锌与浓硝酸:Zn+4HNO₃=Zn(NO₃)₂+2NO₂↑+2H₂O
(2)锌与中等浓度的硝酸:3Zn+8HNO₃=3Zn(NO₃)₂+2NO↑+4H₂O
(3)与一般稀硝酸4Zn+10HNO₃=4Zn(NO₃)₂+N₂O↑+5H₂O
3(4)与较稀硝酸反应:5Zn+12HNO₃=5Zn(NO₃)₂+N₂↑+6H₂O
(5)与极稀硝酸反应:4Zn+10HNO₃=4ZN(NO₃)₂+NH₄NO₃+3H₂O
二、硝酸与金属反应的计算方法
1.原子守恒法
HNO₃与金属反应时,一部分HNO₃起酸的作用,以NO 的形式存在于溶液中;一部分作为氧化剂,转化为
还原产物。这两部分中氮原子的总物质的量等于反应消耗的HNO₃中氮原子的物质的量。
2.得失电子法
HNO₃与金属的反应属于氧化还原反应,HNO₃中氮原子得电子的物质的量等于金属失电子的物质的量。
3.电荷守恒法
HNO₃过量时反应后溶液中(不考虑OH-)有:
( 代表金属离子)。
4.离子方程式计算法
金属与H SO ,HNO₃的混合酸反应时,由于硝酸盐中NO 在H SO 提供的H+的条件下能继续与金属反应,
2 4 2 4
因此此类题目应用离子方程式来计算,先作过量判断,然后根据完全反应的金属或H+或NO 进行相关计算,
且溶液中要符合电荷守恒。
1.(2022·北京·高考真题)下列方程式与所给事实不相符的是
A.加热 固体,产生无色气体:
B.过量铁粉与稀硝酸反应,产生无色气体:
C.苯酚钠溶液中通入 ,出现白色浑浊:
D.乙醇、乙酸和浓硫酸混合加热,产生有香味的油状液体:
4【答案】B
【解析】A.碳酸氢钠受热之后分解生成碳酸钠、水和二氧化碳,A正确;
B.过量的铁粉与稀硝酸反应,应该生成Fe2+,B错误;
C.苯酚钠溶液中通入二氧化碳利用强酸制取弱酸生成苯酚和碳酸氢钠,C正确;
D.乙醇和乙酸在浓硫酸混合加热的条件下发生酯化反应产生有香味的油状液体乙酸乙酯和水,D正确;
故选B。
2.(2021·海南·统考高考真题)用如图装置制取干燥的气体(a、b表示加入的试剂),能实现的是
选项 气体 a b
A 稀
B 溶液
C 浓 铁片
D 浓氨水
A.A B.B C.C D.D
【答案】B
【解析】A. 与浓硫酸反应,故不能用浓硫酸干燥,故A错误;
B.发生反应2H O 2H O+O ,浓硫酸干燥氧气,故B正确;
2 2 2 2
C.铁片和浓硝酸常温下发生钝化,故不能制取二氧化氮气体,故C错误;
5D.氨气与浓硫酸反应,故不能用浓硫酸干燥氨气,故D错误;
故选B。
3.(2021·广东·高考真题)化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是
选
操作或做法 目的
项
A 将铜丝插入浓硝酸中 制备
B 将密闭烧瓶中的 降温 探究温度对平衡移动的影响
C 将溴水滴入 溶液中,加入乙醇并振荡 萃取溶液中生成的碘
D 实验结束,将剩余 固体放回原试剂瓶 节约试剂
A.A B.B C.C D.D
【答案】B
【解析】A.将铜丝插入浓硝酸中开始会产生二氧化氮,不能达到实验目的,A不符合题意;
B.二氧化氮气体在一定条件下存在平衡: ,正反应为放热反应,NO 为红棕色气体,将密
2
闭烧瓶中NO 降温,会使该平衡向正反应方向移动,气体颜色变浅,因此可达到实验目的,B符合题意;
2
C.乙醇与水互溶,不能作碘单质的萃取剂,做法不正确,C不符合题意;
D.一般情况下,剩余试剂需放到指定的容器中,不能放回原试剂瓶,以防污染原试剂,操作错误,D不符
合题意;
故选B。
1.(2023春·福建福州·高一校联考期中)关于硝酸的说法正确的是
A.敞口放置的浓硝酸,浓度会变低是因为浓硝酸有吸水性
B.稀硝酸与Cu反应生成NO和硝酸铜时,硝酸既表现强氧化性又表现酸性
C.硝酸电离出的H+,能被Zn、Fe等金属还原成H
D.常温下,向浓硝酸中投入Fe片,不会产生大量₂的红棕色气体,没有反应发生
【答案】B
【解析】A.敞口放置的浓硝酸浓度变小是因为浓硝酸的挥发性和不稳定性,浓硝酸没有吸水性,故A错
误;
B.稀硝酸与Cu反应生成NO和硝酸铜时,HNO 中N元素化合价部分发生变化,既表现强氧化性又表现酸
3
6性,故B正确;
C.硝酸具有强氧化性,与金属反应不产生氢气,故C错误;
D.常温下,向浓硝酸中投入Fe片,发生钝化,不会产生大量的红棕色气体,钝化不是不反应,而是反应
产生致密的不溶于浓硝酸的氧化物薄膜覆盖在铝的表面阻止了进一步的反应,故D错误;
故选B。
2.(2023春·江西宜春·高一上高中学校考期末)将7.6g铁、铜合金加入100mL某浓度的稀硝酸中,完全
反应后,溶液仍呈强酸性,且共收集到NO气体2.24L(标准状况下)。若反应前后溶液的体积变化忽略不计,
则下列说法不正确的是
A.上述反应中金属共失去电子0.3mol B.原硝酸的浓度:c(HNO )=3mol•L-1
3
C.合金中,铜的质量为4.8g D.反应后,铁的化合价为+3
【答案】B
【解析】A.共收集到NO气体2.24L(标准状况下),NO的物质的量为0.1mol,N元素化合价由+5降低为
+2,根据得失电子守恒,上述反应中金属共失去电子0.3mol,故A正确;
B.完全反应后,溶液仍呈强酸性,硝酸有剩余,所以无法计算原硝酸的浓度,故B错误;
C.根据A选项可知,金属共失去电子0.3mol,设合金中铁的物质的量为xmol、铜的物质的量为ymol,硝
酸有剩余,反应生成硝酸铁、硝酸铜,则 ,x=0.05mol、y=0.075mol,所以铜的质量为
0.075mol×64g/mol=4.8g,故C正确;
D.反应后,硝酸有剩余,铁被氧化为硝酸铁,所以铁的化合价为+3,故D正确;
选B。
3.(2023春·江苏常州·高一常州高级中学校考阶段练习)为了测定铁铜合金的组成,将7.6g铁、铜合金加
入100mL某浓度的稀硝酸中,将合金完全溶解后,共收集到NO气体2.24L(标准状况下),并测得溶液中
H+的浓度为0.5mol•L-1,若反应前后溶液的体积变化忽略不计,则下列判断不正确的是
A.上述反应中金属共失去电子0.3mol
B.合金中,铜的质量为4.8g
C.原硝酸的浓度:c(HNO )=3mol•L-1
3
D.要使溶液中的金属离子完全沉淀,需加5mol•L-1的NaOH溶液70mL
【答案】C
【解析】n(NO)= =0.1mol,转移电子的物质的量为0.1mol×(5-2)=0.3mol,反应后溶液中的
c(H+)=0.5mol/L,则反应后剩余n(HNO )=0.5mol/L×0.1L=0.05mol,设合金中Cu为xmol,Fe为ymol,由电子
3
7守恒可知:2x+3y=0.3mol,由合金的质量可知:64x+56y=7.6,解得x=0.075mol,y=0.05mol。
A.金属失去的电子等于N元素得到的电子,n(NO)= =0.1mol,转移电子为0.1mol×(5-2)=0.3mol,
因此金属共失去电子0.3 mol,故A正确;
B.由上述分析可知,合金中铜的物质的量为0.075mol,质量为0.075mol×64g/mol=4.8 g,故B正确;
C.反应生成Cu(NO ) 、Fe(NO ) 和NO,以及反应后剩余n(HNO )=0.5mol/L×0.1L=0.05mol,根据氮原子守恒
3 2 3 3 3
可知,硝酸的总物质的量n(HNO )=0.075×2+0.05×3+0.1+0.05=0.45mol,则c(HNO )= =4.5mol/L,故C
3 3
错误;
D.要使溶液中的金属离子完全沉淀,溶液中剩余的硝酸先与氢氧化钠反应,则
n(NaOH)=0.075×2+0.05×3+0.05=0.35mol,V= =0.07L=70mL,故D正确;
答案选C。
4.(2023春·四川成都·高一校考期中)我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”
条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是
指硝酸,下列有关硝酸的相关描述中正确的是
A.王水指浓硝酸与浓盐酸按3:1的体积比混合所得的混合物
B.向装有Fe(NO ) 溶液的试管中加入稀硫酸,可在试管口观察到红棕色气体
3 2
C.常温下,浓硝酸可以用铝制容器储存,说明浓硝酸与铝不反应
D.稀HNO 与金属反应时,可被还原为更低价态,说明稀HNO 氧化性强于浓HNO
3 3 3
【答案】B
【解析】A.王水指浓硝酸与浓盐酸按1:3的体积比混合所得的混合物,能溶解金和铂,A错误;
B.酸性溶液中硝酸根离子有强氧化性,与亚铁离子发生氧化还原反应生成一氧化氮,一氧化氮在试管口
与氧气反应生成二氧化氮,可在试管口观察到红棕色气体,B正确;
C.常温下,铝与浓硝酸发生钝化,所以浓硝酸可以用铝制容器储存,C错误;
D.与金属反应时,稀硝酸被还原为一氧化氮,反应较慢,浓硝酸被还原为二氧化氮,反应较快,所以稀
硝酸的氧化性比浓硝酸弱,D错误;
答案选B。
5.(2023春·黑龙江鹤岗·高一鹤岗一中校考期中)将铁粉和铜粉的均匀混合物平均分成四等份,分别加入
同浓度的稀硝酸,充分反应,在标准状况下生成 的体积和剩余金属的质量如下表(设硝酸的还原产物只
有 )。下列说法正确的是
8编号 ① ② ③ ④
硝酸体积/mL 100 200 300 400
剩余金属/g 18.6 9.6 0 0
NO体积/L 2.24 4.48 6.72 V
A.①中溶液存在 B.
C.硝酸的浓度为 D.④中
【答案】B
【解析】(1)由表中数据可知,实验①和实验②都有金属剩余,则溶液中不可能含硝酸铁,溶液中金属
离子为+2价,即实验①和实验②中的反应可以归纳为3M+8HNO (稀)=3M(NO ) +2NO↑+4H O;
3 3 2 2
(2)实验②可以看作是在实验①的基础上继续加入100mL硝酸,在这100mL HNO 参与的反应中,参加反
3
应的金属的质量为18.6g-9.6g=9g,生成NO的体积为4.48L-2.24L=2.24L,则NO(标况下)的物质的量为
0.1mol,根据化学方程式可知,参加反应的金属的物质的量为0.15mol,参加反应的金属的平均摩尔质量为
=60g/mol,该过程既有铁参与反应,又有铜参与反应,利用十字交叉法 ,
则n(Fe)=n(Cu)= 0.15mol=0.075mol,m(Fe)=0.075mol56g/mol=4.2g,m(Cu)=0.075mol64g/mol=4.8g,故
实验①只有铁参与反应;
(3)实验①发生的反应为3Fe+8HNO (稀)=3Fe(NO ) +2NO↑+4H O,生成NO的体积为2.24L,则NO(标况
3 3 2 2
下)的物质的量为0.1mol,根据反应的化学方程式可知,参加反应的铁的物质的量为0.15mol,参加反应
的铁的质量为0.15mol 56g/mol=8.4g,参加反应的硝酸的物质的量为0.1mol 4=0.4mol,硝酸的物质的量
浓度为 =4mol/L;
(4)结合(1)和(2)的分析内容可知,实验②中,参加反应的Fe的物质的量为
0.15mol+0.075mol=0.225mol;
(5)实验③可看作是在实验②的基础上继续加入100mL稀硝酸,此时铁已全部反应,已经有0.075mol的
9铜参与了反应,则在这100mL稀硝酸参与的反应中,9.6g的金属全部为铜,物质的量为
=0.15mol,金属铜与稀硝酸反应的化学方程式为:3Cu+8HNO (稀)=3Cu(NO ) +2NO↑+4H O,0.15mol Cu参与
3 3 2 2
反应生成0.1mol NO,则实验③铜和稀硝酸恰好完全反应,则Cu的总物质的量为
0.075mol+0.15mol=0.225mol;
(6)实验④可以看作是在实验③的基础上再加100mL稀硝酸,则这100mL稀硝酸和Fe2+反应,上述反应
中的Fe全部转化为Fe2+,则Fe2+的物质的量为0.225mol,Fe2+与稀硝酸反应的离子方程式为4H++3Fe2++
=3Fe3++NO↑+2H O,反应生成0.075mol NO,体积为0.075mol 22.4L/mol=1.68L。
2
A.由分析可知,实验①只有铁参与反应,溶液中只有Fe2+,没有Fe3+,A错误;
B.由分析可知,铁的物质的量为0.15mol+0.075mol=0.225mol,铜的物质的量为
0.15mol+0.075mol=0.225mol, ,B正确;
C.由分析可知,硝酸的物质的量浓度为4mol/L,C错误;
D.由分析可知,④中V=6.72L+1.68L=8.4L,D错误;
答案选B。
6.(2023春·福建福州·高一福建省福州第一中学校考期中)某金属单质跟一定浓度的硝酸反应,假定只产
生单一的还原产物。当参加反应的单质与被还原硝酸的物质的量之比为2:1时,还原产物是 ( )
A.NO B.NO C.N O D.N
2 2 2
【答案】C
【解析】假设金属元素化合价由0价变为+1价,设还原产物中N元素化合价为x,根据转移电子相等得
2×(1−0)=1×(5−x),x=3;
假设金属元素化合价由0价变为+2价,设还原产物中N元素化合价为y,根据转移电子相等得
2×(2−0)=1×(5−y),y=1;
假设金属元素化合价由0价变为+3价,设还原产物中N元素化合价为z,根据转移电子相等得
2×(3−0)=1×(5−z),z=−1;
A.NO 中N元素化合价为+4价,不符合,故A错误 ;
2
B.NO中N元素化合价为+2价,不符合,故B错误;
C.N O中N元素化合价为+1,符合,故C正确;
2
D.N 中N元素化合价为0价,不符合,故D错误;
2
答案选C。
107.(2022·山东德州·统考二模)下列有关计算正确的是
A.Na O 作供氧剂时,每生成5.6 L O (标况),转移电子数为0. 25N
2 2 2 A
B.1.92 g Cu与足量稀硝酸反应,被还原硝酸的物质的量为0.02 mol
C.利用铝热反应制备金属时,每得到1 mol Fe,一定消耗0.5 mol氧化剂
D.已知NH 的燃烧热为316.25 kJ/mol,则NH 燃烧的热化学方程式为:4NH (g)+5O (g)=4NO(g)
3 3 3 2
+6H O(g) H=-1265 kJ/mol
2
【答案】B △
【解析】A.Na O 作供氧剂时,发生反应2Na O +2CO =2Na CO +O ,Na O 中氧元素化合价由-1价升高为0
2 2 2 2 2 2 3 2 2 2
价、由-1价降低为-2价,每生成5.6 L O (标况),转移电子数 ,故A错误;
2
B.1.92 g Cu与足量稀硝酸反应,发生反应 ,生成0.02molNO,
被还原硝酸的物质的量为0.02 mol,故B正确;
C.利用铝热反应制备金属铁时,铁的氧化物是氧化剂,若Fe O 和铝反应,每得到1 mol Fe,消耗 mol氧
3 4
化剂,故C错误;
D.氨气燃烧热是1mol氨气燃烧生成氮气和液态水放出的能量,NH 的燃烧热为316.25 kJ/mol,则NH 燃
3 3
烧的热化学方程式为:4NH (g)+3O (g)=2N (g)+6H O(l) △H=-1265 kJ/mol,故D错误;
3 2 2 2
选B。
8.(2022秋·新疆和田·高三统考期中)向mg由铁粉和铜粉组成的混合物中,加入某浓度的稀硝酸,充分
反应后测得生成NO的体积[V(NO)](已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化
如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是
A.稀硝酸的浓度为0.4mol·L-1
11B.a点时,100mL稀硝酸中溶解了Fe和Cu共8.4g
C.b点对应的溶液中可能含有的金属阳离子为Fe2+、Fe3+、Cu2+
D.加入稀硝酸至400mL时,收集到的V(NO)约为6.91L
【答案】D
【解析】由图示数据可得如下表格:
编号 ① ② ③ ④
稀硝酸体积/mL 100 200 300 400
剩余金属/g 12.2 3.2 0 0
NO体积/mL 2240 4480 6720 V
实验①和②都有金属剩余,则溶液中不可能含硝酸铁,溶液中金属离子为+2价,在实验①的基础上加入
100mL硝酸,参加反应的金属的质量为12.2g-3.2g=9g,生成NO的体积为4480mL-2240mL=2240mL,NO的
物质的量为0.1mol,根据电子转移守恒可知,参加反应的金属的物质的量为 =0.15mol,参加
反应的金属的平均摩尔质量为 =60g/mol,该过程既有铁参与反应,又有铜参与反应,利用十字交
叉法 ,则n(Fe)=n(Cu)= 0.15mol=0.075mol,故实验①只有铁参与反应,实验①生
成NO的体积为2240mL,NO的物质的量为0.1mol,根据电子转移守恒可知,参加反应的铁的物质的量为
=0.15mol,质量为0.15mol 56g/mol=8.4g,实验②既有铁参与反应,又有铜参与反应,且
n(Fe)=n(Cu)= 0.15mol=0.075mol,在实验②的基础上继续加入100mL稀硝酸,生成NO的体积为
6720mL-4480mL=2240mL,NO的物质的量为0.1mol,该过程既有铜参加反应,又有亚铁离子参加反应,参
加反应的金属的质量为3.2g,金属全部为铜,物质的量为 =0.05mol,金属铜与稀硝酸反应的化学
方程式为:3Cu+8HNO (稀)=3Cu(NO ) +2NO↑+4H O,0.05molCu参与反应生成 molNO,则亚铁离子参与
3 3 2 2
12反应生成 molNO,硝酸亚铁与稀硝酸反应的化学方程式为:4HNO (稀)
3
+3Fe(NO ) =3Fe(NO ) +NO↑+2H O,则消耗亚铁离子0.2mol,由以上分析可知,总共含亚铁离子
3 2 3 3 2
0.15mol+0.075mol=0.225mol,则加入稀硝酸300mL后还有0.225mol-0.2mol=0.025mol亚铁离子,0.025mol
亚铁离子与稀硝酸反应生成 ≈0.0083molNO,体积为0.0083mol 22.4L/mol≈0.19L。
A.由分析可知,实验①只有铁参与反应,发生反应3Fe+8HNO (稀)=3Fe(NO ) +2NO↑+4H O,生成NO的体
3 3 2 2
积为2240mL,NO的物质的量为0.1mol,则参加反应的硝酸的物质的量为0.1mol 4=0.4mol,硝酸的物质
的量浓度为 =4mol/L,A错误;
B.由分析可知,a点只消耗了铁8.4g,B错误;
C.b点还有金属剩余,因此溶液中不可能有Fe3+,C错误;
D.由分析可知,加入稀硝酸至400mL时,收集到的V(NO)约为6.72L+0.19L=6.91L,D正确;
答案选D。
1.(2022秋·山东聊城·高三聊城二中校考期中)某兴趣小组探究金属与硝酸的还原产物,进行了下列三组
实验,下列说法正确的是
实验操作(室温)及实验现象
① 将足量的铜粉加入 中,溶液呈绿色,产生红棕色气体
② 将足量的铜粉加入 中,溶液呈蓝色,产生无色气体
③ 将足量的铁粉加入 中,溶液呈浅绿色,无气体生成
A.实验①②反应后溶液颜色不同,说明氧化产物不同
B.实验②中产生的气体不能和血红蛋白结合
C.实验③中铁发生了钝化
D.以上实验说明硝酸的还原产物与硝酸的浓度及金属的活泼性有关
【答案】D
【解析】A.实验①②反应后溶液颜色相同都是蓝色,氧化产物都是硝酸铜溶液,A项错误;
13B.②产生的气体是一氧化氮,一氧化氮会和血红蛋白结合,B项错误;
C.将足量的铁粉加入100mL, 中,溶液呈浅绿色,无气体生成,可能发生反应生成了硝酸
亚铁和硝酸铵,常温下铁在浓硝酸下发生钝化,C项错误;
D.实验①②可知,浓硝酸和铜反应生成二氧化氮,铜和稀硝酸反应生成一氧化氮,硝酸的还原产物与硝
酸的浓度有关,与金属活泼性有关,D项正确;
答案选D。
2.(2022秋·山东青岛·高三统考期末)浓硝酸和稀硝酸均具有强氧化性,浓硝酸还原产物为NO ,稀硝酸
2
还原产物为NO。同温同压下,0.1mol金属单质M与足量浓硝酸反应,生成NO 体积为V ;0.1mol金属单
2 1
质N与足量稀硝酸反应,生成NO体积为V 。下列说法错误的是
2
A.M和N反应中,被还原硝酸的物质的量之比一定为
B.M和N反应中,消耗硝酸的物质的量之比一定为
C.产物中M和N化合价之比一定为
D.将生成的气体恰好溶于水生成硝酸,需要通入氧气的体积之比一定为
【答案】B
【解析】A.设该条件下气体摩尔体积为V ,M与浓硝酸反应时,被还原的硝酸n=n(NO )= ,N与稀硝
m 1 2
酸反应时,被还原的硝酸n=n(NO)= ,则两个反应中被还原的硝酸物质的量之比为 ,A正确;
2
B.设反应后M转化为M(NO ),则根据得失电子守恒得:0.1 mol×x= ,解得x= ,则M与硝酸反应
3 x
14中消耗硝酸n=0.1 mol× + = ,设反应后N转化为N(NO ),则根据得失电子守恒得:0.1 mol×y=
3 3 y
,解得y= ,则M与硝酸反应中消耗硝酸n=0.1 mol× + = ,则两个反应中消耗硝酸物
4
质的量之比为 ,B错误;
C.由B选项分析知,反应后M的化合价为+x价,即+ 价,反应后N的化合价为+y价,即+ 价,
故M、N反应后化合价之比为 ,C正确;
D.根据反应4NO +O +2H O=4HNO ,知将生成的NO 完全溶于水需要O 的物质的量n= = ,根
2 2 2 3 2 2 5
据反应4NO+3O +2H O=4HNO ,知将生成的NO完全溶于水需要O 的物质的量n= = ,则两种情
2 2 3 2 6
况下需要O 的物质的量之比(即体积比)为 ,D正确;
2
故答案选B。
3.(2023·全国·高三专题练习)硝酸与金属反应后所得还原产物与硝酸的浓度和金属的活泼性有关。10
mL 0.5 mol·L-1HNO 与0.048 g Mg恰好完全反应。若氮元素只被还原到一种价态,下列说法不正确的是
3
A.HNO 作还原剂
3
B.HNO 浓度越低,N元素还原价态越低
3
C.反应中转移电子数为0.004 mol
D.还原产物可能为NH NO
4 3
【答案】A
15【解析】A.HNO 与金属反应时,表现酸性和强氧化性,故A错误;
3
B.HNO 浓度越高,氧化性越强,氧化同种金属时,N元素被还原的价态就越高,故B正确;
3
C.HNO 与Mg反应,还原剂只有Mg,Mg的化合价由0→+2,0.048g Mg的物质的量为0.002mol,根据得
3
失电子守恒,反应中转移电子为0.004mol,故C正确;
D.硝酸的物质的量为0.01L×0.5mol·L-1=0.005mol,生成0.002mol Mg(NO ) ,根据N原子守恒,可能生成
3 2
0.0005 mol NH NO ,若生成0.0005 mol NH NO 转移电子为0.004mol,符合电子守恒,故D正确;
4 3 4 3
故答案为A。
4.(2023·山东淄博·校联考二模)探究铜与硝酸反应的生成 时的硝酸浓度。如图所示,先通 一段时
间后关闭活塞K,将铜丝伸入溶液中,当A中气体变为无色时,上提铜丝,再将B中溶液稀释至 ,
取 ,用 的 溶液滴定至终点时消耗 (忽略硝酸的挥发、分解及溶液体积变
化)。下列说法正确的是
A.可用盛有 溶液的洗气瓶进行尾气吸收
B.铜与硝酸反应主要生成 时的硝酸浓度不大于
C.若不通 ,可能导致所得实验结果偏高
D.若通过直接滴定A中剩余酸的量(掩蔽掉 的干扰)进行求算,所得实验结果偏低
【答案】D
【解析】A瓶中的反应为4HNO (浓)+Cu=2NO ↑+2H O+Cu(NO ) 。B中发生的反应为3NO +H O=2HNO +NO。
3 2 2 3 2 2 2 3
用0.20mol L−1的NaOH溶液滴定至终点时消耗15.00mL,即n(NaOH)=0.20×15.00×10-3mol=3×10-3mol,有关
系式为NaO⋅H~HNO 则B瓶中产生的n(HNO )= 3×10-3mol×10=3×10-2mol,又3NO ~2HNO 则A瓶中产生的NO
3 3 2 3 2
为3×10-2mol× =4.5×10-2mol。由关系式得4HNO (浓)~2NO 则消耗的浓硝酸为4.5×10-2×2=9×10-2mol。
3 2
16A.NaOH溶液不能直接与NO反应,所以它不能吸收尾气,A项错误;
B.溶液中剩余的硝酸浓度为 。但当反应产生无色NO气体
时停止反应,即硝酸浓度大于8mol L−1也产生了NO,B项错误;
C.若不同如N ,B瓶中NO也转变为⋅ HNO ,从而导致消耗的HNO 偏大,A中剩余HNO 偏低,结果偏低,
2 3 3 3
C项错误;
D.当A中气体变为无色时停止反应,产生NO的浓度应该比A瓶的大。所以直接测定A瓶中的酸可能导致
结果偏低,D项正确;
故选D。
5.(2023·全国·高三专题练习)将1.92g铜粉与一定量的浓硝酸反应,硝酸的还原产物为NO和NO ,当铜
2
粉完全反应时收集到混合气体1.12L(气体体积折算为标准状况)。则所消耗硝酸的物质的量是
A.0.08mol B.0.09mol C.0.11mol D.0.12mol
【答案】C
【解析】将1.92g铜粉与一定量的浓硝酸反应,硝酸的还原产物为NO和NO ,当铜粉完全反应时收集到混
2
合气体1.12L(气体体积折算为标准状况),气体物质的量为0.05mol,生成的盐为硝酸铜,根据铜守恒得到
盐硝酸根物质的量为 ,根据氮元素守恒,则所消耗硝酸的物质的量是
0.05mol+0.06mol=0.11mol,故C符合题意。
综上所述,答案为C。
6.(2023·全国·高三专题练习)用图所示装置进行实验,探究硝酸与铁反应的产物。
主要实验操作 实验现象
①A 中有红棕色气体产生,一段时间后,气体颜
打开弹簧夹,通入一段时间CO 2 后,滴入浓硝酸后无 色逐渐变浅;反应停止后,A 中无固体剩余。
明显现象,加热烧瓶,反应开始后停止加热。
②B 中溶液变棕色。
17取少量A 中溶液,加几滴氯水,再滴入硫氰化钾溶
③溶液变为红色
液
④B中棕色溶液变浅,有无色气体逸出,且在空气
取少量 B 中溶液,加热
中变为红棕色
已知:FeSO +NO=Fe(NO)SO (棕色) ∆H<0 。
4 4
下列说法正确的是
A.滴入浓硝酸加热前没有明显现象的原因是:温度低,反应速率太慢
B.实验现象③说明反应后A 中溶液含有 Fe2+
C.实验现象④说明 A 中有 NO 生成
D.可用浓 NaOH 溶液和湿润的红色石蕊试纸检验硝酸的还原产物中是否有 NH
【答案】D
【解析】A.常温时,铁遇浓硝酸形成致密氧化膜,阻止反应进一步发生,不是因为温度低,反应速率太
慢的缘故,故A错误;
B.取少量A中溶液,加几滴氯水,再滴入KSCN溶液,溶液变为红色,只能说明这时溶液中有三价铁离子,
无法说明原溶液中是二价铁还是三价铁,故B错误;
C.取少量B中溶液加热,B中棕色溶液变浅,无色气体逸出,且在空气中变为红棕色,只能说明
Fe(NO)SO 分解生成NO,但由于铜和浓硝酸反应生成红棕色气体二氧化氮,二氧化氮和水反应生成一氧化
4
氮,一氧化氮能使硫酸亚铁溶液变成棕色,所以不能证明铁和浓硝酸反应过程中NO生成,故C错误;
D.浓NaOH溶液和湿润的红色石蕊试纸可检验A溶液中是否有NH ,即可以检验硝酸的还原产物中是否
有NH ,若产生使湿润的红色石蕊试纸变蓝的气体,证明硝酸的还原产物中有NH ,故D正确;
故选D。
7.(2023·全国·高三专题练习)将质量为32g的铜与150mL的一定浓度的硝酸反应,铜完全溶解,产生标
准状况下11.2L的NO和NO 的混合气体,将生成的混合气体与一定体积的氧气一起通入足量NaOH溶液中,
2
气体恰好被吸收生成NaNO 。下列说法不正确的是
3
A.标准状况下,通入的O 体积为5.6L
2
B.向反应后的溶液加NaOH,使铜沉淀完全,需要NaOH的物质的量至少为1.0mol
C.标准状况下,混合气体构成是5.6L的NO和5.6L的NO
2
D.硝酸的物质的量浓度为10.0mol·L−1
【答案】D
18【解析】32g的铜的物质的量为0.5mol;11.2L的NO和NO 的物质的量为0.5mol,设混合气体中NO的物质
2
的量为x,NO 的物质的量为y,则x+y=0.5,反应过程中铜全部被氧化成Cu2+,根据电子守恒有
2
3x+y=0.5×2,和前式联立可得x=0.25mol,y=0.25mol;
设氧气的物质的量为z,NO和NO 全部转化为NaNO ,则根据电子守恒有0.5×2=4z,解得z=0.25mol;根据
2 3
元素守恒可知生成的n(NaNO )=0.5mol。
3
A.根据分析可知通入的O 为0.25mol,标况下体积为0.25mol×22.4L/mol=5.6L,故A正确;
2
B.当硝酸无剩余时消耗的NaOH最少,此时NaOH只与Cu2+反应生成Cu(OH) 沉淀,根据元素守恒可知此
2
时n(NaOH)=2n(Cu2+)=0.5mol×2=1mol,故B正确;
C.根据分析可知,混合气体中有0.25molNO和0.25molNO ,即标准状况下的5.6L的NO和5.6L的NO ,故
2 2
C正确;
D.由于不知道和铜反应后硝酸是否有剩余,所以无法计算硝酸的浓度,故D错误;
故答案为D。
8.(2023春·重庆万州·高三重庆市万州第二高级中学校考阶段练习)将一定质量的镁铜合金加入到稀硝酸
中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3 mol·L-1
NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g,则下列有关叙述中正确的是
( )
A.加入合金的质量不可能为6.4 g
B.参加反应的硝酸的物质的量为0.1 mol
C.沉淀完全时消耗NaOH溶液的体积为150 mL
D.溶解合金时收集到NO气体的体积在标准状况下为2.24 L
【答案】D
【解析】将一定量的镁和铜合金加入到稀HNO 中,二者恰好反应,金属、硝酸都没有剩余,反应中还原
3
产物只有NO,发生反应:3Mg+8HNO (稀)═3Mg(NO ) +2NO↑+4H O、3Cu+8HNO (稀)═3Cu
3 3 2 2 3
(NO ) +2NO↑+4H O;向反应后的溶液中加入3mol/LNaOH溶液至沉淀完全,发生反应:Mg(NO )
3 2 2 3
+2NaOH═Mg(OH) ↓+2NaNO 、Cu(NO ) +2NaOH═Cu(OH) ↓+2NaNO ,沉淀为氢氧化镁和氢氧化铜,
2 2 3 3 2 2 3
生成沉淀的质量比原合金的质量增加5.1g,则氢氧化镁和氢氧化铜含有氢氧根的质量为5.1g,氢氧根的物
质的量为 =0.3mol,根据电子转移守恒,则镁和铜的总的物质的量为 =0.15mol,生成NO为
=0.1mol。
19A.镁和铜的总的物质的量为0.15mol,假定全为镁,质量为0.15mol×24g/mol=3.6g,若全为铜,质量为
0.15mol×64g/mol=9.6g,所以参加反应的金属的总质量(m)为3.6g<m<9.6g,则合金的质量可能为
6.4g,A错误;
B.根据方程式可知参加反应的n (HNO )= n(金属)= ×0.15mol=0.4mol,故B错误;
反应 3
C.加入的氢氧化钠恰好与硝酸镁、硝酸铜反应,由上述分析可知,加入的NaOH为0.3mol,故加入NaO溶
液的体积为 =0.1L=100mL,C错误;
D.标准状况下0.1molNO的体积为2.24L,D正确。
故选D,
9.(2023·高一课时练习)关于硝酸的说法正确的是
A.硝酸电离出的H+离子,能被Zn、Fe等金属还原成H
2
B.浓HNO 与浓HCl按3∶1的体积比所得的混合物叫王水
3
C.硝酸与金属反应时,主要是+5价的氮元素得电子
D.常温下,向浓HNO 中投入Fe片,会产生大量的红棕色气体
3
【答案】C
【解析】A.硝酸电离出的H+离子,但硝酸是氧化性酸,不能被Zn、Fe等金属还原成H ,A错误;
2
B.浓HNO 与浓HCl按1∶3的体积比所得的混合物叫王水,B错误;
3
C.硝酸与金属反应时,主要是+5价的氮元素得电子,C正确;
D.常温下,向浓HNO 中投入Fe片,发生钝化,不会产生大量的红棕色气体,D错误;
3
答案选C。
10.(2023春·甘肃张掖·高一高台县第一中学校考阶段练习)在某100mL混酸中,硝酸的物质的量浓度为
0.4mol/L,硫酸的物质的量浓度为0.2mol/L,加入2.56g铜粉,微热,待充分反应后,溶液中Cu2+的物质的
量浓度为
A.0.15mol/L B.0.3mol/L C.0.225mol/L D.无法计算
【答案】B
【解析】在某100mL混酸中,硝酸的物质的量n(HNO )=0.1L×0.4mol/L=0.04mol,硫酸的物质的量
3
n(H SO )=0.1L×0.2moL/L=0.02moL,所以氢离子的物质的量n(H+)=0.04moL+2×0.02moL=0.08mol,铜粉的物质
2 4
20的量= =0.04mol,依据方程式: ,可知氢离子
不足,故根据H+计算,由方程式可知n(Cu2+)= ×0.08mol=0.03mol,所以c(Cu2+)= =0.3mol/L,故答案
为:B。
11.(2022秋·湖南岳阳·高三校考阶段练习)实验研究发现,金属与硝酸发生氧化还原反应时,硝酸的浓
度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与足量很稀的硝酸充分
反应,反应过程中无气体放出,在反应结束后的溶液中逐滴加入5mol/LNaOH溶液,所加NaOH溶液的体
积 与产生沉淀的物质的量 关系如图所示,下列说法正确的是
A. 点到 点的反应为:
B.样品中铝粉和铁粉的质量之比为 :
C. 点对应 溶液的体积为
D.原硝酸溶液中硝酸的物质的量为
【答案】AD
【分析】根据题意,稀硝酸的还原产物为 ,铝粉和铁粉反应后溶液中含 ,
0 →a的反应是 ,a→b的反应是 ,b→c的反应
是 ,此时溶液只含NaNO 和 ,c→d的反应是 。
3
【解析】A.根据分析, 点到 点的反应为: ,A正确;
21B.根据分析, , ,
根据电子得失守恒 , ,
B错误;
C.c点溶液中硝酸根刚好生成NaNO ,则 , 点对应 溶液
3
的体积 ,C错误;
D.根据氮元素守恒,原硝酸溶液中硝酸的物质的量为 ,D正确;
答案选AD。
12.(2023·全国·高三专题练习)铁粉与硝酸反应可制备硝酸铁,硝酸铁溶液可用于刻蚀银器。铁粉用量
和硝酸浓度都会影响反应产物。
I.常温下过量铁粉与不同浓度硝酸反应的还原产物的探究。利用如图装置进行实验,其中装置A为氮气氛
围。
(1)实验一:硝酸初始浓度为12.0mol•L-1时,硝酸的还原产物主要是NO 。装置B中NO 发生反应的化学方
2 2
程式为 。
(2)实验二:硝酸浓度为6.0mol•L-1时,硝酸的还原产物主要是NO。利用上述装置进行实验时,证明还原产
物主要是NO的现象是 。
(3)实验三:硝酸浓度为0.5mol•L-1时,过量铁粉与硝酸反应产生H ,充分反应后所得溶液几乎无色。取装
2
置A中上层清液,加入过量NaOH溶液并煮沸,产生的气体能使湿润的红色石蕊试纸变蓝。过量铁粉与
0.5mol•L-1硝酸混合发生反应的离子方程式有:①Fe+2H+=Fe2++H ↑;② 。
2
II.硝酸铁溶液刻蚀银器的原理探究。
(4)已知:①0.1mol•L-1硝酸铁溶液pH的为1.6。
22②将5mL0.1mol•L-1硝酸铁溶液滴加到有银镜的试管中,1min银镜完全溶解。
提出猜想猜想a:Fe3+具有氧化性,能氧化Ag。
猜想b:酸性条件下NO ,能氧化Ag。
设计实验,验证猜想
序号 实验方案 实验现象 结论
①将5mLpH约为1.6的0.05mol•L-1 溶液滴加到有银镜
猜想
的试管甲中
猜想a成
a 立
②将5mLpH约为1.6的硫酸溶液滴加到有银镜的试管乙中
猜想 1.2min试管丙中银镜完全 猜想b成
将5mL 溶液滴加到有银镜的试管丙中
b 溶解 立
实验结论:硝酸铁溶液刻蚀银器原理是0.1mol•L-1硝酸铁溶液中的Fe3+和NO 均能氧化Ag。
【答案】(1)3NO +H O=2HNO +NO
2 2 3
(2)A装置中产生无色气体,到B装置中有大量气泡,B装置液面以上和装置C中充满红棕色气体
(3)4Fe+ +10H+=4Fe2++ +3H O
2
(4) Fe (SO ) 银镜完全溶解 pH约为1.6的硫酸酸化的0.3mol/LKNO
2 4 3 3
【解析】(1)NO 和H O反应生成HNO 和NO,故装置B中NO 发生反应的化学方程式为
2 2 3 2
3NO +H O=2HNO +NO,故答案为:3NO +H O=2HNO +NO;
2 2 3 2 2 3
(2)无色气体NO很容易与O 反应生成红棕色的NO ,故利用上述装置进行实验时,证明还原产物主要是
2 2
NO的现象是A装置中产生无色气体,到B装置中有大量气泡,B装置液面以上和装置C中充满红棕色气体,
故答案为:A装置中产生无色气体,到B装置中有大量气泡,B装置液面以上和装置C中充满红棕色气体;
(3)取装置A中上层清液,加入过量NaOH溶液并煮沸,产生的气体能使湿润的红色石蕊试纸变蓝,该气
体溶于水显碱性为NH ,即过量铁粉与0.5mol•L-1硝酸混合发生反应生成了 ,根据氧化还原反应配平
3
可得该反应的离子方程式有:①Fe+2H+=Fe2++H ↑;②4Fe+ +10H+=4Fe2++ +3H O,故答案为:4Fe+
2 2
+10H+=4Fe2++ +3H O;
2
(4)由题干信息可知,猜想a为Fe3+具有氧化性,能氧化Ag,根据对照实验控制变量的要求可知,实验①
23中只能出现Fe3+,不能出现 ,且保证Fe3+浓度为0.1mol/L,并结合对照实验②可知加入的试剂为5mLpH
约为1.6的0.05mol•L-1Fe (SO ) 溶液,若观察到银镜完全溶解,则证明猜想a成立,故答案为:Fe (SO ) ;
2 4 3 2 4 3
银镜完全溶解;
由题干信息可知,猜想b为酸性条件下NO ,能氧化Ag,根据对照实验控制变量的要求可知,实验③中只
能出现 ,不能出现Fe3+,且保证 浓度为0.3mol/L,pH约为1.6的溶液,结合对照实验②可知,加
入5mL pH约为1.6的硫酸酸化的0.3mol/LKNO 溶液,若观察到1.2min试管丙中银镜完全溶解,证明猜想b
3
成立,故答案为:pH约为1.6的硫酸酸化的0.3mol/LKNO 。
3
24