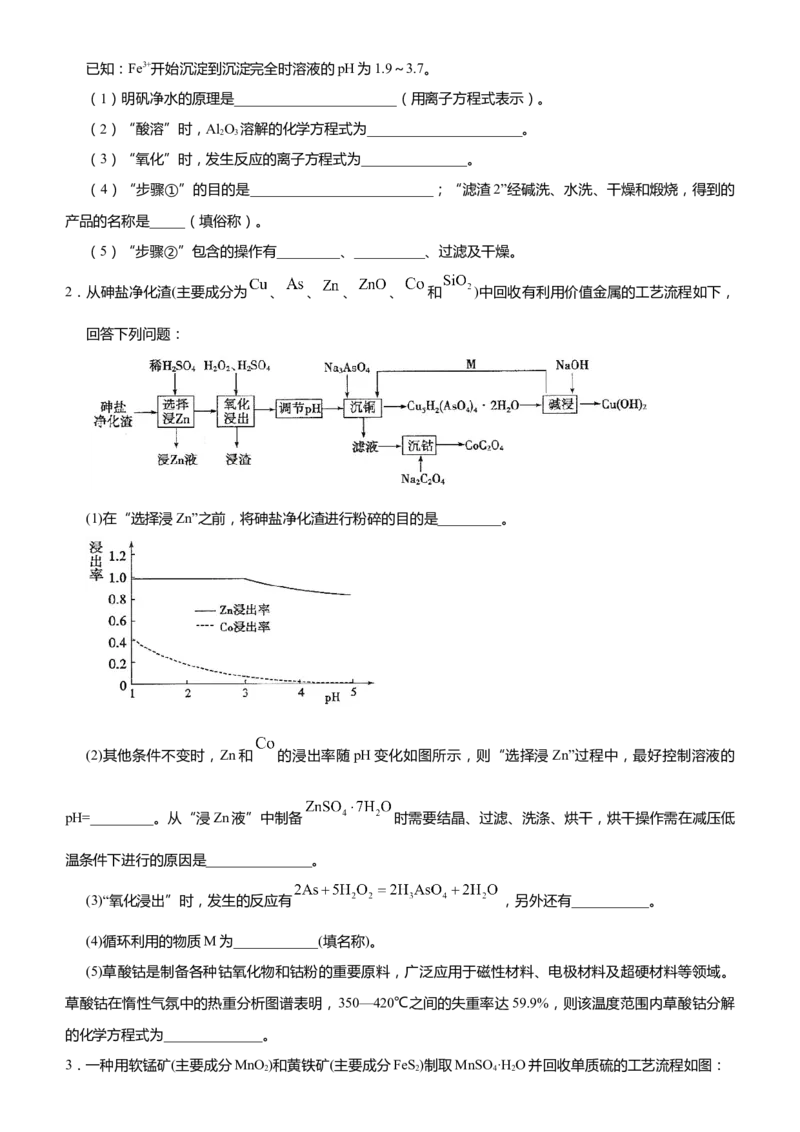
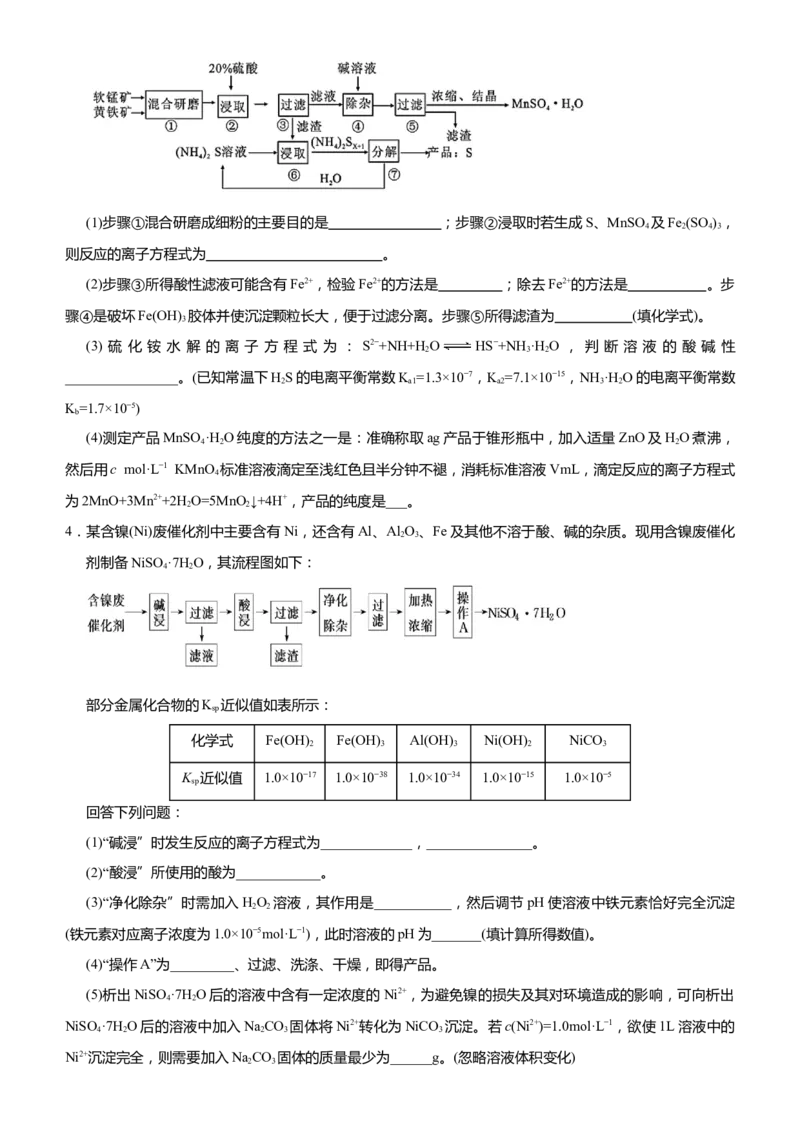
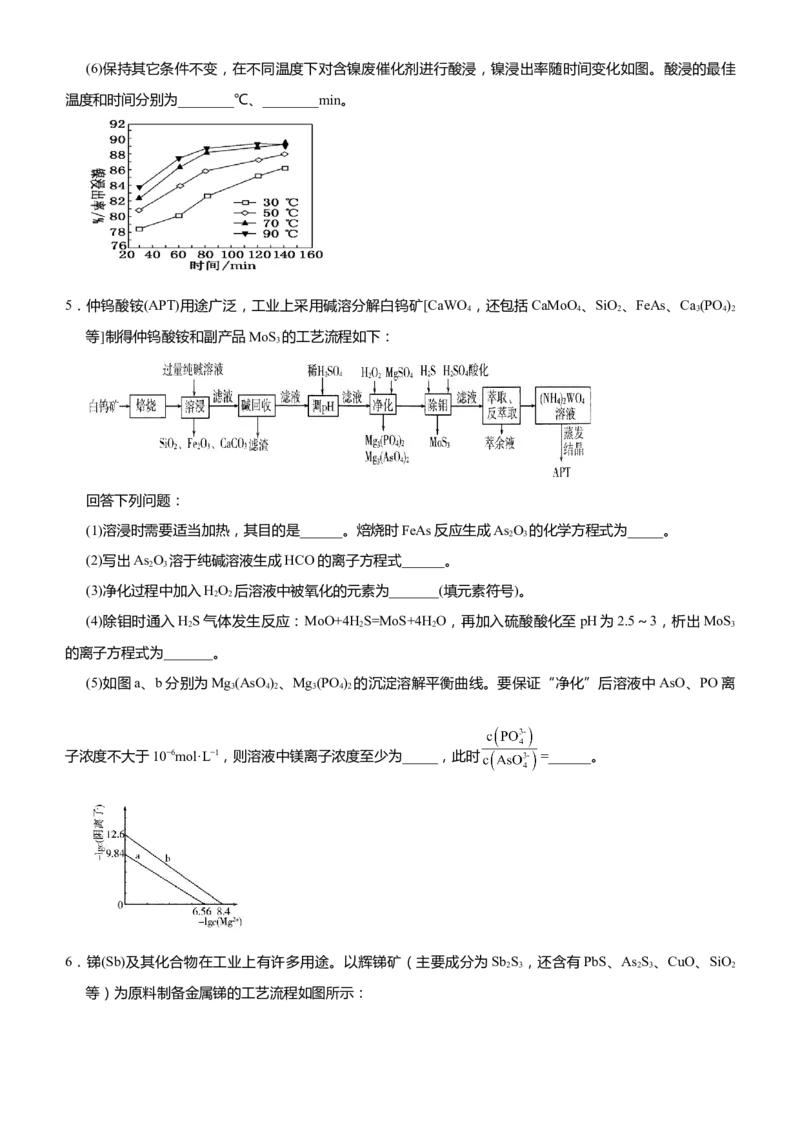
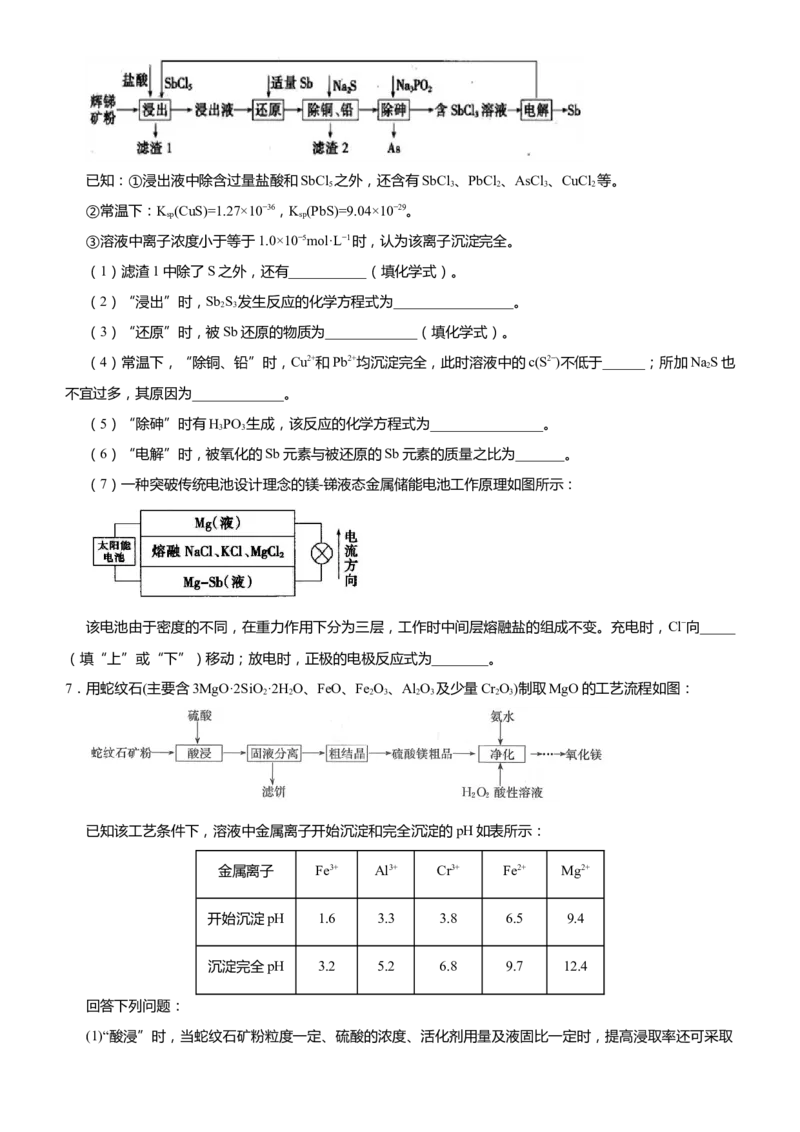
文档内容
专题 十
化学工艺流程
××
命 题 趋 势
全国卷化学试题的考查中,工艺流程题已成为核心题型。此类题目信息含量多,难度大。选择的素材往
往来自于实际的生产工艺,以符合高中学生知识和能力要求的方式呈现,以流程图的形式给出。工艺流程题
以化学产品的工业生产流程为载体,联系氧化还原反应原理、电离平衡和沉淀溶解平衡理论、电化学理论、
物质制备和分离、绿色化学知识,考查学生综合分析和解决问题的能力,高度体现了化学学科核心素养,是
高考化学试题最大点和热点。
Ⅰ.客观题
化工生产流程相结合以客观题形式呈现,考查物质制备和分离,绿色化学,盐类水解、溶解平衡、电化
学原理等知识的应用。
Ⅱ.主观题
以流程图、表格、图像的形式出现考查对关键信息的提取和处理,考查措施、成分、物质、化学方程式
的书写、叙述实验操作和步骤、分析操作目的、数据分析和处理结果。
考 点 清 单
一、盐溶液的分离提纯方法:结晶法
结晶法有蒸发结晶和冷却结晶两种方法,大多数同学通过一轮的复习已经明白纯物质溶液要得到晶体的
方法,难点在于混合溶液得到晶体的操作。
(1)纯物质溶液得到晶体:蒸发结晶(NaCl型:溶解度随温度变化小的物质);
蒸发浓缩(至有晶膜出现为止),冷却结晶(KNO 型:溶解度随温度变化大的物质和含有结晶水的晶体)
3
(2)混合溶液(分离A和B):要得到溶解度受温度变化小的溶质:蒸发结晶,趁热过滤要得到溶解度
受温度变化大的物质和含有结晶水的晶体:蒸发浓缩,冷却结晶,过滤
二、预处理的各种方法
工艺流程中的预处理分析进行分类,并形成一定的答题模板。
(1) 粉碎或研磨:增大固液(或固气或固固)接触面积,加快反应(溶解)速率,增大原料的转化率
(或浸取率)。
(2) 煅烧或灼烧:不易转化的物质转为容易提取的物质:其他矿转化为氧化物;除去有机物;除去热不稳定的杂质
(3) 酸浸:溶解、去氧化物(膜)、调节pH促进水解(沉淀)
(4)碱溶:去油污,去铝片氧化膜,溶解铝、二氧化硅,调节pH促进水解(沉淀)
(5)循环利用的物质:同学理解物质循环利用的目的:节能减排,“绿色化学”,降低成本等;
生产问题中提炼出:一定不会用于循环的物质:目标产物,杂质,可以用于循环的物质:辅助试剂、母
液。
三、控制温度的目的
1、加热:加快反应速率或溶解速率;促进平衡向吸热方向移动;除杂,除去热不稳定的杂质,如
NaHCO 、Ca(HCO )z、KMnO 、I、NH Cl等物质;使沸点相对较低的原料气化。
3 3 4 2 4
2、降温:防止某物质在高温时会溶解(或分解);使化学平衡向着题目要求的方向移动(放热方向);使某
个沸点较高的产物液化,使其与其他物质分离;降低晶体的溶解度,减少损失。
3、控温:(用水浴或油浴控温)
防止某种物质温度过高时会分解或挥发;为了使某物质达到沸点挥发出来;使催化剂的活性达到最好;
防止副反应的发生:降温或减压可以减少能源成本,降低对设备的要求,达到绿色化学的要求。
四、注重文字叙述的规范性
1、洗涤沉淀:往漏斗中加入蒸馏水至浸没沉淀,待水自然流下后,重复以上操作2~3次。
2、从溶液中得到晶体:蒸发浓缩—冷却结品—过滤—洗涤—干燥。
3、在写某一步骤是为了除杂时,应该注明“是为了除去 XX杂质”,只写“除杂”等一类万金油式的回
答是不给分的。
4、检验沉淀是否洗涤干净:取最后一次洗涤液少许于试管中,逐滴滴加XX试剂,振荡,若没有……现
象,则沉淀洗涤干净。
5、检验是否沉淀完全:
表达一:静置,往上层清夜中继续滴加XX试剂
表达二:过滤,取滤液少许于试管中,滴加XX试剂
五、高频问题:注意答题技巧
1、“浸出”步骤中,为提高镁的浸出率,可采取的措施有:适当提高反应温度、增加浸出时间,加入过
量硫酸,边加硫酸边搅拌。
2、如何提高吸收液和SO 反应速率:适当提高温度、增大吸收液、增大SO 与吸收液的接触面积或搅
2 2
拌。
3、从溶液中得到晶体:蒸发浓缩-冷却结晶-过滤-洗涤-干燥。
4、过滤用到的三个玻璃仪器:普通漏斗、玻璃棒、烧杯。
5、过滤后滤液仍然浑浊的可能的操作原因:玻璃棒下端靠在滤纸的单层处,导致滤纸破损:漏斗中液面
高于滤纸边缘。6、沉淀洗涤操作:往漏斗中(工业上改为往过滤器中)加入蒸馏水至没没沉淀,待水自然流下后,重复以
上操作2-3次。
7、检验沉淀Fe(OH) 是否洗涤干净(含SO):取最后一次洗涤液,加入BaCl 溶液,若有白色沉淀则说明
3 2
未洗涤干净,若无白色沉淀则说明洗涤干净。
8、如何从MgCl ·6HO中得到无水MgCl :在干燥的HCl气流中加热,干燥的HCl气流中抑制了MgCl
2 2 2 2
的水解,且带走MgCl ·6HO受热产生的水汽。
2 2
10、CuCl 中混有Fe3+加何种试剂调pH值:CuO、Cu(OH) 、CuCO 、Cu (OH) CO 。原因:加CuO消耗
2 2 3 2 2 3
溶液中的H+的,促进Fe3+的水解,生成Fe(OH) 沉淀析出。
3
11、调pH值使得Cu2+(4.7-6.2)中的Fe3+(2.1-3.2)沉淀,pH值范围是:3.2~4.7。原因:调节溶液的pH值至
3.2-4.7,使Fet全部以Fe(OH) 沉淀的形式析出而Cu2+不沉淀,且不会引入新杂质。
3
12、产品进-步提纯的操作:重结晶。
13、趁热过滤的原因及操作:减少过滤时间、保持过滤温度,防止xx杂质析出或防止降温过程中xx析
出而损耗;操作:已预热的布氏漏斗趁热抽滤。
14、水浴加热的好处:受热均匀,温度可控,且温度不超过100℃
15、减压蒸发(小心烘干):常压蒸发温度过高,xx易分解或者减压蒸发降低了蒸发温度,可以防止xx分
解。
16、Mg(OH) 沉淀中混有Ca(OH) 应怎样除去:加入MgCl 溶液,充分搅拌,过滤,沉淀用蒸馏水水洗
2 2 2
涤。
17、蒸发浓缩用到的主要仪器有__、烧杯、酒精灯等:蒸发皿、玻璃棒。还有取蒸发皿用坩埚钳。
18、不用其它试剂,检查NH Cl产品是否纯净的方法及操作是:加热法:取少量氯化铵产品于试管底
4
部,加热,若试管底部无残留物,表明氯化铵产品纯净。
19、检验NH的方法是:取xx少许,加入NaOH溶液后加热,生成的气体能使润湿的红色石蕊试纸变
蓝。
20、过滤的沉淀欲称重之前的操作:过滤,洗涤,干燥,(在干燥器中)冷却,称重。
21、“趁热过滤”后,有时先往滤液中加入少量水,加热至沸,然后再“冷却结晶”:稀释溶液,防止
降温过程中xx析出,提高产品的纯度。
22、检验Fe(OH) 是否沉淀完全的试验操作是:取少量上层清液或过滤后的滤液,滴加几滴 KSCN溶
3
液,若不出现血红色,则表明Fe(OH) 沉淀完全。
3
23、检验滤液中是否含有Fe3+的方法是:答:滴入少量KSCN溶液,若出现血红色,则证明有Fe3+(或加
NaOH,根据情况而定)。
24、检验溶液中是否含有Fe2+的方法是:答:滴加铁氰化钾溶液。精 题 集 训
(70分钟)
经典训练题
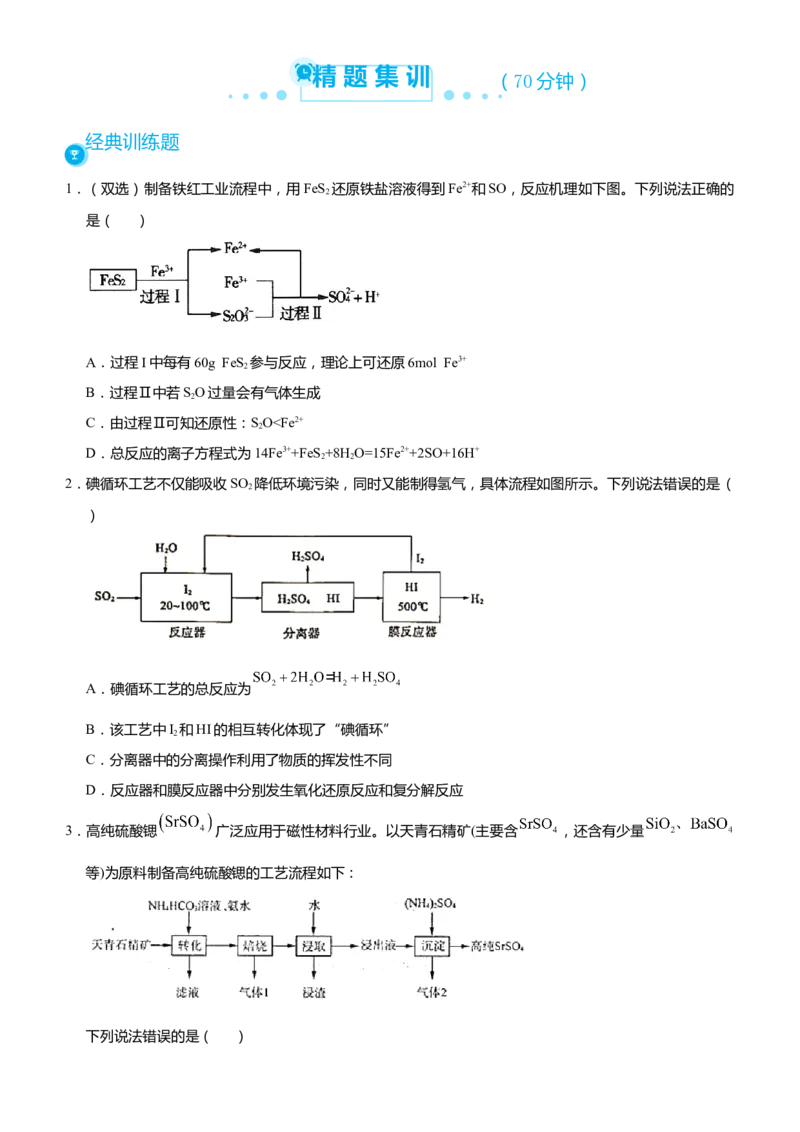
1.(双选)制备铁红工业流程中,用FeS 还原铁盐溶液得到Fe2+和SO,反应机理如下图。下列说法正确的
2
是( )
A.过程I中每有60g FeS 参与反应,理论上可还原6mol Fe3+
2
B.过程Ⅱ中若SO过量会有气体生成
2
C.由过程Ⅱ可知还原性:SO