文档内容
绝密 ★ 启用前 3.为实现随处可上网,中国发射了“中星16号”卫星。NH ClO 是火箭的固体燃料,发生反应为
4 4
2NH ClO ====N↑+Cl↑+2O ↑+4H O,N 代表阿伏加德罗常数,下列说法正确的是
4 4 2 2 2 2 A
2021 年普通高等学校招生全国统一考试
班级
A.1mol NH ClO 固体中含有N 个NH ClO 分子
4 4 A 4 4
姓名
化 学 B.反应转移2.8mol电子时产生氯气为4.48L
准考证号
C.常温常压下,14g N 分子中含有的中子数为7N
2 A
注意事项:
考场号
D.反应中还原产物分子数与氧化产物分子总数之比为1∶1
此卷只
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答题前,考生务必将自己
装订座不位密号封
4.不能正确表示下列反应的离子方程式是
的姓名、考生号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题的答案后,用铅笔把答题卡上对应题目的答案标号涂黑,
A.在氯化亚铁溶液中通入氧气:4Fe2++O +4H+=4Fe3++2H O
2 2
如需改动,用橡皮擦干净后,再选涂其他答案标号。写在试卷上无效。
B.用石墨作阴极、铁作阳极电解饱和食盐水:2Cl−+2H O=====2OH−+Cl↑+H ↑
3.回答第Ⅱ卷时,将答案填写在答题卡上,写在试卷上无效。 2 2 2
4.考试结束,将本试卷和答题卡一并交回。
C.向稀硝酸中加入少量FeS:
可能用到的相对原子质量:H 1 C 12 O 16 F 19 Al 27 Cl 35.5 K 39 Cu 64 Ba 137
D.NaAlO 溶液中通入过量CO:AlO+CO+2H O=Al(OH) ↓+HCO
2 2 2 2 3
5.下列叙述中不正确的是
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
A.核酸是生命体遗传信息的分子载体,结构中含有磷酯键
1.新型材料在各领域中的应用越来越广泛,下列相关说法错误的是
B.氨基酸种类很多,任何一种氨基酸至少含有两个或者两个以上官能团
A.嫦娥5号上升起的“高科技国旗”具有“耐热性、耐高低温、抗静电”等特点,它是以高性
C.我国最新研制免费注射的新冠疫苗,其主要成分含有蛋白质
能的芳纶纤维材料为主的复合材料
D.用来煎炸食物的花生油和牛油都是饱和高级脂肪酸甘油酯,可发生皂化反应
B.将脱脂棉加入深蓝色的铜氨溶液中可以制备铜氨纤维
6.药物H的结构简式如图所示,下列有关药物H的说法正确的是
C.飞机上所用由碳纤维和环氧树脂合成的材料属于复合材料
D.以高纯硅制成的光导纤维内窥镜可直接窥视有关器官部位的变化
2.下列关于化学用语的表述错误的是
A.分子式为C H NOCl
A.BF 的电子式: B.HS的结构式:H—S—H 16 10 2 2
3 2
B.该物质苯环上的一氯代物有6种
C.碱性条件下水解产物酸化后都能与NaHCO 溶液反应
3
C.O2−的结构示意图: D.乙烯的比例模型:
D.1mol该物质最多能与8mol氢气加成
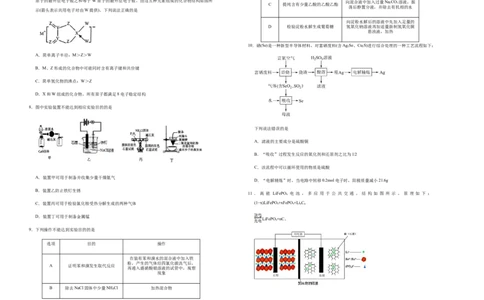
7.X、Y、Z、W、M是原子序数依次增大的短周期元素,Z的一种单质具有漂白性,X和Y二者原子的最外层电子数之和等于W原子的最外层电子数。由这五种元素组成的化合物结构如图所
向混合液中加入过量NaCO 溶液,振
C 提纯含有少量乙酸的乙酸乙酯 2 3
荡后静置分液,并除去有机相的水
示(箭头表示共用电子对由W提供)。下列说法正确的是
向淀粉水解后的溶液中先加入足量的
D 检验淀粉水解生成葡萄糖 氢氧化钠溶液再加适量新制氢氧化铜
悬浊液,加热
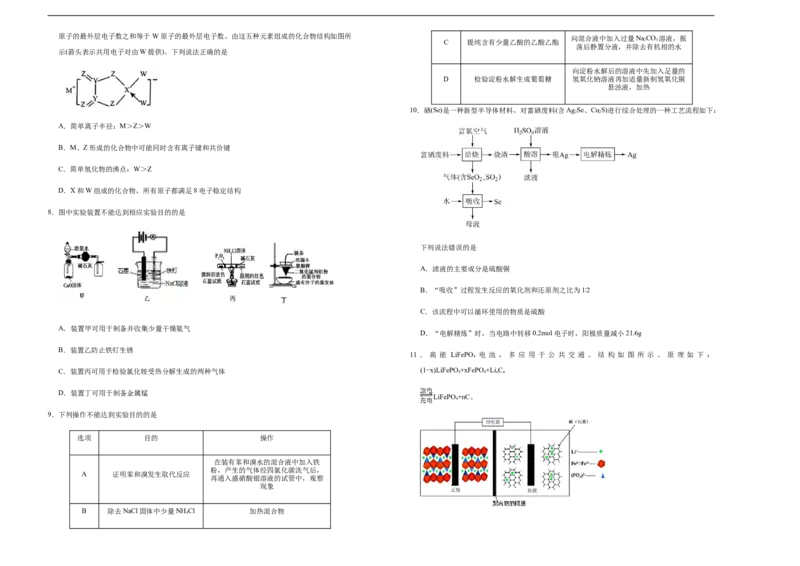
10.硒(Se)是一种新型半导体材料,对富硒废料(含Ag Se、Cu S)进行综合处理的一种工艺流程如下:
2 2
A.简单离子半径:M>Z>W
B.M、Z形成的化合物中可能同时含有离子键和共价键
C.简单氢化物的沸点:W>Z
D.X和W组成的化合物,所有原子都满足8电子稳定结构
8.图中实验装置不能达到相应实验目的的是
下列说法错误的是
A.滤液的主要成分是硫酸铜
B.“吸收”过程发生反应的氧化剂和还原剂之比为1∶2
C.该流程中可以循环使用的物质是硫酸
A.装置甲可用于制备并收集少量干燥氨气
D.“电解精炼”时,当电路中转移0.2mol电子时,阳极质量减小21.6g
B.装置乙防止铁钉生锈
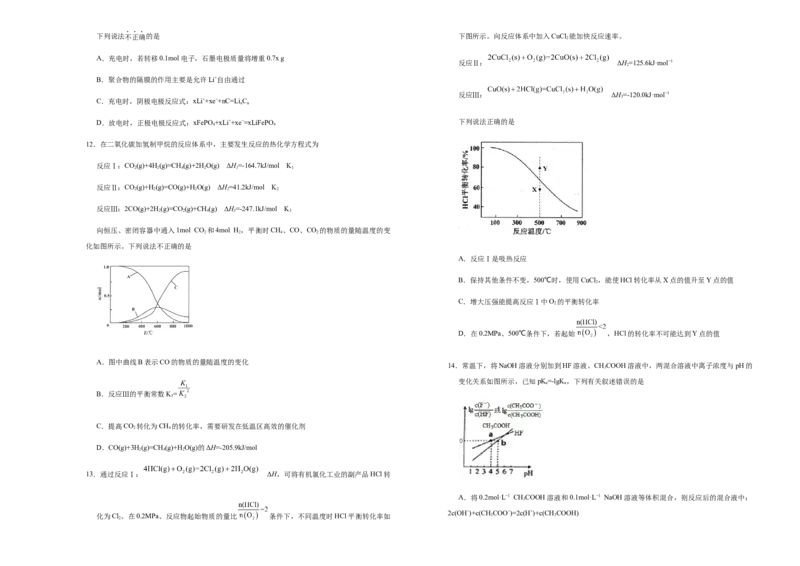
11 . 高 能 LiFePO 电 池 , 多 应 用 于 公 共 交 通 。 结 构 如 图 所 示 。 原 理 如 下 :
4
C.装置丙可用于检验氯化铵受热分解生成的两种气体 (1−x)LiFePO 4 +xFePO 4 +Li x C n
D.装置丁可用于制备金属锰
LiFePO +nC。
4
9.下列操作不能达到实验目的的是
选项 目的 操作
在装有苯和溴水的混合液中加入铁
粉,产生的气体经四氯化碳洗气后,
A 证明苯和溴发生取代反应
再通入盛硝酸银溶液的试管中,观察
现象
B 除去NaCl固体中少量NH Cl 加热混合物
4下列说法不正确的是 下图所示。向反应体系中加入CuCl 能加快反应速率。
2
A.充电时,若转移0.1mol电子,石墨电极质量将增重0.7x g
反应Ⅱ: ΔH=125.6kJ·mol−1
2
B.聚合物的隔膜的作用主要是允许Li+自由通过
反应Ⅲ: ΔH=-120.0kJ·mol−1
3
C.充电时,阴极电极反应式:xLi++xe−+nC=Li C
x n
D.放电时,正极电极反应式:xFePO +xLi++xe−=xLiFePO 下列说法正确的是
4 4
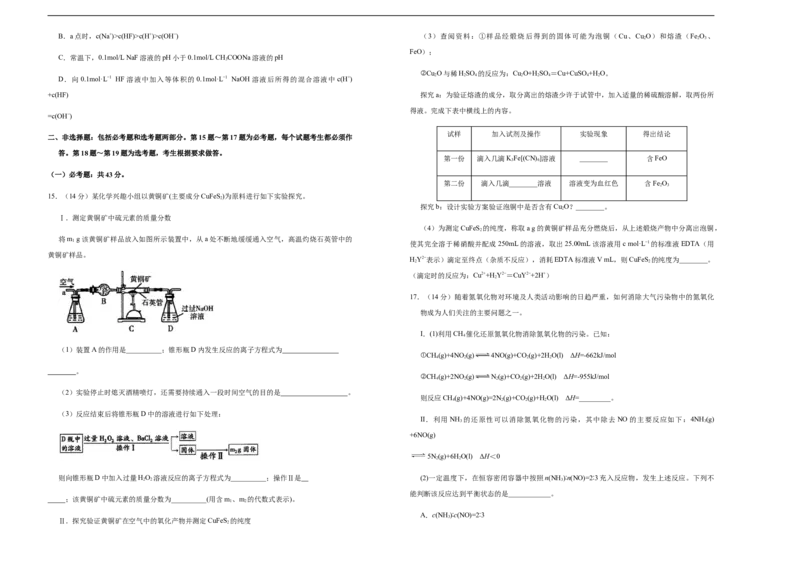
12.在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ:CO(g)+4H(g)=CH (g)+2HO(g) ΔH=-164.7kJ/mol K
2 2 4 2 1 1
反应Ⅱ:CO(g)+H(g)=CO(g)+HO(g) ΔH=41.2kJ/mol K
2 2 2 2 2
反应Ⅲ:2CO(g)+2H(g)=CO (g)+CH (g) ΔH=-247.1kJ/mol K
2 2 4 3 3
向恒压、密闭容器中通入1mol CO 和4mol H ,平衡时CH 、CO、CO 的物质的量随温度的变
2 2 4 2
化如图所示。下列说法不正确的是
A.反应Ⅰ是吸热反应
B.保持其他条件不变,500℃时,使用CuCl ,能使HCl转化率从X点的值升至Y点的值
2
C.增大压强能提高反应Ⅰ中O 的平衡转化率
2
D.在0.2MPa、500℃条件下,若起始 ,HCl的转化率不可能达到Y点的值
A.图中曲线B表示CO的物质的量随温度的变化
14.常温下,将NaOH溶液分别加到HF溶液、CHCOOH溶液中,两混合溶液中离子浓度与pH的
3
变化关系如图所示,已知pK=-lgK,下列有关叙述错误的是
a a
B.反应Ⅲ的平衡常数K=
3
C.提高CO 转化为CH 的转化率,需要研发在低温区高效的催化剂
2 4
D.CO(g)+3H(g)=CH (g)+HO(g)的ΔH=-205.9kJ/mol
2 4 2
13.通过反应Ⅰ: ΔH,可将有机氯化工业的副产品HCl转
A.将0.2mol·L−1 CHCOOH溶液和0.1mol·L−1 NaOH溶液等体积混合,则反应后的混合液中:
3
2c(OH−)+c(CH COO−)=2c(H+)+c(CH COOH)
化为Cl 。在0.2MPa、反应物起始物质的量比 条件下,不同温度时HCl平衡转化率如 3 3
2B.a点时,c(Na+)>c(HF)>c(H+)>c(OH−) (3)查阅资料:①样品经煅烧后得到的固体可能为泡铜(Cu、Cu O)和熔渣(Fe O 、
2 2 3
FeO);
C.常温下,0.1mol/L NaF溶液的pH小于0.1mol/L CH COONa溶液的pH
3
②Cu O与稀HSO 的反应为:Cu O+HSO =Cu+CuSO +H O。
2 2 4 2 2 4 4 2
D.向0.1mol·L−1 HF溶液中加入等体积的 0.1mol·L−1 NaOH溶液后所得的混合溶液中 c(H+)
+c(HF) 探究a:为验证熔渣的成分,取分离出的熔渣少许于试管中,加入适量的稀硫酸溶解,取两份所
得液。完成下表中横线上的内容。
=c(OH−)
试样 加入试剂及操作 实验现象 得出结论
二、非选择题:包括必考题和选考题两部分。第15题~第17题为必考题,每个试题考生都必须作
答。第18题~第19题为选考题,考生根据要求做答。
第一份 滴入几滴KFe[(CN) ]溶液 ________ 含FeO
3 6
(一)必考题:共43分。
第二份 滴入几滴________溶液 溶液变为血红色 含Fe O
2 3
15.(14分)某化学兴趣小组以黄铜矿(主要成分CuFeS)为原料进行如下实验探究。
2
探究b:设计实验方案验证泡铜中是否含有Cu O?________。
2
Ⅰ.测定黄铜矿中硫元素的质量分数
(4)为测定CuFeS 的纯度,称取a g的黄铜矿样品充分燃烧后,从上述煅烧产物中分离出泡铜,
2
将m g该黄铜矿样品放入如图所示装置中,从a处不断地缓缓通入空气,高温灼烧石英管中的
1 使其完全溶于稀硝酸并配成250mL的溶液,取出25.00mL该溶液用c mol·L−1的标准液EDTA(用
黄铜矿样品。
HY2−表示)滴定至终点(杂质不反应),消耗EDTA标准液V mL,则CuFeS 的纯度为________。
2 2
(滴定时的反应为:Cu2++H Y2−=CuY2−+2H+)
2
17.(14分)随着氮氧化物对环境及人类活动影响的日趋严重,如何消除大气污染物中的氮氧化
物成为人们关注的主要问题之一。
I.(1)利用CH 催化还原氮氧化物消除氮氧化物的污染。已知:
4
(1)装置A的作用是__________;锥形瓶D内发生反应的离子方程式为
①CH(g)+4NO (g) 4NO(g)+CO (g)+2HO(l) ΔH=-662kJ/mol
4 2 2 2
。
②CH (g)+2NO (g) N(g)+CO (g)+2HO(l) ΔH=-955kJ/mol
4 2 2 2 2
(2)实验停止时熄灭酒精喷灯,还需要持续通入一段时间空气的目的是 。
则反应CH(g)+4NO(g)=2N (g)+CO (g)+HO(l) ΔH=_________。
4 2 2 2
(3)反应结束后将锥形瓶D中的溶液进行如下处理:
II.利用NH 的还原性可以消除氮氧化物的污染,其中除去 NO的主要反应如下:4NH (g)
3 3
+6NO(g)
5N(g)+6HO(l) ΔH<0
2 2
则向锥形瓶D中加入过量HO 溶液反应的离子方程式为__________;操作Ⅱ是 (2)一定温度下,在恒容密闭容器中按照n(NH )∶n(NO)=2∶3充入反应物,发生上述反应。下列不
2 2 3
能判断该反应达到平衡状态的是____________。
;该黄铜矿中硫元素的质量分数为__________(用含m、m 的代数式表示)。
1 2
A.c(NH )∶c(NO)=2∶3
3
Ⅱ.探究验证黄铜矿在空气中的氧化产物并测定CuFeS 的纯度
2B.1mol N—H键断裂的同时,断裂1mol O—H键 (4)“系列操作”包含___________。
C.容器内压强不变 (5)“合成”时发生反应的化学方程式为___________,“萃取”过程可表示为Fe (SO )(水层)
2 4 3
+6RH(有机层) 2R Fe(有机层)+3HSO (水层),由有机层获取 Fe (SO ) 溶液的操作是
3 2 4 2 4 3
D.容器内混合气体的密度不变
___________。
(3)实验测得v =k ·c4(NH )·c6(NO),v =k ·c5(N )(k 、k 为速率常数,只与温度有关)。
正 正 3 逆 逆 2 正 逆
(6)测定产品纯度:准确称量mg产品,加入高氯酸充分转化后,加入稍过量 EDTA络合Al3+;
①达到平衡后,仅降低温度,k 增大的倍数_________(填“>”“<”或“=”)k 增大的倍数。
正 逆 过量的EDTA用c mol·L−1 Pb(NO ) 标准溶液滴定,达到滴定终点时消耗标准液体积为VmL;向滴
3 2 1
②若在1L的恒容密闭容器中充入2mol CO和3mol NO,在一定温度下达到平衡时,CO的转化 定后溶液中加入NH 4 F形成AlF同时释放出EDTA,继续用相同Pb(NO 3 ) 2 标准溶液滴定,消耗标准
率为80%,则k 正 ︰k 逆 =_____L/mol(用数字表达式表示)。 液体积为V 2 mL。(已知:EDTA与Al3+、Pb2+反应的物质的量之比均为1∶1,杂质不参加反应)
Ⅲ.利用燃料电池的原理来处理氮氧化物是一种新方向。装置如图所示,在处理过程中石墨电 则产品中钾冰晶石的纯度为 。
极I上反应生成一种氧化物Y。
(二)选考题(共 15分,请考生从2道题中任选一题作答,如果多做,则按所做的第一题计
分。)
19.人类使用铜和它的合金具有悠久的历史,铜及其化合物在电子工业、材料工业、工农业生产及
日常生活方面用途非常广泛。试回答下列问题。
(1)Cu+的核外电子排布式为___________________。
(2)CuSO 和Cu(NO ) 是自然界中重要的铜盐,SO的立体构型是________,S、O、N三种元
4 3 2
(4)石墨II电极为______(填“正”或“负”)极,该电极反应为______。
素的第一电离能由大到小为____________。
(5)写出该电池反应的方程式______。
(3)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反
18.(15分)钾冰晶石(K AlF)是用作电解铝工艺的助熔剂,已知KAlF 微溶于水。以超细含铝废渣
3 6 3 6 应,其原因是_______________,反应的离子方程式为_____________________。
(主要成分Al O,含有少量Fe O、PbO杂质)为原料制备钾冰晶石的工艺流程如图:
2 3 3 4
(4)丁炔铜是一种优良的催化剂,已知:CH≡CH+2HCHO OHC-CHCHOH。则
2 2
OHC-CHCHOH中碳原子杂化方式有__________。
2 2
(5)利用CuSO 和NaOH制备的Cu(OH) 检验醛基时,生成红色的Cu O,其晶胞结构如图所
4 2 2
示。
回答下列问题:
(1)为了提高“酸浸”时速率,可以采取的措施有:_________、________(填写2条)。
(2)滤渣是___________。
(3)“氧化”过程中HO 的作用是___________(用离子方程式表示),反应液的pH控制在较低
2 2
水平,原因是___________。①该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为( , , )。则D原
子的坐标参数为________,它代表________原子。
②若Cu O晶体密度为d g·cm−3,晶胞参数为a pm,则阿伏加德罗常数值N =________。
2 A
20.(15分)芳香族化合物I在消灭或抑制植物生长方面具有很高的选择性,其合成路线如下:
已知:R CHO+R NH R CH=N-R
1 2 2 1 2
回答下列问题:
(1)A中含有的官能团为___________,由B生成C的反应类型为___________。
(2)D的结构简式为___________,H的结构简式为___________。
(3)由E生成G的化学方程式为___________。
(4)芳香族化合物J的相对分子质量比A少14,且发生银镜反应,J的同分异构体有 种。其
中核磁共振氢谱有四组峰,且峰面积之比为1∶2∶2∶1的结构简式为___________。
(5) 参 照 上 述 合 成 路 线 , 设 计 由 和 为 原 料 制 备
的合成路线:___________(无机试剂任选)。