文档内容
培优训练4:工艺流程题专项训练
1.(2018·江苏化学,16)以高硫铝土矿(主要成分为Al O 、Fe O 、SiO ,少量FeS 和
2 3 2 3 2 2
金属硫酸盐)为原料,生产氧化铝并获得Fe O 的部分工艺流程如下:
3 4
(1)焙烧过程均会产生 SO ,用 NaOH 溶液吸收过量 SO 的离子方程式为
2 2
____________________________________________________________________。
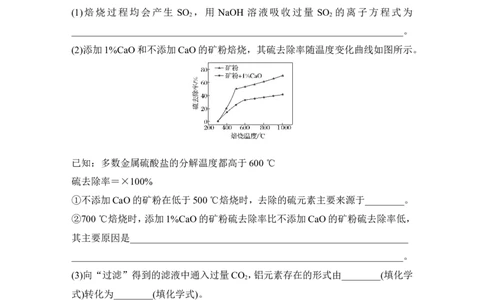
(2)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如图所示。
已知:多数金属硫酸盐的分解温度都高于600 ℃
硫去除率=×100%
①不添加CaO的矿粉在低于500 ℃焙烧时,去除的硫元素主要来源于________。
②700 ℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,
其主要原因是_________________________________________________________
____________________________________________________________________。
(3)向“过滤”得到的滤液中通入过量CO ,铝元素存在的形式由________(填化学
2
式)转化为________(填化学式)。
(4)“过滤”得到的滤渣中含大量的Fe O 。Fe O 与FeS 混合后在缺氧条件下焙烧
2 3 2 3 2
生成Fe O 和SO ,理论上完全反应消耗的n(FeS )∶n(Fe O )=________。
3 4 2 2 2 3
解析 (1)二氧化硫是酸性氧化物,少量二氧化硫与 NaOH 溶液反应生成正盐
Na SO ,过量二氧化硫与NaOH溶液反应生成NaHSO 。(2)①根据高硫铝土矿的
2 3 3
成分中含FeS 和金属硫酸盐,而已知多数金属硫酸盐的分解温度都高于600 ℃,
2
如果不添加CaO在低于500 ℃焙烧,则去除的硫元素主要来源于FeS ,具体的反
2
应原理为4FeS +11O =====2Fe O +8SO 。②添加的CaO吸收SO 生成CaSO ,
2 2 2 3 2 2 3CaSO 易被空气中的氧气氧化为 CaSO 。根据题目所给“多数金属硫酸盐的分解
3 4
温度都高于600 ℃”,可知700 ℃时CaSO 可能未分解或未完全分解而留在矿粉
4
中,从而导致添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低。(3)
高硫铝土矿中的氧化铝溶于 NaOH生成NaAlO :Al O +2NaOH===2NaAlO +
2 2 3 2
H O;向NaAlO 溶液中通入过量的二氧化碳,生成氢氧化铝:CO (过量)+2H O+
2 2 2 2
NaAlO ===Al(OH) ↓+NaHCO 。(4)根据得失电子守恒可知 FeS 与Fe O 的物质
2 3 3 2 2 3
的量之比为1∶16。
答案 (1)OH-+SO ===HSO
2
(2)①FeS ②硫元素转化为CaSO 而留在矿粉中
2 4
(3)NaAlO Al(OH)
2 3
(4)1∶16
2.(2019·苏州市高三期初调研,16)以白云石(化学式表示为MgCO ·CaCO )为原料
3 3
制备氢氧化镁的工艺流程如下:
已知:①白云石加热过程中,固体失重百分比与温度的关系如图所示:
②K [Mg(OH) ]=5. 61×10-12。
sp 2
(1) 根 据 流 程 图 判 断 白 云 石 “ 轻 烧 ” 后 固 体 产 物 的 主 要 成 分 是
_____________________________________________________________________
(填化学式)。结合图判断“轻烧” 温度应不超过________。
(2)“加热反应”的化学方程式为_____________________________________。
(3)沉淀过程控制溶液的pH为9.5,此时溶液中c(Mg2+)=________。
(4)该工艺中可以循环使用的物质是___________________________________(填化
学式)。(5)传统工艺将白云石分解为氧化镁和氧化钙后提取,从环境保护的角度分析,该
工艺采用轻烧白云石的方法,其优点是____________________________________。
解析 流程分析白云石主要成分为 MgCO ·CaCO 轻烧,从过滤中可以得到
3 3
CaCO 来进行判断,分解的只是碳酸镁,研磨加入水和硫酸铵加热,硫酸铵和氧化
3
镁反应生成氨气、硫酸镁和水,过滤加入氨水生成氢氧化镁沉淀,过滤得到氢氧化
镁固体;则
(1)从过滤中可以得到CaCO 来进行判断分解的只是碳酸镁,分解生成氧化镁,因
3
此白云石“轻烧”后固体产物的主要成份CaCO 、MgO;从表中可以看出,温度低
3
于540 ℃时,物质不分解,高于840℃时,碳酸钙和碳酸镁都分解,因此该温度不超
过700 ℃;(2)加热的过程是放出氨气的过程,该过程中因为氧化镁跟水反应很少,
因此涉及到的反应应该为:(NH ) SO +MgO=====MgSO +2NH ↑+H O;(3)依
4 2 4 4 3 2
据溶度积常数计算得到,沉淀过程溶液的pH=9.5,c(OH-)=10-4.5 mol/L,c(Mg2+)
=K [Mg(OH) ]/c2(OH-)=5.61×10-12/(10-4.5)2=5.61×10-3mol/L;(4)该工艺中可
sp 2
以循环使用的物质是参加反应过程,反应后又生成的物质,流程图分析判断
(NH ) SO 、NH 或NH ·H O可以循环使用;(5)分析流程可知,传统工艺将白云石
4 2 4 3 3 2
分解为氧化镁和氧化钙后提取,该工艺采用轻烧白云石的方法可以减少能源消耗、
便于CaCO 分离,同时也减少CO 排放。
3 2
答案 (1)CaCO 、MgO 700 ℃ (2) (NH ) SO +MgO===MgSO +2NH +H O
3 4 2 4 4 3 2
(3)5.61×10-3mol/L
(4) (NH ) SO 、NH 或NH ·H O (5)减少能源消耗、减少CO 的排放、便于CaCO
4 2 4 3 3 2 2 3
分离
3.[(2018·厦门外国语学校5月适应性考试(最后压轴模拟),27)]
从废旧锂离子二次电池(主要成分为LiCoO ,还含有少量石墨和镀镍金属钢壳、铝
2
箔以及钙等杂质)中回收钴和锂的工艺流程如下:
回答下列问题:
(1)“ 碱 浸 ” 的 目 的 是____________________________________________________。
(2)“ 酸 浸 ” 过 程 中 LiCoO 发 生 反 应 的 离 子 方 程 式 为 :
2
______________________________________________________________________
_____________________________________________________________________
,
浸渣中含有的主要成分是________。
(3)“ 萃 取 净 化 ” 除 去 的 杂 质 离 子 有 Ni2 + 外 , 还 有
_____________________________________________________________________。
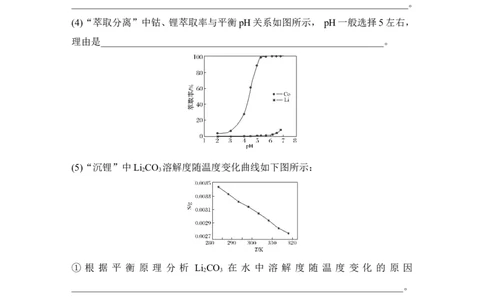
(4)“萃取分离”中钴、锂萃取率与平衡pH关系如图所示, pH一般选择5左右,
理由是__________________________________________________________。
(5)“沉锂”中Li CO 溶解度随温度变化曲线如下图所示:
2 3
① 根 据 平 衡 原 理 分 析 Li CO 在 水 中 溶 解 度 随 温 度 变 化 的 原 因
2 3
____________________________________________________________________。
②为获得高纯Li CO ,提纯操作依次为趁热过滤、________、干燥。
2 3
③若“沉锂”中c(Li+)=1.0 mol·L-1,加入等体积等浓度Na CO 溶液,此时实验
2 3
所得沉锂率为________。(已知Li CO 的K 为9.0×10-4)
2 3 sp
解析 (1)“碱浸”的目的是用氢氧化钠溶液将其中的Al溶解。
(2)LiCoO 中Co为+3价,最后生成的CoSO 中Co为+2价,所以酸浸这一步中,
2 4
加入H O 的目的是为了将+3价Co还原为+2价Co,所以反应的离子方程式为:
2 2
2 LiCoO + H O + 6H+===2Li++2Co2+ + O ↑ + 4 H O。浸渣中主要是不与
2 2 2 2 2酸反应的石墨以及生成的硫酸钙沉淀。
(3)整个提取的过程中需要除去的杂质是Ca、Fe、Al、Ni;在前面的步骤中已经除去
了Al和Ca,所以萃取净化应该要除去Ni2+和Fe3+。
(4)由图示在pH为5左右的时候,Co和Li的萃取率差异最大,此时分离的效果最
好。
(5)①图中显示随着温度升高,碳酸锂的溶解度逐渐减小,所以推测该物质溶于水
的过程是放热的。
②提取的过程为趁热过滤,洗涤,干燥,所以答案为:洗涤。
③c(Li+)=1.0 mol·L-1,加入等体积等浓度Na CO 溶液,则碳酸钠的浓度也是
2 3
1.0 mol·L-1,加入的瞬间溶液体积转化为原来的2倍,浓度都是原来的一半,即
c(Li+)=c(CO)=0.5 mol·L-1,沉淀出碳酸锂,所以碳酸根过量1倍,剩余c(CO)=
0.25 mol·L-1,代入K 的计算式得到c(Li+)===0.06(mol/L)。因为两溶液混合的
sp
瞬间c(Li+)=0.5mol/L,所以沉锂率为(0.5-0.06)÷0.5=88%。
答案 (1)除去铝 (2)2LiCoO +H O +6H+===2Li++2Co2++O ↑ + 4H O
2 2 2 2 2
石墨、硫酸钙 (3)Fe3+
(4)分离效率最高
(5)①Li CO 溶解过程为放热反应 ②洗涤 ③88.0%
2 3
4.(2018·福州市高三下学期 5月模拟考试理综,28)辉铜矿石主要含有硫化亚铜
(Cu S)及少量脉石(SiO )。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下所示
2 2
(1) 写 出 “ 浸 取 ” 过 程 中 Cu S 溶 解 时 发 生 反 应 的 离 子 方 程 式 :
2
_____________________________________________________________________。
(2)“矿渣”中除了S以外,还有____________________________________(填化
学式);
“回收 S”过程中温度控制在 50~60 ℃之间,不宜过高或过低的原因是
____________________________________________________________________。
(3)“保温除铁”过程中,加入CuO的目的是______________________________;
“蒸发浓缩、冷却结晶”过程中,要用 HNO 溶液调节溶液的 pH,其理由是
3____________________________________________________________________。
(4)气体NO 与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应
x
的化学方程式为_____________________________________________________
__________________________________________________________________;
向“滤液M”中加入(或通入) ________(填下列选项代号),可得到另一种流程中
可循坏利用的物质。
a.铁 b.氯气 c.高锰酸钾
解析 考查化学工艺流程,(1)Cu S中Cu显+1价,S显-2价,都具有还原性,
2
FeCl 中 Fe3+具有强氧化性,根据流程,浸取发生的离子反应是 Cu S+4Fe3+
3 2
===2Cu2++4Fe2++S;(2)根据辉铜矿的成分,含有少量的脉石,SiO 不与FeCl 发
2 3
生反应,因此矿渣中还含有SiO ;苯的沸点较低,温度过高,苯易挥发,温度过低,
2
反应速率慢或溶解度小;(3)置换过程过滤后,得到固体物质是Cu和Fe,Cu和Fe
与硝酸反应生成Cu(NO ) 和Fe(NO ) ,Fe3+水解:Fe3++3H O Fe(OH) +
3 2 3 3 2 3
3H+,加入CuO的目的是调节pH,促使Fe3+水解,生成氢氧化铁沉淀;Cu(NO ) 溶
3 2
液中Cu2+发生水解,Cu2++2H O===Cu(OH) +2H+,加入硝酸,抑制Cu2+水解;
2 2
(4)氮的氧化物与氧气、H O反应生成HNO ,硝酸是循环利用的一种物质,该反应
2 3
的化学方程式为 4NO +(5-2x)O +2H O===4HNO ;置换中发生 Fe+
x 2 2 3
CuCl ===FeCl +Cu、Fe+2FeCl ===3FeCl ,滤液M中成分是FeCl ,根据流程图,
2 2 3 2 2
FeCl 是循环物质,即需要加入Cl ,把FeCl 氧化成FeCl ,故选项b正确。
3 2 2 3
答案 (1)Cu S+4Fe3+===2Cu2++4Fe2++S (2)SiO 温度过高苯易挥发,温度
2 2
过低硫的溶解速率(或溶解度)小 (3)提升溶液的pH,促进Fe3+水解生成Fe(OH)
3
沉淀 抑制Cu2+水解 (4)4NO +(5-2x)O +2H O===4HNO b
x 2 2 3
5.(2019·河南师范大学附属中学高三月考,27)铁的化合物有广泛用途,如碳酸亚
铁(FeCO )可作为补血剂,铁红(Fe O )可作为颜料。利用某硫酸厂产生的烧渣(主要
3 2 3
含Fe O 、FeO,还有一定量的SiO )制备FeCO 的流程如下:
2 3 2 3
(1)“酸溶”时加快反应速率的方法有________(写出一种)。
(2)①“还原”时,FeS 与H SO 不反应,Fe3+通过两个反应被还原,其中一个反应
2 2 4如下:
FeS +14Fe3++8H O===15Fe2++2SO+16H+,则另一个反应的离子方程式为
2 2
____________________________________________________________________。
② 加 入 FeS 还 原 后 , 检 验 Fe3 + 是 否 反 应 完 全 的 方 法 是
2
_____________________________________________________________________
_____________________________________________________________________
。
(3)①“ 沉 淀 ” 时 , 需 要 控 制 温 度 在 35 ℃ 以 下 , 其 可 能 原 因 是
_____________________________________________________________________。
② 所 得 FeCO 需 充 分 洗 涤 , 检 验 沉 淀 已 洗 净 的 方 法 是
3
_____________________________________________________________________
_____________________________________________________________________
。
(4)FeCO 浊液长时间暴露在空气中,会有部分固体表面变为红褐色,同时释放出
3
CO ,则与FeCO 反应的物质为________(填化学式)。
2 3
(5) 写 出 在 空 气 中 煅 烧 FeCO 制 备 高 纯 氧 化 铁 的 化 学 方 程 式 :
3
____________________________________________________________________。
FeCO 在空气中煅烧生成Fe O 时,也会生成FeO。现煅烧23.2 kg的FeCO ,得到
3 2 3 3
Fe O 和FeO的混合物15.84 kg,则Fe O 的质量为________ kg。
2 3 2 3
解析 烧渣(主要含Fe O 、FeO,还有一定量的SiO )用硫酸浸取,过滤后滤液中含
2 3 2
有硫酸铁、硫酸亚铁、未反应的硫酸,滤渣为二氧化硅,用二硫化亚铁还原Fe3+后
过滤,得滤液中含有硫酸亚铁,向滤液中加入碳酸铵,过滤得碳酸亚铁,滤液中含
有硫酸铵、碳酸铵。
(5) 在 空 气 中 煅 烧 FeCO 制 备 高 纯 氧 化 铁 的 化 学 方 程 式 为 4FeCO +
3 3
O =====2Fe O +4CO ,设Fe O 的质量为x,根据化学反应前后铁元素质量不变:
2 2 3 2 2 3
×100%×x+×100%×(15.84 kg-x)=×100%×23.2 kg,解得x=14.4 kg。
答案 (1)加热(或适当增加硫酸的浓度、将烧渣粉碎、搅拌等)
(2)①FeS +2Fe3+ ===3Fe2++2S↓
2
②取少量溶液,滴入几滴KSCN溶液,若溶液变为红色,说明其中含有Fe3+,未反
应完全(3)①防止碳酸铵分解,减小亚铁离子的水解程度
②取少许最后一次洗涤液于试管中,滴加稀盐酸,无明显现象,再滴加BaCl 溶液,
2
若无白色沉淀生成,则表明沉淀已洗涤干净,反之,则说明没洗涤干净
(4)O 、H O (5)4FeCO +O =====2Fe O +4CO 14.4
2 2 3 2 2 3 2
6.(2018·周口市上学期期末抽测调研)某化学兴趣小组对一种废旧合金(含有Cu、
Fe、Si等元素)进行分离、回收再利用,所设计工艺流程如下。
已知:298 K时,K [Fe(OH) ]=4.0×10-38,
sp 3
K [Cu(OH) ]=2.2×10-20,K [Mn(OH) ]=1.9×10-13
sp 2 sp 2
回答下列问题:
(1)操作Ⅰ、Ⅱ、Ⅲ为________,固体B为________(填化学式)。
(2)加入过量 FeCl 溶液过程中与较不活泼的金属反应的离子方程式
3
____________________________________________________________________。
(3)调节pH至2.9~3.2的目的是分离________(填离子符号)
(4)① 向 溶 液 b 中 加 入 酸 性 KMnO 溶 液 发 生 反 应 的 离 子 方 程 式 为
4
____________________________________________________________________。
②若用a mol/L KMnO 溶液处理溶液b,当恰好反应时消耗KMnO 溶液V mL,所
4 4
得红棕色固体C的物质的量为________(用含a、V的代数式表示)
(5)常温下,若溶液c中所含的金属阳离子浓度相等,向溶液c中逐滴加入KOH溶
液,最后生成的沉淀为_________________________________________________
______________________________________________________________________
_(填化学式)。
(6)用惰性电极电解时阳极产生标准状况下的气体 6.72 L,阴极得到的电子数为
0.8N ,则生成氧气的物质的量为________mol。
A
解析 试题分析:由流程可知,合金经氯化铁溶液溶解后把其中的铁和铜溶解,过
滤后除去硅;向滤液中加入过量的铜,把过量的Fe3+还原,过滤得到铜,再向滤液
中加入酸性高锰酸钾溶液把亚铁离子完全氧化为+3价铁离子,然后再加碱调节pH使+3价铁离子转化为氢氧化铁沉淀;滤液经处理后电解,阳极得到氯气和氧
气、阴极得到铜。
(1)操作I、Ⅱ、Ⅲ为过滤,固体B为Cu。
(2) FeCl 溶液与较不活泼的金属铜反应的离子方程式为2Fe3++Cu===2Fe2++
3
Cu2+。
(3)调节pH至2.9~3.2的目的是分离Fe3+。
(4)①向溶液b中加入酸性KMnO 溶液发生反应的离子方程式为MnO+5Fe2++
4
8H+===Mn2++5Fe3++4H O。
2
②若用 a mol/LKMnO 溶液处理溶液b,当恰好反应时消耗KMnO 溶液V mL,由
4 4
反应的离子方程式可知,n(Fe3+)=5n(KMnO )=5×V×10-3L×a mol/L=5aV×10
4
-3mol,所得红棕色固体C为Fe O ,其物质的量为2.5aV×10-3mol 。
2 3
(5)常温下,溶液c中所含的金属阳离子为Fe3+、Cu2+和Mn2+,若三者浓度相等,向
溶液c中逐滴加入KOH溶液,因为K [Fe(OH) ] K [Cu(OH) ] K [Mn(OH) ],所
sp 3 sp 2 sp 2
以先生成的沉淀是Fe(OH) (由流程可知,pH=3.2时,Fe3+沉淀完全,而Cu2+和
3 ≪ ≪
Mn2+尚未开始沉淀),最后生成的沉淀为Mn(OH) 。
2
(6)用惰性电极电解时阳极产生标准状况下的气体 6.72 L,阴极得到的电子数为
0.8N ,由电子转移守恒得,4n(O )+ =0.8 mol,则生成
A 2
氧气的物质的量为0.1 mol。
答案 (1)过滤 Cu (2)2Fe3++Cu===2Fe2++Cu2+ (3)Fe3+ (4)①MnO+
5Fe2+ +8H+===Mn2++5Fe3++4H O ②2.5aV×10-3 mol (5)Mn(OH) (6)0.1
2 2