文档内容
热点强化 20 化学反应速率和化学平衡简答题
文字描述代表一种开放性思维与能力,一般从速率问题、平衡(转化率)问题、安全问题、节
能减排等角度作答(考查前两个角度居多),实际上就是效益最大化的问题。
1.条件选择类
(1)实验最佳条件的选择或控制就是为了又“快”又“好”地生产,即主要是从反应速率与
转化率(化学平衡)两个角度来分析。“快”就是提高反应速率,“好”就是提高转化率,原
料利用率高,而影响速率与转化率的主要因素就是浓度、温度、压强与催化剂,其中温度与
压强是试题中经常考查的因素。
(2)从速率、转化率、产率、纯度等角度分析,选择最佳条件。如针对反应速率时,思考方
向为如何提高浸出速率、如何提高反应速率等;针对平衡转化率、产率时,可运用平衡移动
原理解释(其他条件不变的情况下,改变××条件,可逆反应平衡向××方向移动,导致
××发生变化);针对综合生产效益时,可从原料成本,原料来源是否广泛、是否可再生,
能源成本,对设备的要求,环境保护,绿色化学等方面作答。
(3)选择当前条件的优势,其他条件的不足,往往不足的描述比较容易疏忽,如温度过高或
过低,压强过小或过大,也要进行分析。
2.原因分析类
(1)依据化学反应速率和平衡移动原理,分析造成图像曲线变化的原因。
(2)催化剂对反应的影响、不同反应的选择性问题是这类题目的难点,解题时要多加关注,
不同的条件会有不同的选择性。
(3)这类题目一般都是多因素影响,需要多角度分析原因。
一、曲线上特殊点的分析
1.用(NH )CO 捕碳的反应:(NH )CO(aq)+HO(l)+CO(g)2NH HCO (aq)。为研究温
4 2 3 4 2 3 2 2 4 3
度对(NH )CO 捕获CO 效率的影响,将一定量的(NH )CO 溶液置于密闭容器中,并充入一
4 2 3 2 4 2 3
定量的CO 气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得 CO
2 2
气体浓度,得到趋势图如图。
(1)c点的逆反应速率和d点的正反应速率的大小关系为 v逆 (c)________(填“>”“=”或
“<”)v正 (d)。
(2)b、c、d三点的平衡常数K 、K、K 从大到小的顺序为________。
b c d(3)T ~T 温度区间,容器内 CO 气体浓度呈现增大的变化趋势,其原因是
3 4 2
________________________________________________________________________
________________________________________________________________________。
答案 (1)< (2)K >K>K (3)T ~T 温度区间,化学反应已达到平衡,由于正反应是放
b c d 3 4
热反应,温度升高平衡向逆反应方向移动,不利于CO 的捕获
2
解析 (1)温度越高,反应速率越快,d点温度高,则c点的逆反应速率和d点的正反应速率
的大小关系为v (c)<v (d)。(2)根据图像,温度为 T 时反应达平衡,此后温度升高,
逆 正 3
c(CO)增大,平衡逆向移动,说明正反应是放热反应。升高温度,平衡逆向移动,平衡常数
2
减小,故K >K>K 。
b c d
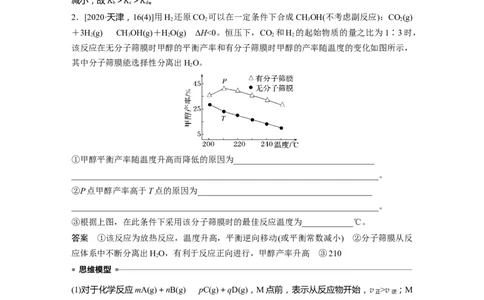
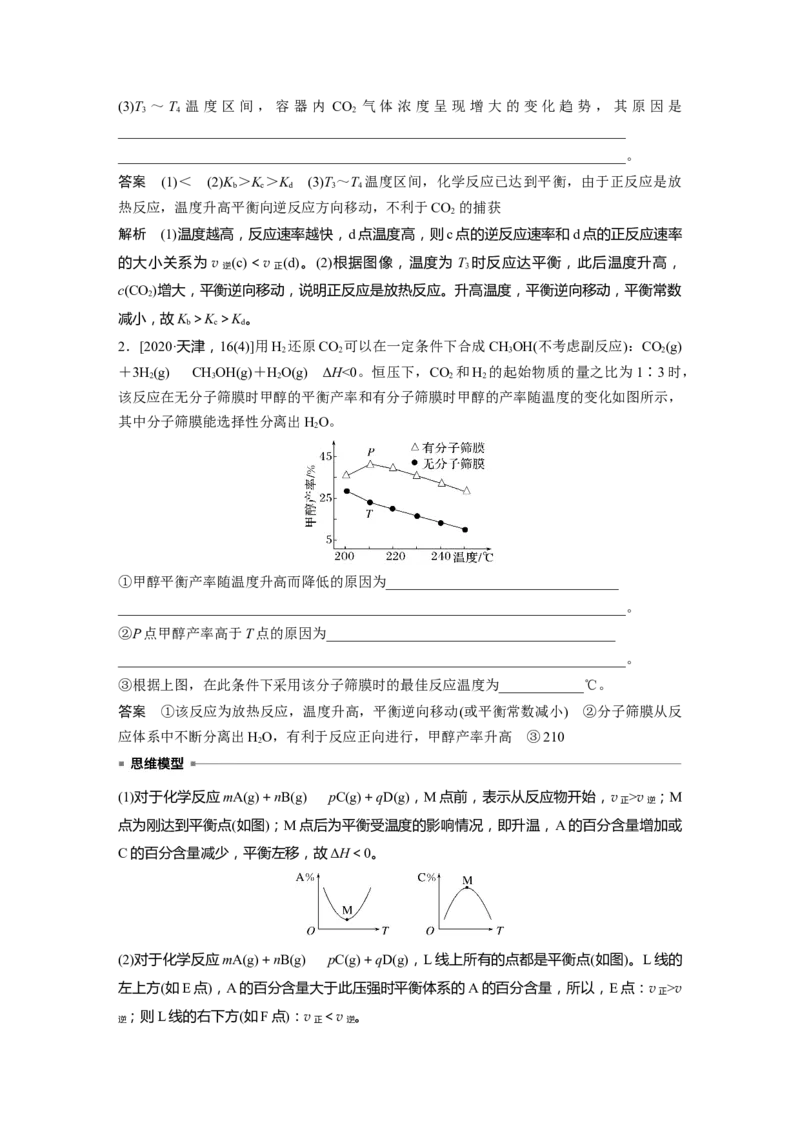
2.[2020·天津,16(4)]用H 还原CO 可以在一定条件下合成CHOH(不考虑副反应):CO(g)
2 2 3 2
+3H(g)CHOH(g)+HO(g) ΔH<0。恒压下,CO 和H 的起始物质的量之比为1∶3时,
2 3 2 2 2
该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,
其中分子筛膜能选择性分离出HO。
2
①甲醇平衡产率随温度升高而降低的原因为_________________________________
________________________________________________________________________。
②P点甲醇产率高于T点的原因为_________________________________________
________________________________________________________________________。
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为____________℃。
答案 ①该反应为放热反应,温度升高,平衡逆向移动(或平衡常数减小) ②分子筛膜从反
应体系中不断分离出HO,有利于反应正向进行,甲醇产率升高 ③210
2
(1)对于化学反应mA(g)+nB(g)pC(g)+qD(g),M点前,表示从反应物开始,v >v ;M
正 逆
点为刚达到平衡点(如图);M点后为平衡受温度的影响情况,即升温,A的百分含量增加或
C的百分含量减少,平衡左移,故ΔH<0。
(2)对于化学反应mA(g)+nB(g)pC(g)+qD(g),L线上所有的点都是平衡点(如图)。L线的
左上方(如E点),A的百分含量大于此压强时平衡体系的A的百分含量,所以,E点:v >v
正
;则L线的右下方(如F点):v <v 。
逆 正 逆二、曲线变化趋势的分析
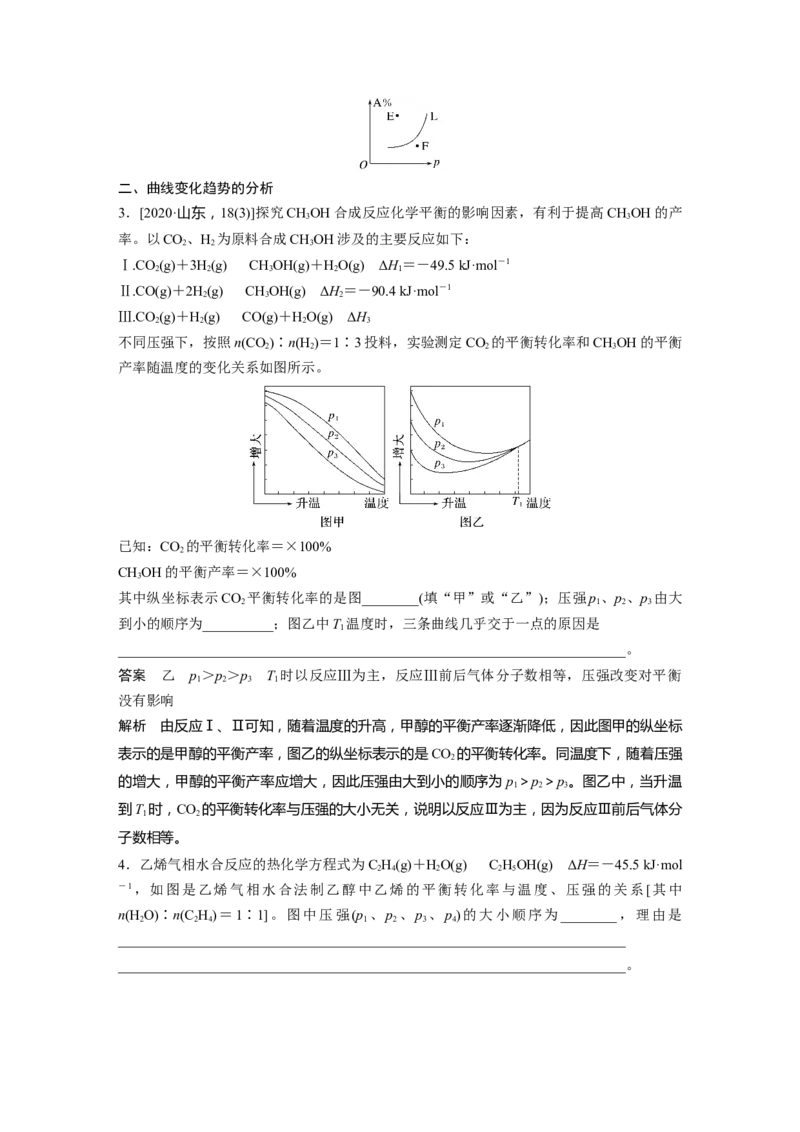
3.[2020·山东,18(3)]探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产
3 3
率。以CO、H 为原料合成CHOH涉及的主要反应如下:
2 2 3
Ⅰ.CO (g)+3H(g)CHOH(g)+HO(g) ΔH=-49.5 kJ·mol-1
2 2 3 2 1
Ⅱ.CO(g)+2H(g)CHOH(g) ΔH=-90.4 kJ·mol-1
2 3 2
Ⅲ.CO (g)+H(g)CO(g)+HO(g) ΔH
2 2 2 3
不同压强下,按照n(CO)∶n(H )=1∶3投料,实验测定CO 的平衡转化率和CHOH的平衡
2 2 2 3
产率随温度的变化关系如图所示。
已知:CO 的平衡转化率=×100%
2
CHOH的平衡产率=×100%
3
其中纵坐标表示CO 平衡转化率的是图________(填“甲”或“乙”);压强p 、p 、p 由大
2 1 2 3
到小的顺序为__________;图乙中T 温度时,三条曲线几乎交于一点的原因是
1
________________________________________________________________________。
答案 乙 p >p >p T 时以反应Ⅲ为主,反应Ⅲ前后气体分子数相等,压强改变对平衡
1 2 3 1
没有影响
解析 由反应Ⅰ、Ⅱ可知,随着温度的升高,甲醇的平衡产率逐渐降低,因此图甲的纵坐标
表示的是甲醇的平衡产率,图乙的纵坐标表示的是CO 的平衡转化率。同温度下,随着压强
2
的增大,甲醇的平衡产率应增大,因此压强由大到小的顺序为p >p >p 。图乙中,当升温
1 2 3
到T 时,CO 的平衡转化率与压强的大小无关,说明以反应Ⅲ为主,因为反应Ⅲ前后气体分
1 2
子数相等。
4.乙烯气相水合反应的热化学方程式为C H(g)+HO(g)C HOH(g) ΔH=-45.5 kJ·mol
2 4 2 2 5
-1,如图是乙烯气相水合法制乙醇中乙烯的平衡转化率与温度、压强的关系[其中
n(H O)∶n(C H)=1∶1]。图中压强(p 、p 、p 、p)的大小顺序为________,理由是
2 2 4 1 2 3 4
________________________________________________________________________
________________________________________________________________________。答案 p>p>p>p 该反应正向是气体分子数减小的反应,相同温度下,压强升高乙烯平衡
4 3 2 1
转化率升高
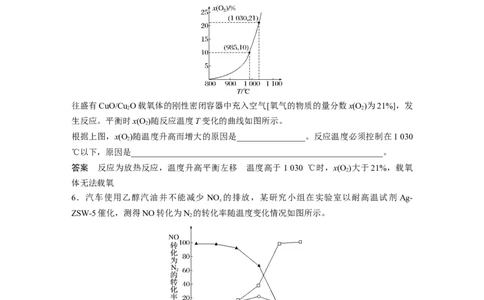
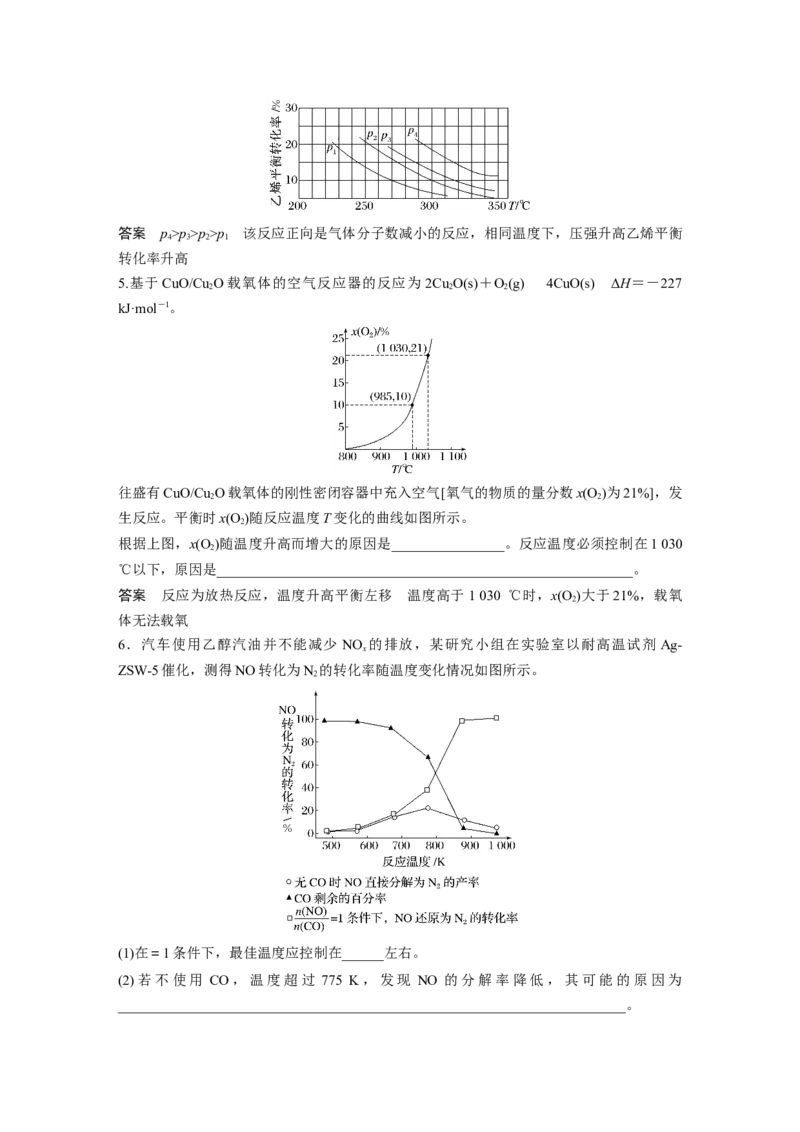
5.基于CuO/Cu O载氧体的空气反应器的反应为 2Cu O(s)+O(g)4CuO(s) ΔH=-227
2 2 2
kJ·mol-1。
往盛有CuO/Cu O载氧体的刚性密闭容器中充入空气[氧气的物质的量分数x(O )为21%],发
2 2
生反应。平衡时x(O )随反应温度T变化的曲线如图所示。
2
根据上图,x(O )随温度升高而增大的原因是________________。反应温度必须控制在1 030
2
℃以下,原因是___________________________________________________________。
答案 反应为放热反应,温度升高平衡左移 温度高于1 030 ℃时,x(O )大于21%,载氧
2
体无法载氧
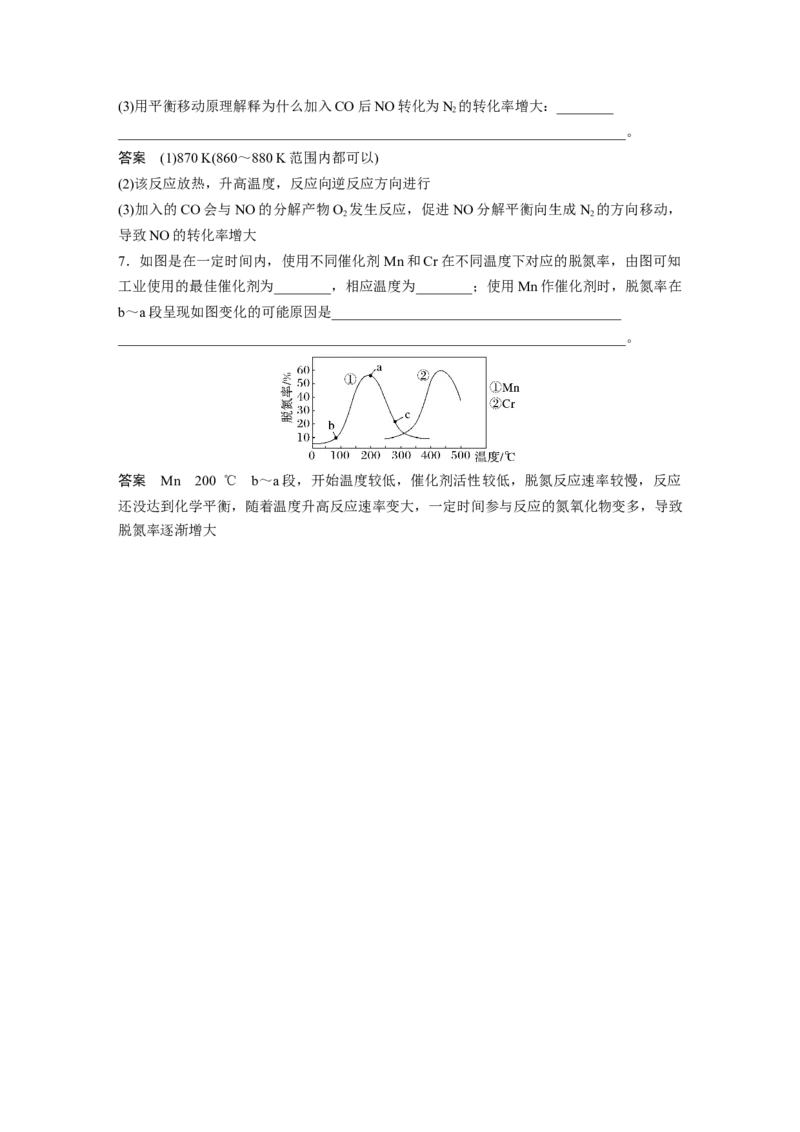
6.汽车使用乙醇汽油并不能减少 NO 的排放,某研究小组在实验室以耐高温试剂 Ag-
x
ZSW-5催化,测得NO转化为N 的转化率随温度变化情况如图所示。
2
(1)在=1条件下,最佳温度应控制在______左右。
(2)若不使用 CO,温度超过 775 K,发现 NO 的分解率降低,其可能的原因为
________________________________________________________________________。(3)用平衡移动原理解释为什么加入CO后NO转化为N 的转化率增大:________
2
________________________________________________________________________。
答案 (1)870 K(860~880 K范围内都可以)
(2)该反应放热,升高温度,反应向逆反应方向进行
(3)加入的CO会与NO的分解产物O 发生反应,促进NO分解平衡向生成N 的方向移动,
2 2
导致NO的转化率增大
7.如图是在一定时间内,使用不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知
工业使用的最佳催化剂为________,相应温度为________;使用Mn作催化剂时,脱氮率在
b~a段呈现如图变化的可能原因是_________________________________________
________________________________________________________________________。
答案 Mn 200 ℃ b~a段,开始温度较低,催化剂活性较低,脱氮反应速率较慢,反应
还没达到化学平衡,随着温度升高反应速率变大,一定时间参与反应的氮氧化物变多,导致
脱氮率逐渐增大