文档内容
第 54 讲 盐类的水解
[复习目标] 1.了解盐类水解的原理及一般规律。2.了解影响盐类水解程度的主要因素。3.了
解盐类水解的应用。
考点一 盐类的水解及其规律
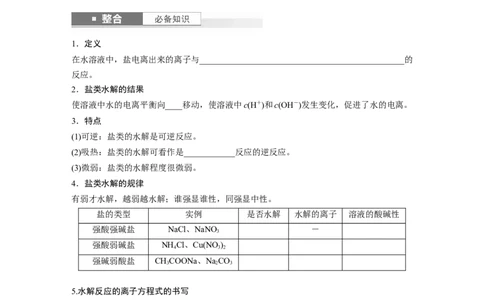
1.定义
在水溶液中,盐电离出来的离子与________________________________________________的
反应。
2.盐类水解的结果
使溶液中水的电离平衡向____移动,使溶液中c(H+)和c(OH-)发生变化,促进了水的电离。
3.特点
(1)可逆:盐类的水解是可逆反应。
(2)吸热:盐类的水解可看作是____________反应的逆反应。
(3)微弱:盐类的水解程度很微弱。
4.盐类水解的规律
有弱才水解,越弱越水解;谁强显谁性,同强显中性。
盐的类型 实例 是否水解 水解的离子 溶液的酸碱性
强酸强碱盐 NaCl、NaNO -
3
强酸弱碱盐 NH Cl、Cu(NO )
4 3 2
强碱弱酸盐 CHCOONa、NaCO
3 2 3
5.水解反应的离子方程式的书写
(1)盐类水解的离子方程式一般用“”连接,且一般不标“↑”“↓”等状态符号。
(2)多元弱酸盐:分步书写,以第一步为主。
(3)多元弱碱盐:水解反应的离子方程式一步完成。
(4)阴、阳离子相互促进的水解
①若水解程度不大,用“”表示。
②相互促进的水解反应程度较大的,书写时用“===”“↑”“↓”。
[应用举例]
写出下列盐溶液水解的离子方程式。(1)NH Cl:___________________________________________________________________。
4
(2)Na CO:___________________________________________________________________、
2 3
______________________________________________________________________________。
(3)FeCl :_____________________________________________________________________。
3
(4)CH COONH:______________________________________________________________
3 4
______________________________________________________________________________。
(5)AlS:_____________________________________________________________________。
2 3
(6)AlCl 溶液和NaHCO 溶液混合:_______________________________________________
3 3
______________________________________________________________________________。
1.盐溶液显酸碱性,一定是由水解引起的( )
2.溶液呈中性的盐一定是强酸、强碱反应生成的盐( )
3.pH相同的盐酸和氯化铵溶液中由水电离出的c(H+)相同( )
4.NaHCO 、NaHSO 都能促进水的电离( )
3 4
5.向NaAlO 溶液中滴加NaHCO 溶液,有沉淀和气体生成( )
2 3
一、盐溶液酸碱性及离子浓度大小判断
1.25 ℃时浓度都是1 mol·L-1的四种正盐溶液:AX、BX、AY、BY;AX的溶液pH=7且
溶液中c(X-)=1 mol·L-1,BX的溶液pH=4,BY的溶液pH=6。下列说法正确的是( )
A.电离平衡常数K (BOH)小于K(HY)
b a
B.AY溶液的pH小于BY溶液的pH
C.稀释相同倍数,溶液pH变化BX等于BY
D.将浓度均为1 mol·L-1的HX和HY溶液分别稀释10倍后,HX溶液的pH大于HY
2.根据相关物质的电离常数(25 ℃),回答下列问题:
CHCOOH K=1.8×10-5,
3 a
HCN K=4.9×10-10,
a
HCO K =4.3×10-7 K =5.6×10-11
2 3 a1 a2
(1)相同物质的量浓度的①CHCOONa、②NaCO 、③NaHCO 、④NaCN溶液,pH由大到
3 2 3 3
小的顺序:________________,水的电离程度由大到小的顺序:________________。
(2)相同pH的①CHCOONa、②NaCO、③NaHCO 、④NaCN溶液,物质的量浓度由大到
3 2 3 3
小的顺序:________________。
(3)NaCN 溶 液 中 , c(Na + ) 、 c(CN - ) 、 c(HCN) 由 大 到 小 的 顺 序 :
______________________________________________________________________________。
(4)常温下,NH ·H O(K =1.8×10-5), 则 CHCOONH 溶液显____性(填“酸”“碱”或
3 2 b 3 4“中”,下同),NH HCO 溶液显____性。
4 3
二、广义的水解规律应用
3.广义的水解观认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水
分别解离成两部分,然后两两重新组合成新的物质。根据上述观点,下列说法错误的是(
)
A.BaO 的水解产物是Ba(OH) 和HO
2 2 2 2
B.PCl 的水解产物是HClO和HPO
3 3 4
C.Al C 的水解产物是Al(OH) 和CH
4 3 3 4
D.CHCOCl的水解产物是两种酸
3
4.如图为钛铁矿提取金属Ti部分流程:
(1)TiO2 + 易 水 解 , 只 能 存 在 于 强 酸 性 溶 液 , 则 TiO2 + 水 解 的 离 子 方 程 式 为
______________________________________________________________________________
______________________________________________________________________________。
(2)写出加入碳酸钠粉末时反应的离子方程式:______________________________________。
5.写出亚硫酰氯(SOCl )在潮湿的空气中产生白雾的化学方程式:_____________________
2
______________________________________________________________________________。
广义水解原理
广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果都是参与反应的物质和水
分别解离成两部分,再重新组合成新的物质。
考点二 外因对水解平衡的影响
1.温度
盐类水解反应是中和反应的逆反应,因而盐类的水解为________反应,升高温度,水解平衡
向右移动。
2.浓度
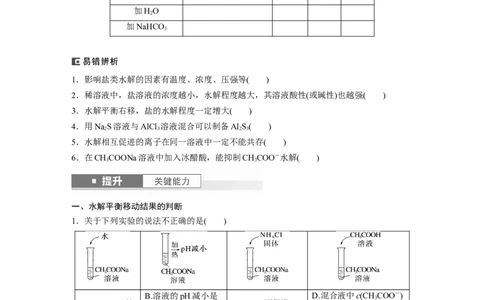
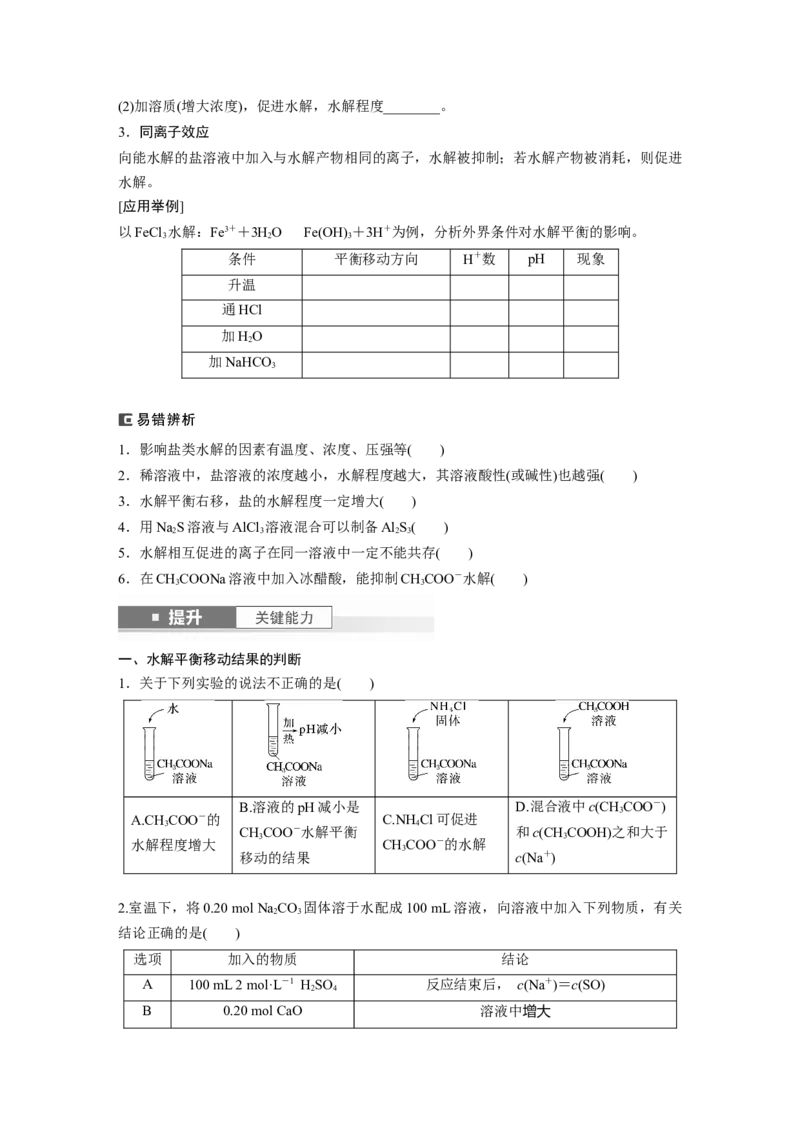
(1)加水稀释,促进水解,水解程度________。(2)加溶质(增大浓度),促进水解,水解程度________。
3.同离子效应
向能水解的盐溶液中加入与水解产物相同的离子,水解被抑制;若水解产物被消耗,则促进
水解。
[应用举例]
以FeCl 水解:Fe3++3HOFe(OH) +3H+为例,分析外界条件对水解平衡的影响。
3 2 3
条件 平衡移动方向 H+数 pH 现象
升温
通HCl
加HO
2
加NaHCO
3
1.影响盐类水解的因素有温度、浓度、压强等( )
2.稀溶液中,盐溶液的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强( )
3.水解平衡右移,盐的水解程度一定增大( )
4.用NaS溶液与AlCl 溶液混合可以制备Al S( )
2 3 2 3
5.水解相互促进的离子在同一溶液中一定不能共存( )
6.在CHCOONa溶液中加入冰醋酸,能抑制CHCOO-水解( )
3 3
一、水解平衡移动结果的判断
1.关于下列实验的说法不正确的是( )
B.溶液的pH减小是 D.混合液中c(CHCOO-)
3
A.CHCOO-的 C.NHCl可促进
3 4
CHCOO-水解平衡 和c(CHCOOH)之和大于
3 3
水解程度增大 CHCOO-的水解
3
移动的结果 c(Na+)
2.室温下,将0.20 mol Na CO 固体溶于水配成100 mL溶液,向溶液中加入下列物质,有关
2 3
结论正确的是( )
选项 加入的物质 结论
A 100 mL 2 mol·L-1 HSO 反应结束后, c(Na+)=c(SO)
2 4
B 0.20 mol CaO 溶液中增大C 200 mL H O 由水电离出的c(H+)·c(OH-)不变
2
D 0.4 mol NaHSO 固体 反应完全后,溶液pH减小,c(Na+)不变
4
二、不同盐溶液中指定粒子浓度的比较
3.25 ℃时,相同物质的量浓度的下列溶液中:
①NH Cl、②CHCOONH、③NH HSO 、
4 3 4 4 4
④(NH )SO 、⑤(NH )Fe(SO ),c(NH)由大到小的顺序为____________________(填序号)。
4 2 4 4 2 4 2
4.25 ℃时,比较下列几组溶液中指定离子浓度的大小。
(1)浓度均为0.1 mol·L-1的①HS、②NaHS、③NaS、④HS和NaHS混合液,溶液pH从
2 2 2
大到小的顺序是_______________________(填序号,下同)。
(2)相同浓度的下列溶液中:①CHCOONH 、②CHCOONa、③CHCOOH,c(CHCOO-)
3 4 3 3 3
由大到小的顺序是__________________________________________________________。
(3)c(NH)相等的①(NH )SO 溶液、②NH HSO 溶液、③(NH )CO 溶液、④NH Cl溶液,其
4 2 4 4 4 4 2 3 4
物质的量浓度由大到小的顺序为__________________________________________。
比较不同溶液中同一离子浓度大小的方法:选好参照物,分组比较,各个击破。
答题规范(8) 利用平衡移动原理解释问题
(1)解答此类题的思维过程
①找出存在的平衡体系(即可逆反应或可逆过程)
②找出影响平衡的条件
③判断平衡移动的方向
④分析平衡移动的结果及移动结果与所解答问题的联系(2)答题模板
……存在……平衡,……(条件)……(变化),使平衡向……(方向)移动,……(结论)。
1.实验测得0.5 mol·L-1 CHCOONa溶液、0.5 mol·L-1 CuSO 溶液以及HO的pH随温度
3 4 2
变化的曲线如图所示。
(1) 随 温 度 升 高 , HO 的 pH________( 填 “ 变 大 ” 或 “ 变 小 ” ) , 原 因 是
2
____________________
______________________________________________________________________________。
(2) 随 温 度 升 高 , CHCOONa 溶 液 pH 降 低 的 原 因 是
3
_____________________________________
_______________________________________________________________________________
。
(3)随温度升高,CuSO 溶液的pH变化受哪些因素的影响?
4
_______________________________________________________________________________
_______________________________________________________________________________
。
2.为探究盐类水解吸热,请用NaCO 溶液和其他必要试剂,设计一个简单的实验方案:
2 3
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
。
3.Mg粉可溶解在NH Cl溶液中,分析其原因。
4
_______________________________________________________________________________
_______________________________________________________________________________
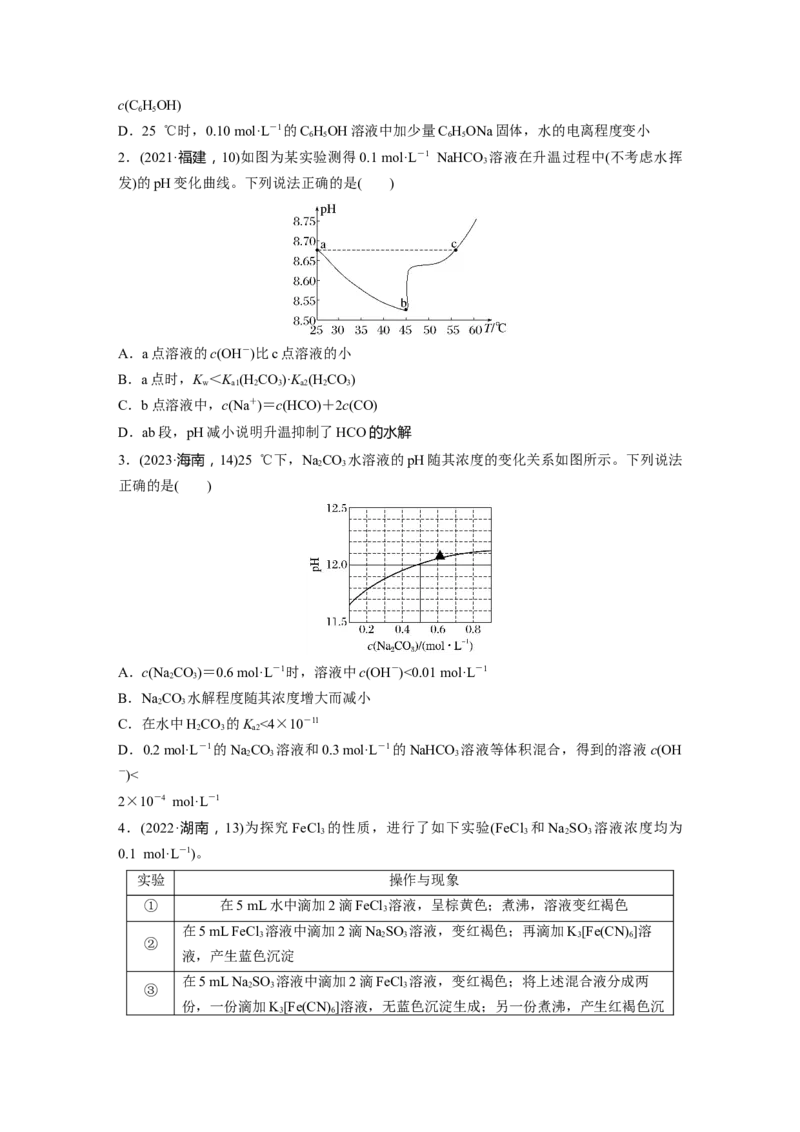
1.(2022·浙江6月选考,17)25 ℃时,苯酚(C HOH)的K=1.0×10-10,下列说法正确的是(
6 5 a
)
A.相同温度下,等pH的C HONa和CHCOONa溶液中,c(C HO-)>c(CHCOO-)
6 5 3 6 5 3
B.将浓度均为0.10 mol·L-1的C HONa和NaOH溶液加热,两种溶液的pH均变大
6 5
C.25 ℃时,C HOH溶液与NaOH溶液混合,测得pH=10.00,则此时溶液中c(C HO-)=
6 5 6 5c(C HOH)
6 5
D.25 ℃时,0.10 mol·L-1的C HOH溶液中加少量C HONa固体,水的电离程度变小
6 5 6 5
2.(2021·福建,10)如图为某实验测得0.1 mol·L-1 NaHCO 溶液在升温过程中(不考虑水挥
3
发)的pH变化曲线。下列说法正确的是( )
A.a点溶液的c(OH-)比c点溶液的小
B.a点时,K <K (H CO)·K (H CO)
w a1 2 3 a2 2 3
C.b点溶液中,c(Na+)=c(HCO)+2c(CO)
D.ab段,pH减小说明升温抑制了HCO的水解
3.(2023·海南,14)25 ℃下,NaCO 水溶液的pH随其浓度的变化关系如图所示。下列说法
2 3
正确的是( )
A.c(Na CO)=0.6 mol·L-1时,溶液中c(OH-)<0.01 mol·L-1
2 3
B.NaCO 水解程度随其浓度增大而减小
2 3
C.在水中HCO 的K <4×10-11
2 3 a2
D.0.2 mol·L-1的NaCO 溶液和0.3 mol·L-1的NaHCO 溶液等体积混合,得到的溶液c(OH
2 3 3
-)<
2×10-4 mol·L-1
4.(2022·湖南,13)为探究FeCl 的性质,进行了如下实验(FeCl 和Na SO 溶液浓度均为
3 3 2 3
0.1 mol·L-1)。
实验 操作与现象
① 在5 mL水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色
3
在5 mL FeCl 溶液中滴加2滴NaSO 溶液,变红褐色;再滴加K[Fe(CN) ]溶
3 2 3 3 6
②
液,产生蓝色沉淀
在5 mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;将上述混合液分成两
③ 2 3 3
份,一份滴加K[Fe(CN) ]溶液,无蓝色沉淀生成;另一份煮沸,产生红褐色沉
3 6淀
依据上述实验现象,结论不合理的是( )
A.实验①说明加热促进Fe3+水解反应
B.实验②说明Fe3+既发生了水解反应,又发生了还原反应
C.实验③说明Fe3+发生了水解反应,但没有发生还原反应
D.整个实验说明SO对Fe3+的水解反应无影响,但对还原反应有影响