文档内容
第 59 讲 无机化工流程题的解题策略
[复习目标] 1.提升应用物质的转化及条件控制、分离提纯操作等相关知识解决实际问题的
能力。2.树立“绿色化学”的观念,形成资源综合利用、物能充分利用的意识。
1.常考无机化工流程的呈现形式
2.读图要领
(1)箭头:进入的是投料(反应物),出去的是含产品中元素的物质(流程方向)、副产物或杂质
(支线方向)。
(2)三线:出线和进线均表示物料流向或操作流程,可逆线表示物质循环。
3.流程图中主要环节的分析
(1)原料的预处理
①溶解:通常用酸溶,如用硫酸、盐酸等。
水浸 与水接触发生反应或溶解
浸出 固体加水(酸)溶解得到离子
酸浸 在酸溶液中反应,使可溶性金属离子进入溶液,不溶物通过过滤除去
浸出率 固体溶解后,离子在溶液中的含量的多少
②灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质在高温下氧化、分解。
③审题时要“瞻前顾后”,注意物质性质及反应原理的前后联系。
(2)核心反应——陌生方程式的书写
①氧化还原反应:熟练应用氧化还原反应规律判断产物,并根据化合价升降相等配平。
②非氧化还原反应:结合物质性质和反应实际判断产物。
(3)常用的分离方法
①过滤:分离难溶物和易溶物,根据特殊需要采用趁热过滤或者抽滤等方法。
②萃取和分液:利用溶质在互不相溶的溶剂里的溶解度不同提取分离物质,如用 CCl 或苯
4
萃取溴水中的溴。
③蒸发结晶:提取溶解度随温度变化不大的溶质,如从溶液中提取NaCl。
④冷却结晶:提取溶解度随温度变化较大的溶质、易水解的溶质或结晶水合物,如KNO 、
3FeCl 、CuCl 、CuSO ·5H O、FeSO ·7H O等。
3 2 4 2 4 2
⑤蒸馏或分馏:分离沸点不同且互溶的液体混合物,如分离乙醇和甘油。
⑥冷却法:利用气体液化的特点分离气体,如合成氨工业采用冷却法分离平衡混合气体中的
NH 。
3
一、调控化学反应速率提高效率
1.向铬铁矿(FeCrO)中通入 O 进行焙烧,焙烧时气体与矿料逆流而行,目的是
2 4 2
___________。
答案 增大反应物接触面积,提高化学反应速率
2.将催化剂负载在玻璃棉上而不直接平铺在玻璃管中,目的是_____________________。
答案 增大接触面积,提高催化效果,加快反应速率
3.[2020·北京,18(1)①]酸、过量铁屑对软锰矿(MnO )进行溶出前需研磨。目的是
2
________________________________________________________________________
________________________________________________________________________。
答案 增大反应物接触面积,加快溶出速率
4.向金属Bi中加入稀HNO 酸浸,过程中分次加入稀HNO 可降低反应剧烈程度,其原理
3 3
是________________________________________________________________________
________________________________________________________________________。
答案 减少稀HNO 的用量,降低反应剧烈程度,使HNO 充分反应防止挥发
3 3
解析 强调分次加入对反应的影响:①控制用量,防止过量发生副反应;②降低反应剧烈程
度;③防止放热反应温度过高,造成副反应的发生,以及物质的挥发、分解。
二、结晶与分离提纯操作应用
5.[2021·河北,14(4)②]向含 NH Cl 的滤液中加入 NaCl 粉末,存在 NaCl(s)+
4
NH Cl(aq)―→NaCl(aq)+NH Cl(s)过程。为使NH Cl沉淀充分析出并分离,根据 NaCl和
4 4 4
NH Cl溶解度曲线,需采用的操作__________、__________、洗涤、干燥。
4
答案 冷却结晶 过滤
解析 由曲线NH Cl的溶解度随升温而增大,NaCl的溶解度随升温变化不明显,使NH Cl
4 4
沉淀充分析出,采用冷却结晶析出NH Cl→过滤→洗涤→干燥。
4
6.[2019·全国卷Ⅰ,27(4)]由硫酸铁与硫酸铵的混合溶液,通过________________操作,经干燥得到硫酸铁铵晶体样品。
答案 加热浓缩、冷却结晶、过滤洗涤
7.[2019·全国卷Ⅲ,27(5)改编]过滤得到乙酰水杨酸结晶粗品,该固体经纯化得白色的乙酰
水杨酸晶体,采用的“纯化”方法为_______________________________________。
答案 重结晶
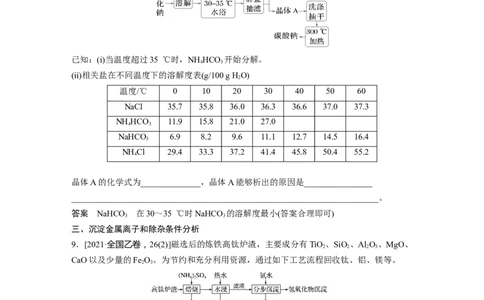
8.[2021·湖南,15(1)]以碳酸氢铵和氯化钠为原料制备碳酸钠,并测定产品中少量碳酸氢钠
的含量,过程如下:
已知:(i)当温度超过35 ℃时,NH HCO 开始分解。
4 3
(ii)相关盐在不同温度下的溶解度表(g/100 g HO)
2
温度/℃ 0 10 20 30 40 50 60
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
NH HCO 11.9 15.8 21.0 27.0
4 3
NaHCO 6.9 8.2 9.6 11.1 12.7 14.5 16.4
3
NH Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.2
4
晶体A的化学式为______________,晶体A能够析出的原因是________________
________________________________________________________________________。
答案 NaHCO 在30~35 ℃时NaHCO 的溶解度最小(答案合理即可)
3 3
三、沉淀金属离子和除杂条件分析
9.[2021·全国乙卷,26(2)]磁选后的炼铁高钛炉渣,主要成分有TiO、SiO、Al O、MgO、
2 2 2 3
CaO以及少量的Fe O。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
2 3
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表。
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依次析
出的金属离子是__________________________。
答案 Fe3+、Al3+、Mg2+
10.[2020·北京,18(2)]由硫酸浸出的Mn2+溶出液(含Mn2+、Fe2+、Al3+、Fe3+、H+等)经纯
化得Mn2+纯化液。已知:MnO 的氧化性与溶液pH有关。金属离子沉淀的pH如下表:
2
Fe3+ Al3+ Mn2+ Fe2+
开始沉淀时 1.5 3.4 5.8 6.3
完全沉淀时 2.8 4.7 7.8 8.3
纯化时先加入MnO ,后加入NH ·H O,调溶液pH≈5,说明试剂加入顺序及调节pH的原
2 3 2
因:________________________________________________________________________
________________________________________________________________________。
答案 先加 MnO ,可利用溶液的酸性将 Fe2+全部氧化为 Fe3+,再加 NH ·H O 调溶液
2 3 2
pH≈5,将Fe3+和Al3+沉淀除去
四、温度控制分析
11.TiO·xHO沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
2 2
温度/℃ 30 35 40 45 50
TiO·xHO转化率/% 92 95 97 93 88
2 2
分析40 ℃时,TiO·xHO转化率最高的原因:_______________________________
2 2
________________________________________________________________________。
答案 低于40 ℃ TiO·xHO转化反应速率随温度的升高而增加;超过40 ℃,双氧水分解
2 2
与氨气逸出导致TiO·xHO转化率下降
2 2
12.[2021·福建,11(1)(2)(5)]四钼酸铵是钼深加工的重要中间产品,具有广泛的用途。一种
以钼精矿(主要含MoS ,还有Cu、Fe的化合物及SiO 等)为原料制备四钼酸铵的工艺流程如
2 2
图所示。
回答下列问题:
(1)“焙烧”产生的气体用________吸收后可制取氮肥。
(2)“ 浸 出 ” 时 , MoO 转 化 为 MoO 。 提 高 单 位 时 间 内 钼 浸 出 率 的 措 施 有
3
_________________________________________________________(任写两种)。
温度对90 min内钼浸出率的影响如图所示。当浸出温度超过80 ℃后,钼的浸出率反而降低,主要原因是温度升高使水大量蒸发,导致____________________________________。
(5)“沉淀”时,加入NH NO 的目的是____________________。
4 3
答案 (1)氨水 (2)适当升温、搅拌、增加NaCO 用量、增大NaCO 浓度等 NaMoO 晶
2 3 2 3 2 4
体析出,混入浸渣 (5)提供NH,使MoO充分转化为沉淀析出
解析 (1)“焙烧”产生的气体为SO ,用氨水吸收后可制取氮肥。
2
五、信息的提取与加工
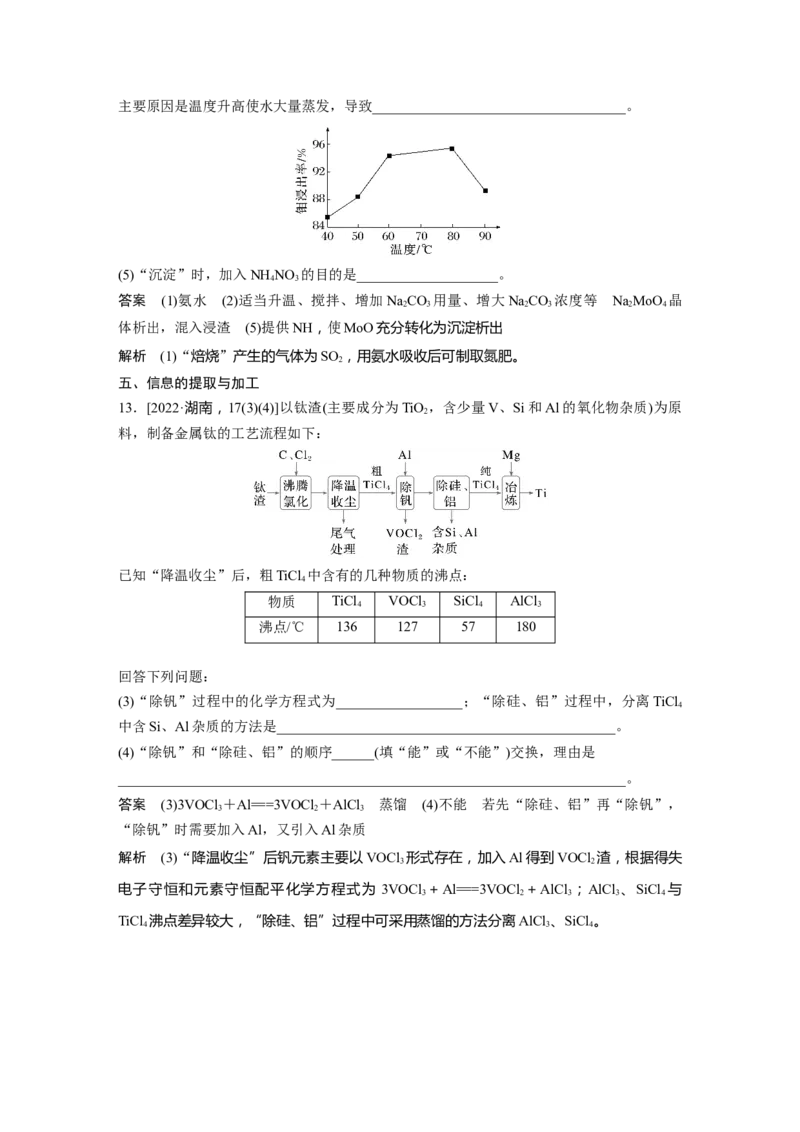
13.[2022·湖南,17(3)(4)]以钛渣(主要成分为TiO ,含少量V、Si和Al的氧化物杂质)为原
2
料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗TiCl 中含有的几种物质的沸点:
4
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
(3)“除钒”过程中的化学方程式为__________________;“除硅、铝”过程中,分离TiCl
4
中含Si、Al杂质的方法是________________________________________________。
(4)“除钒”和“除硅、铝”的顺序______(填“能”或“不能”)交换,理由是
________________________________________________________________________。
答案 (3)3VOCl +Al===3VOCl +AlCl 蒸馏 (4)不能 若先“除硅、铝”再“除钒”,
3 2 3
“除钒”时需要加入Al,又引入Al杂质
解析 (3)“降温收尘”后钒元素主要以VOCl 形式存在,加入Al得到VOCl 渣,根据得失
3 2
电子守恒和元素守恒配平化学方程式为 3VOCl +Al===3VOCl +AlCl ;AlCl 、SiCl 与
3 2 3 3 4
TiCl 沸点差异较大,“除硅、铝”过程中可采用蒸馏的方法分离AlCl 、SiCl 。
4 3 4课时精练
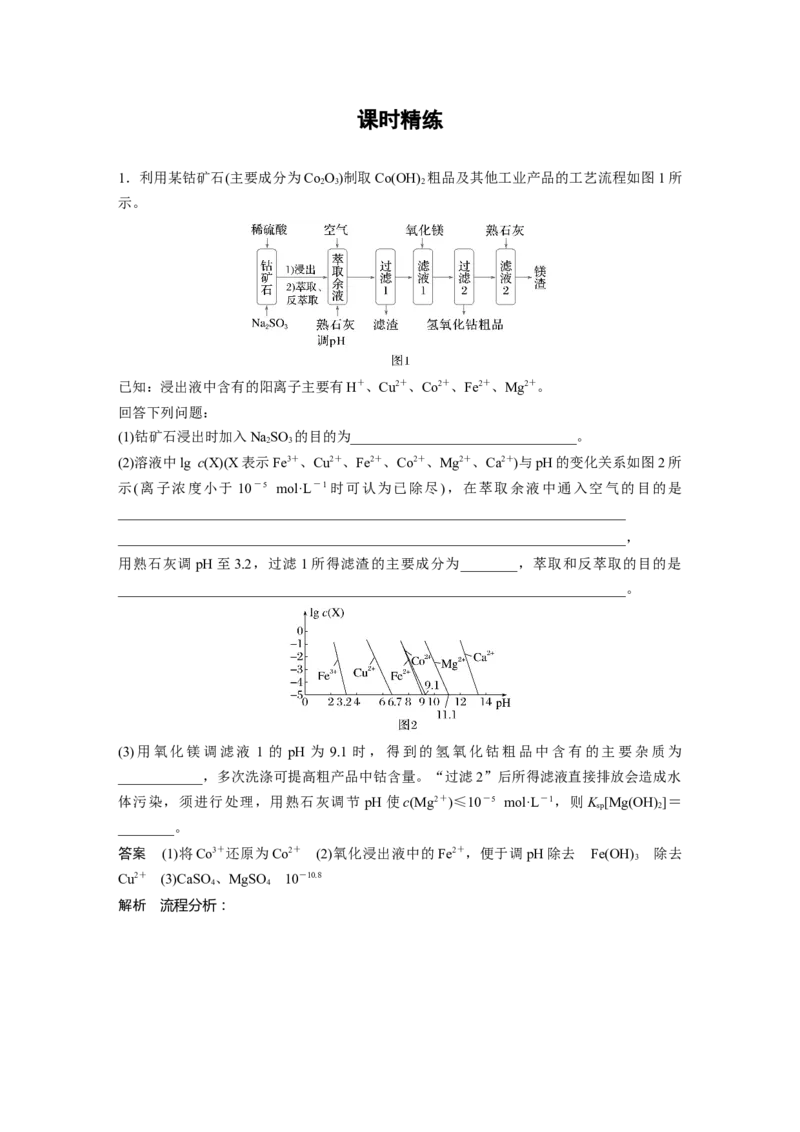
1.利用某钴矿石(主要成分为Co O)制取Co(OH) 粗品及其他工业产品的工艺流程如图1所
2 3 2
示。
已知:浸出液中含有的阳离子主要有H+、Cu2+、Co2+、Fe2+、Mg2+。
回答下列问题:
(1)钴矿石浸出时加入NaSO 的目的为________________________________。
2 3
(2)溶液中lg c(X)(X表示Fe3+、Cu2+、Fe2+、Co2+、Mg2+、Ca2+)与pH的变化关系如图2所
示(离子浓度小于 10-5 mol·L-1时可认为已除尽),在萃取余液中通入空气的目的是
________________________________________________________________________
________________________________________________________________________,
用熟石灰调pH至3.2,过滤1所得滤渣的主要成分为________,萃取和反萃取的目的是
________________________________________________________________________。
(3)用氧化镁调滤液 1 的 pH 为 9.1 时,得到的氢氧化钴粗品中含有的主要杂质为
____________,多次洗涤可提高粗产品中钴含量。“过滤2”后所得滤液直接排放会造成水
体污染,须进行处理,用熟石灰调节 pH使c(Mg2+)≤10-5 mol·L-1,则K [Mg(OH) ]=
sp 2
________。
答案 (1)将Co3+还原为Co2+ (2)氧化浸出液中的Fe2+,便于调pH除去 Fe(OH) 除去
3
Cu2+ (3)CaSO 、MgSO 10-10.8
4 4
解析 流程分析:2.锰常用于制造合金锰钢。某化工厂以软锰矿(主要成分是MnO ,含有SiO 、Fe O 、CaO
2 2 2 3
等少量杂质)为主要原料制取金属锰的工艺流程如图1所示。
(1)“浸锰”步骤中往往有副产物MnS O 生成,温度对“浸锰”反应的影响如图2所示。为
2 6
减少 MnS O 的生成,“浸锰”的适宜温度是________,“滤渣Ⅰ”的成分是
2 6
____________(填化学式)。该步骤中可以再加入MnSO 以促进“滤渣Ⅰ”析出,结合平衡移
4
动 原 理 分 析 其 原 因 :
____________________________________________________________________
________________________________________________________________________。
(2)“滤液Ⅰ”中需要先加入MnO 充分反应后再调pH,写出加入MnO 时发生反应的离子方
2 2
程式:
________________________________________________________________________。
(3)“滤液Ⅱ”中加入MnF 的目的是除去溶液中的Ca2+,已知25 ℃时,K (CaF )=3.2×10
2 sp 2
-11,则常温下CaF 在纯水中的溶解度为________g。
2答案 (1)90 ℃ SiO 、CaSO c(SO)增大,使平衡Ca2+(aq)+SO(aq)CaSO(s)正向移动,
2 4 4
促进CaSO 析出 (2)MnO +2Fe2++4H+===Mn2++2Fe3++2HO (3)1.56×10-3
4 2 2
解析 流程分析:
(3)常温下CaF 溶解在纯水中,则溶液中2c(Ca2+)=c(F-),由K (CaF )=c(Ca2+)·c2(F-)可知
2 sp 2
K (CaF )=4c3(Ca2+)=3.2×10-11,解得c(Ca2+)=2×10-4 mol·L-1,则饱和CaF 溶液中
sp 2 2
c(CaF )=c(Ca2+)=2×10-4 mol·L-1,则常温下CaF 在纯水中的溶解度为1.56×10-3 g。
2 2
3.(2023·全国甲卷,26)BaTiO 是一种压电材料。以BaSO 为原料,采用下列路线可制备粉
3 4
状BaTiO 。
3
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是_______________________________________。
(2)“焙烧”后固体产物有BaCl 、易溶于水的BaS和微溶于水的CaS。“浸取”时主要反应
2
的离子方程式为_________________________________________________________。
(3)“酸化”步骤应选用的酸是____________(填标号)。
a.稀硫酸 b.浓硫酸
c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?__________________,其原因是
________________________________________________________________________。
(5)“沉淀”步骤中生成BaTiO(C O) 的化学方程式为________________________。
2 4 2(6)“热分解”生成粉状钛酸钡,产生的 ∶n =__________________。
CO
答案 (1)做还原剂,将BaSO 还原 (2)S2-+Ca2+===CaS↓ (3)c (4)不可行 CaS也会与
4
盐酸反应生成有毒气体和可溶于水的CaCl ,影响产品纯度 (5)BaCl +TiCl +2(NH )C O
2 2 4 4 2 2 4
+HO===BaTiO(C O)↓+4NH Cl+2HCl (6)1∶1
2 2 4 2 4
解析 由流程和题中信息可知,BaSO 与过量的碳粉及过量的氯化钙在高温下焙烧得到
4
CO、BaCl 、易溶于水的BaS和微溶于水的CaS;烧渣经水浸取后过滤,滤渣中含碳粉和
2
CaS,滤液中有BaCl 和BaS;滤液经酸化后浓缩结晶得到BaCl 晶体,溶于水后,加入
2 2
TiCl 和(NH )C O 将钡离子充分沉淀得到 BaTiO(C O) ;BaTiO(C O) 经热分解得到
4 4 2 2 4 2 4 2 2 4 2
BaTiO 。(3)浸取后滤液中主要为BaCl 和BaS,为不引入杂质,“酸化”步骤应选用盐酸。
3 2
(6)“热分解”生成粉状钛酸钡,该反应的化学方程式为BaTiO(C O)=====BaTiO +2CO↑
2 4 2 3 2
+2CO↑,因此,产生的 ∶n =1∶1。
CO
4.[2022·辽宁,16(1)(2)(3)(4)(5)(6)]某工厂采用辉铋矿(主要成分为BiS ,含有FeS 、SiO
2 3 2 2
杂质)与软锰矿(主要成分为MnO )联合焙烧法制备BiOCl和MnSO ,工艺流程如下:
2 4
已知:①焙烧时过量的MnO 分解为MnO,FeS 转变为Fe O;
2 2 3 2 2 3
②金属活动性:Fe>(H)>Bi>Cu;
③相关金属离子形成氢氧化物的pH范围如下:
开始沉淀pH 完全沉淀pH
Fe2+ 6.5 8.3
Fe3+ 1.6 2.8
Mn2+ 8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为_________________________。
a.进一步粉碎矿石
b.鼓入适当过量的空气
c.降低焙烧温度(2)Bi S 在空气中单独焙烧生成BiO,反应的化学方程式为___________________。
2 3 2 3
(3)“ 酸 浸 ” 中 过 量 浓 盐 酸 的 作 用 为 : ① 充 分 浸 出 Bi3 + 和 Mn2 + ;
②_______________________。
(4)滤渣的主要成分为________________(填化学式)。
(5)生成气体A的离子方程式为____________________________________________
________________________________________________________________________。
(6)加入金属Bi的目的是__________________________________________________。
答案 (1)ab (2)2Bi S +9O=====2BiO +6SO (3)抑制金属离子水解 (4)SiO (5)Mn O
2 3 2 2 3 2 2 2 3
+6H++2Cl-===2Mn2++Cl↑+3HO (6)将Fe3+转化为Fe2+
2 2
解析 (1)联合焙烧时,进一步粉碎矿石,可以增大矿石与空气的接触面积,能够提高焙烧
效率,选项a符合题意;鼓入适当过量的空气有利于矿石充分反应,选项b符合题意;降低
焙烧温度,反应速率减慢,不利于提高焙烧效率,选项c不符合题意。(6)由已知信息③知,
调pH=2.6时,Fe3+会水解生成Fe(OH) 沉淀,但Fe2+还没开始沉淀,故要将 Fe3+转化为
3
Fe2+,在调pH后获得含FeCl 的滤液,为了不引入新的杂质,加入Bi作还原剂。
2
5.以固体废锌催化剂(主要成分为ZnO及少量Fe O 、CuO、MnO、SiO)为原料制备锌的工
2 3 2
艺流程如图。
已知:①“浸取”时,ZnO、CuO转化为[Zn(NH )]2+、[Cu(NH )]2+进入溶液;
3 4 3 4
②25 ℃时,K (CuS )=6.4×10-36,K (ZnS )=1.6×10-24;
sp sp
③深度除杂标准:溶液中≤2.0×10-6。
(1)为提高锌浸出率,采取的措施是______________________________;“浸取”温度为30
℃时,锌浸出率可达90.6%,继续升温浸出率反而下降,其原因为________________。
(2)“操作a”的名称为___________________________________________________。
(3)“深度除锰”是在碱性条件下将残留的 Mn2+转化为 MnO ,离子方程式为
2
________________________________________________________________________。
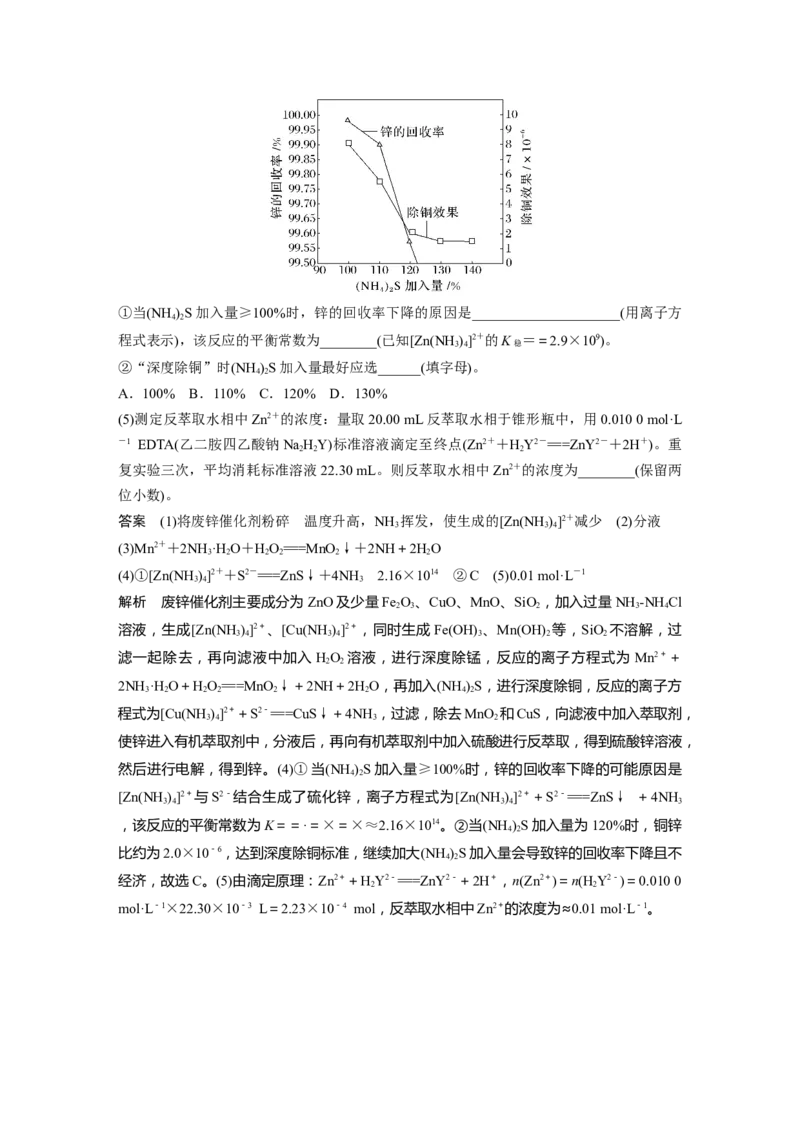
(4)“深度除铜”时,锌的回收率、除铜效果[除铜效果以反应后溶液中铜锌比表示]与
(NH )S加入量[以×100%表示]的关系曲线如图所示。
4 2①当(NH )S加入量≥100%时,锌的回收率下降的原因是_____________________(用离子方
4 2
程式表示),该反应的平衡常数为________(已知[Zn(NH )]2+的K ==2.9×109)。
3 4 稳
②“深度除铜”时(NH )S加入量最好应选______(填字母)。
4 2
A.100% B.110% C.120% D.130%
(5)测定反萃取水相中Zn2+的浓度:量取20.00 mL反萃取水相于锥形瓶中,用0.010 0 mol·L
-1 EDTA(乙二胺四乙酸钠NaHY)标准溶液滴定至终点(Zn2++HY2-===ZnY2-+2H+)。重
2 2 2
复实验三次,平均消耗标准溶液22.30 mL。则反萃取水相中Zn2+的浓度为________(保留两
位小数)。
答案 (1)将废锌催化剂粉碎 温度升高,NH 挥发,使生成的[Zn(NH )]2+减少 (2)分液
3 3 4
(3)Mn2++2NH ·H O+HO===MnO ↓+2NH+2HO
3 2 2 2 2 2
(4)①[Zn(NH )]2++S2-===ZnS↓+4NH 2.16×1014 ②C (5)0.01 mol·L-1
3 4 3
解析 废锌催化剂主要成分为ZnO及少量Fe O 、CuO、MnO、SiO ,加入过量NH -NH Cl
2 3 2 3 4
溶液,生成[Zn(NH )]2+、[Cu(NH )]2+,同时生成Fe(OH) 、Mn(OH) 等,SiO 不溶解,过
3 4 3 4 3 2 2
滤一起除去,再向滤液中加入 HO 溶液,进行深度除锰,反应的离子方程式为 Mn2++
2 2
2NH ·H O+HO===MnO ↓+2NH+2HO,再加入(NH )S,进行深度除铜,反应的离子方
3 2 2 2 2 2 4 2
程式为[Cu(NH )]2++S2-===CuS↓+4NH ,过滤,除去MnO 和CuS,向滤液中加入萃取剂,
3 4 3 2
使锌进入有机萃取剂中,分液后,再向有机萃取剂中加入硫酸进行反萃取,得到硫酸锌溶液,
然后进行电解,得到锌。(4)①当(NH )S加入量≥100%时,锌的回收率下降的可能原因是
4 2
[Zn(NH )]2+与S2-结合生成了硫化锌,离子方程式为[Zn(NH )]2++S2-===ZnS↓ +4NH
3 4 3 4 3
,该反应的平衡常数为K==·=×=×≈2.16×1014。②当(NH )S加入量为120%时,铜锌
4 2
比约为2.0×10-6,达到深度除铜标准,继续加大(NH )S加入量会导致锌的回收率下降且不
4 2
经济,故选C。(5)由滴定原理:Zn2++HY2-===ZnY2-+2H+,n(Zn2+)=n(H Y2-)=0.010 0
2 2
mol·L-1×22.30×10-3 L=2.23×10-4 mol,反萃取水相中Zn2+的浓度为≈0.01 mol·L-1。