文档内容
热点强化 17 多池电化学装置
1.常见多池串联装置图
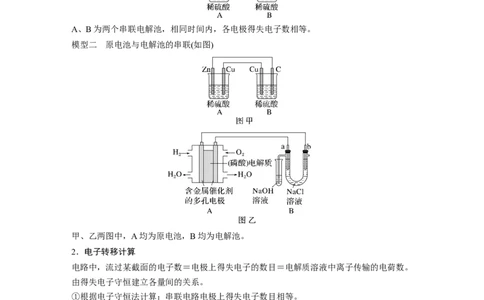
模型一 外接电源与电解池的串联(如图)
A、B为两个串联电解池,相同时间内,各电极得失电子数相等。
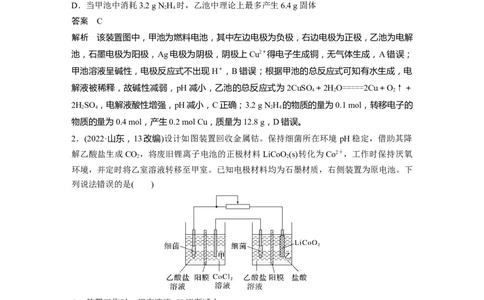
模型二 原电池与电解池的串联(如图)
甲、乙两图中,A均为原电池,B均为电解池。
2.电子转移计算
电路中,流过某截面的电子数=电极上得失电子的数目=电解质溶液中离子传输的电荷数。
由得失电子守恒建立各量间的关系。
①根据电子守恒法计算:串联电路电极上得失电子数目相等。
②根据电解方程式或电极反应式计算。
③根据关系式计算,由得失电子守恒关系建立各量间的关系,如串联电池各电极产物的关系:
O~2Cl~2Br ~4H+~4e-~2H~2Cu~4Ag~4OH-
2 2 2 2
涉及气体体积计算,使用22.4 L·mol-1时务必看清条件(标准状况),然后再进行计算。
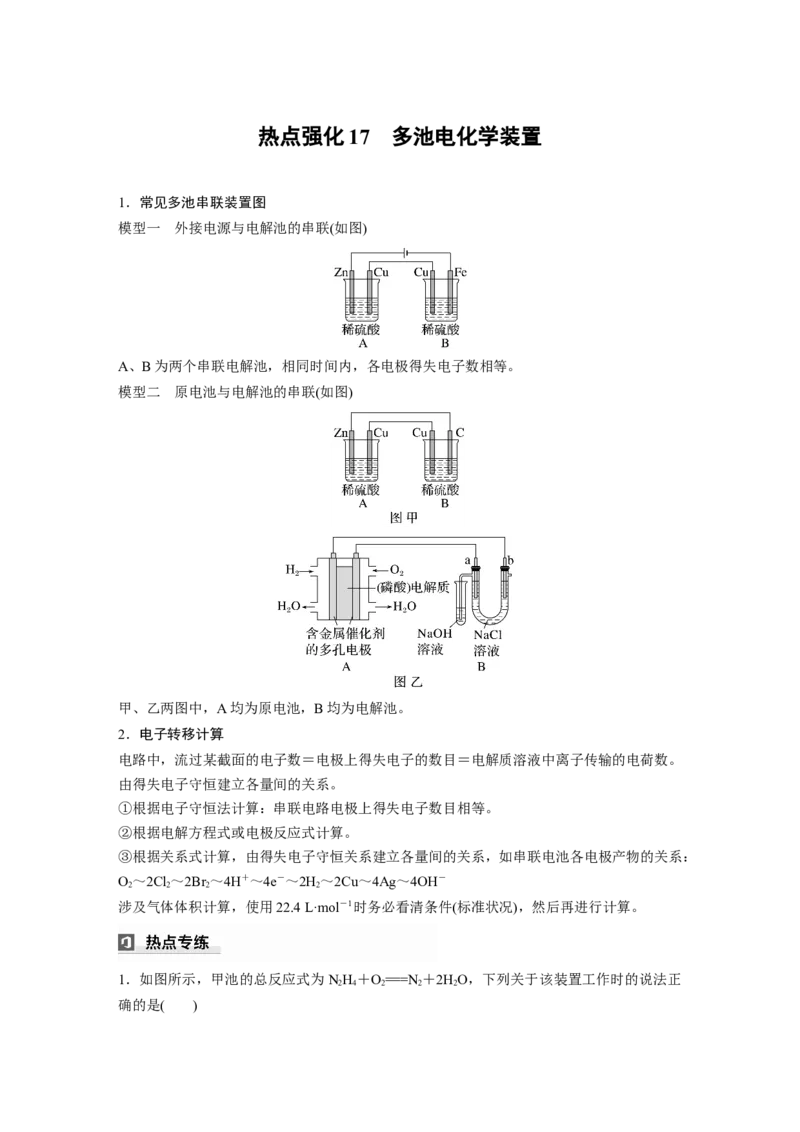
1.如图所示,甲池的总反应式为NH +O===N +2HO,下列关于该装置工作时的说法正
2 4 2 2 2
确的是( )A.该装置工作时,Ag电极上有气体生成
B.甲池中负极反应式为NH-4e-===N+4H+
2 4 2
C.甲池和乙池中溶液的pH均减小
D.当甲池中消耗3.2 g N H 时,乙池中理论上最多产生6.4 g固体
2 4
答案 C
解析 该装置图中,甲池为燃料电池,其中左边电极为负极,右边电极为正极,乙池为电解
池,石墨电极为阳极,Ag电极为阴极,阴极上Cu2+得电子生成铜,无气体生成,A错误;
甲池溶液呈碱性,电极反应式不出现H+,B错误;根据甲池的总反应式可知有水生成,电
解液被稀释,故碱性减弱,pH减小,乙池的总反应式为2CuSO +2HO=====2Cu+O↑+
4 2 2
2HSO ,电解液酸性增强,pH减小,C正确;3.2 g N H 的物质的量为0.1 mol,转移电子的
2 4 2 4
物质的量为0.4 mol,产生0.2 mol Cu,质量为12.8 g,D错误。
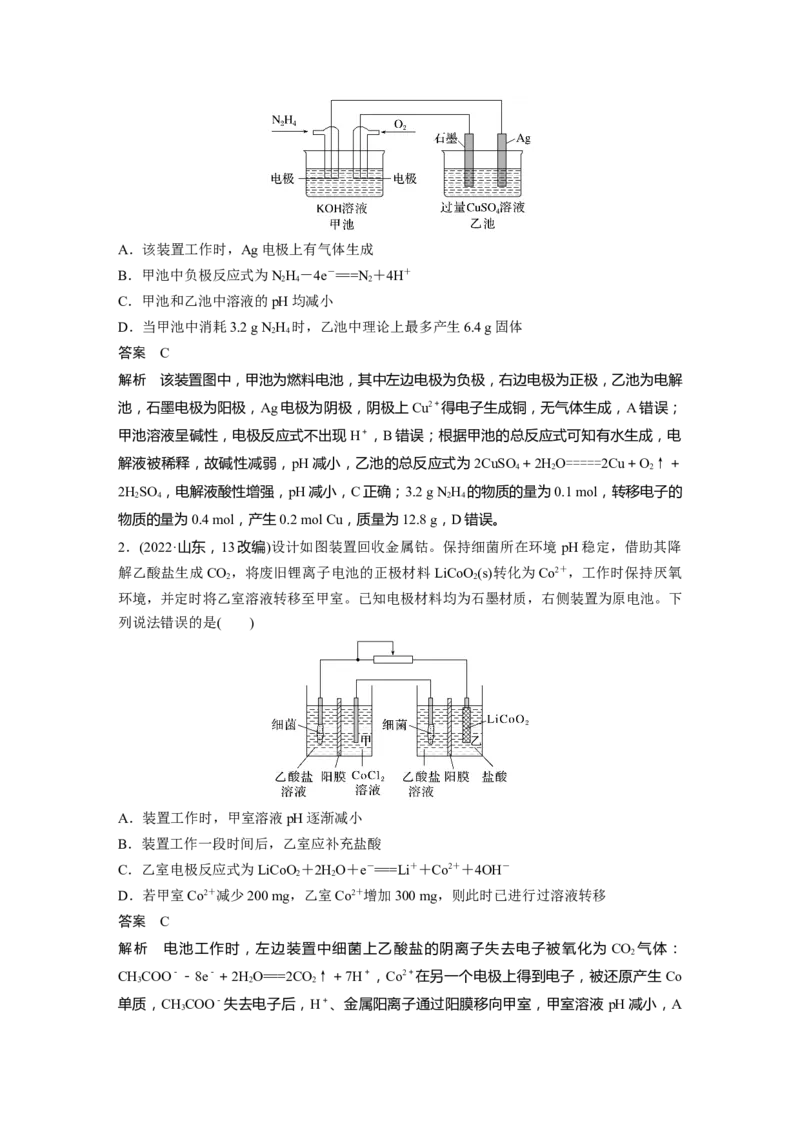
2.(2022·山东,13改编)设计如图装置回收金属钴。保持细菌所在环境 pH稳定,借助其降
解乙酸盐生成CO ,将废旧锂离子电池的正极材料LiCoO (s)转化为Co2+,工作时保持厌氧
2 2
环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下
列说法错误的是( )
A.装置工作时,甲室溶液pH逐渐减小
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为LiCoO +2HO+e-===Li++Co2++4OH-
2 2
D.若甲室Co2+减少200 mg,乙室Co2+增加300 mg,则此时已进行过溶液转移
答案 C
解析 电池工作时,左边装置中细菌上乙酸盐的阴离子失去电子被氧化为 CO 气体:
2
CHCOO--8e-+2HO===2CO↑+7H+,Co2+在另一个电极上得到电子,被还原产生Co
3 2 2
单质,CHCOO-失去电子后,H+、金属阳离子通过阳膜移向甲室,甲室溶液 pH减小,A
3正确;对于乙室,正极上LiCoO 得到电子,被还原为Co2+,同时得到Li+,电极反应式为
2
LiCoO +e-+4H+===Li++Co2++2HO,C错误;依据电子守恒,乙室消耗的 H+比负极
2 2
CHCOO-反应产生的H+多,因而需补充盐酸,B正确;根据转移电子守恒,可知没有进行
3
溶液转移时,乙室 Co2+增加的质量是甲室 Co2+减少质量的 2倍,而实际二者倍数为=
1.5<2,故此时已进行过溶液转移,D正确。
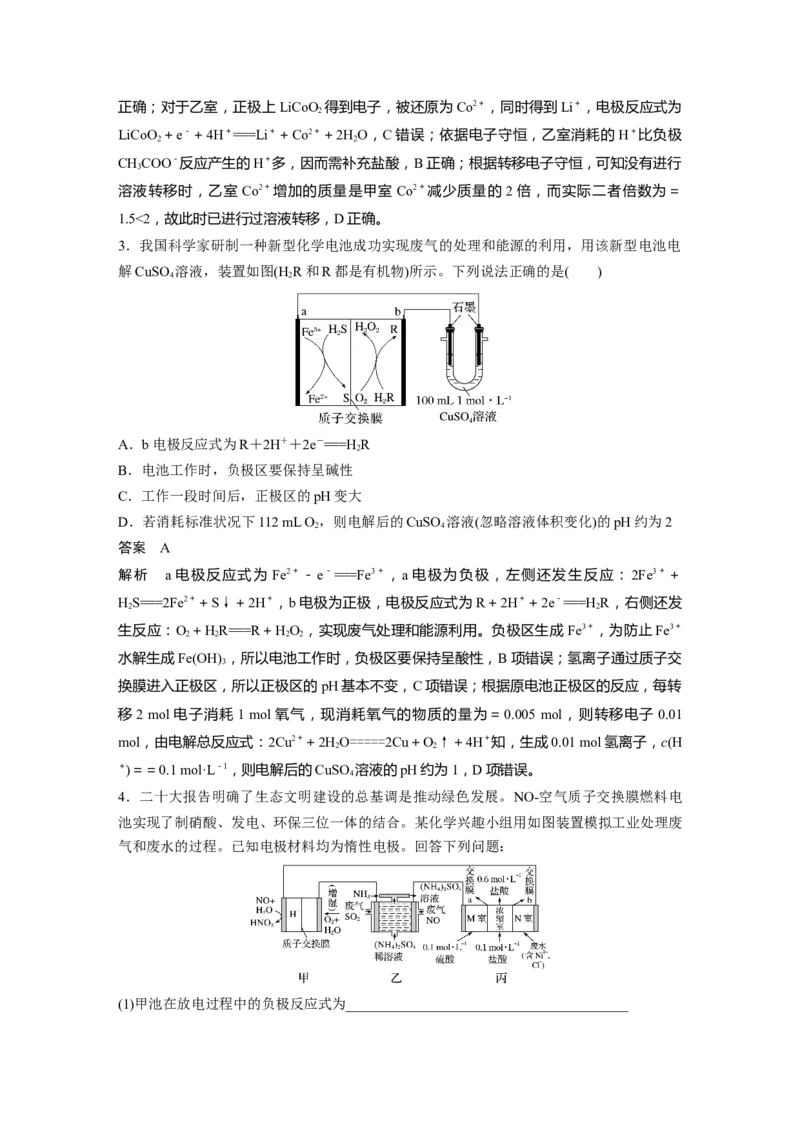
3.我国科学家研制一种新型化学电池成功实现废气的处理和能源的利用,用该新型电池电
解CuSO 溶液,装置如图(H R和R都是有机物)所示。下列说法正确的是( )
4 2
A.b电极反应式为R+2H++2e-===HR
2
B.电池工作时,负极区要保持呈碱性
C.工作一段时间后,正极区的pH变大
D.若消耗标准状况下112 mL O,则电解后的CuSO 溶液(忽略溶液体积变化)的pH约为2
2 4
答案 A
解析 a 电极反应式为 Fe2+-e-===Fe3+,a 电极为负极,左侧还发生反应:2Fe3++
HS===2Fe2++S↓+2H+,b电极为正极,电极反应式为R+2H++2e-===HR,右侧还发
2 2
生反应:O +HR===R+HO ,实现废气处理和能源利用。负极区生成 Fe3+,为防止Fe3+
2 2 2 2
水解生成Fe(OH) ,所以电池工作时,负极区要保持呈酸性,B项错误;氢离子通过质子交
3
换膜进入正极区,所以正极区的pH基本不变,C项错误;根据原电池正极区的反应,每转
移2 mol 电子消耗1 mol 氧气,现消耗氧气的物质的量为=0.005 mol,则转移电子0.01
mol,由电解总反应式:2Cu2++2HO=====2Cu+O↑+4H+知,生成0.01 mol氢离子,c(H
2 2
+)==0.1 mol·L-1,则电解后的CuSO 溶液的pH约为1,D项错误。
4
4.二十大报告明确了生态文明建设的总基调是推动绿色发展。NO-空气质子交换膜燃料电
池实现了制硝酸、发电、环保三位一体的结合。某化学兴趣小组用如图装置模拟工业处理废
气和废水的过程。已知电极材料均为惰性电极。回答下列问题:
(1)甲池在放电过程中的负极反应式为________________________________________________________________________________________________________________。
(2) 乙 池 中 通 入 废 气 SO 的 电 极 为 ____ 极 , 电 池 总 反 应 的 离 子 方 程 式 为
2
________________________________________________________________________。
(3)b为____________(填“阳”或“阴”)离子交换膜。当浓缩室得到4 L浓度为0.6 mol·L-1
的盐酸时,M室中的溶液的质量变化为____________(溶液体积变化忽略不计)。
(4)若在标准状况下,甲池有5.6 L O 参加反应,则乙池中处理废气(SO 和NO)的总体积为
2 2
____________L。
答案 (1)NO+2HO-3e-===NO+4H+ (2)阳 5SO +2NO+8HO=====2NH+5SO+8H+
2 2 2
(3)阴 减小18 g (4)15.68
解析 (1)甲池在放电过程中,负极上一氧化氮失去电子发生氧化反应生成硝酸根离子,反
应为NO+2HO-3e-===NO+4H+。(2)乙池中通入废气SO 的电极连接电源的正极,为阳
2 2
极;阳极二氧化硫发生氧化反应生成硫酸根离子,阴极一氧化氮发生还原反应生成铵根离子,
电池总反应的离子方程式为5SO +2NO+8HO=====2NH+5SO+8H+。(3)丙中阳极上水放
2 2
电发生氧化反应生成氧气和氢离子,氢离子从M室通过a膜进入浓缩室;N室中氯离子通
过b膜进入浓缩室,最终得到较浓的盐酸,故b为阴离子交换膜。当浓缩室得到4 L浓度为
0.6 mol·L-1盐酸时,迁移过来的氢离子为4 L×(0.6 mol·L-1-0.1 mol·L-1)=2 mol;2HO-
2
4e-===4H++O↑,则反应1 mol水,M室中溶液的质量变化为减少1 mol×18 g·mol-1=18
2
g。(4)乙池中SO 转化为硫酸根离子、NO转化为铵根离子;若标准状况下,甲池有 5.6 L
2
O(为0.25 mol)参加反应,根据得失电子守恒可知,O ~4e-~2SO ~NO,则乙池中处理废
2 2 2
气(SO 和NO)共0.7 mol,总体积为15.68 L。
2