文档内容
第 39 讲 盖斯定律及应用
[复习目标] 1.掌握盖斯定律的内容及意义,并能进行有关反应热的计算。2.能综合利用反
应热和盖斯定律比较不同反应体系反应热的大小。
考点一 盖斯定律与反应热的计算
1.盖斯定律的内容
一个化学反应,不管是一步完成的还是分几步完成的,其反应热是相同的。即化学反应的反
应热只与反应体系的____________有关,而与____________无关。
2.盖斯定律的意义
间接计算某些反应的反应热。
3.盖斯定律的应用
转化关系 反应热间的关系
aA――→B;A――→B ΔH=________
1
AB ΔH=________
1
ΔH=________
一、应用循环图分析焓变关系
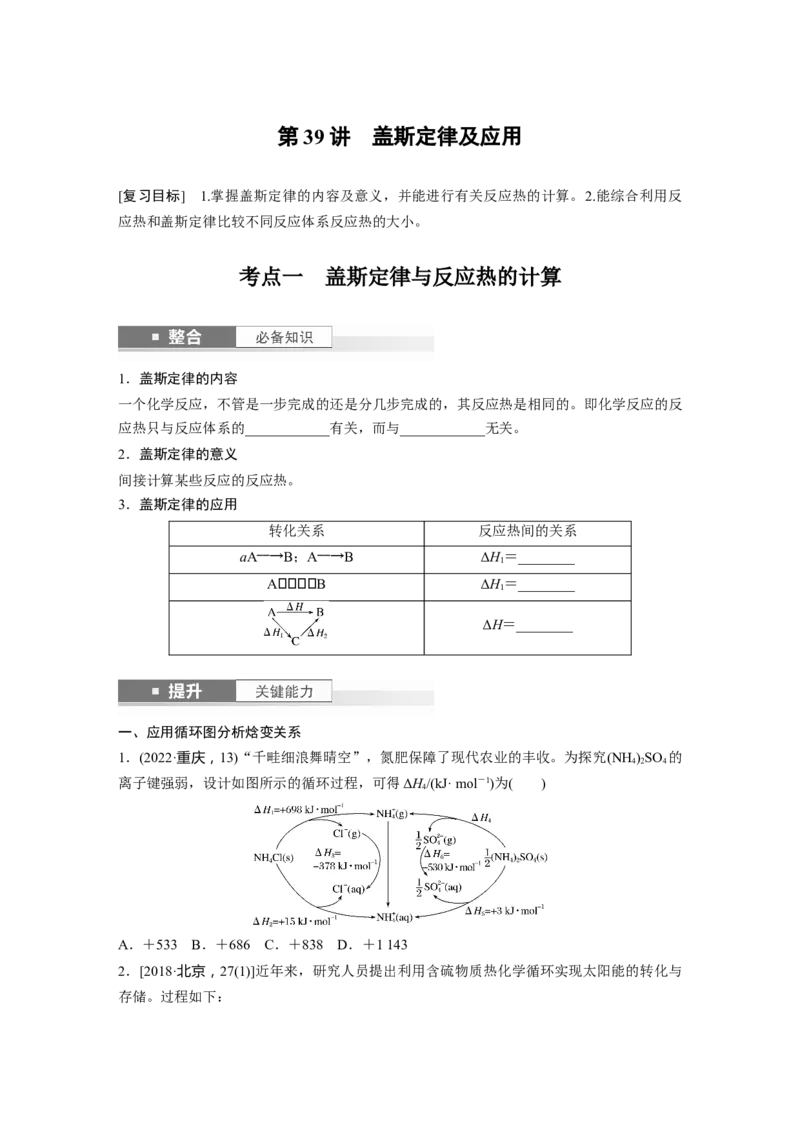
1.(2022·重庆,13)“千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为探究(NH )SO 的
4 2 4
离子键强弱,设计如图所示的循环过程,可得ΔH/(kJ· mol-1)为( )
4
A.+533 B.+686 C.+838 D.+1 143
2.[2018·北京,27(1)]近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与
存储。过程如下:反应 Ⅰ:2HSO (l)===2SO (g)+2HO(g)+O(g) ΔH=+551 kJ·mol-1
2 4 2 2 2 1
反应Ⅲ:S(s)+O(g)===SO (g)
2 2
ΔH=-297 kJ·mol-1
3
反应Ⅱ的热化学方程式:________________________________________________________
______________________________________________________________________________。
二、消元法计算反应热
3.[2023·山东,20(1)]一定条件下,水气变换反应 CO+HOCO +H 的中间产物是
2 2 2
HCOOH。为探究该反应过程,研究HCOOH水溶液在密封石英管中的分解反应:
Ⅰ.HCOOHCO+HO(快)
2
Ⅱ.HCOOHCO+H(慢)
2 2
一定条件下,反应Ⅰ、Ⅱ的焓变分别为ΔH 、ΔH ,则该条件下水气变换反应的焓变ΔH=
1 2
__________(用含ΔH、ΔH 的代数式表示)。
1 2
4.[2023·全国乙卷,28(2)改编]硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小
麦黑穗病,制造磁性氧化铁、铁催化剂等。
已知下列热化学方程式:
FeSO ·7H O(s)===FeSO (s)+7HO(g) ΔH=a kJ·mol-1
4 2 4 2 1
FeSO ·4H O(s)===FeSO (s)+4HO(g) ΔH=b kJ·mol-1
4 2 4 2 2
FeSO ·H O(s)===FeSO (s)+HO(g) ΔH=c kJ·mol-1
4 2 4 2 3
则FeSO ·7H O(s)+FeSO ·H O(s)===2(FeSO ·4H O)(s)的ΔH=________________________
4 2 4 2 4 2
____________________________________________________________________kJ·mol-1。
5.[2023·湖南,16(1)]已知下列反应的热化学方程式:
①C HC H(g)+O(g)===8CO(g)+5HO(g) ΔH=-4 386.9 kJ·mol-1
6 5 2 5 2 2 2 1
②C HCH===CH(g)+10O(g)===8CO(g)+4HO(g) ΔH=-4 263.1 kJ·mol-1
6 5 2 2 2 2 2
③H(g)+O(g)===HO(g) ΔH=-241.8 kJ·mol-1
2 2 2 3
计算反应④C HC H(g)C HCH===CH(g)+H(g)的ΔH=____________kJ·mol-1。
6 5 2 5 6 5 2 2 4
消元法计算反应热的思维流程考点二 反应热大小的比较
比较反应热大小注意事项
(1)在比较反应热(ΔH)的大小时,应带符号比较。
(2)同一物质,不同聚集状态时具有的能量不同,相同量的某物质的能量关系:
E(物质R,g)>E(物质R,l)>E(物质R,s)。
(3)同一化学反应,反应物的用量越多,|ΔH|越大。对于可逆反应,因反应不能进行完全,实
际反应过程中放出或吸收的热量要小于理论数值。
(4)等量的可燃物完全燃烧所放出的热量比不完全燃烧所放出的热量多,则完全燃烧的ΔH较
小。
一、画能量变化图比较反应热大小(同一反应,物质聚集状态不同时)
1.已知:
S(g)+O(g)===SO (g) ΔH<0
2 2 1
S(s)+O(g)===SO (g) ΔH<0
2 2 2
比较ΔH 与ΔH 的大小。
1 2
______________________________________________________________________________
2.已知石墨比金刚石稳定,
C(s,石墨)+O(g)===CO(g)
2 2
ΔH=-a kJ·mol-1
1
C(s,金刚石)+O(g)===CO(g)
2 2
ΔH=-b kJ·mol-1
2
比较ΔH 与ΔH 的大小。
1 2
______________________________________________________________________________
二、利用盖斯定律计算比较反应热大小
3.已知:
①2Al(s)+O(g)===Al O(s) ΔH
2 2 3 1
②2Fe(s)+O(g)===Fe O(s) ΔH
2 2 3 2
比较ΔH 与ΔH 的大小,写出分析过程。
1 2
______________________________________________________________________________
______________________________________________________________________________
4.对于反应a:C H(g)C H(g)+H(g),反应b:2CH(g)C H(g)+2H(g),当升高温
2 4 2 2 2 4 2 4 2
度时平衡都向右移动。①C(s)+2H(g)===CH(g) ΔH;②2C(s)+H(g)===C H(g)
2 4 1 2 2 2
ΔH ;③2C(s)+2H(g)===C H(g) ΔH 。则①②③中ΔH 、ΔH 、ΔH 的大小顺序排列正确
2 2 2 4 3 1 2 3的是( )
A.ΔH>ΔH>ΔH
1 2 3
B.ΔH>ΔH>2ΔH
2 3 1
C.ΔH>2ΔH>ΔH
2 1 3
D.ΔH>ΔH>ΔH
3 2 1