文档内容
巴蜀中学 2023 届高考适应性月考卷(一)
化学参考答案
一、选择题:本题共14小题,每小题3分。
题号 1 2 3 4 5 6 7
答案 C C A B D A C
题号 8 9 10 11 12 13 14
答案 B D C D D D C
【解析】
1.在水溶液中电离出的阴离子全部是OH−的化合物是碱,故答案选C。
2.汽车尾气催化转化器可有效地将CO转化为CO ,不能减少CO 的排放,故A错误。锡比
2 2
铅活泼,锡做负极,加速锡的腐蚀,故B错误。石墨烯可导电,具有金属晶体的性质,原
子间形成共价键,具有共价晶体的性质,石墨烯属于混合型晶体,故C正确。聚氯乙烯塑
料中加入增塑剂会释放有毒物质,不可用于制作不粘锅的耐热涂层,故D错误。
3.OH−电子式为 ,故A错误。
4.甲烷与氯气反应需要光照,故A错误。FeCl 溶液蒸干过程中促进FeCl 水解得到Fe(OH)
3 3 3
固体,故C错误。实验室用NaOH溶液吸收SO 尾气,故D错误。
2
5.每个Ca2+周围距离最近且等距的F−有8个,故D错误。
6.石灰石难溶物,不能拆为离子,故A错误。
7.K c(CO ),温度不变,K 不变,c(CO )不变,故C错误。
c 2 c 2
8.乙酸与乙醇的酯化反应是可逆反应,故A错误。Fe2+还原性强于Br−,Cl 先氧化Fe2+再氧
2
化Br−,0.2mol Fe2+需要0.1mol Cl ,余下0.05mol Cl 只能氧化0.1mol Br−,故C错误。根
2 2
据质量守恒可得6X,0.5mol X的中子数为2N ,故D错误。
2 A
9.根据化合物的结构可推出M为Na、X为O、Y为B、Z为H。Na+半径小于O2−,故A错
误。阴离子中的B有sp2和sp3两种杂化方式,阴离子的所有原子不可能共平面,故B错
误。X与Z可形成H O ,该物质既含极性键也含非极性键,故C错误。X、Y、Z三种元
2 2
素可形成H BO ,故D正确。
3 3
化学参考答案·第1页(共6页)10.根据推断M为 ,N为 或 ,L
为 。N 没有顺反异构,故 A 错误。M 的同分异构体有
、 、
CH Cl—CH —CH —CH —CH 、 、 、
2 2 2 2 3
、 ,最多有 1 个手性碳原子,故 B 错误。M 的同
分异构体中核磁共振氢谱只有两组峰的是 ,共1种,故C正确。L的同分异
构体中能被氧化成酮的有 、 、
,共3种,故D错误。
11.Mn元素肯定参与的氧化还原反应有KMnO 受热分解、K MnO 、MnO 分别与浓盐酸反
4 2 4 2
应。若 KMnO 没有完全分解,它还会与浓盐酸反应。Mn元素至少参与了 3个氧化还
4
原反应,故 C 正确。利用整体法依据得失电子守恒可知,4n(O )+2n(Cl )=0.5,n(O )=
2 2 2
0.02mol时,n(Cl )=0.21mol,故D错误。
2
12.(CH ) CBr到(CH ) C+碳原子由sp3杂化变为sp2杂化,(CH ) C+到(CH ) COH碳原子由sp2
3 3 3 3 3 3 3 3
杂化变为sp3杂化,故A正确。根据反应热等于生成物能量减去反应物能量,H (E E )
5 1
kJ/mol,故 B 正确。E E E E 移项得E E E E ,第一步反应的活化能大于
3 2 4 1 2 1 4 3
第二步,第一步速率慢,是决速步,故C正确。H 反应物键能总和−生成物键能总和,
75E(C—Br)351,E(C—Br)276kJ/mol,故D错误。
13.由题意可知,二氧化硫在电解池中与溶液中I−反应生成碘离子、硫酸根离子和氢离子,离
3
子方程式为SO +I−+2H O=3I−+SO2−+4H+,故A正确。由题意可知,测硫仪工作时,
2 3 2 4
碘离子在阳极失去电子发生氧化反应生成碘三离子,电极反应式为3I−−2e−=I−,故B
3
化学参考答案·第2页(共6页)正确。碘离子与电解生成的碘反应生成碘三离子,不会影响测得的全硫含量,故C正确。
由题意可得如下关系:S—SO —I−—2e−,电解消耗的电量为x库仑,则煤样中硫的质量分
2 3
x
32
296500 16x
数为 100% %,故D错误。
a 965a
14.步骤Ⅰ实验现象说明存在还原性微粒,根据离子共存原则,只存在 Fe2+和 SO2−中的一种
3
微粒。若存在Fe2+,根据步骤Ⅱ现象一定存在SO2−,根据电荷守恒,K+、Na+、Al3+一定
4
不存在;若存在 SO2−,一定没有 Al3+,根据电荷守恒一定有 K+、Na+,一定没有 SO2−,
3 4
故C正确。
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空2分,共14分)
(1)[Ar]3d14s2(1分) 高(1分)
(2)分液
(3)2OH−+Sc(OH) =[Sc(OH) ]2−
3 5
(4)加入大量水,同时加热
(5)AlCl +FeCl +(6−m)NaHCO =AlFe(OH) Cl ↓+(6−m)CO ↑+(6−m)NaCl
3 3 3 (6-m) m 2
(6)ScF+
2
k c
(7)lg 2
3 k
3
a2
【解析】(1)因为Sc是21号元素,所以基态Sc原子的核外电子排布式为[Ar]3d14s2;H C O
2 2 4
分子间氢键比CH COOH多,沸点高。
3
(2)据流程图可知:操作①为分液。
(3)据题意可知离子方程式为2OH−+Sc(OH) =[Sc(OH) ]2−。
3 5
(4)用TiCl 制备TiO ·xH O的反应为TiCl +(x+2)H O=TiO ·xH O↓+4HCl;在制
4 2 2 4 2 2 2
备时加入大量水,同时加热,可使水解趋于完全。
(5)据题意可知化学方程式为 AlCl +FeCl +(6−m)NaHCO =AlFe(OH) Cl ↓+
3 3 3 (6−m) m
(6−m)CO ↑+(6−m)NaCl。
2
(6)若溶液中c(F)4106,则lgc(F)lg4106 5.4,调节pH4,据图可知三价
Sc的存在形式为ScF+。
2
c(H)c(C O2) K c
(7)∵K c2[Sc3]c3[C O2],且K 2 4 ,可知c(C O2) a2 代入
sp 2 4 a2 c(HC O) 2 4 c(H)
2 4
化学参考答案·第3页(共6页)3
K c K c k c k c
K 表达式,推出K a2 a2 ,c(H) a2 2 ,∴pHlgc(H) lg 2
sp sp c(H) 3 K 3 k 3 k
sp 3 3
a2 a2 a2
(表达式合理即可)。
16.(除特殊标注外,每空2分,共14分)
(1)Ⅲ Ⅱ Ⅰ(共2分)
(2)浓硫酸(1分)
(3)MnO +2Cl−+4H+== △ ===Mn2++Cl ↑+2H O
2 2 2
(4)Ⅲ(1分)
(5)烧杯、漏斗、玻璃棒
催化剂
(6)10NH +2CoCl +2NH Cl+H O =====2[Co(NH ) ]Cl +2H O(写NH ·H O也可给分)
3 2 4 2 2 △ 3 6 3 2 3 2
(7)当滴入最后一滴Na S O 标准溶液,溶液由蓝色褪为无色,并且半分钟内不再恢复蓝色
2 2 3
(8)65
【解析】(1)据题意可知,Ⅰ为发生装置,Ⅱ为除杂装置,Ⅲ为 Cl 制备装置,∴顺序为
2
Ⅲ→Ⅱ→Ⅰ。
(2)∵CoCl 易潮解,∴试剂X为浓硫酸。
2
(3)据题意可知,Ⅲ中离子方程式为MnO +4H++2Cl−== △ === Mn2++Cl ↑+2H O。
2 2 2
(4)因为要用产生的Cl 排尽装置中空气,所以先加热Ⅲ。
2
(5)过滤时用到的玻璃仪器为烧杯、漏斗、玻璃棒。
催化剂
(6)Ⅳ中总反应为10NH +2CoCl +2NH Cl+H O =====2[Co(NH ) ]Cl +2H O。
3 2 4 2 2 △ 3 6 3 2
(8)据方程式的得失电子数目守恒可得如下转化关系:2[Co(NH ) ]Cl ~2Co3+~I ~2Na S O ,
3 6 3 2 2 2 3
250
0.1000molL126103L 267.5g/mol
25
∴样品纯度为 100%65%。
10.7g
17.(除特殊标注外,每空2分,共15分)
(1)>(1分)
(2)①由3d64s2变为3d6
② 2Fe+O 2FeO为放热反应,温度升高平衡左移,x(O )增大 温度高于T ℃
2 2 1
时,x(O )大于21%,载氧体无法载氧
2
③1∶1 p2
0
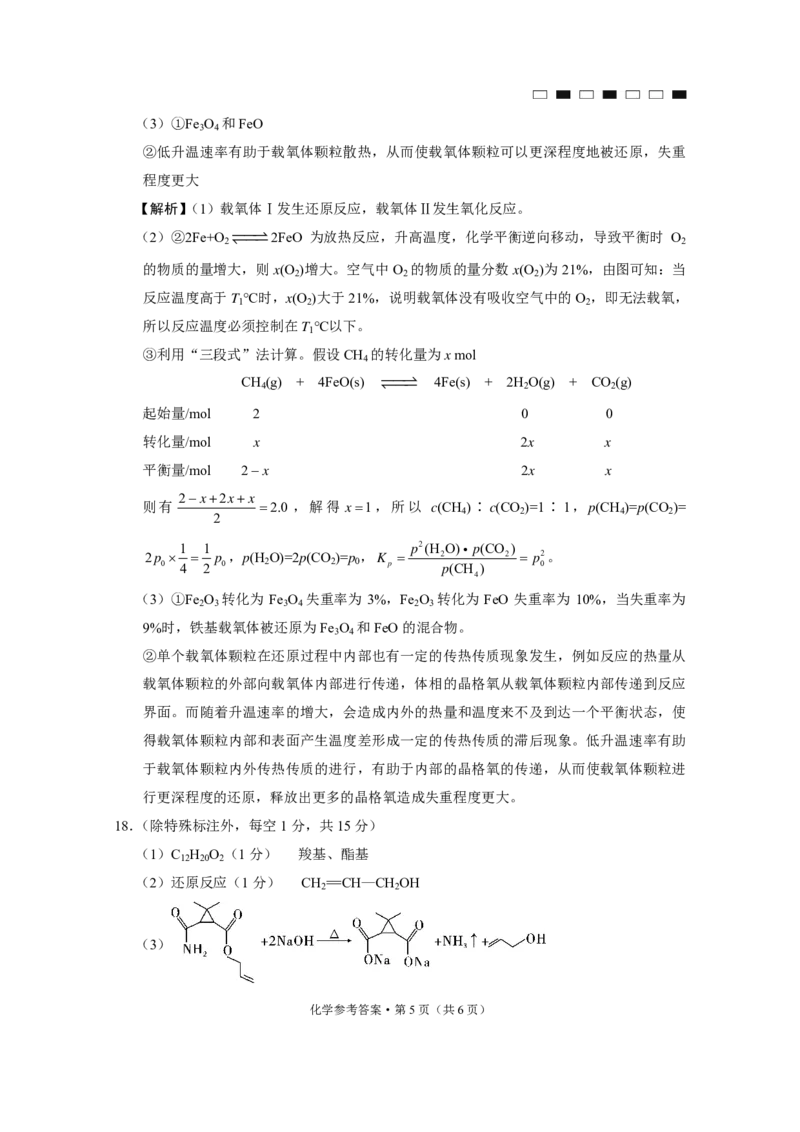
化学参考答案·第4页(共6页)(3)①Fe O 和FeO
3 4
②低升温速率有助于载氧体颗粒散热,从而使载氧体颗粒可以更深程度地被还原,失重
程度更大
【解析】(1)载氧体Ⅰ发生还原反应,载氧体Ⅱ发生氧化反应。
(2)②2Fe+O 2FeO 为放热反应,升高温度,化学平衡逆向移动,导致平衡时 O
2 2
的物质的量增大,则 x(O )增大。空气中O 的物质的量分数x(O )为21%,由图可知:当
2 2 2
反应温度高于T ℃时,x(O )大于21%,说明载氧体没有吸收空气中的O ,即无法载氧,
1 2 2
所以反应温度必须控制在T ℃以下。
1
③利用“三段式”法计算。假设CH 的转化量为x mol
4
CH (g) + 4FeO(s) 4Fe(s) + 2H O(g) + CO (g)
4 2 2
起始量/mol 2 0 0
转化量/mol x 2x x
平衡量/mol 2x 2x x
2x2xx
则有 2.0 ,解得 x1,所以 c(CH )∶c(CO )=1∶1,p(CH )=p(CO )=
4 2 4 2
2
1 1 p2(H O) p(CO )
2p p ,p(H O)=2p(CO )=p ,K 2 2 p2。
0 4 2 0 2 2 0 p p(CH ) 0
4
(3)①Fe O 转化为 Fe O 失重率为 3%,Fe O 转化为 FeO 失重率为 10%,当失重率为
2 3 3 4 2 3
9%时,铁基载氧体被还原为Fe O 和FeO的混合物。
3 4
②单个载氧体颗粒在还原过程中内部也有一定的传热传质现象发生,例如反应的热量从
载氧体颗粒的外部向载氧体内部进行传递,体相的晶格氧从载氧体颗粒内部传递到反应
界面。而随着升温速率的增大,会造成内外的热量和温度来不及到达一个平衡状态,使
得载氧体颗粒内部和表面产生温度差形成一定的传热传质的滞后现象。低升温速率有助
于载氧体颗粒内外传热传质的进行,有助于内部的晶格氧的传递,从而使载氧体颗粒进
行更深程度的还原,释放出更多的晶格氧造成失重程度更大。
18.(除特殊标注外,每空1分,共15分)
(1)C H O (1分) 羧基、酯基
12 20 2
(2)还原反应(1分) CH =CH—CH OH
2 2
(3)
化学参考答案·第5页(共6页)(4)
(5) 或
(6)
(3分)
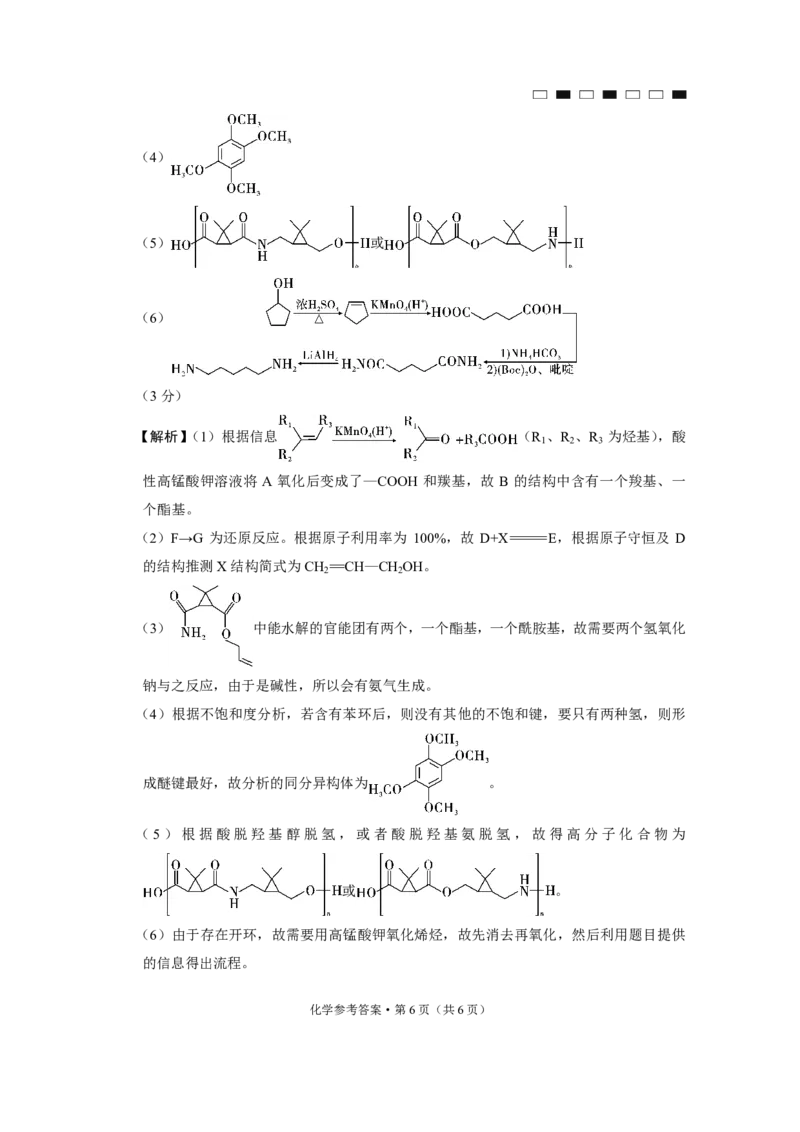
【解析】(1)根据信息 (R 、R 、R 为烃基),酸
1 2 3
性高锰酸钾溶液将 A 氧化后变成了—COOH 和羰基,故 B 的结构中含有一个羧基、一
个酯基。
(2)F→G 为还原反应。根据原子利用率为 100%,故 D+X=E,根据原子守恒及 D
的结构推测X结构简式为CH =CH—CH OH。
2 2
(3) 中能水解的官能团有两个,一个酯基,一个酰胺基,故需要两个氢氧化
钠与之反应,由于是碱性,所以会有氨气生成。
(4)根据不饱和度分析,若含有苯环后,则没有其他的不饱和键,要只有两种氢,则形
成醚键最好,故分析的同分异构体为 。
(5)根据酸脱羟基醇脱氢,或者酸脱羟基氨脱氢,故得高分子化合物为
或 。
(6)由于存在开环,故需要用高锰酸钾氧化烯烃,故先消去再氧化,然后利用题目提供
的信息得出流程。
化学参考答案·第6页(共6页)