文档内容
2024 届新高三开学摸底考试卷
化 学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干
净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cu 64 Zn 65
第Ⅰ卷(选择题 共42分)
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.我国力争2030年前实现碳达峰,2060年前实现碳中和,事关中华民族永续发展和构建人类命运共同
体。下列措施中不能减少污染并降碳排放的是
A.完善充电桩、自行车道等相应的配套设施建设,引导公众优先绿色出行
B.大规模开采可燃冰作为新能源和通过清洁煤技术减少煤燃烧污染
C.支持风力发电、光伏发电、潮汐发电等行业健康有序发展
D.加大农村房屋建筑节能改造力度,降低冬季取暖燃料的使用
2.下列化学用语表示正确的是
A.镁原子的结构示意图: B.2-丁烯的键线式:
C.邻羟基苯甲醛分子内氢键: D.乙烯的空间填充模型:
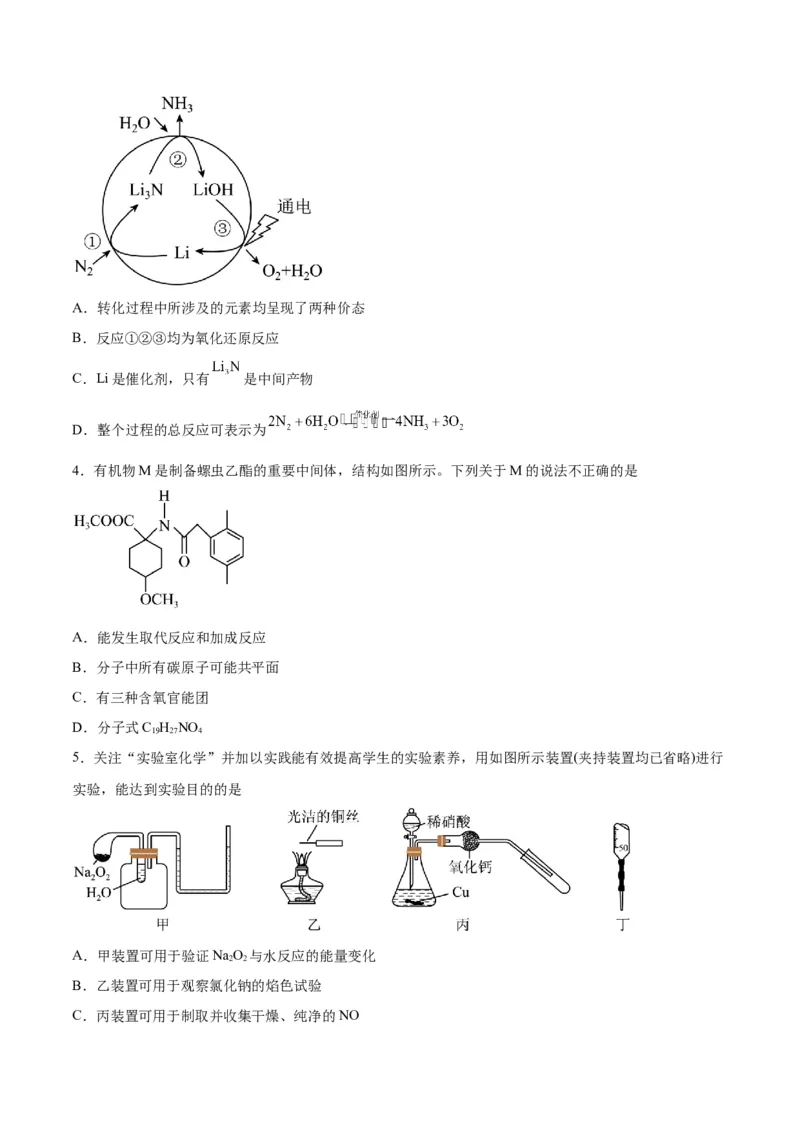
3.固氮是将游离态的氮转变为氮的化合物,一种新型人工固氮的原理如图所示。下列叙述正确的是A.转化过程中所涉及的元素均呈现了两种价态
B.反应①②③均为氧化还原反应
C.Li是催化剂,只有 是中间产物
D.整个过程的总反应可表示为
4.有机物M是制备螺虫乙酯的重要中间体,结构如图所示。下列关于M的说法不正确的是
A.能发生取代反应和加成反应
B.分子中所有碳原子可能共平面
C.有三种含氧官能团
D.分子式C H NO
19 27 4
5.关注“实验室化学”并加以实践能有效提高学生的实验素养,用如图所示装置(夹持装置均已省略)进行
实验,能达到实验目的的是
A.甲装置可用于验证NaO 与水反应的能量变化
2 2
B.乙装置可用于观察氯化钠的焰色试验
C.丙装置可用于制取并收集干燥、纯净的NOD.丁装置可用于准确量取一定体积的KCr O 溶液
2 2 7
6.能正确表示下列反应的离子方程式的是
A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H ↑
2
B.钠与硫酸铜溶液反应:2Na+Cu2+=Cu+2Na+
C.过量铁与稀硝酸反应:Fe+4H++ =3Fe3++2H O+NO↑
2
D.等物质的量的Ba(OH) 与NaHSO 在溶液中反应:Ba2++OH−+H++ =BaSO ↓+H O
2 4 4 2
7.设 为阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,48gO 的价层电子中所含的孤电子对数为
3
B.1mol液态水完全转化为固态冰,则最多新形成的氢键数为
C.40g的金刚砂(SiC)中,所含的碳硅键个数为
D.标准状况下22.4L的乙炔与氢气完全加成,共有 的共价键发生断裂
8.X、Y、Z、J、Q是原子序数依次增大,且分布在三个短周期的主族元素,Y元素原子的核外未成对电
子数在同周期中最多,Y、Z同周期,Z、J同主族.下列说法错误的是
A.电负性:Q>J;第一电离能:Y>Z B.最高价含氧酸的酸性:Q>J
C. 、 的中心原子杂化方式相同 D.简单离子半径:Y>Z、J>Q
9.某溶液仅由 、Cl-、 、 、 、Fe3+、Al3+和K+中的若干种离子组成,且各离子浓度相
等,取适量溶液进行如下实验:
①取该溶液加入过量NaOH溶液,加热,产生无色气体;
②将①过滤、洗涤、灼烧,得到固体a;
③向上述滤液中加足量BaCl 溶液,产生白色沉淀:
2
根据以上实验,下列推断错误的是
A.根据操作①,推断一定存在
B.②中固体a为氧化铁C.原溶液中一定不存在 、Al3+,可能含有K+
D.说明原溶液中一定存在 、Cl-、 、 、Fe3+、
10.一种利用废旧镀锌铁皮制备磁性Fe O 纳米粒子的工艺流程如图。
3 4
下列有关说法不正确的是
A.“碱洗”是为了去除废旧镀锌铁皮表面的油污
B.“氧化”时发生反应的离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H O
2
C.“氧化”后的溶液中金属阳离子主要有Fe2+、Fe3+、Na+
D.用激光笔照射“加热沉铁”后所得分散系,产生丁达尔效应
11.将amolX、Y混合气体(物质的量之比为1∶1)加入某容积可变的密闭容器中,发生反应:
,保持一定温度,改变压强分别达到平衡时,测得不同压强下气体X的物质的量浓度如表所示:
压强p/Pa 2×105 5×105 1×106 3×106
0.08 0.20 0.40 0.80
下列说法正确的是
A.保持一定温度,增大压强,平衡正向移动
B.当压强为3×106Pa时,此反应的平衡常数表达式为
C.2×105Pa时X的平衡转化率大于5×105Pa时X的平衡转化率
D.当压强为2×105Pa时,若再向体系中加入bmolY,重新达到平衡时,体系中气体总物质的量为
12.下列实验操作及现象、实验结论均正确的是
选
实验操作及现象 实验结论
项NO 一定为碳还原浓硝酸的产
A 将炽热的木炭加入浓硝酸中,产生红棕色气体 2
物
B 用pH计测量NaHCO 溶液呈碱性,NaHSO 溶液呈酸性 碳酸、亚硫酸均为弱酸
3 3
向装有溴水的分液漏斗中加入苯,振荡静置,溶液分层,上层为橙
C 苯萃取了溴水中的溴
红色
D 向HO 溶液中滴入几滴酸性高锰酸钾溶液,高锰酸钾紫色褪去 HO 有氧化性
2 2 2 2
A.A B.B C.C D.D
13.据2022年1月统计,我国光伏发电并网装机容量突破3亿千瓦,连续七年稳居全球首位。已知四甲基
氢氧化铵[(CH )NOH]常用作电子工业清洗剂,以四甲基氯化铵[(CH )NCl]为原料,采用电渗析法合成
3 4 3 4
[(CH )NOH],工作原理如图。下列说法错误的是
3 4
A.光伏并网发电装置中P型半导体为正极
B.c为阳离子交换膜,d、e均为阴离子交换膜
C.阳极的电极反应为4OH--4e-=2H O+O↑
2 2
D.制备182g四甲基氢氧化铵,两极共产生33.6L气体(标准状况)
14.某温度下,25mL含KX和KY的混合溶液,用0.1000mol•L-1的硝酸银标准溶液对该混合液进行电位滴
定(在滴定过程中,随着滴定剂的不断加入,电极电位E不断发生变化,电极电位发生突跃时,说明滴定到
达终点)、获得电动势(E)和银硝酸银标准溶液体积(V)的电位滴定曲线如图所示。
已知:I.Ag+与Y-反应过程为:①Ag++2Y- [AgY ]-、②[AgY ]-+Ag+ 2AgY↓。
2 2
II.该温度下,K (AgY)=2×10-16,K (AgX)=2×10-10
sp sp
III.Y-与H+的反应可以忽略。
下列说法不正确的是
A.若HY为弱酸,则从开始到A点,水的电离程度不断减小
B.原混合溶液中c(KX)=0.02000mol•L-1,c(KY)=0.03000mol•L-1
C.若反应①的平衡常数为K,反应②的平衡常数为K,则 =K (AgY)
1 2
D.将AgX和AgY的饱和溶液等体积混合,加入足量硝酸银溶液,析出固体AgX多于AgY
第 II 卷(非选择题 共 58 分)
二、非选择题:本题共4个小题,共58分。
15.(14分)以盐湖锂精矿(主要成分为LiCO,还含有少量的CaCO )和盐湖卤水(含一定浓度的LiCl 和
2 3 3
MgCl )为原料均能制备高纯LiCO。回答下列问题:
2 2 3
(1)由锂精矿为原料制取碳酸锂的过程中,需要先“碳化溶解”使LiCO 转为LiHCO ,实验装置如图所
2 3 3
示。
已知: I.20℃时LiOH的溶解度为12.8g。
II.LiCO 在不同温度下的溶解度:0℃ 1.54 g,20℃ 1.33 g,80℃ 0.85 g。
2 3
①装有盐酸的仪器的名称为 。
②装置B中盛放的试剂为 ,其作用是 。
③装置C中除了生成LiHCO ,还可能生成的杂质为 (填化学式)。
3
④装置C中的反应需在常温下进行,温度越高锂精矿转化率越小的原因可能是 。保持温度、反应时
间、反应物和溶剂的量不变,实验中提高锂精矿转化率的操作有 。
⑤热解过滤获得的LiCO 表面有少量LiC O,不进行洗涤也不会影响最终LiCO 产品的纯度,其原因是
2 3 2 2 4 2 3
。(2)设计由盐湖卤水制取高纯LiCO 的实验方案:向浓缩后的盐湖卤水中 。(实验中必须使用的试
2 3
剂:NaOH溶液、NaCO 溶液;已知:pH= 10时Mg(OH) 完全沉淀)
2 3 2
16.(14分)某湿法炼锌的萃余液中含有 及二价钴离子( )、镍离子( )、镉
离子( )和 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
已知:
沉淀物
(1)“氧化、调 ”时,先加入适量的石灰石调节pH为1.0,加入适量的 ,再加入石灰石 为
4.0,
①“沉渣”的主要成分除 外还有_______。
②若加入过量的 ,钴元素会被氧化进入“沉渣”中,则溶液中残留 的浓度为____ 。
(2)“沉锌”时,在近中性条件下加入 可得碱式碳酸锌 固体,同时产生大量
的气体,试分析产生大量气体的原因是_____________________________。
(3)由碱式碳酸锌生成氧化锌的化学方程式为______________________________。
(4)沉锌后的滤液经过一系列操作后得到的副产品为________________________(填化学式)。
(5) 的晶胞结构如图,则锌的配位数为___________;已知晶胞参数为acm,该晶体的密度为
___________ (写出计算式,阿佛加德罗常数的值为 )。17.(15分) 循环再利用制备甲烷、甲醇等有机燃料,变废为宝历来是化学重要的研究领域。为了减
少 的排放,可用下列方法把 转化成燃料,试回答下列问题:
a.
b.
(1)已知c. ,则 ;反应a在
(选填“高温”、“低温”或“任意温度”)下,易自发进行。
(2)向刚性容器中充入一定量的 和 ,在不同催化剂(Cat.1,Cat.2)下经相同反应时间, 的转化率和
甲醇的选择性[甲醇的选择性 ]随温度的变化如图:
①由图可知,催化效果Cat.1 Cat.2(填“>”“<”或“=”)。
②在210~270℃间, 的选择性随温度的升高而下降,请写出一条可能原因 。(3)一定条件下,向刚性容器中充入物质的量之比为1:3的 和 发生上述反应。
①有利于提高甲醇平衡产率的条件是 (填标号)。
A.高温高压 B.低温高压 C.高温低压 D.低温低压
②达到平衡时 的转化率为20%, 的选择性为75%,则 的转化率为 ;反应b的压
强平衡常数 。(压强平衡常数为用分压表示的化学平衡常数,分压=总压×物质的量分数)
18.(15分)高聚物G是一种广泛用在生产生活中的合成纤维,由A与E为原料制备J和G的合成路线如
下:
已知:①酯能被LiAlH 还原为醇
4
②
回答下列问题:
(1)A的名称为 ,E中官能团的名称为 。
(2)B生成C的化学方程式为 。
(3)D转化为H的反应类型为 。
(4)I的结构简式为 。
(5)芳香族化合物M是B的同分异构体,符合下列要求的M有 种(不考虑立体异构)。
①能发生银镜反应
②能与FeCl 溶液发生显色反应
3
③苯环上有4个取代基,且核磁共振氢谱显示有3种不同化学环境的氢,且峰面积之比为1:1:1(6)请以1-氯乙烷为原料,写出合成丙酸乙酯的合成路线,其他无机试剂可以任选。 。