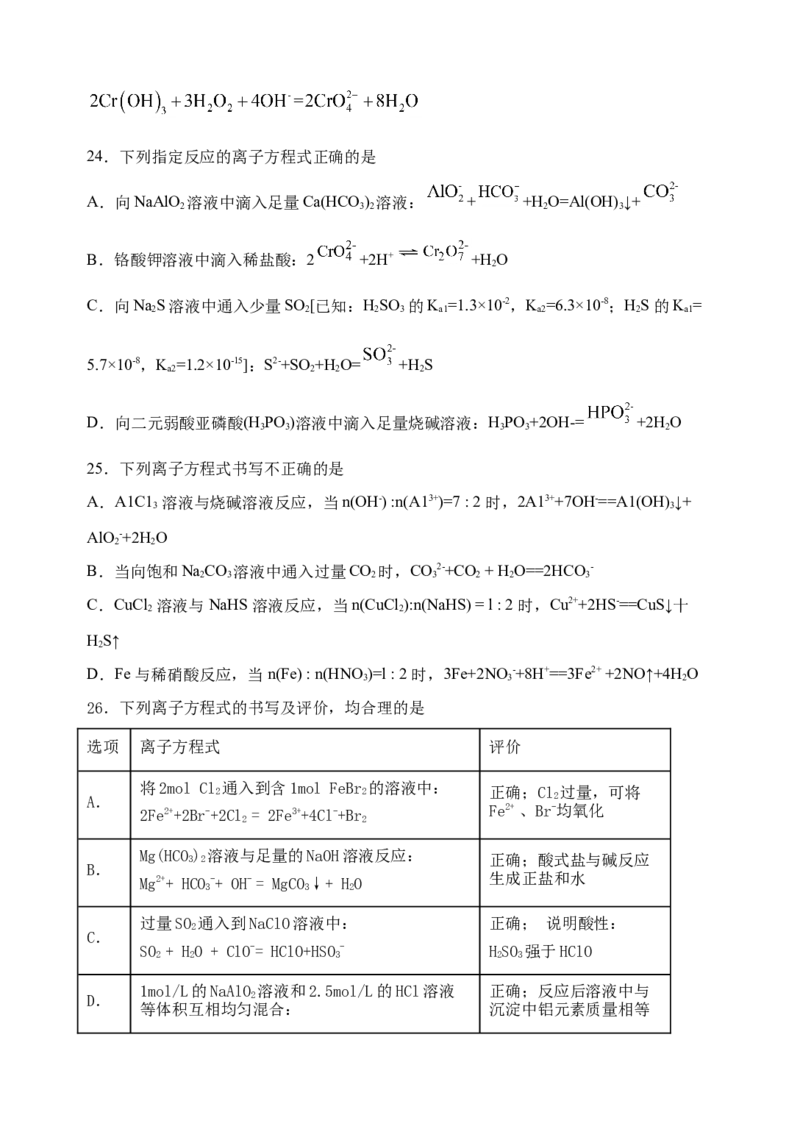文档内容
微专题 04 突破离子方程式书写正误判断中的
“六大陷阱”
陷阱一、是否符合反应事实
离子反应必须符合客观事实,而命题者往往设置不符合“反应原理”的陷阱,如 Fe和非
氧化性酸反应生成Fe2+,金属和氧化性酸反应不放H ,Na不能置换出CuSO 中的Cu;忽
2 4
略氧化还原反应等。
【对点训练】
1.判断下列离子方程式的正误(正确的“√”错误的打“ ”)。
(1)向AlCl 溶液中通入过量氨水:Al3++4NH ·H O AlO-+4NH ++2HO( )
3 3 2 2 4 2
(2)往NaClO溶液中通入少量SO :2ClO-+SO +HO 2HClO+SO 2-( )
2 2 2 3
(3)将Na投入到FeCl 溶液中:3Na+Fe3+ 2Na++Fe( )
3
(4)Fe和稀盐酸反应:2Fe+6H+ 2Fe3++3H↑( )
2
(5)Zn和浓硫酸反应:Zn+2H+ H↑+Zn2+( )
2
(6)Fe O 与稀硝酸反应:2Fe O+18H+ 6Fe3++H↑+8HO( )
3 4 3 4 2 2
陷阱二、“ ”“ ”“↑”“↓”是否使用恰当
弱电解质水解的离子方程式用“ ”,若两种离子水解相互促进,可以进行到底,
则要写成“ ”,如Al3++3HCO - AJ(OH) ↓+3CO↑, NH +和OH-的反应,条件
3 3 2 4
为浓溶液或加热,生成的NH 要标明气体,若为稀溶液,则写成NH ·H O。
3 3 2
【对点训练】
2. 判断下列离子方程式的正误(正确的“√”错误的打“ ”)。(1)用饱和FeCl 溶液制备胶体:Fe3++3HO Fe(OH)↓+3H+( )
3 2 3
△
(2)NaHCO 溶液因水解呈碱性:HCO-+HO HCO+OH-( )
3 3 2 2 3
(3)碳酸钾溶于稀硝酸中:CO2-+2H+ HCO( )
3 2 3
(4)向NH Cl溶液中滴入烧碱溶液并加热:NH ++OH- △ NH ·H O( )
4 4 3 2
(5)AlCl 水解:Al3++3HO Al(OH) ↓+3H+( )
3 2 3
陷阱三、拆分是否正确
△ △
(1)氧化物、弱电解质、沉淀、弱酸的酸式酸根在离子方程式中都不能拆分。
(2)强酸、强碱、可溶性盐的化学式必须拆分(浓硝酸、浓盐酸的化学式需要拆分,浓
硫酸的化学式不拆分)。
(3)对于微溶性的强电解质,在反应物中视情况而定。如澄清石灰水中 Ca(OH) 以Ca2+
2
、 OH-存在,可拆成离子形式,如生成物中一般不能拆,以化学式形式表示。
(4)可溶性多元弱酸的酸式酸根一律保留酸式酸根的形式,如在水溶液中 HSO -写成 H
3
+、SO 2-是错误的。
3
【对点训练】
3. 判断下列离子方程式的正误(正确的“√”错误的打“ ”)。
(1)醋酸与氨水混合:CHCOOH+NH ·H O CHCOONH+HO( )
3 3 2 3 4 2
(2)碳酸氢钙溶液加到醋酸中:Ca(HCO ) +2CHCOOH Ca2++2CHCOO-+2CO↑
3 2 3 3 2
+2HO( )
2
(3)碳酸锌溶液于稀硝酸中:CO2-+2H+ HO+CO↑( )
3 2 2
(4)Mg(OH) 和稀盐酸的反应:OH-+H+ HO( )
2 2(5)CuSO 和氢硫酸反应:Cu2++S2- CuS↓( )
4
陷阱四、是否“漏写”离子反应
判断离子方程式的书写正误时,只注重常见的沉淀反应,忽略不常见的沉淀反应或忽略
中和反应,如Ba(OH) 溶液与CuSO 溶液反应,既要写Ba2+与SO 2-生成BaSO 沉淀,又
2 4 4 4
不能漏掉Cu2+与OH-生成Cu(OH) 沉淀。仔细审题,不放过任何一个小的细节,才能确
2
保不漏掉离子反应。
【对点训练】
4. 判断下列离子方程式的正误(正确的“√”错误的打“ ”)。
(1)CuSO 溶液和Ba(OH) 溶液反应:Ba2++SO 2- BaSO↓( )
4 2 4 4
(2)稀硫酸与氢氧化钡溶液反应:Ba2++SO 2- BaSO↓( )
4 4
(3)(NH )SO 与Ba(OH) 反应:Ba2++SO 2- BaSO↓( )
4 2 4 2 4 4
(4)NH HCO 与NaOH反应:NH ++OH- NH ·H O( )
4 3 4 3 2
陷阱五、是否符合反应的“量”——过量、少量、足量等
看是否符合题设条件的要求,吉过量、少量、等物质的量、任意量以及滴加顺序对反应
产物的影响。如在 FeBr 溶液中通入少量 Cl 的离子方程式为2Fe2++Cl 2Fe3+ +
2 2 2
2Cl-,在 FeBr 溶液中通入过量 Cl 的离子方程式为2Fe2++4Br-+3Cl 2Fe3++
2 2 2
6Cl-+2Br 。
2
【对点训练】
5. 判断下列离子方程式的正误(正确的“√”错误的打“ ”)。
(1)向FeI 中通入少量Cl:2Fe2++Cl 2Fe3++2Cl-( )
2 2 2(2)向Ca(ClO) 溶液中通入少量CO:ClO-+HO+CO HClO+HCO -( )
2 2 2 2 3
(3)向NaAlO 溶液中通入少量CO:2AlO-+CO+3HO 2Al(OH) ↓+CO2-
2 2 2 2 2 3 3
( )
(4)向盐酸中滴加少量NaAlO 溶液:H++AlO-+HO Al(OH) ↓( )
2 2 2 3
(5)少量SO 和NaOH溶液反应:SO +OH- HSO -( )
2 2 3
(6)向NaCO 溶液中滴加少量盐酸:CO2-+2H+ H O+CO↑( )
2 3 3 2 2
(7)少量Ca(OH) 和NaHCO 反应:Ca2++OH-+HCO - CaCO ↓+HO( )
2 3 3 3 2
(8)NH HSO 与NaOH等物质的量的反应:NH ++HSO -+2OH- NH ·H O+SO 2-
4 3 4 3 3 2 3
( )
陷阱六、是否符合三个守恒
离子方程式要符合质量守恒、电荷守恒、得失电子守恒。
【对点训练】
6. 判断下列离子方程式的正误(正确的“√”错误的打“ ”)。
(1)锌片插入硝酸银溶液中:Zn+Ag+ Zn2++Ag( )
(2)向稀Fe(NO ) 溶液中加入稀盐酸:Fe2++2H++NO - Fe3++NO↑+HO( )
3 2 3 2
(3)向FeCl 溶液中通入Cl:Fe2++Cl Fe3++2Cl-( )
2 2 2
(4)向稀硝酸溶液中加入铜片:Cu+2H++NO - Cu2++NO↑+HO( )
3 2
【实战演练】
【基础题】
1.下列离子方程式中,不正确的是
A.将浓硝酸溶液与碳单质混合共热:C+2HNO CO↑+2NO↑+2H O
3 2 2 2
B.将碳酸钠溶液与稀盐酸混合: +2H+=H O+CO↑
2 2
C.将氯化铵溶液与氢氧化钠溶液混合共热: +OH- NH ↑+H O
3 2D.将浓硫酸滴在铁片上:Fe+ 2H+=Fe2++ H ↑
2
2.下列离子方程式错误的是
A.碳酸氢钠溶液加到醋酸中:HCO +CH COOH=CH COO-+CO ↑+H O
3 3 2 2
B.用银氨溶液检验乙醛中的醛基:CHCHO +2[Ag(NH )]+ + 2OH- CHCOO-+ NH
3 3 2 3
→
+3NH + 2Ag↓+ H O
3 2
C.苯酚钠溶液中通入少量二氧化碳:2C HO-+CO +H O→2C HOH+CO
6 5 2 2 6 5
D.硝酸银溶液中加入过量氨水:Ag++2NH·H O=[Ag(NH)]++2H O
3 2 3 2 2
3.下列解释事实的方程式正确的是
A. 与稀盐酸反应:
B.向 溶液中通入过量 :
C.向NH Al(SO ) 溶液中滴加Ba(OH) 溶液使 完全沉淀: +Al3++2 +2Ba2+
4 4 2 2
+4OH-=NH·H O+Al(OH) ↓+2BaSO ↓
3 2 3 4
D.NaS溶液吸收少量CO[已知:K (H CO)>K (H S)>K (H CO)]:S2-+CO +H O=
2 2 a1 2 3 a1 2 a2 2 3 2 2
+H S↑
2
4.下列离子方程式表达不正确的是
A.用氨水吸收废气中的氮氧化物:NO + NO + 2OH-=2NO + H O
2 2
B.用烧碱溶液除去铝片表面的氧化膜:Al O + 2OH-=2AlO + H O
2 3 2
C.用亚硫酸钠溶液处理纸浆中残氯:SO + 2OH-+ Cl =2Cl-+ SO + H O
2 2
D.用食醋消除松花蛋中的氨味:CHCOOH + NH =CHCOO-+ NH
3 3 3
5.下列离子方程式的书写正确的是A.氯化铁溶液与硫化钠溶液混合:2Fe3+ + 3S2- = Fe S↓
2 3
B.钠和冷水反应:Na + 2HO = Na+ + 2OH- + H ↑
2 2
C.向饱和NaCO 溶液中通入足量CO:2Na+ + CO + CO + H O = 2NaHCO ↓
2 3 2 2 2 3
D.稀硝酸和FeO反应:FeO+2H+ = Fe2+ + H O
2
6.下列指定反应的离子方程式正确的是
A.NaS溶液中通入Cl:S2−+Cl=S↓+2Cl-
2 2 2
B.电解饱和食盐水:2Cl-+2H+ Cl↑+H ↑
2 2
C.将SO 通入过量冷氨水中:SO +NH•H O= +
2 2 3 2
D.向NaClO溶液中通入足量SO 气体:ClO-+SO+H O=HClO+
2 2 2
7.下列解释事实的离子方程式不正确的是
A.纯碱溶液中滴入酚酞呈红色: +H O +OH-
2
B.Ba(ClO) 溶液中通入少量SO :SO + Ba2++ 2ClO- + H O= BaSO ↓ + 2HClO
2 2 2 2 3
C.NH Al(SO ) 溶液中滴入过量NaOH溶液: +Al3++5OH-=Al(OH) +NH·H O
4 4 2 3 2
D.AgNO 溶液滴入足量氨水中:Ag++2NH·H O=Ag(NH) +2H O
3 3 2 3 2
8.下列离子方程式书写错误的是
A.二氧化硫使酸性高锰酸钾溶液褪色:3SO +2MnO +4H+=3SO +2Mn2++2H O
2 2
B.泡沫灭火器工作原理:Al3++3HCO =Al(OH) ↓+3CO ↑
3 2
C.工业上用FeS除去废水中的Hg2+:FeS+Hg2+=HgS+Fe2+
D.NaClO溶液中通入少量二氧化碳:ClO-+CO +H O=HClO+HCO [已知电离常数:
2 2
K(HClO)=3×10-8;K(H CO)=4.31×10-7,K(HCO )=5.61×10-11]
2 39.已知K (HgS)=4×10-53,K (FeS)=6×10-18。利用多硫化物(如NaS)可有助于吸收HS,
sp sp 2 x 2
其吸收原理可用以下四步反应表示:
ⅰ.H S+OH-=HS-+H O ⅱ.2HS- H↑+S
2 2 2
ⅲ.H S+S =2HS-+S↓ ⅳ.HS-+H O=HS+OH-
2 2 2
下列说法不正确的是
A.四步反应的总反应中的生成物是H 和S
2
B.在总反应中,加入的多硫化物作用之一是催化剂
C.用过量NaClO溶液吸收HS的离子方程式为HS+4ClO-=4Cl-+SO +2H+
2 2
D.可用FeS除去废水中的Hg2+
10.下列离子或化学方程式正确的是
A.金属钠与水反应:
B.碳酸氢钙溶液中加入足量的澄清石灰水:
C. 中投入
D.常温下,向饱和 溶液中通入过量 ,溶液变浑浊: 饱和
【能力题】
11.对于下列实验,能正确描述其反应的离子方程式是
A.将少量SO 通入次氯酸钠溶液中:ClO-+SO+H O=Cl-+ +2H+
2 2 2B.向含CaSO 的水垢中滴入饱和NaCO 溶液:CaSO(s)+ (aq) (aq)+CaCO (s)
4 2 3 4 3
⇌
C.用铁电极电解饱和MgCl 溶液:Mg2++2C1-+2H O Mg(OH) ↓+Cl↑+H ↑
2 2 2 2 2
D.向(NH )Fe(SO ) 溶液中加入含等物质的量溶质的Ba(OH) 溶液:Ba2++ +
4 2 4 2 2
+OH-=BaSO ↓+NH·H O
4 3 2
12.下列反应的离子方程式表达不正确的是
A.将SO 通入酸性FeCl 溶液中:SO +2Fe3++2H O=2Fe2++ +4H+
2 3 2 2
B.某消毒液的主要成分为NaClO,加白醋可增强消毒效果:
C.向草酸溶液中逐滴加入酸性高锰酸钾溶液,溶液褪色:
D.向碳酸氢钡溶液中加入过量氢氧化钾溶液:
13.下列反应的离子方程式正确的是
A.用CuSO 溶液除去电石气中的少量硫化氢:Cu2++S2-=CuS↓
4
B.向NaClO溶液中通入少量SO :ClO-+SO+H O=SO +C1-+2H+
2 2 2
C.向稀AgNO 溶液中加入过量稀氨水:Ag++2NH·H O=[Ag(NH)]++2H O
3 3 2 3 2 2
D.向苯酚钠溶液中通入少量CO:CO+H O+2 CO +2
2 2 2
→
14.化学与生活关系密切,解释下列应用的离子方程式正确的是
选
应用 解释(离子方程式)
项淀粉—KI溶液(稀硫酸酸化)检验碘盐中含
A
KIO
3
B 电解饱和食盐水制氢气和氯气
C 醋酸用于除去水垢
D 氯化铁用于蚀刻铜板
A.A B.B C.C D.D
15.下列离子方程式书写不正确的是
A.将过量SO 气体通入NaClO溶液中:SO +HO+ClO-=SO +Cl-+2H+
2 2 2
B.标准状况下将112 mL氯气通入10 mL 1 mol·L-1溴化亚铁溶液中:2Fe2++4Br-
+3Cl=2Br +2Fe3++6Cl-
2 2
C.向FeSO 溶液中滴加NaHCO 溶液和稀氨水,产生大量白色沉淀:Fe2++HCO
4 3
+NH·H O=FeCO↓+NH +HO
3 2 3 2
D.向明矾溶液中滴加Ba(OH) 溶液,使沉淀的物质的量最大时:2Al3++ 3SO + 3Ba2+
2
+6OH- = 2Al(OH) ↓+3BaSO ↓
3 4
16.下列离子反应方程式正确的是
A.Fe与稀硝酸反应,当n(Fe):n(HNO)=1:2时,3Fe+2NO +8H+=3Fe2++2NO↑+4HO
3 2
B.CuSO 与过量浓氨水反应的离子方程式:Cu2++2NH·H O=Cu(OH) ↓+2NH
4 3 2 2
C.向硫酸铝铵溶液滴加足量的氢氧化钡溶液:Al3++2SO +2Ba2++4OH-=AlO
+2BaSO ↓+2H O
4 2
D.向NaHSO 溶液中逐滴加入Ba(OH) 溶液至SO 刚好沉淀完全:2H++SO +Ba2+
4 2
+2OH-=2H O+BaSO↓
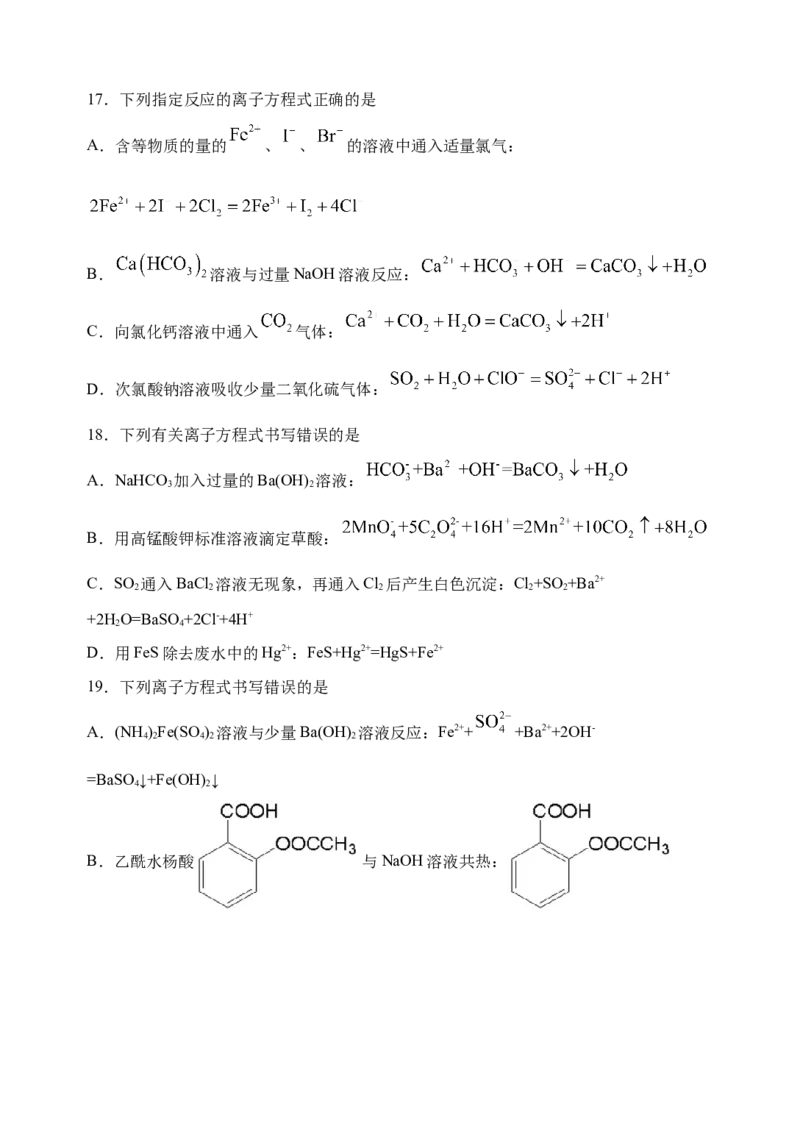
2 417.下列指定反应的离子方程式正确的是
A.含等物质的量的 、 、 的溶液中通入适量氯气:
B. 溶液与过量NaOH溶液反应:
C.向氯化钙溶液中通入 气体:
D.次氯酸钠溶液吸收少量二氧化硫气体:
18.下列有关离子方程式书写错误的是
A.NaHCO 加入过量的Ba(OH) 溶液:
3 2
B.用高锰酸钾标准溶液滴定草酸:
C.SO 通入BaCl 溶液无现象,再通入Cl 后产生白色沉淀:Cl+SO+Ba2+
2 2 2 2 2
+2H O=BaSO+2Cl-+4H+
2 4
D.用FeS除去废水中的Hg2+:FeS+Hg2+=HgS+Fe2+
19.下列离子方程式书写错误的是
A.(NH )Fe(SO ) 溶液与少量Ba(OH) 溶液反应:Fe2++ +Ba2++2OH-
4 2 4 2 2
=BaSO ↓+Fe(OH) ↓
4 2
B.乙酰水杨酸 与NaOH溶液共热:+3OH- +CH COO-+2H O
3 2
C.AgCl溶于过量浓氨水中:
D.向碘化亚铁溶液中滴加少量稀硝酸:
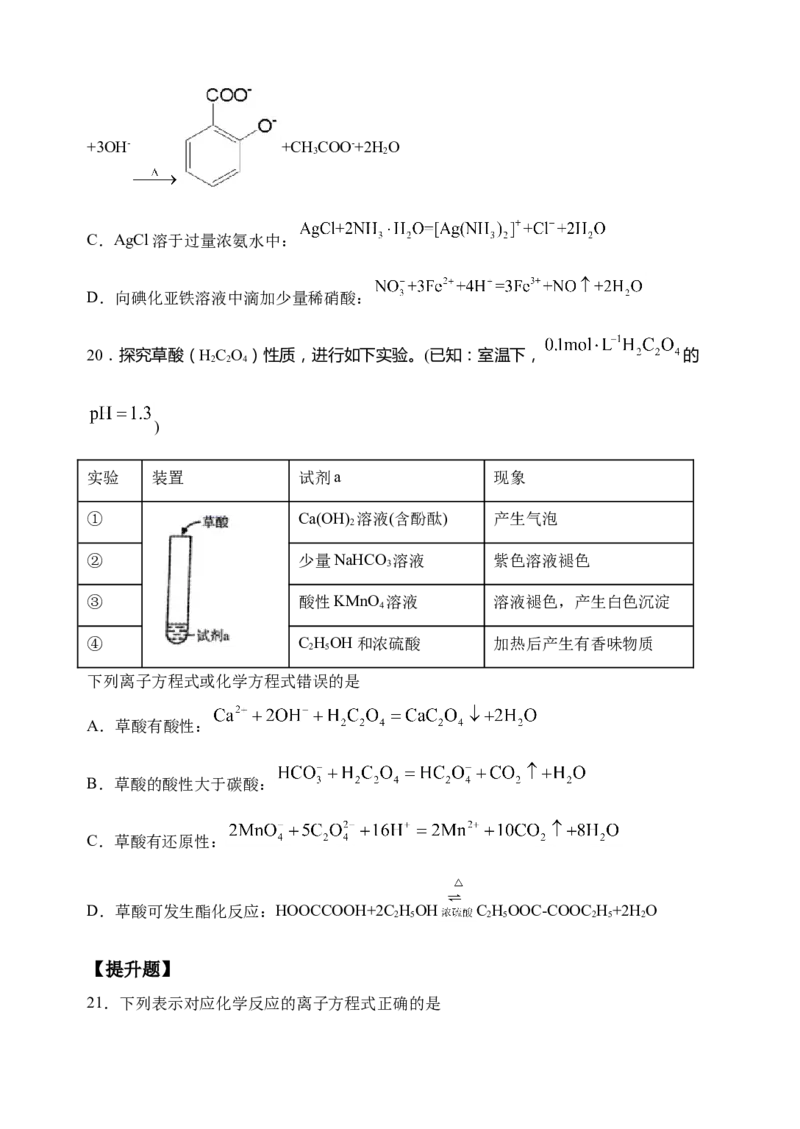
20.探究草酸(HC O)性质,进行如下实验。(已知:室温下, 的
2 2 4
)
实验 装置 试剂a 现象
① Ca(OH) 溶液(含酚酞) 产生气泡
2
② 少量NaHCO 溶液 紫色溶液褪色
3
③ 酸性KMnO 溶液 溶液褪色,产生白色沉淀
4
④ C HOH和浓硫酸 加热后产生有香味物质
2 5
下列离子方程式或化学方程式错误的是
A.草酸有酸性:
B.草酸的酸性大于碳酸:
C.草酸有还原性:
D.草酸可发生酯化反应:HOOCCOOH+2C HOH C HOOC-COOC H+2H O
2 5 2 5 2 5 2
【提升题】
21.下列表示对应化学反应的离子方程式正确的是A.过氧化氢使酸性高锰酸钾褪色:3HO+2MnO +6H+=4O ↑+2Mn2++6H O
2 2 2 2
B.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO =Ag++NO↑+HO
2
C.用石墨做电极电解CuSO 溶液:2Cu2++2H O 2Cu+O ↑+4H+
4 2 2
D.向CHBrCOOH中加入足量的氢氧化钠溶液并加热:CHBrCOOH+OH-
2 2
CHBrCOO-+H O
2 2
22.下列反应的方程式正确的是
A.用惰性电极电解氯化镁溶液时阴极的电极反应式:
B.工业制备粗硅的主要反应:
C.过量二氧化硫通入 溶液:
D.将 溶液和1.5mol/L的HCl溶液等体积混合:
23.下列有关反应的离子方程式正确的是
A.Sn溶于 溶液:
B. 溶液中通入 :
C. 溶液中加入足量 溶液:
D. 中同时加入NaOH溶液和 制 :24.下列指定反应的离子方程式正确的是
A.向NaAlO 溶液中滴入足量Ca(HCO ) 溶液: + +H O=Al(OH) ↓+
2 3 2 2 3
B.铬酸钾溶液中滴入稀盐酸:2 +2H+ +H O
2
C.向NaS溶液中通入少量SO [已知:HSO 的K =1.3×10-2,K =6.3×10-8;HS 的K =
2 2 2 3 a1 a2 2 a1
5.7×10-8,K =1.2×10-15]:S2-+SO+H O= +H S
a2 2 2 2
D.向二元弱酸亚磷酸(H PO )溶液中滴入足量烧碱溶液:HPO +2OH-= +2H O
3 3 3 3 2
25.下列离子方程式书写不正确的是
A.A1C1 溶液与烧碱溶液反应,当n(OH-) :n(A13+)=7 : 2 时,2A13++7OH-==A1(OH) ↓+
3 3
AlO-+2H O
2 2
B.当向饱和NaCO 溶液中通入过量CO 时,CO2-+CO + H O==2HCO-
2 3 2 3 2 2 3
C.CuCl 溶液与 NaHS 溶液反应,当n(CuCl ):n(NaHS) = l : 2 时,Cu2++2HS-==CuS↓十
2 2
HS↑
2
D.Fe 与稀硝酸反应,当 n(Fe) : n(HNO )=l : 2 时,3Fe+2NO-+8H+==3Fe2+ +2NO↑+4H O
3 3 2
26.下列离子方程式的书写及评价,均合理的是
选项 离子方程式 评价
A. 将2mol Cl 2 通入到含1mol FeBr 2 的溶液中: 正确;Cl 2 过量,可将
2Fe2++2Br-+2Cl = 2Fe3++4Cl-+Br Fe2+ 、Br-均氧化
2 2
Mg(HCO 3 ) 2 溶液与足量的NaOH溶液反应: 正确;酸式盐与碱反应
B.
Mg2++ HCO-+ OH- = MgCO↓+ HO 生成正盐和水
3 3 2
过量SO 通入到NaClO溶液中: 正确; 说明酸性:
2
C.
SO + HO + ClO-= HClO+HSO- HSO 强于HClO
2 2 3 2 3
1mol/L的NaAlO 溶液和2.5mol/L的HCl溶液 正确;反应后溶液中与
D. 2
等体积互相均匀混合: 沉淀中铝元素质量相等2AlO- + 5H+ = Al3+ + Al(OH)↓+ HO
2 3 2
A.A B.B C.C D.D
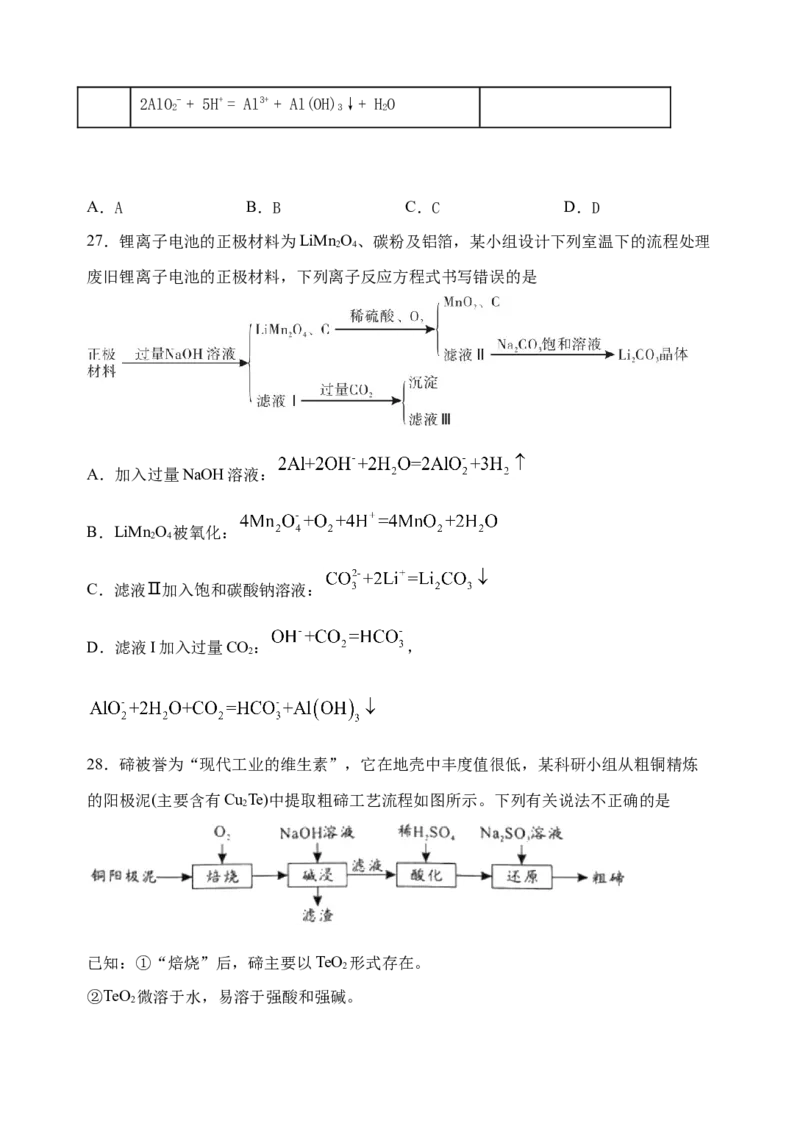
27.锂离子电池的正极材料为LiMn O、碳粉及铝箔,某小组设计下列室温下的流程处理
2 4
废旧锂离子电池的正极材料,下列离子反应方程式书写错误的是
A.加入过量NaOH溶液:
B.LiMn O 被氧化:
2 4
C.滤液Ⅱ加入饱和碳酸钠溶液:
D.滤液I加入过量CO: ,
2
28.碲被誉为“现代工业的维生素”,它在地壳中丰度值很低,某科研小组从粗铜精炼
的阳极泥(主要含有Cu Te)中提取粗碲工艺流程如图所示。下列有关说法不正确的是
2
已知:①“焙烧”后,碲主要以TeO 形式存在。
2
②TeO 微溶于水,易溶于强酸和强碱。
2A.“焙烧”用到的硅酸盐仪器主要有:坩埚、泥三角、酒精灯、玻璃棒
B.“碱浸”时反应的离子方程式为TeO +2OH-= +HO
2 2
C.“碱浸”后所得的滤渣中含有Au、Ag,可用稀盐酸将其分离
D.“还原”时氧化剂与还原剂的物质的量之比为1:2
29.下列离子方程式中正确的是
A.向 CHBrCOOH中加入足量的氢氧化钠溶液并加热:
2
B.用氢氧化钠溶液除去铝片表面的氧化膜:Al3++4OH-→AlO-+2H O
2 2
C.次氯酸钠溶液中通入少量的CO 气体:ClO-+CO +H O→HClO+HCO -
2 2 2 3
D.等体积、等浓度的Ca(HCO) 溶液和NaOH溶液混合:
2
30.下列离子方程式书写及评价合理的是
选
离子方程式 评价
项
溶液中加入足量 溶液
正确, 过量,酸式盐与碱完全
A
反应生成正盐和水:
正确, 与H按物质的量1:1反
的 溶液与 的
B 溶液等体积混合 应转化为 ,过量的 再将
一半 转化为
正确, 化学式可改写为
将少量的 溶解在过量的稀 中
C
, 与 ,物质的
量之比为1:2
D
将 溶液加入到足量的 溶液中 错误, 与 发生氧化还原反应:2Fe2++ClO-+5H O=2Fe(OH) +Cl-
2 3
+4H+
↓
A.A B.B C.C D.D