文档内容
微专题28 非金属氧化物的污染与防治
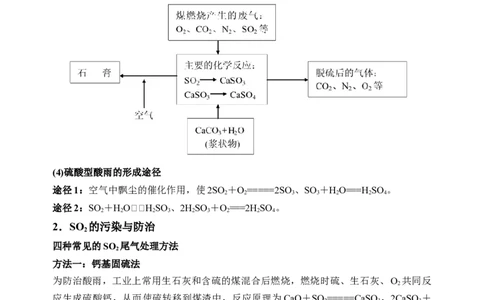
1.硫的氧化物
(1)来源:含硫化石燃料的燃烧及金属矿物的冶炼等。
(2)危害:危害人体健康,形成酸雨(pH小于5.6)。
(3)治理:燃煤脱硫,改进燃烧技术。
(4)硫酸型酸雨的形成途径
途径1:空气中飘尘的催化作用,使2SO +O=====2SO 、SO +HO===H SO 。
2 2 3 3 2 2 4
途径2:SO +HOH SO 、2HSO +O===2H SO 。
2 2 2 3 2 3 2 2 4
2.SO 的污染与防治
2
四种常见的SO 尾气处理方法
2
方法一:钙基固硫法
为防治酸雨,工业上常用生石灰和含硫的煤混合后燃烧,燃烧时硫、生石灰、O 共同反
2
应生成硫酸钙,从而使硫转移到煤渣中,反应原理为CaO+SO =====CaSO ,2CaSO +
2 3 3
O=====2CaSO,总反应的化学方程式为 2CaO+2SO +O=====2CaSO。
2 4 2 2 4
方法二:氨水脱硫法
该脱硫法采用喷雾吸收法,雾化的氨水与烟气中的SO 直接接触吸收SO ,其反应的化学
2 2
方程式为 2NH +SO +HO===(NH)SO ,2(NH )SO +O===2(NH)SO (或生成
3 2 2 4 2 3 4 2 3 2 4 2 4
NH HSO ,然后进一步氧化)。
4 3
方法三:钠、碱脱硫法
钠、碱脱硫法是用NaOH/Na CO 吸收烟气中的SO ,得到NaSO 和NaHSO ,发生反应
2 3 2 2 3 3的化学方程式为2NaOH+SO ===Na SO +HO,NaCO +SO ===Na SO +CO ,NaSO
2 2 3 2 2 3 2 2 3 2 2 3
+SO +HO===2NaHSO 。
2 2 3
方法四:双碱脱硫法
先利用烧碱吸收SO ,再利用熟石灰浆液进行再生,再生后的NaOH可循环使用,化学反
2
应原理为
①吸收反应:2NaOH+SO ===Na SO +HO,2NaSO +O===2Na SO 。
2 2 3 2 2 3 2 2 4
②再生反应:NaSO +Ca(OH) ===CaSO ↓+2NaOH,NaSO +Ca(OH) ===CaSO ↓+
2 3 2 3 2 4 2 4
2NaOH。
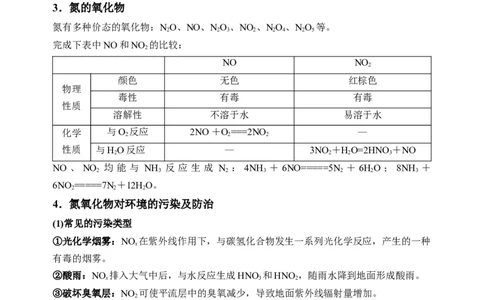
3.氮的氧化物
氮有多种价态的氧化物:NO、NO、NO、NO 、NO、NO 等。
2 2 3 2 2 4 2 5
完成下表中NO和NO 的比较:
2
NO NO
2
颜色 无色 红棕色
物理
毒性 有毒 有毒
性质
溶解性 不溶于水 易溶于水
化学 与O 反应 2NO +O===2NO —
2 2 2
性质 与HO反应 — 3NO +HO=2HNO +NO
2 2 2 3
NO 、 NO 均 能 与 NH 反 应 生 成 N : 4NH + 6NO=====5N + 6HO ; 8NH +
2 3 2 3 2 2 3
6NO =====7N+12HO。
2 2 2
4.氮氧化物对环境的污染及防治
(1)常见的污染类型
①光化学烟雾:NO 在紫外线作用下,与碳氢化合物发生一系列光化学反应,产生的一种
x
有毒的烟雾。
②酸雨:NO 排入大气中后,与水反应生成HNO 和HNO,随雨水降到地面形成酸雨。
x 3 2
③破坏臭氧层:NO 可使平流层中的臭氧减少,导致地面紫外线辐射量增加。
2
(2)常见的NO 尾气处理方法
x
①碱液吸收法
2NO +2NaOH===NaNO +NaNO +HO;
2 3 2 2
NO +NO+2NaOH===2NaNO +HO。
2 2 2
NO 、NO的混合气体能被足量烧碱溶液完全吸收的条件是n(NO )≥n(NO),一般适合工业
2 2
尾气中NO 的处理。
x
NO 与NaOH溶液反应的有关问题分析
x(1)NO 能被NaOH溶液吸收生成两种盐。
2
(2)NO不能被NaOH溶液吸收。
(3)n(NO )∶n(NO)≥1时,NO 、NO的混合气体能完全被NaOH溶液吸收。
2 2
②催化转化法
在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体(N );NO 与CO在一定温度下
2 x
催化,转化为无毒气体(N 和CO),此法一般适用于汽车尾气的处理。
2 2
【专题精练】
一、SO 的污染与防治
2
1.(1)下列物质中,可形成酸雨的是________。
A.二氧化硫 B.氟氯代烃
C.二氧化碳 D.甲烷
(2)现有以下几种措施:①对燃煤产生的尾气进行脱硫处理;
②少用原煤做燃料;③燃煤时鼓入足量空气;④开发清洁能源。其中能减少酸雨产生的
措施是________。
A.①②③ B.②③④
C.①②④ D.①③④
【答案】(1)A (2)C
【解析】
(1)SO 溶于雨水生成亚硫酸,进而被空气中的氧气氧化为硫酸,降落到地面即为酸雨;氟
2
氯代烃破坏臭氧层;CO 、CH 均属于温室气体,不能形成酸雨。(2)二氧化硫是形成酸雨
2 4
的主要原因,而大气中二氧化硫的主要来源之一是含硫燃料(包括煤、石油、天然气等)的
燃烧,所以减少酸雨的重要措施是对煤等燃料进行脱硫处理,或者开发新能源来代替煤
等燃料。
2.食品、大气、工业尾气中SO 均需严格检测或转化吸收,下列有关 SO 的检测或吸收
2 2
方法正确的是( )
A.滴定法:用酸性KMnO 溶液滴定葡萄酒试样以测定葡萄酒中SO 的浓度
4 2
B.沉淀法:用Ba(OH) 溶液沉淀SO ,然后将沉淀在空气中洗涤、过滤、干燥、称重以
2 2
测定大气中SO 的浓度
2
C.氨酸法:用氨水吸收尾气中的SO 后再将吸收液与硫酸反应,将富集后的SO 循环使
2 2
用
D.石灰石膏法:常温下用石灰石吸收尾气中的SO 得到CaSO ,再经氧化可用于生产石
2 3
膏【答案】C
【解析】
A项,葡萄酒中的乙醇也能被酸性高锰酸钾溶液氧化,对SO 的检测有干扰;B项,大气
2
中的 CO 能被 Ba(OH) 溶液沉淀,对 SO 的检测有干扰;C 项,氨水吸收 SO 生成
2 2 2 2
(NH )SO 或NH HSO ,(NH )SO 或NH HSO 与硫酸反应能产生SO ,SO 可以循环使用;
4 2 3 4 3 4 2 3 4 3 2 2
D项,石灰石吸收SO ,需要在高温下才能进行。
2
SO 对环境的污染及治理
2
3.如图所示是一种综合处理SO 废气的工艺流程,若每步都完全反应。下列说法正确的
2
是( )
A.溶液B中发生的反应为2SO +O===2SO
2 2 3
B.可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
C.由以上流程可推知氧化性:Fe3+>O >SO
2
D.此工艺的优点之一是物质能循环利用
【答案】D
【解析】
酸性Fe (SO ) 溶液能吸收SO ,反应的离子方程式为2Fe3++SO +2HO===2Fe2++SO4
2 4 3 2 2 2
+4H+。溶液B中通入空气发生反应:4Fe2++O +4H+===4Fe3++2HO。其氧化性:O
2 2 2
>Fe3+,A、C两项错误;溶液C中含有Fe (SO ) ,可用KSCN溶液检验Fe3+,B项错误;
2 4 3
Fe (SO ) 可循环利用,D项正确。
2 4 3
4.如图所示,硫酸工业中产生的SO 通过下列过程既能制得HSO 又能制得H。
2 2 4 2
请回答:
(1)该过程可循环利用的物质是________(写化学式)。
(2)该过程总反应的化学方程式为
_____________________________________________________________________________
______________________________。【答案】(1)I 和HI (2)SO +2HO===H SO +H
2 2 2 2 4 2
【解析】
根据题给流程和信息知,反应Ⅰ为SO +I +2HO===H SO +2HI,反应Ⅱ为2HI===H ↑
2 2 2 2 4 2
+I 。(1)分析题给流程知该过程可循环利用的物质是I 和HI。(2)根据题给流程和信息知,
2 2
该过程总反应的化学方程式是SO +2HO===H SO +H。
2 2 2 4 2
二、氮氧化物对环境的污染及防治
1.研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如图所示)。下列叙
述错误的是( )
A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH 是形成无机颗粒物的催化剂
3
D.雾霾的形成与过度施用氮肥有关
【答案】C
【解析】
雾和霾的分散剂均为空气,A项正确;结合图示可知形成雾霾的无机颗粒物中含有
NH NO 和(NH )SO ,B项正确;根据图示可知空气中NO 、SO 等分别转化为HNO 、
4 3 4 2 4 x 2 3
HSO 后,吸收空气中的NH 生成NH NO 和(NH )SO ,即NH 是形成无机颗粒物的反应
2 4 3 4 3 4 2 4 3
物,C项错误;过度施用氮肥,会导致空气中挥发的NH 浓度增大,与雾霾的形成有关,
3
D项正确。
2.汽车排放的尾气中含有NO ,NO 是城市大气污染的主要污染物之一。在日光照射下,
2 2
NO 发生一系列光化学烟雾的循环反应,从而不断产生O ,加重空气污染。反应过程为
2 3
①2NO ===2NO+2O,②2NO+O===2NO ,③O+O===O 。下列对该反应过程及生成
2 2 2 2 3
物叙述正确的是( )
A.NO 起催化剂作用
2
B.NO起催化剂作用
C.NO 只起氧化剂作用
2
D.O 与O 互为同分异构体
3 2【答案】A
【解析】
反应过程①+②得O===2O,③O+O===O ,NO 起催化剂作用,反应过程中NO 还做
2 2 3 2 2
氧化剂,A项正确,B、C项错误;O 与O 不是同分异构体,互为同素异形体,D项错误。
3 2
3.NO 可以用氢氧化钠溶液吸收,或在一定条件下用氨与其反应使之转化为无污染的物
2
质,发生反应的化学方程式分别是 2NO +2NaOH===M+NaNO +HO,8NH +
2 3 2 3
6NO ===7X+12HO。则M、X代表的物质的化学式分别是( )
2 2
A.NaNO 、N B.HNO、N C.NO、HNO D.N、N
2 2 2 2 3 2 2
【答案】A
4. 随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气装置里,气
体在催化剂表面吸附与解吸作用的过程如图所示,下列说法
正确的是( )
A.反应中NO为氧化剂,N 为氧化产物
2
B.汽车尾气的主要污染成分包括CO、NO和N
2
C.NO和O 必须在催化剂表面才能反应
2
D.催化转化总化学方程式为2NO+O+4CO=====4CO+N
2 2 2
【答案】D
【解析】
反应过程中NO、O 为氧化剂,N 为还原产物;汽车尾气中的N 不是污染物;NO和O
2 2 2 2
的反应不需要催化剂;根据题中的图示,可将反应的过程分成如下两步写:2NO+
O===2NO 2NO +4CO===N +4CO ,将两步反应式合并可得总化学方程式为2NO+O
2 2, 2 2 2 2
+4CO=====4CO+N。
2 2
5.氮的氧化物(用NO 表示)是大气污染物,必须进行处理。
x
(1)汽车尾气主要含有CO、CO、SO 、NO 等物质,这种尾气逐渐成为城市空气污染的主
2 2 x
要来源之一。
①汽车尾气中的CO来自于
_____________________________________________________,
NO来自于__________________________。汽车尾气对环境的危害主要有________(至少
填两种)。
②汽车尾气中的CO、NO 在适宜温度下采用催化转化法处理,使它们相互反应生成参与
x
大气循环的无毒气体。反应的化学方程式可表示为
_____________________________________________________________________________
______________________________。(2)用氨可将氮氧化物转化为无毒气体。已知:4NH +6NO=====5N +6HO,8NH +
3 2 2 3
6NO =====7N +12HO。同温同压下,3.5 L NH 恰好将3.0 L NO和NO 的混合气体完全
2 2 2 3 2
转化为N,则原混合气体中NO和NO 的体积之比是________。
2 2
(3)工业尾气中氮的氧化物常采用碱液吸收法处理,若 NO与NO 按物质的量之比1∶1被
2
足量NaOH溶液完全吸收后,得到一种钠盐,该钠盐的化学式是________。
【答案】(1)①汽油的不完全燃烧 N 与O 在汽车汽缸内的高温环境下的反应 形成硝酸
2 2
型酸雨、导致光化学烟雾、产生温室效应(任填两种即可)
②2xCO+2NO=====2xCO+N
x 2 2
(2)1∶3
(3)NaNO
2
【解析】
(2)V(NO)+V(NO )=3.0 L,①
2
V(NO)+ V(NO )=3.5 L,②
2
联立①②得:V(NO)=0.75 L,V(NO )=2.25 L。
2
V(NO)∶V(NO )=1∶3。
2