文档内容
易错点 17 晶体结构与性质
易错题【01】等离子体、液晶和离子液体的比较
等离子体 液晶 离子液体
构成 电子、阳离子和电中 苯甲酸胆甾酯 体积很大的阴离
性粒子(分子或原 子、
子)
阳离子
特性 具有良好的导电性和 具有液体的流动性、黏度、形 难挥发、良好导电
流动性 变性等,具有晶体的各向异性 性、作溶剂
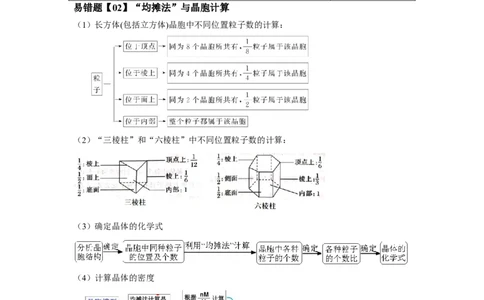
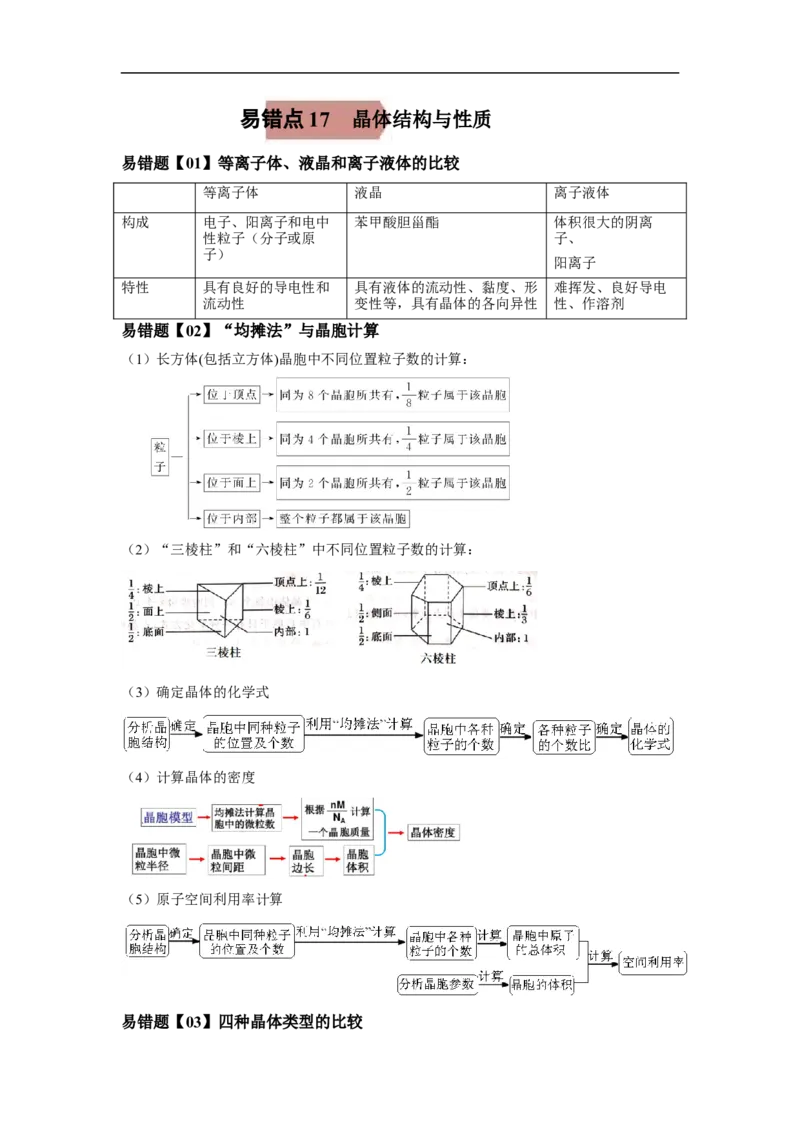
易错题【02】“均摊法”与晶胞计算
(1)长方体(包括立方体)晶胞中不同位置粒子数的计算:
(2)“三棱柱”和“六棱柱”中不同位置粒子数的计算:
(3)确定晶体的化学式
(4)计算晶体的密度
(5)原子空间利用率计算
易错题【03】四种晶体类型的比较类型
分子晶体 共价晶体 金属晶体 离子晶体
比较
金属阳离子
构成粒子 分子 原子 阴、阳离子
和自由电子
粒子间的相
分子间作用力 共价键 金属键 离子键
互作用力
有的很大,
硬度 较小 很大 较大
有的很小
有的很高,
熔、沸点 较低 很高 较高
有的很低
难溶于任何溶 常见溶剂难 大多易溶于水等极
溶解性 相似相溶
剂 溶 性溶剂
一般不导电,
导电、传热 一般不具有导 电和热的 晶体不导电,水溶
溶于水后有的
性 电性 良导体 液或熔融态导电
导电
易错题【04】晶体类型判断
(1)依据构成晶体的微粒和微粒间作用力判断
由阴、阳离子形成离子键构成的晶体为离子晶体;由原子形成的共价键构成的晶体为共价
晶体;由分子依靠分子间作用力形成的晶体为分子晶体;由金属阳离子、自由电子以金属
键形成的晶体为金属晶体。
(2)依据晶体的熔点判断
不同类型晶体熔点的一般规律:共价晶体>离子晶体>分子晶体。金属晶体的熔点差别很大,
如钨、铂等熔点很高,铯等熔点很低。
易错题【05】晶体熔、沸点高低的比较
(1)看物质所属晶体类型,一般情况下,晶体的熔点:共价晶体>离子晶体>分子晶体。
(2)同类晶体熔、沸点判断思路:
易错题【06】晶胞投影图的分析
(1)分析晶胞沿x轴方向(yz)、y轴方向(xz)、z轴方向(xy)的投影图,确定晶胞
中各粒子的具体位置。
(2)结合晶胞参数,利用“均摊法”计算晶体的密度、原子的空间利用率等。
(3)结合三维坐标系及晶胞中原子的位置,确定相关原子的坐标参数(或分数坐标)。易错题【07】
典例分析
例题1、理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的
拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb
取代后形成。
(1)图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞
单元,理由是__________________。
(2)图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为_________;该晶胞中粒
子个数比Hg:Ge:Sb = _________。
(3)设X的最简式的式量为M,则X晶体的密度为________g/cm3(列出算式)。
r
【解析】(1)对比图b和图c可知,X晶体的晶胞中上下两个单元内的原子位置不完全相
同,不符合晶胞晶胞是晶体的最小重复单位要求,可能还有其他形式。
(2)以晶胞上方立方体中右侧面心中Hg原子为例,同一晶胞中与Hg距离最近的Sb的数
目为2,右侧晶胞中有2个Sb原子与Hg原子距离最近,因此X的晶体中与Hg距离最近的
Sb的数目为4。该晶胞中Sb原子均位于晶胞内,因此1个晶胞中含有Sb原子数为8,Ge
原子位于晶胞顶点、面心、体心,则1个晶胞中含有Ge原子数为1+8× +4× =4;Hg原
子位于棱边、面心,则1个晶胞中含有Hg原子数为6× +4× =4,则该晶胞中粒子个数比
Hg:Ge:Sb =4:4:8=1:1:2。
(3)1个晶胞的质量m= 4×M g,1个晶胞的体积V=(x×10-7 cm)2×(y×10-7 cm)=x2y×10—21
r
N
A4×M
cm3,则X晶体的密度为 m N r g = 4×M r ×1021 g·cm-3。
= A x2y×N
V x2y×10-21cm3 A
【答案】(1)图b不具有“无隙并置”的特点
4×M
r
(2)4 1:1:2 (3) ×1021
x2y×N
A
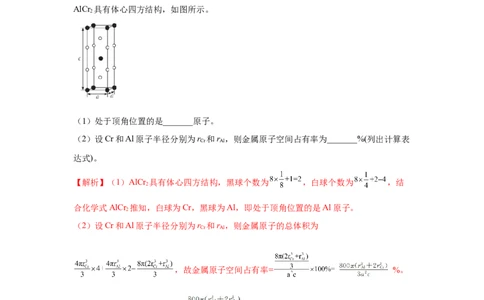
例题2、在金属材料中添加AlCr 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
2
AlCr 具有体心四方结构,如图所示。
2
(1)处于顶角位置的是_______原子。
(2)设Cr和Al原子半径分别为r 和r ,则金属原子空间占有率为_______%(列出计算表
Cr Al
达式)。
【解析】(1)AlCr 具有体心四方结构,黑球个数为 ,白球个数为 ,结
2
合化学式AlCr 推知,白球为Cr,黑球为Al,即处于顶角位置的是Al原子。
2
(2)设Cr和Al原子半径分别为r 和r ,则金属原子的总体积为
Cr Al
,故金属原子空间占有率= %。
【答案】(1)Al (2)
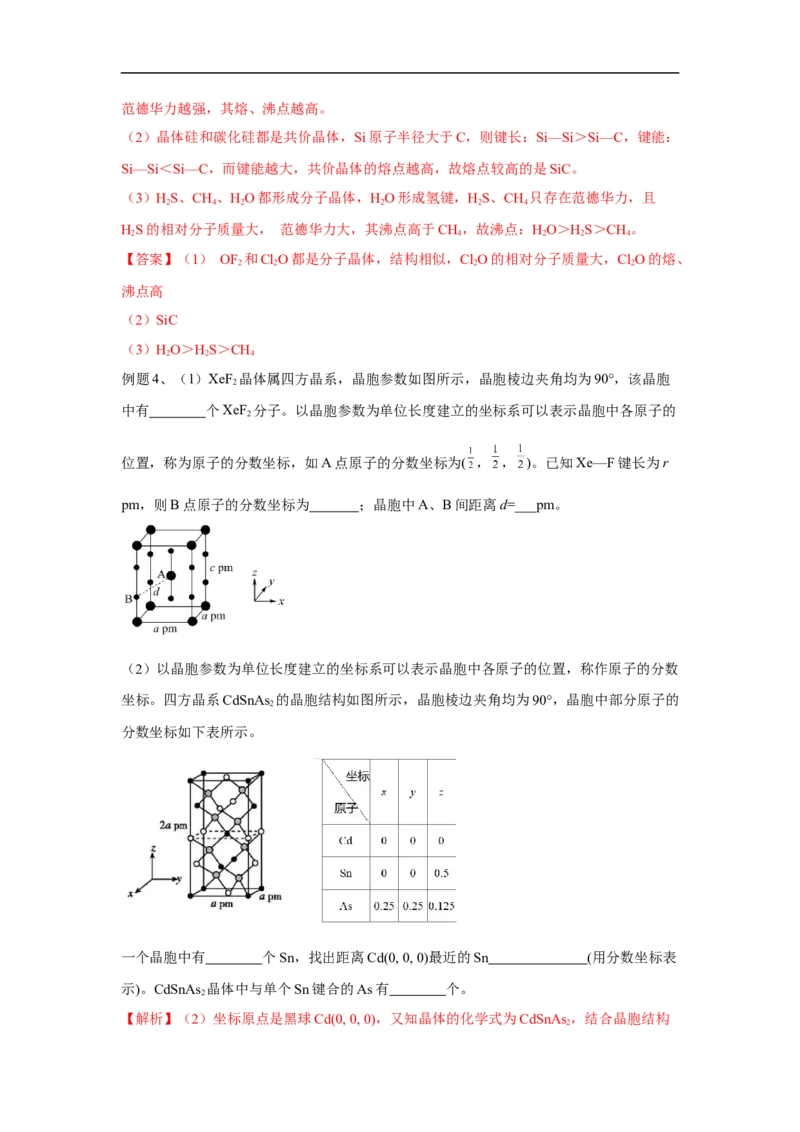
例题3、(1)OF 的熔、沸点 (填“高于”或“低于”)Cl O,原因是 。
2 2
(2)硅、锗(Ge)及其化合物广泛应用于光电材料领域,晶体硅和碳化硅熔点较高的是
_______(填化学式)。
(3)HS、CH、HO的沸点由高到低顺序为 。
2 4 2
【解析】(1)OF 和ClO都是分子晶体,范德华力影响其熔、沸点,而相对分子质量越大,
2 2范德华力越强,其熔、沸点越高。
(2)晶体硅和碳化硅都是共价晶体,Si原子半径大于C,则键长:Si—Si>Si—C,键能:
Si—Si<Si—C,而键能越大,共价晶体的熔点越高,故熔点较高的是SiC。
(3)HS、CH、HO都形成分子晶体,HO形成氢键,HS、CH 只存在范德华力,且
2 4 2 2 2 4
HS的相对分子质量大, 范德华力大,其沸点高于CH,故沸点:HO>HS>CH。
2 4 2 2 4
【答案】(1) OF 和ClO都是分子晶体,结构相似,ClO的相对分子质量大,ClO的熔、
2 2 2 2
沸点高
(2)SiC
(3)HO>HS>CH
2 2 4
例题4、(1)XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞
2
中有 个XeF 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的
2
位置,称为原子的分数坐标,如A点原子的分数坐标为( , , )。已知Xe—F键长为r
pm,则B点原子的分数坐标为 ;晶胞中A、B间距离d=___pm。
(2)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数
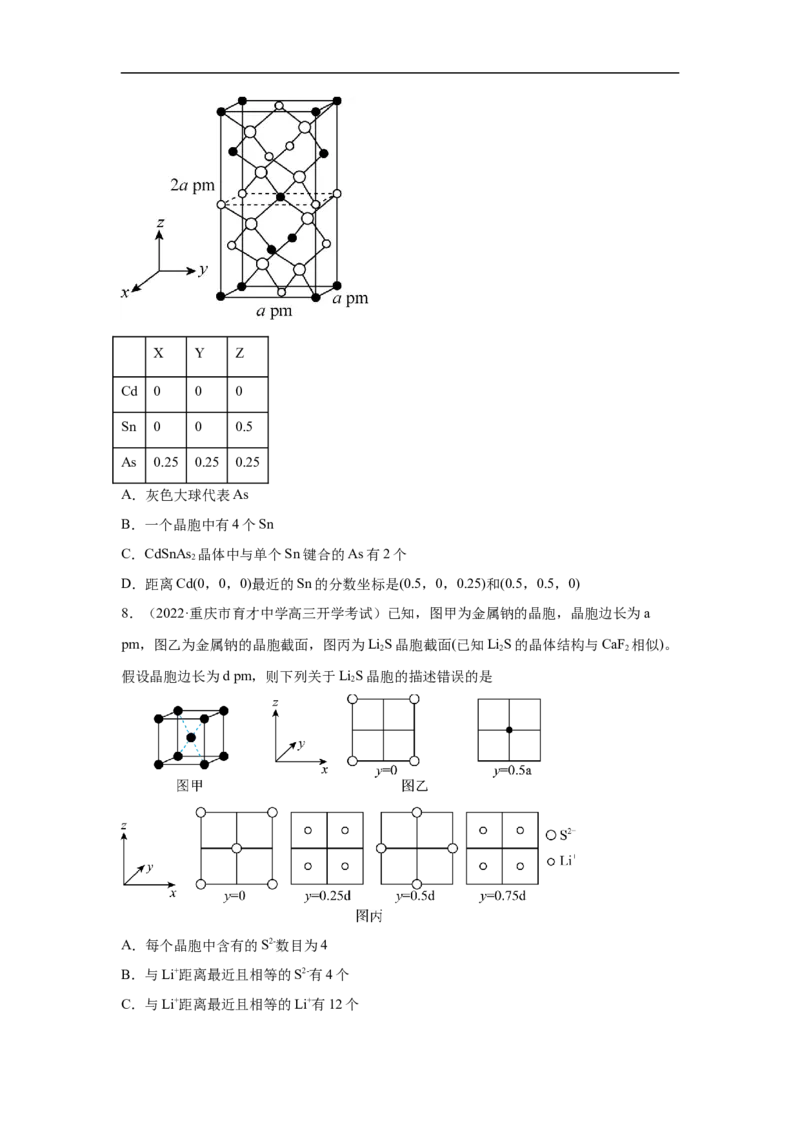
坐标。四方晶系CdSnAs 的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的
2
分数坐标如下表所示。
一个晶胞中有 个Sn,找出距离Cd(0, 0, 0)最近的Sn (用分数坐标表
示)。CdSnAs 晶体中与单个Sn键合的As有 个。
2
【解析】(2)坐标原点是黑球Cd(0, 0, 0),又知晶体的化学式为CdSnAs ,结合晶胞结构
2推知,Sn是白球,As是灰球。有4个Sn位于棱上(折合为1个),另外有6个Sn位于面上
(折合为3个),共4个Sn。距离Cd(0,0,0)最近的Sn有两个,分数坐标分别为(0.5,0,0.25)、
(0.5,0.5,0)。观察图中白球和灰球的关系,可知与单个Sn结合的As有4个。
【答案】(1)2 (0,0, )
(2)4 (0.5,0,0.25)、(0.5,0.5,0) 4
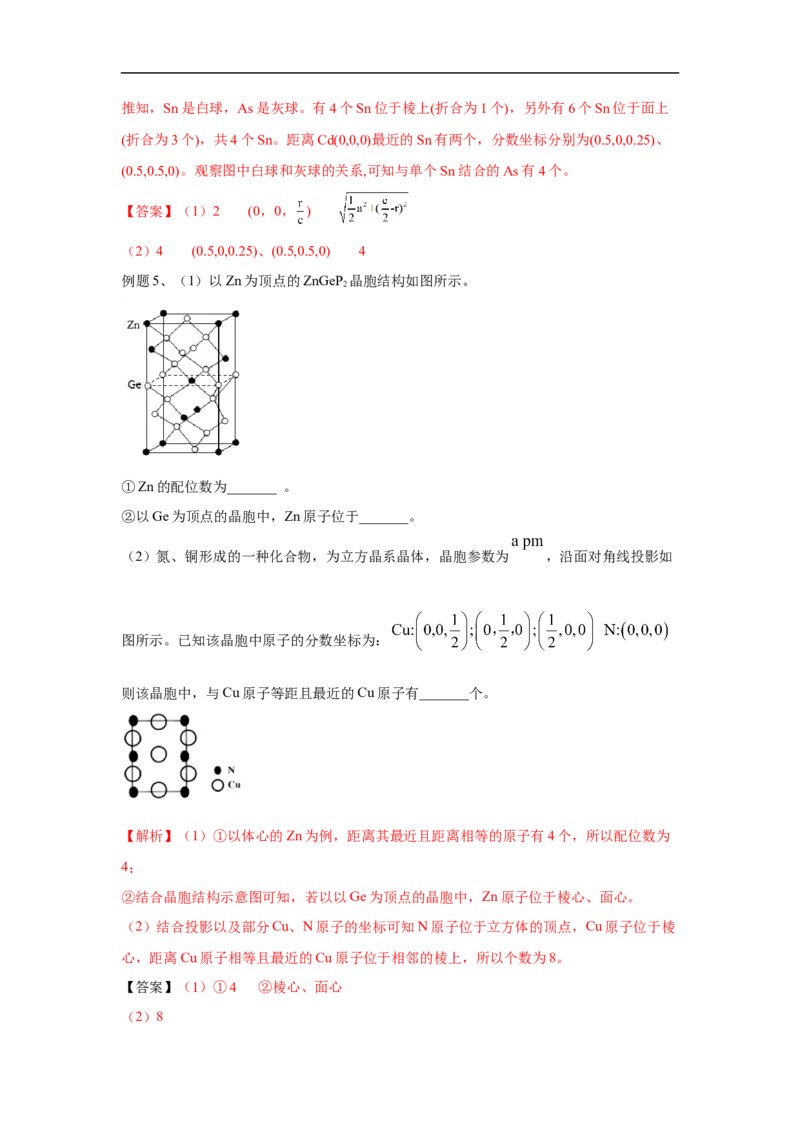
例题5、(1)以Zn为顶点的ZnGeP 晶胞结构如图所示。
2
①Zn的配位数为_______ 。
②以Ge为顶点的晶胞中,Zn原子位于_______。
(2)氮、铜形成的一种化合物,为立方晶系晶体,晶胞参数为 ,沿面对角线投影如
图所示。已知该晶胞中原子的分数坐标为:
则该晶胞中,与Cu原子等距且最近的Cu原子有_______个。
【解析】(1)①以体心的Zn为例,距离其最近且距离相等的原子有4个,所以配位数为
4;
②结合晶胞结构示意图可知,若以以Ge为顶点的晶胞中,Zn原子位于棱心、面心。
(2)结合投影以及部分Cu、N原子的坐标可知N原子位于立方体的顶点,Cu原子位于棱
心,距离Cu原子相等且最近的Cu原子位于相邻的棱上,所以个数为8。
【答案】(1)①4 ②棱心、面心
(2)81.(2022·广东·佛山市南海区九江中学高三阶段练习)我国科学家以碳60为原料,制造
出一种单层碳60聚合物单晶新材料(局部结构如图)。下列有关说法不正确的是
A.单层聚合C 与金刚石互为同素异形体
60
B.C 中的12C中子数为6
60
C.C 和石墨均为分子晶体
60
D.单层聚合碳60中有非极性共价键
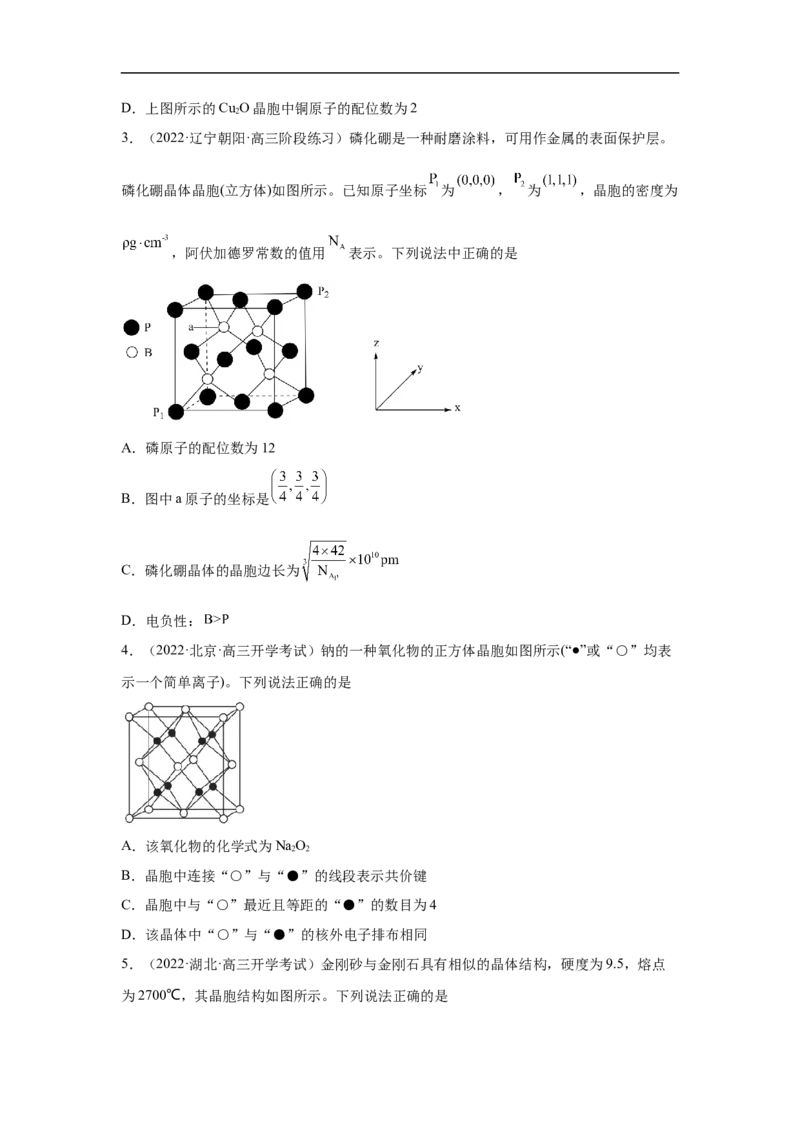
2.(2022·江苏省包场高级中学高三开学考试)乙醛与新制氢氧化铜悬浊液反应的实验如
下:
步骤1:向试管中加入 溶液,边振荡边滴加4~6滴 溶液,观察
到有蓝色絮状沉淀产生。
步骤2:再向试管中加入 乙醛溶液,加热,观察到有红色沉淀产生。
下列说法不正确的是
A.乙醛分子中元素的电负性:
B.步骤1中可用过量的氨水代替NaOH溶液
C.上述实验说明新制氢氧化铜能被乙醛还原D.上图所示的Cu O晶胞中铜原子的配位数为2
2
3.(2022·辽宁朝阳·高三阶段练习)磷化硼是一种耐磨涂料,可用作金属的表面保护层。
磷化硼晶体晶胞(立方体)如图所示。已知原子坐标 为 , 为 ,晶胞的密度为
,阿伏加德罗常数的值用 表示。下列说法中正确的是
A.磷原子的配位数为12
B.图中a原子的坐标是
C.磷化硼晶体的晶胞边长为
D.电负性:
4.(2022·北京·高三开学考试)钠的一种氧化物的正方体晶胞如图所示(“●”或“○”均表
示一个简单离子)。下列说法正确的是
A.该氧化物的化学式为NaO
2 2
B.晶胞中连接“○”与“●”的线段表示共价键
C.晶胞中与“○”最近且等距的“●”的数目为4
D.该晶体中“○”与“●”的核外电子排布相同
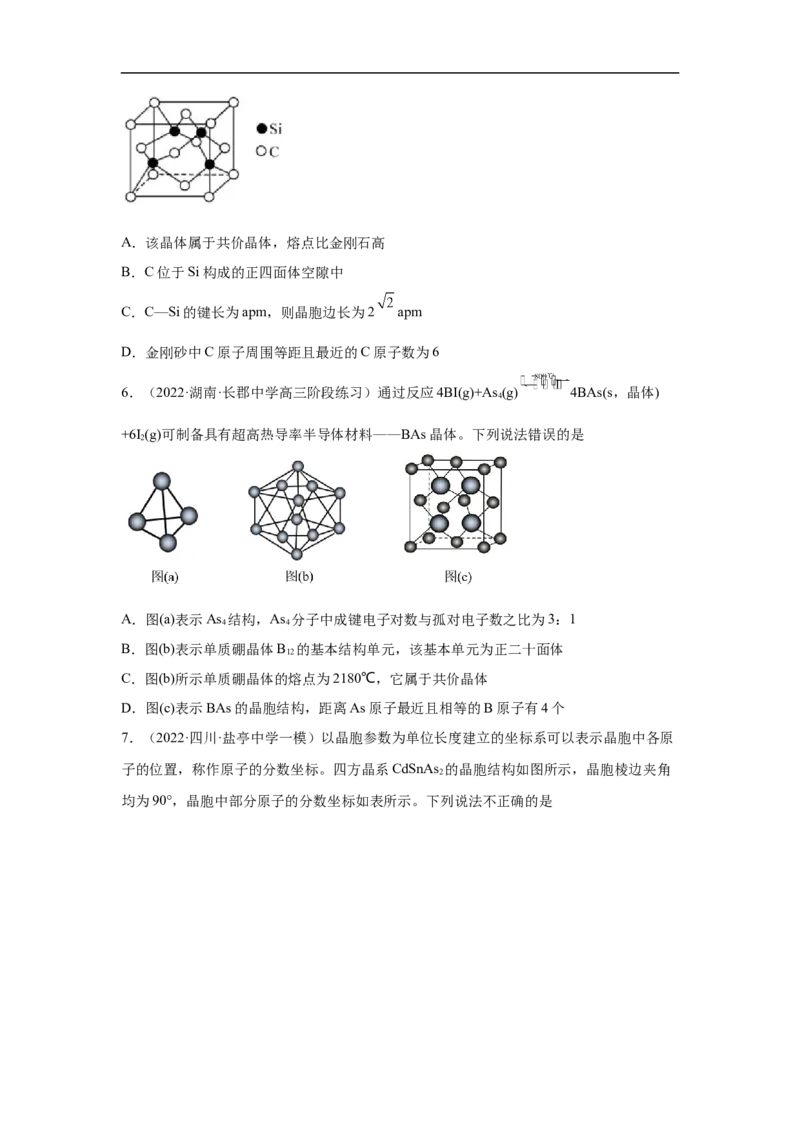
5.(2022·湖北·高三开学考试)金刚砂与金刚石具有相似的晶体结构,硬度为9.5,熔点
为2700℃,其晶胞结构如图所示。下列说法正确的是A.该晶体属于共价晶体,熔点比金刚石高
B.C位于Si构成的正四面体空隙中
C.C—Si的键长为apm,则晶胞边长为2 apm
D.金刚砂中C原子周围等距且最近的C原子数为6
6.(2022·湖南·长郡中学高三阶段练习)通过反应4BI(g)+As (g) 4BAs(s,晶体)
4
+6I (g)可制备具有超高热导率半导体材料——BAs晶体。下列说法错误的是
2
A.图(a)表示As 结构,As 分子中成键电子对数与孤对电子数之比为3:1
4 4
B.图(b)表示单质硼晶体B 的基本结构单元,该基本单元为正二十面体
12
C.图(b)所示单质硼晶体的熔点为2180℃,它属于共价晶体
D.图(c)表示BAs的晶胞结构,距离As原子最近且相等的B原子有4个
7.(2022·四川·盐亭中学一模)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原
子的位置,称作原子的分数坐标。四方晶系CdSnAs 的晶胞结构如图所示,晶胞棱边夹角
2
均为90°,晶胞中部分原子的分数坐标如表所示。下列说法不正确的是X Y Z
Cd 0 0 0
Sn 0 0 0.5
As 0.25 0.25 0.25
A.灰色大球代表As
B.一个晶胞中有4个Sn
C.CdSnAs 晶体中与单个Sn键合的As有2个
2
D.距离Cd(0,0,0)最近的Sn的分数坐标是(0.5,0,0.25)和(0.5,0.5,0)
8.(2022·重庆市育才中学高三开学考试)已知,图甲为金属钠的晶胞,晶胞边长为a
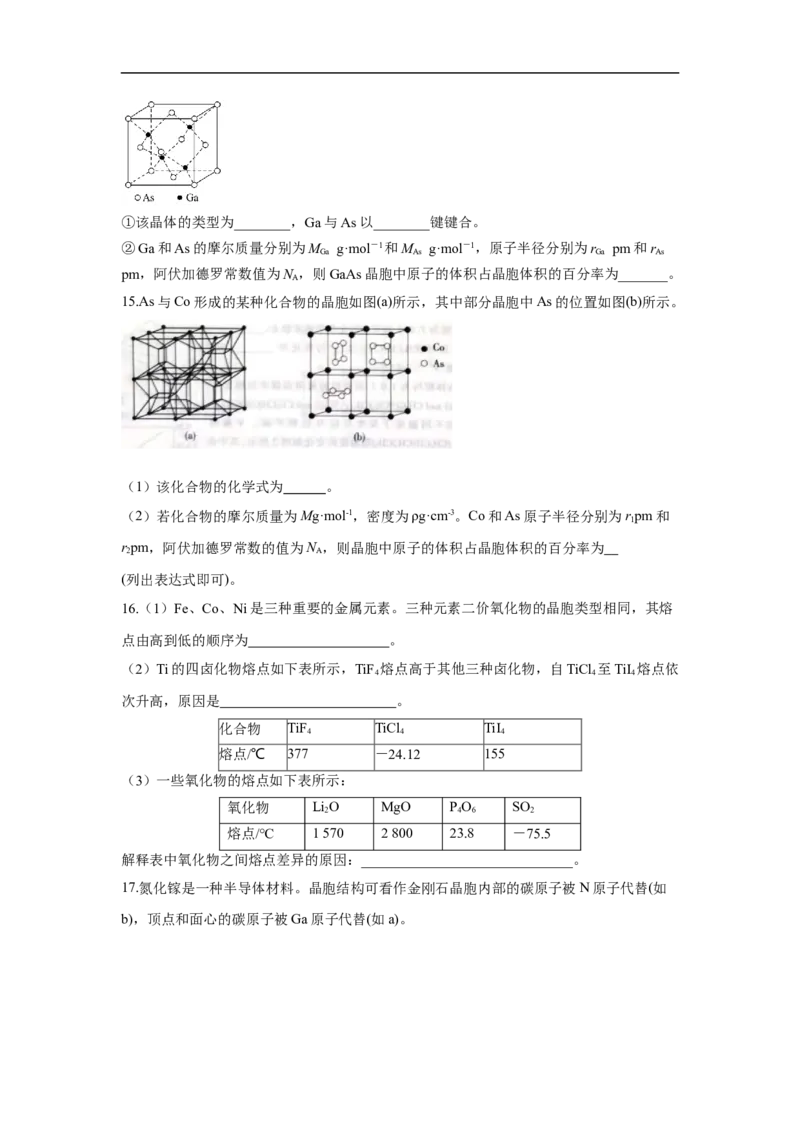
pm,图乙为金属钠的晶胞截面,图丙为LiS晶胞截面(已知LiS的晶体结构与CaF 相似)。
2 2 2
假设晶胞边长为d pm,则下列关于LiS晶胞的描述错误的是
2
A.每个晶胞中含有的S2-数目为4
B.与Li+距离最近且相等的S2-有4个
C.与Li+距离最近且相等的Li+有12个D.该晶胞中两个距离最近的Li+和S2-的核间距的计算表达式为
9.(2022·江苏南通·高三开学考试) 能与悬浮在大气中的海盐粒子作用,反应为
(CINO各原子均达到8电子稳定结构)。下列说法正确的是
A. 晶体属于分子晶体 B.ClNO的结构式为
C.NaCl晶胞中 的配位数为12 D. 是由极性键构成的非极性分子
10.(2022·山西·大同市第二中学校高三开学考试)某Ba-Ti-O晶体具有良好的电学性能,
其晶胞为立方晶胞(如图),晶胞参数为a pm。设阿伏加德罗常数的值为N ,下列说法错误
A
的是
A.化学式为 B. 的配位数为6
C. 位于 的八面体空隙 D.晶体的密度为
11.(2022·浙江·高三开学考试)已知非金属元素A、B、C、D是原子序数依次增大的4
种短周期元素,其中A是元素周期表中原子半径最小的元素,D是地壳中含量最多的元素,
B原子核外电子数是未成对电子数的3倍,E原子核外电子层数为4,其基态原子的内层轨
道全部排满电子,且最外层电子数与A相同。下列有关说法正确的是
A.元素B、C、D的第一电离能由大到小的顺序为:D>C>BB.由A与C以个数比1∶1组成的化合物中不可能含有离子键
C.A与B、A与C、A与D均能形成18电子的分子
D.如图为D和E两种元素组成的化合物的晶胞,则E离子的配位数为4
12.(2022·山东日照·高三开学考试) 的晶胞结构示意图如(a)所示。其中O围绕
Fe和P分别形成正八面体和正四面体。电池充电时, 脱出 转化如图,下列说
法正确的是
A.每个 晶胞中 个数为
B. 晶胞完全转化为 晶胞,转移电子数为
C. 晶胞中 价 原子个数为
D.当 转化为 时,每转移 电子,消耗
13. 我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO 固
2
溶体,四方ZrO 晶胞如图所示。
2
(1)Zr4+离子在晶胞中的配位数是________。晶胞参数为a pm、a pm、c pm,该晶体密度
为______g·cm-3(写出表达式)。
(2)在ZrO 中掺杂少量ZrO后形成的催化剂,化学式可表示为ZnZr O,则
2 x 1-x y
y=________(用x表达)。
14.GaAs的熔点为1 238 ℃,密度为ρ g·cm-3,其晶胞结构如图所示。①该晶体的类型为________,Ga与As以________键键合。
②Ga和As的摩尔质量分别为M g·mol-1和M g·mol-1,原子半径分别为r pm和r
Ga As Ga As
pm,阿伏加德罗常数值为N ,则GaAs晶胞中原子的体积占晶胞体积的百分率为_______。
A
15.As与Co形成的某种化合物的晶胞如图(a)所示,其中部分晶胞中As的位置如图(b)所示。
(1)该化合物的化学式为 。
(2)若化合物的摩尔质量为Mg·mol-1,密度为ρg·cm-3。Co和As原子半径分别为rpm和
1
rpm,阿伏加德罗常数的值为N ,则晶胞中原子的体积占晶胞体积的百分率为
2 A
(列出表达式即可)。
16.(1)Fe、Co、Ni是三种重要的金属元素。三种元素二价氧化物的晶胞类型相同,其熔
点由高到低的顺序为 。
(2)Ti的四卤化物熔点如下表所示,TiF 熔点高于其他三种卤化物,自TiCl 至TiI 熔点依
4 4 4
次升高,原因是 。
化合物 TiF TiCl TiI
4 4 4
熔点/℃ 377 -24.12 155
(3)一些氧化物的熔点如下表所示:
氧化物 LiO MgO PO SO
2 4 6 2
熔点/°C 1 570 2 800 23.8 -75.5
解释表中氧化物之间熔点差异的原因:______________________________。
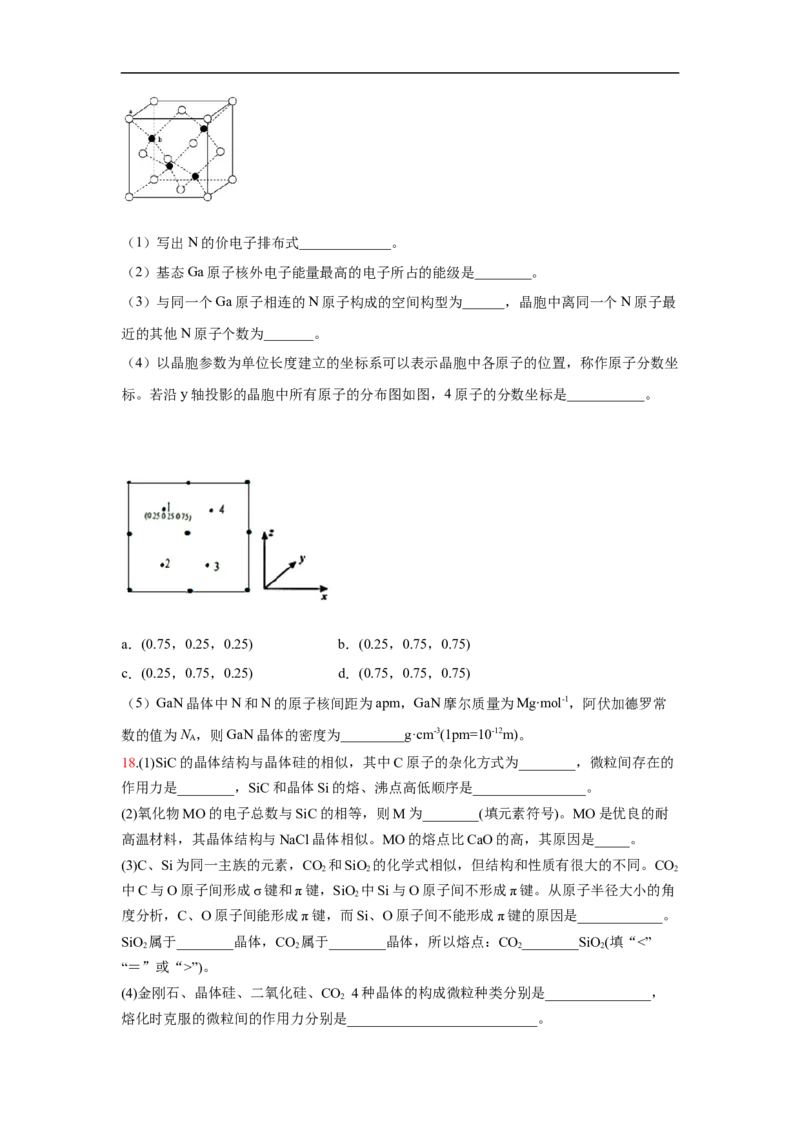
17.氮化镓是一种半导体材料。晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替(如
b),顶点和面心的碳原子被Ga原子代替(如a)。(1)写出N的价电子排布式_____________。
(2)基态Ga原子核外电子能量最高的电子所占的能级是________。
(3)与同一个Ga原子相连的N原子构成的空间构型为______,晶胞中离同一个N原子最
近的其他N原子个数为_______。
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐
标。若沿y轴投影的晶胞中所有原子的分布图如图,4原子的分数坐标是___________。
a.(0.75,0.25,0.25) b.(0.25,0.75,0.75)
c.(0.25,0.75,0.25) d.(0.75,0.75,0.75)
(5)GaN晶体中N和N的原子核间距为apm,GaN摩尔质量为Mg∙mol-1,阿伏加德罗常
数的值为N ,则GaN晶体的密度为_________g·cm-3(1pm=10-12m)。
A
18.(1)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为________,微粒间存在的
作用力是________,SiC和晶体Si的熔、沸点高低顺序是________________。
(2)氧化物MO的电子总数与SiC的相等,则M为________(填元素符号)。MO是优良的耐
高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是_____。
(3)C、Si为同一主族的元素,CO 和SiO 的化学式相似,但结构和性质有很大的不同。CO
2 2 2
中C与O原子间形成σ键和π键,SiO 中Si与O原子间不形成π键。从原子半径大小的角
2
度分析,C、O原子间能形成π键,而Si、O原子间不能形成π键的原因是____________。
SiO 属于________晶体,CO 属于________晶体,所以熔点:CO________SiO(填“<”
2 2 2 2
“=”或“>”)。
(4)金刚石、晶体硅、二氧化硅、CO 4种晶体的构成微粒种类分别是_______________,
2
熔化时克服的微粒间的作用力分别是___________________________。参考答案
1.C【详解】A.单层聚合C 与金刚石都是由碳元素组成的单质,两者互为同素异形体,
60
故A正确;
B.12C原子的质量数为12,则中子数为12-6=6,故B正确;
C.C 分子是由60个碳原子通过共价键结合形成的分子,其固体为分子晶体,而石墨晶体
60
形成二维网状结构,层内每个碳原子以共价键与周围的三个碳原子结合,层间为分子间作
用力,是一种混合晶体,故C错误;
D.由图可知,单层聚合碳60由碳60簇笼在平面上通过碳碳键结合而成,碳碳键属于非极
性共价键,故D正确;
答案选C。
2.B【详解】A.同周期主族元素从左向右电负性逐渐变大,所以O>C。在烃类有机物中,
C常显负价,H常显正价,说明在化合物中共用电子对更偏向C,说明电负性C>H。于是,
电负性O>C>H。A正确。
B.在氨水中滴加CuSO ,由于氨水过量发生如下反应:
4
和 ,不能
得到蓝色絮状沉淀。B错误。
C.实验过程中Cu(OH) 转化成Cu O,铜元素化合价从+2减低到+1,发生还原反应。C正
2 2
确。
D.依据分摊法可知白色圆点个数为 个;黑色圆点个数为4个。据此可知白色圆
点代表O2-,黑色圆点代表Cu+。4个Cu+分别位于4条体对角线的上 处或下 处,于是距
离Cu+最近的O2-有2个(1个在顶点,1个在体心),即配位数为2。D正确。
综上所述,应选B。
3.C【详解】A.以上底面面心P原子为研究对象,与之距离最近且相等的硼原子为该晶
胞内部上层2个B原子,还有上层晶胞内部下层2个B原子,即磷原子的配位数为4,A错
误;
B.图中a原子处于上层、左侧、后方 晶胞体心位置,可知a左侧面距离为晶胞棱长的 ,即 ,到前平面、下底面距离均为晶胞棱长的 ,则坐标参数 ,则a原子的坐
标为 ,B错误;
C.根据均摊法一个晶胞中含有P个数为 ,含有B个数为4,设晶胞边长为
xcm,则 ,C正确;
D.电负性P大于B,D错误;
故答案选C。
4.D【详解】由晶胞图可知,黑色原子有8个在体内,白色原子有8个在顶点、6个在面
心,根据均摊法进行计算, ,可知白色原子和黑色原子之比为1:2,故该
氧化物为NaO,白色的为氧离子,黑色的为钠离子,据此分析解答。
2
A.由分析可知,该氧化物的化学式为NaO,A错误;
2
B.氧化钠中含有离子键,晶胞中连接氧离子与钠离子的线段表示离子键,B错误;
C.由晶胞图可知,晶胞中与氧离子最近且等距的钠离子的数目为8,C错误;
D.钠离子和氧离子的核外电子数均为10,最外层电子均为8,核外电子排布相同,D正确;
故答案选D。
5.B【详解】A.金刚砂与金刚石具有相似的晶体结构,SiC属于共价晶体,C-Si键长长
于C-C键,故熔点比金刚石低,故A错误;
B.距离C原子最近且等距离的Si原子个数是4,且四个Si原子构成正四面体结构,所以
C位于Si构成的四面体空隙中,故B正确;
C.C-Si键的长度为晶胞体对角线长度的 ,设晶胞棱长为x,则 ,所以x=
,故C错误;D.以SiC晶胞顶角上的碳原子为研究对象,每个C原子周围最近且等距的C原子位于面
心,由于顶点碳原子为8个晶胞共有,则C原子周围等距且最近的C原子数为12,故D错
误;
故选B。
6.A【详解】A.图(a)表示 结构,每个 原子最外层有5个电子,形成3个 键,还
有1对孤对电子, 分子中成键电子对数(共6对)与孤对电子数(共4对)之比为3∶2,A
错误;
B.图(b)表示单质硼晶体 的基本结构单元,每个面都是由3个B原子形成的正三角形,
一共有20个正三角形,所以该基本单元为正二十面体,B正确;
C.单质硼晶体的熔点为 ,熔点较高,且原子间通过共价键结合,属于共价晶体,C
正确;
D. 晶胞中,较大的原子为 原子,距离 原子最近且相等的B原子有4个,D正确;
答案选A。
7.C【详解】由部分Cd原子的分数坐标(0,0,0),可知8个Cd在晶胞的顶点,4个Cd
在晶胞的面心,1个在晶胞的体心;部分Sn原子的分数坐标为(0,0,0.5),4个Sn在晶胞
的棱上,6个Sn在晶胞的面心,部分As原子的坐标为(0.25,0.25,0.125),8个As在晶胞
的体心;所以一个晶胞中含有Sn的个数为: ;距离Cd(0,0,0)最近的Sn
是(0.5,0,0.25)、(0.5,05,0);由图可知,CdSnAs 晶体中与单个Sn键合的As有4个,
2
以此解答该题。
A.由以上分析可知,部分As原子的坐标为(0.25,0.25,0.125),则As位于晶胞的体心,
可知灰色大球代表As,故A正确;
B.4个Sn在晶胞的棱上, 6个Sn在晶胞的面心,则一个晶胞中含有Sn的个数为:
,故B正确;
C.CdSnAs 晶体中,晶胞面上的Sn除与该晶胞中的2个As键合外,还有相邻晶胞中的2
2
个As键合,晶胞棱上的Sn除与该晶胞中的1个As键合外,还与相邻晶胞中的3个As键
合,故晶体中与单个Sn键合的As有4个,故C错误;D.距离Cd(0,0,0)最近的Sn是(0.5,0,0.25)、(0.5,05,0),故D正确;
故答案选C。
8.C【详解】根据图丙可知LiS的晶胞结构为: ,据此分析解答。
2
A.根据晶胞结构可知在该晶胞中S2-个数=8× +6× =4,A正确;
B.每个Li+连接4个距离最近且相等的S2-,所以与Li+距离最近且相等的S2-有4个,B正
确;
C.该晶胞中含有8个Li+,两个距离最近的Li+之间距离为晶胞边长d的一半,与Li+距离
最近且相等的Li+有6个,分别位于该Li+的上、下、前、后、左、右六个方向,C错误;
D.该晶胞中该晶胞中两个距离最近的Li+和S2-的核间距为晶胞体对角线的 ,该晶胞边长
为d pm,体对角线为 ,则该晶胞中该晶胞中两个距离最近的Li+和S2-的核间距的计
算表达式为 ,D正确;
故合理选项是C。
9.B【详解】A. 晶体属于离子晶体,故A错误;
B.ClNO各原子均达到8电子稳定结构则,O原子要连两根共价键,N原子要连三根共价
键,Cl原子要连一根共价键,结构式为 ,故B正确;
C. 配位数指的是某个离子周围的异种电荷的离子数,所以,NaCl中Na+周围的Cl-是6个,
配位数为6,故C错误;
D. 是由极性键构成的极性分子,故D错误;
正确答案是B。
10.B【详解】A. 位于顶点,晶胞中其数目为1, 位于体心,晶胞中其数目为1, 位于面心,晶胞中其数目为3,故化学式为 ,A正确;
B.由晶胞结构可知, 周围有12个 ,则 的配位数为12,B错误;
C. 位于 的八面体空隙,C正确;
D. 位于面心,晶胞中其数目为3,分子式为 ,所以其密度为 ,
D正确;
故选B。
11.C【详解】A是元素周期表中原子半径最小的元素,则为H元素;D是地壳中含量最
多的元素,为O元素;B原子核外电子数是未成对电子数的3倍,假设未成对电子数为
1,则核外电子数为3,不符合题意,假设未成对电子数为2,则核外电子数为6,为C元
素;非金属元素A、B、C、D是原子序数依次增大的4种短周期元素,所以C为N元素;
E原子核外电子层数为4,其基态原子的内层轨道全部排满电子,且最外层电子数与A相
同,则E为Cu元素,据此分析解答。
根据上述分析可知,A、B、C、D、E分别为H、C、N、O、Cu元素,据此分析解答。
A.VA族的p能级处于半充满的稳定结构,比同周期VIA族的第一电离能大,元素B、
C、D的第一电离能由大到小的顺序为:C(N) > D(O) >B(C),A错误;
B.C为N元素,则含N和H的化合物中含铵根离子,铵根离子与阴离子之间存在离子键,
B错误;
C.A与B可形成C H、A与C可形成NH、A与D可形成HO,均能形成18电子的分
2 6 2 4 2 2
子,C正确;
D.D为O元素,E为Cu元素,根据晶胞结构可知,白球与黑球的个数比为
=1:2,所以白球是O,黑球为Cu,则E离子的配位数为2,D错误;
故选C。
12.C【详解】由(a)图可知,LiFePO 晶胞中小球表示锂离子,位于顶点、面心和棱上的锂
4
离子个数为 ,则晶胞中含有4个LiFePO ;由(b)图可知,与LiFePO 晶
4 4
胞相比,Li FePO 晶胞缺失1个面心和1个棱上锂离子,晶胞中锂离子的个数为
1—x 4,则 ,解得x=0.1875,Li FePO 为Li FePO ,设
1—x 4 0.8125 4
Li FePO 中亚铁离子和铁离子数目分别为a和b,由铁原子个数守恒可得:a+b=1,由化
0.8125 4
合价代数和为0可得:0.8125+2a+3b+5=8,解得a=0.8125、b=0.1875。
A.由分析可知,每个Li FePO 晶胞中含有4(1—x)个锂离子,故A错误;
1—x 4
B.由分析可知,Li FePO 中铁离子数目为0.1875,则1molLiFePO 晶胞完全转化为Li
0.8125 4 4 1—
FePO 晶胞失去电子的数目为1mol×0.1875×4×N mol—1=0.75N ,故B错误;
x 4 A A
C.由分析可知,Li FePO 中亚铁离子数目为0.8125,则1molLi FePO 晶胞中亚铁离
0.8125 4 1—x 4
子的数目为1mol×0.8125×4×N mol—1=3.25N ,故C正确;
A A
D.由分析可知,FePO 转化为Li FePO 时,得到(1—x)个电子,消耗(1—x)个锂离子,
4 1—x 4
则1mol FePO 转化为Li FePO 时,得到(1—x)mol电子,消耗(1—x)mol锂离子,故D错
4 1—x 4
误;
故选C。
13.(1)8
(2)2-x
【解析】(1)以晶胞中右侧面心的Zr4+为例,同一晶胞中与Zr4+最近且等距离的O2—有4
个,同理可知右侧晶胞中也有4个O2—,故在晶胞中Zr4+的配位数为4+4=8。1个晶胞中含
有4个ZrO 微粒,1个晶胞的质量m(晶胞)= ;1个晶胞的体积为
2
V(晶胞)=(a×10—10cm)×(a×10—10cm)×(c×10—10cm)=a2c×10—30cm3,故该晶体密度为ρ=m(晶
胞)/V(晶胞)= = g·cm—3。
(2)在ZrO 中掺杂少量ZrO后形成的催化剂,化学式可表示为ZnZr O,其中Zn元素
2 x 1-x y
为+2价,Zr为+4价,O元素为-2价,根据化合物化合价为0可知2x+4×(1-x)=2y,解得
y=2-x。
14.(1)共价晶体 共价
(2)
【解析】(1)GaAs的熔点很高,则其晶体类型为共价晶体,Ga和As以共价键键合。
(2)由晶胞结构可知一个晶胞中含有As、Ga原子的个数均为4,则晶胞的体积为,又知二者的原子半径分别为r pm和r pm,则GaAs晶胞中原子的体积占
Ga As
晶胞体积的百分率为 ×100%= 。
15.(1)CoAs (2)
3
【解析】(1)根据晶胞结构,b为晶胞的一半,As在晶胞的内部,则晶胞中含有As的个
数=4×3×2=24,Co在晶胞的顶点、棱上、面心和体内,个数=8× +12× +6× +1=8,
N(Co):N(As)=8:24=1:3,则化学式为CoAs 。
3
(2)根据晶胞的化学式及结构,则1mol晶胞的质量为8M g,晶胞的体积为 cm3,晶
胞中Co和As原子的体积= (8r +24r )×10-30cm3,则晶胞中原子的体积占晶胞体积的百
分率为 。
16.(1)NiO>CoO>FeO
(2)TiF 为离子化合物,熔点高,其他三种均为共价化合物,随相对分子质量的增大分子
4
间作用力增大,熔点逐渐升高
(3)LiO、MgO为离子晶体,PO、SO 为分子晶体,离子键MgO>LiO,分子间作用力
2 4 6 2 2
(相对分子质量)P O>SO
4 6 2
【解析】(1)三种元素二价氧化物的晶胞类型相同,离子半径Fe2+>Co2+>Ni2+,离子键按
FeO、CoO、NiO的顺序依次增强,而离子键越强,离子晶体的熔点越高,故其熔点由高到
低的顺序为NiO>CoO>FeO。
(2)根据表格中数据,可以得出TiF 的熔点最高,其晶体类型应该为离子晶体,其他三种
4
卤化物晶体类型应该为分子晶体,根据影响晶体熔点的因素,离子键强度大于分子间作用
力,所以TiF 熔点最高,其他三种卤化物随相对分子质量的增大,分子间作用力增大,熔
4点逐渐升高。
(3)LiO、MgO为离子晶体,PO、SO 为分子晶体。离子半径:Mg2+>Li+,则离子键的
2 4 6 2
强弱:MgO>LiO;由于相对分子质量:PO>SO ,则分子间力:PO>SO ,故熔点大
2 4 6 2 4 6 2
小顺序是MgO>LiO>PO>SO 。
2 4 6 2
17.(1)2s22p3 (2)4p
(3)正四面体 12
(4)d (5)
【解析】(1)根据核外电子的排布规律可知:N的价电子排布式2s22p3;
(2)基态Ga原子核外电子排布式为1s22s22p63s23p63d104s24P1,能量最高的电子所占的能级是
4P;
(3)由图可知,与同一个Ga原子相连的N原子构成的空间构型为正四面体型,Ga位于正四
面体的中心,晶胞中,以上底面的N原子为参照,与上底面顶点的四个氮原子,与下面晶
胞和上面晶胞面上的氮原子距离都相等,故晶胞中离同一个N原子最近的其他N原子个数
为12;
(4)若沿y轴投影的晶胞中所有原子的分布图如图,已知1原子的分数坐标是(0.25,0.25,
0.75),4原子和1原子的Z轴坐标相等,x、y的坐标加0.5,故4原子的分数坐标是(0.75,
0.75,0.75),答案选d;
(5)GaN晶体中N和N的原子核间距为apm,GaN摩尔质量为Mg∙mol-1,阿伏加德罗常数的
值为N ,Ga位于顶点和面心,个数为 =4,N原子位于体心,个数也为4,则GaN
A
晶体的密度为ρ= ,设N和N的原子核间距为apm,晶胞的边长为
apm,将边长代入密度公式可得:ρ= g·cm-3= g·cm-3。
18.(1)sp3 共价键 SiC>Si
(2)Mg Mg2+半径比Ca2+小,MgO晶格能大
(3)Si的原子半径较大,Si、O原子间距离较大,pp轨道肩并肩重叠程度较小,不能形成稳
定的π键 原子 分子 <
(4)原子、原子、原子、分子 共价键、共价键、共价键、分子间作用力
【解析】(1)SiC与晶体硅结构相似,晶体硅中一个硅原子与周围四个硅原子相连,呈正四
面体结构,所以杂化方式是sp3,则SiC晶体中C原子杂化方式为sp3;因为SiC的键长小
于SiSi,所以熔、沸点高低顺序:SiC>Si。
(2)SiC电子总数是20个,则该氧化物为MgO;晶格能与所构成离子所带电荷成正比,与离子半径成反比,MgO与CaO的离子电荷数相同,Mg2+半径比Ca2+小,MgO晶格能大,
熔点高。
(3)Si的原子半径较大,Si、O原子间距离较大,pp轨道肩并肩重叠程度较小,不能形成稳
定的π键。SiO 为原子晶体,CO 为分子晶体,所以熔点:SiO>CO 。
2 2 2 2
(4)金刚石、晶体硅、二氧化硅均为原子晶体,构成微粒为原子,熔化时破坏共价键;CO
2
为分子晶体,由分子构成,以分子间作用力结合。