文档内容
易错点 21 化学反应速率
易错题【01】化学反应速率的计算
在解题过程中先写出有关反应的化学方程式;找出各物质的起始量、转化量、某时刻量;根据已知条件列
方程式计算。例如,对于反应mA+nB===pC+qD,A的浓度为a mol·L-1,B的浓度为b mol·L-1,反应
进行至t s时,A消耗了x mol·L-1,则反应速率可计算如下:
1
mA(g)+nB(g)===pC(g)+qD(g)
a b 0 0
x
a-x b-
则v(A)= mol·L-1·s-1,同一反应不同物质的反应速率之间的关系如下:
易错题【02】化学反应速率的比较
同一化学反应中,不同物质来表示化学反应速率时,数值可能不同,需要进行转化。常用以下两种方法:
①看化学反应速率的单位是否一致,若不一致,需转化为同一单位;将不同物质的化学反应速率转化成同
一物质的化学反应速率,或分别除去相应物质的化学计量数;标准统一后比较数值大小,数值越大,反应
速率越大。
②比值法通过化学反应速率与其对应的化学计量数的比值进行比较,比值大的化学反应速率大。如对于反
应aA(g)+bB(g) cC(g)+dD(g),若:>,则A表示的化学反应速率较大。
易错题【03】催化剂的特点和影响因素
⇌
①催化剂具有高度的选择性(或专一性)。一种催化剂并非对所有的化学反应都有催化作用,例如二氧化锰
在氯酸钾受热分解中起催化作用,加快化学反应速率,但对其他的化学反应就不一定有催化作用。
②某些化学反应并非只有唯一的催化剂,例如氯酸钾受热分解中能起催化作用的还有氧化镁、氧化铁和氧
化铜等。
③绝大多数催化剂都有其活性温度范围,温度过高或过低,催化活性都会降低。
④在有的反应中催化剂参与化学反应,其作用是降低该反应发生所需要的活化能,可以把一个较难发生的
反应变成几个较容易发生的化学反应。
⑤催化剂能改变反应的活化能,但不能改变反应的ΔH 。4.控制变量法探究影响反应速率的因素
(1)确定变量:理清影响实验探究结果的所有因素。
(2)定多变一:在探究时,先确定其他的因素不变,只变化一种因素,看这种因素与探究的问题存在怎样的
关系;这样确定一种以后,再确定另一种,通过分析每种因素与所探究问题之间的关系,得出所有影响因
素与所探究问题之间的关系。
(3)数据有效:解答时注意选择数据(或设置实验)要有效,且变量统一,否则无法作出正确判断。
易错题【04】速率常数与化学平衡常数之间的关系
一定温度下, 可逆反应:aA(g)+bB(g) gG(g)+hH(g),达到平衡状态时,v =k ca(A)·cb(B),v
正 正
=k ·cg(G)·ch(H),由于平衡时 v =v ,则k ca(A)·cb(B)=k ·cg(G)·ch(H),所以==K。
逆 逆 正 逆 正 逆
典例分析
例1、在C(s)+CO(g) 2CO(g)反应中可使反应速率增大的措施是( )
2
①减小容器体积使增大压强 ②增加碳的量 ③恒容时通入CO ④恒压下充入N ⑤恒容下充入
2 2
N
2
A.①③⑤ B.②④ C.①③ D.③⑤
C【解析】该反应为气体参加的反应,增大压强,反应速率加快,①正确;增加碳的量,固体物质的浓度
不变不影响化学反应速率,②错误;恒容通入CO,反应物浓度增大,反应速率加快,③正确;恒压下充
2
入N,体积增大反应物浓度减小,反应速率减小,④错误;恒容下充入N,反应物的浓度不变,反应速率
2 2
不变,⑤错误。
例2、已知反应2NO(g)+2H(g) N(g)+2HO(g) ΔH=-752 kJ·mol-1的反应机理如下:
2 2 2
①2NO(g) NO(g) (快)
2 2
②NO(g)+H(g) NO(g)+HO(g) (慢)
2 2 2 2 2
③NO(g)+H(g) N(g)+HO(g) (快)
2 2 2 2
下列有关说法错误的是( )
A.①的逆反应速率大于②的正反应速率
B.②中NO 与H 的碰撞仅部分有效
2 2 2
C.NO 和NO是该反应的催化剂
2 2 2
D.总反应中逆反应的活化能比正反应的活化能大
C【解析】①为快反应,说明反应物的活化能和生成物的活化能都较小,反应更容易发生;②为慢反应,
说明反应物的活化能和生成物的活化能都较大,②中反应物的活化能大于①中生成物的活化能,因此①的
逆反应速率大于②的正反应速率,A项正确;②反应为慢反应,反应慢说明反应的活化能大,物质微粒发
生碰撞时,许多碰撞都不能发生化学反应,因此碰撞仅部分有效,B项正确;反应过程中NO 和NO是中
2 2 2
间产物,不是催化剂,C项错误;总反应为放热反应,则总反应中逆反应的活化能比正反应的活化能大,
D项正确。
例3、(1)某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
序号 纯锌 2.0 mol·L-1 温度 硫酸铜 加入蒸粉/g 硫酸溶液/mL / ℃ 固体/g 馏水/mL
Ⅰ 2.0 50.0 25 0 0
Ⅱ 2.0 40.0 25 0 10.0
Ⅲ 2.0 50.0 25 0.2 0
Ⅳ 2.0 50.0 25 4.0 0
①本实验待测数据可以是_________________________________,
实验Ⅰ和实验Ⅱ可以探究 对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是____________________________________,
写出有关反应的离子方程式____________________________________。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验 体积V/mL
序号 KSO 溶液 水 KI溶液 NaSO 溶液 淀粉溶液
2 2 8 2 2 3
① 10.0 0.0 4.0 4.0 2.0
② 9.0 1.0 4.0 4.0 2.0
③ 8.0 V 4.0 4.0 2.0
x
表中V= ,理由是______________________________。
x
【答案】(1)①反应结束所需要的时间(或相同条件下产生等体积的氢气所需要的时间) 硫酸浓度
②探究硫酸铜的质量对反应速率的影响 Zn+Cu2+===Zn2++Cu,Zn+2H+===Zn2++H↑
2
(2)2.0 保证反应物KSO 浓度的改变,而其他物质浓度不变
2 2 8
【解析】(1)实验Ⅰ和实验Ⅱ中,锌的质量和状态相同,硫酸的浓度不同,实验Ⅲ和实验Ⅳ中加入硫酸铜,
Cu2+的氧化性强于H+,首先发生反应Zn+Cu2+===Zn2++Cu,生成的铜附着在锌表面,在稀硫酸溶液中
构成原电池,加快化学反应速率。但是加入的硫酸铜过多,生成的铜会覆盖在锌表面,阻止锌与稀硫酸进
一步反应,产生氢气的速率又会减慢。①本实验待测数据可以是“反应结束所需要的时间”或“相同条件
下产生等体积的氢气所需要的时间”,实验Ⅰ和实验Ⅱ可以探究硫酸的浓度对反应速率的影响。②实验Ⅲ
和实验Ⅳ加入的硫酸铜的质量不同,可以探究加入硫酸铜的质量与反应速率的关系。(2)实验的目的是探究
KSO 溶液的浓度对化学反应速率的影响,故应保证每组实验中其他物质的浓度相等,即溶液的总体积相
2 2 8
等(即为20.0 mL),从而可知V=2.0。
x
例4、将氨氧化法制硝酸过程中氨经催化氧化后的气体(高于800 ℃)急剧冷却到100 ℃以下,一方面除去大
量的HO,使NO(g)和O(g)发生反应,另一方面温度低有利于生成NO (g)。
2 2 2
2NO(g)+O(g) 2NO (g)的反应历程分两步:
2 2
Ⅰ.2NO(g) NO(g)(反应快,瞬间达到平衡) ΔH<0
2 2 1
v =k ·c2(NO) v =k ·c(N O)
1正 1正 1逆 1逆 2 2
Ⅱ.N O(g)+O(g) 2NO (g)(反应慢) ΔH<0
2 2 2 2 2
v =k ·c(N O)·c(O ) v =k ·c2(NO )
2正 2正 2 2 2 2逆 2逆 2
其中k、k 是速率常数,随温度上升而增大。
1 2则:一定温度下,反应2NO(g)+O(g) 2NO (g)达到平衡状态,请写出用k 、k 、k 、k 表示
2 2 1正 1逆 2正 2逆
的平衡常数表达式K=________,根据速率方程分析,升高温度该总反应速率减小的原因是
_____________________________。
【答案】 温度升高,反应Ⅰ逆向移动并迅速达到平衡,导致NO 浓度减小,虽然升高温度k 、k 均增
2 2 2正 2逆
大,但对反应Ⅱ影响弱于NO 浓度减小的影响,导致反应Ⅱ速率变小,总反应的速率由较慢的一步决定,
2 2
所以总反应速率减小
【解析】已知①2NO(g)N O(g);②NO(g)+O(g) 2NO (g),而目标反应2NO(g)+
2 2 2 2 2 2
O(g)2NO (g)的ΔH=①+②=ΔH+ΔH,由反应达平衡状态,所以v =v 、v =v ,所以v
2 2 1 2 1正 1逆 2正 2逆 1正
×v =v ×v ,即k ·c2(NO)×k ·c(N O)·c(O )=k ·c(N O)×k ·c2(NO ),整理得==K;温度升高,反
2正 1逆 2逆 1正 2正 2 2 2 1逆 2 2 2逆 2
应Ⅰ逆向移动并迅速达到平衡,导致NO 浓度减小,虽然温度k 、k 均增大,但对反应Ⅱ影响弱于
2 2 2正 2逆
NO 浓度减小的影响,导致反应Ⅱ速率变小,总反应的速率由较慢的一步决定,所以总反应速率减小。
2 2
1.(2022·辽宁·高考真题)某温度下,在 恒容密闭容器中 发生反应 ,
有关数据如下:
时间段/ 产物Z的平均生成速率/
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是A. 时,Z的浓度大于
B. 时,加入 ,此时
C. 时,Y的体积分数约为33.3%
D. 时,X的物质的量为
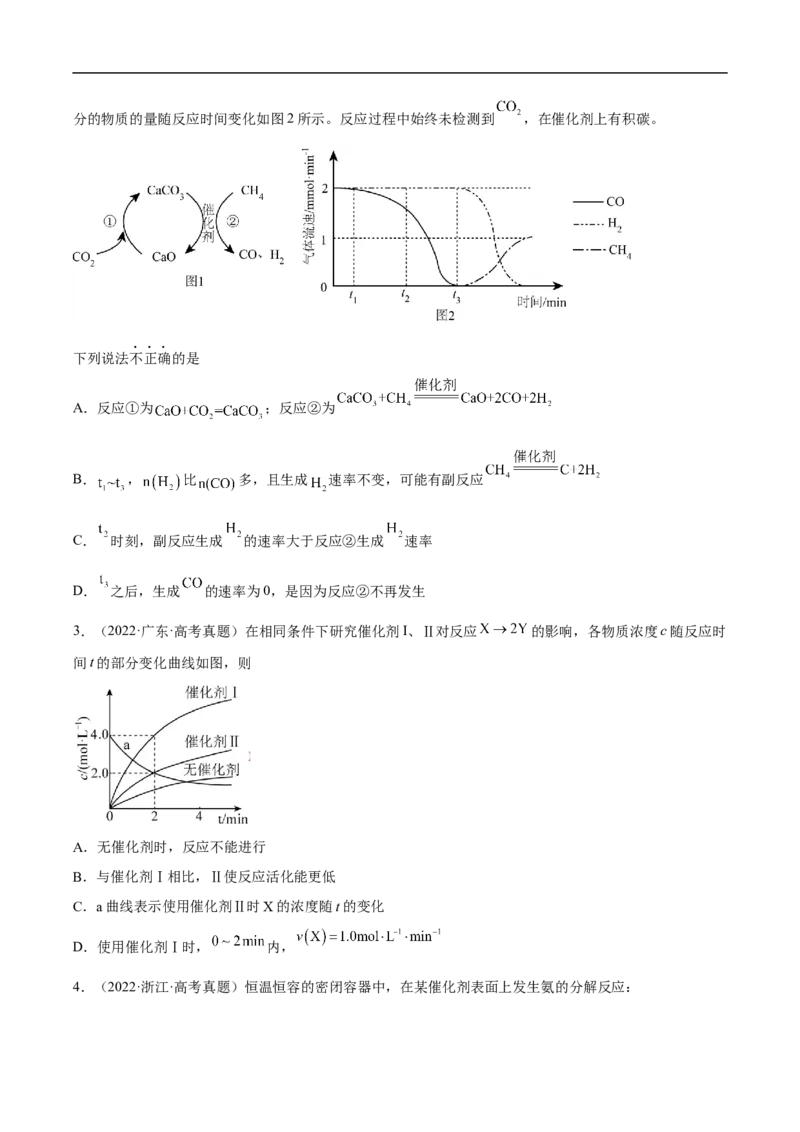
2.(2022·北京·高考真题) 捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应①完
成之后,以 为载气,以恒定组成的 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。
下列说法不正确的是
A.反应①为 ;反应②为
B. , 比 多,且生成 速率不变,可能有副反应
C. 时刻,副反应生成 的速率大于反应②生成 速率
D. 之后,生成 的速率为0,是因为反应②不再发生
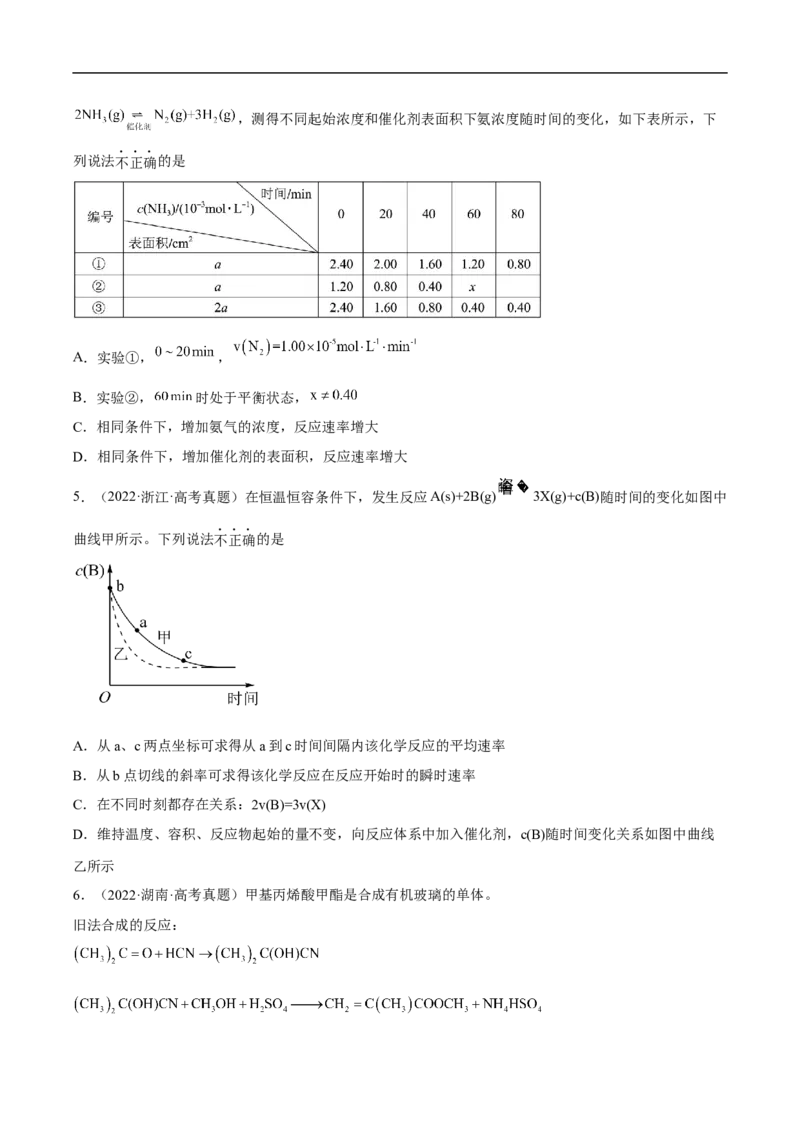
3.(2022·广东·高考真题)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时
间t的部分变化曲线如图,则
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时, 内,
4.(2022·浙江·高考真题)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
5.(2022·浙江·高考真题)在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g)+c(B)随时间的变化如图中
曲线甲所示。下列说法不正确的是
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线
乙所示
6.(2022·湖南·高考真题)甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应:新法合成的反应:
下列说法错误的是(阿伏加德罗常数的值为 )
A. 的电子式为
B.新法没有副产物产生,原子利用率高
C. 的 溶液中 的微粒数小于
D. 的作用是降低反应的活化能,使活化分子数目增多,百分数不变
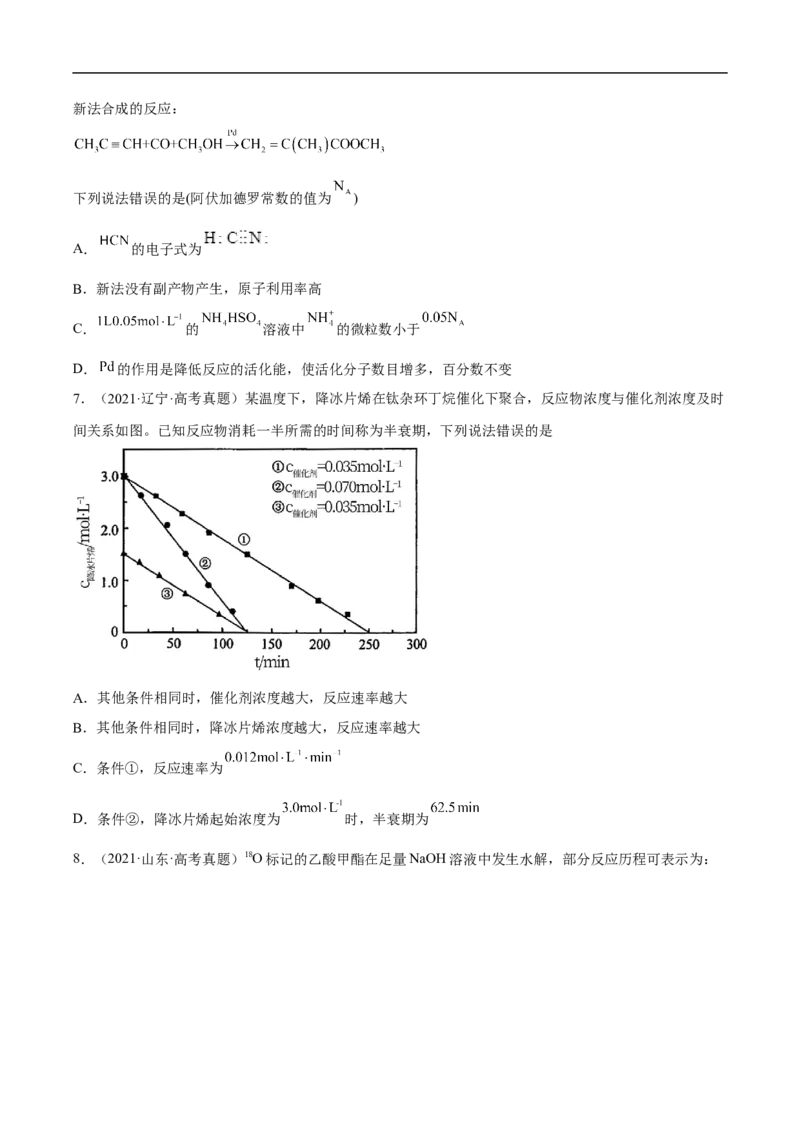
7.(2021·辽宁·高考真题)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度及时
间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为
D.条件②,降冰片烯起始浓度为 时,半衰期为
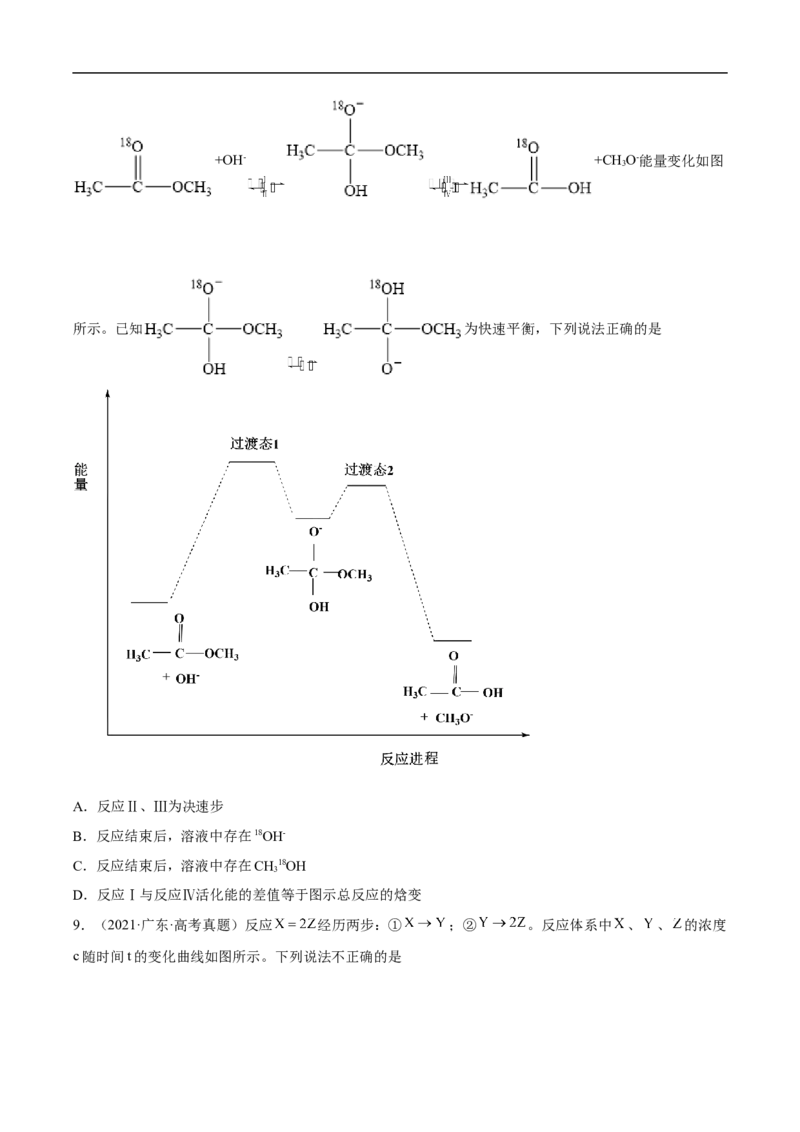
8.(2021·山东·高考真题)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:+OH- +CH O-能量变化如图
3
所示。已知 为快速平衡,下列说法正确的是
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
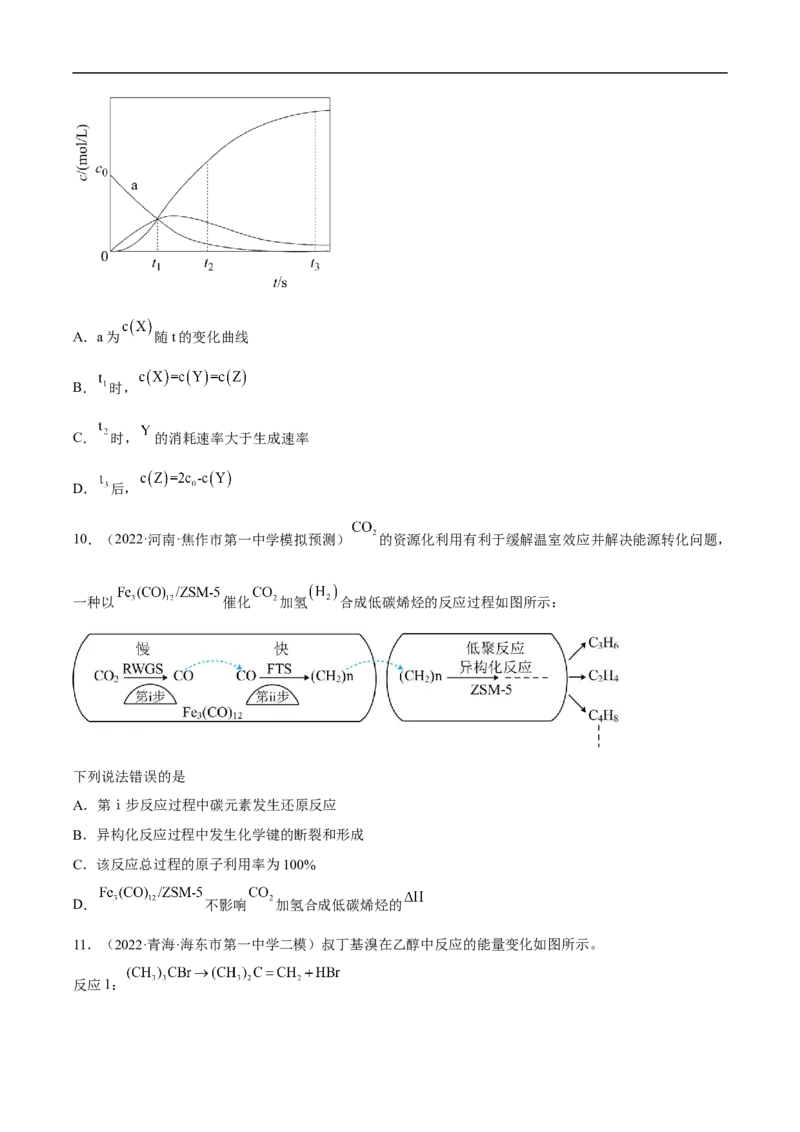
9.(2021·广东·高考真题)反应 经历两步:① ;② 。反应体系中 、 、 的浓度
c随时间t的变化曲线如图所示。下列说法不正确的是A.a为 随t的变化曲线
B. 时,
C. 时, 的消耗速率大于生成速率
D. 后,
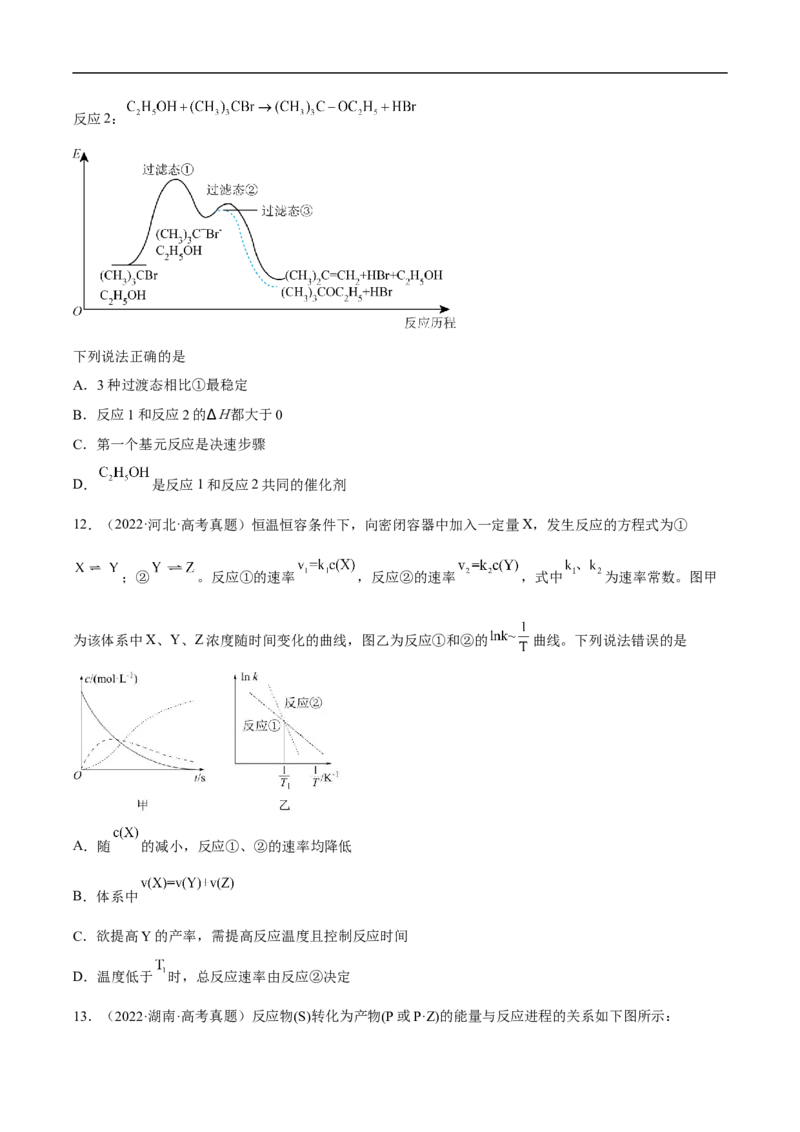
10.(2022·河南·焦作市第一中学模拟预测) 的资源化利用有利于缓解温室效应并解决能源转化问题,
一种以 催化 加氢 合成低碳烯烃的反应过程如图所示:
下列说法错误的是
A.第ⅰ步反应过程中碳元素发生还原反应
B.异构化反应过程中发生化学键的断裂和形成
C.该反应总过程的原子利用率为100%
D. 不影响 加氢合成低碳烯烃的
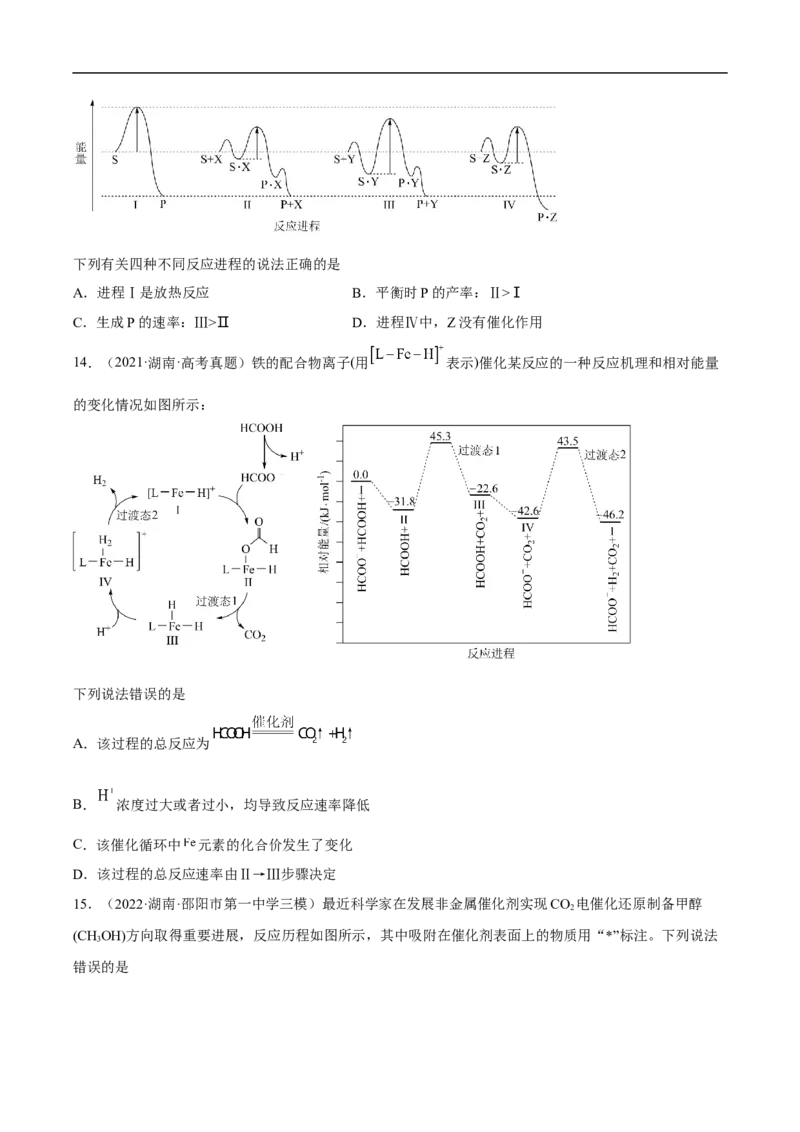
11.(2022·青海·海东市第一中学二模)叔丁基溴在乙醇中反应的能量变化如图所示。
反应1:反应2:
下列说法正确的是
A.3种过渡态相比①最稳定
B.反应1和反应2的∆H都大于0
C.第一个基元反应是决速步骤
D. 是反应1和反应2共同的催化剂
12.(2022·河北·高考真题)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为①
;② 。反应①的速率 ,反应②的速率 ,式中 为速率常数。图甲
为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是
A.随 的减小,反应①、②的速率均降低
B.体系中
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于 时,总反应速率由反应②决定
13.(2022·湖南·高考真题)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:下列有关四种不同反应进程的说法正确的是
A.进程Ⅰ是放热反应 B.平衡时P的产率:Ⅱ>Ⅰ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
14.(2021·湖南·高考真题)铁的配合物离子(用 表示)催化某反应的一种反应机理和相对能量
的变化情况如图所示:
下列说法错误的是
A.该过程的总反应为
B. 浓度过大或者过小,均导致反应速率降低
C.该催化循环中 元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
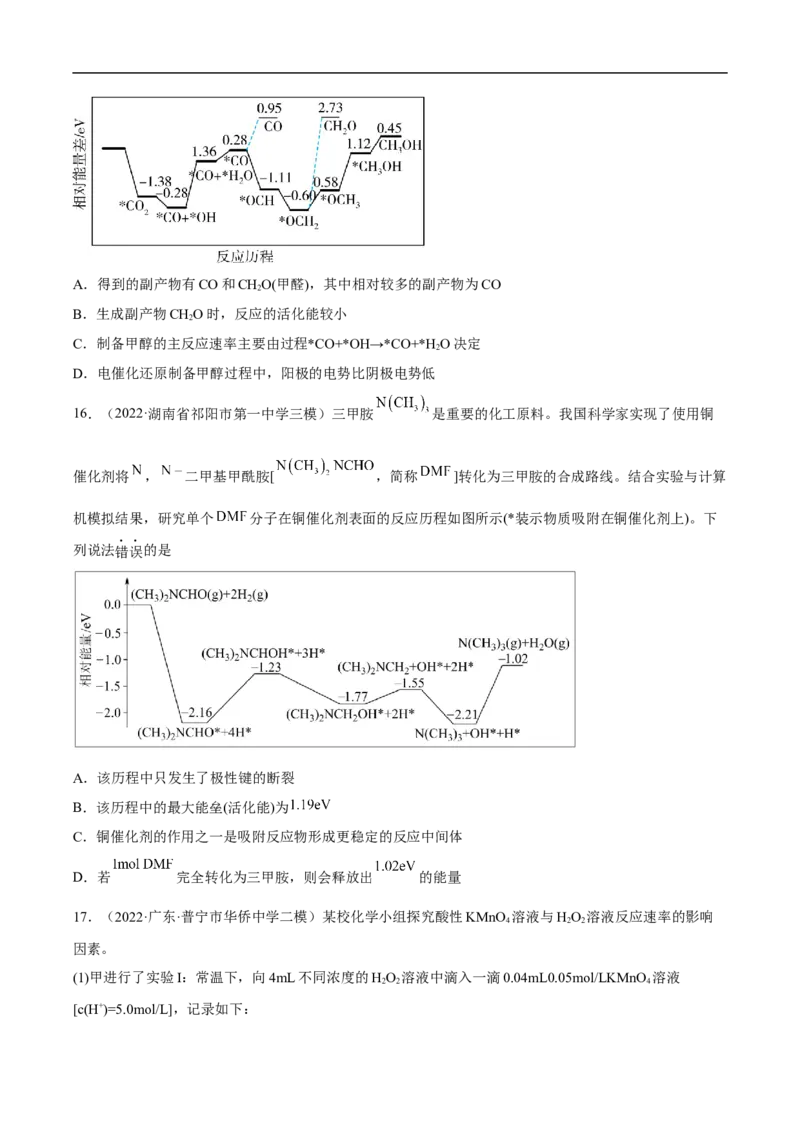
15.(2022·湖南·邵阳市第一中学三模)最近科学家在发展非金属催化剂实现CO 电催化还原制备甲醇
2
(CHOH)方向取得重要进展,反应历程如图所示,其中吸附在催化剂表面上的物质用“*”标注。下列说法
3
错误的是A.得到的副产物有CO和CHO(甲醛),其中相对较多的副产物为CO
2
B.生成副产物CHO时,反应的活化能较小
2
C.制备甲醇的主反应速率主要由过程*CO+*OH→*CO+*H O决定
2
D.电催化还原制备甲醇过程中,阳极的电势比阴极电势低
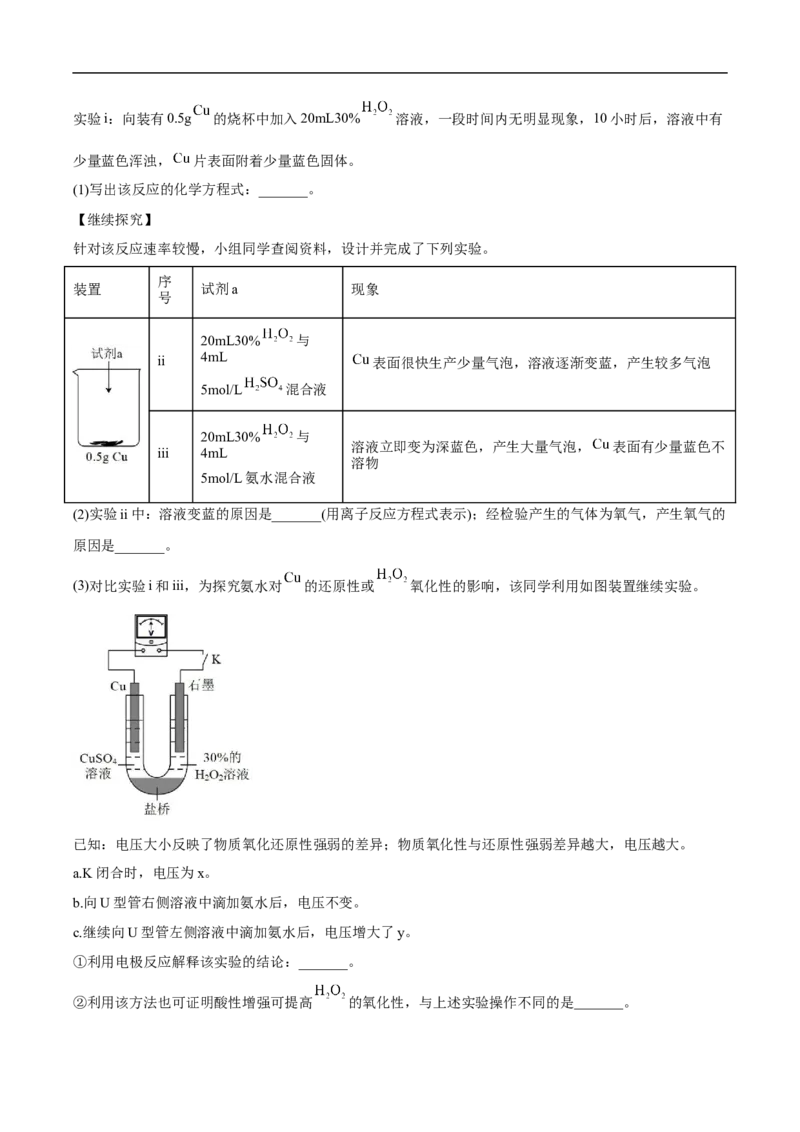
16.(2022·湖南省祁阳市第一中学三模)三甲胺 是重要的化工原料。我国科学家实现了使用铜
催化剂将 , 二甲基甲酰胺[ ,简称 ]转化为三甲胺的合成路线。结合实验与计算
机模拟结果,研究单个 分子在铜催化剂表面的反应历程如图所示(*装示物质吸附在铜催化剂上)。下
列说法错误的是
A.该历程中只发生了极性键的断裂
B.该历程中的最大能垒(活化能)为
C.铜催化剂的作用之一是吸附反应物形成更稳定的反应中间体
D.若 完全转化为三甲胺,则会释放出 的能量
17.(2022·广东·普宁市华侨中学二模)某校化学小组探究酸性KMnO 溶液与HO 溶液反应速率的影响
4 2 2
因素。
(1)甲进行了实验I:常温下,向4mL不同浓度的HO 溶液中滴入一滴0.04mL0.05mol/LKMnO 溶液
2 2 4
[c(H+)=5.0mol/L],记录如下:c(HO)/mol/L 0.0010 0.0015 0.0125 0.0312 0.044 0.0620
2 2
完全褪色时间/s 25 15 12 23 60 370
无色气泡 一样多
①请写出反应的离子方程式_______。
②对于c(HO)增大引起的速率异常现象,根据上述实验结果,甲排除了一种可能,请用化学方程式表示这
2 2
种可能性_______。
③为了解释c(HO)增大到一定浓度后速率减小,乙查得了如下资料:
2 2
资料显示:c(HO)>0.02mol,HO 溶液中存在平衡:2HO HO
2 2 2 2 2 2 4 4
请用平衡移动原理解释c(H
2
O
2
)=0.0312mol/L速率忽然减小的⇌原因_______。
(2)乙继续进行实验II,并记录如下:
操作 现象
第1-9滴溶液滴下,完全褪色所
需时间很长;
实验 往2mL0.2mol/LH O 溶液中逐滴滴加0.05mol/
2 2
II LKMnO [c(H+)=5.0mol/L]溶液 第10滴溶液滴下迅速褪色。
4
整个过程中几乎无温度变化。
①对于第10滴溶液与HO 溶液反应速率剧烈变化的原因,乙提出如下假设:_______。
2 2
②乙设计实验方案证实了上述假设合理,请补全他的方案:
操作 现象
往2mL0.2mol/LH O 溶液中滴入5滴0.05mol/LKMnO[c(H+)=5.0mol/L]溶 完全褪色时间为t
实验III 2 2 4
液 秒
_______
实验
往2mL0.2mol/LH O 溶液中_______
IV 2 2
(3)综合上述实验,对于酸性KMnO 溶液与HO 溶液反应速率,丙进行了总结。下列因素一定能加快反应
4 2 2
速率的是_______。
a.增大KMnO 溶液浓度 b.增大HO 溶液浓度 c.增大HSO 浓度
4 2 2 2 4
d.加热适当温度 e.加入合适的催化剂
18.(2022·北京·和平街第一中学三模)某小组探究 和 的反应的氧化还原反应,从电极反应角度
分析物质氧化性和还原性的变化规律。
【实验探究】实验i:向装有0.5g 的烧杯中加入20mL30% 溶液,一段时间内无明显现象,10小时后,溶液中有
少量蓝色浑浊, 片表面附着少量蓝色固体。
(1)写出该反应的化学方程式:_______。
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
序
装置 试剂a 现象
号
20mL30% 与
ii 4mL 表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡
5mol/L 混合液
20mL30% 与
溶液立即变为深蓝色,产生大量气泡, 表面有少量蓝色不
iii 4mL
溶物
5mol/L氨水混合液
(2)实验ii中:溶液变蓝的原因是_______(用离子反应方程式表示);经检验产生的气体为氧气,产生氧气的
原因是_______。
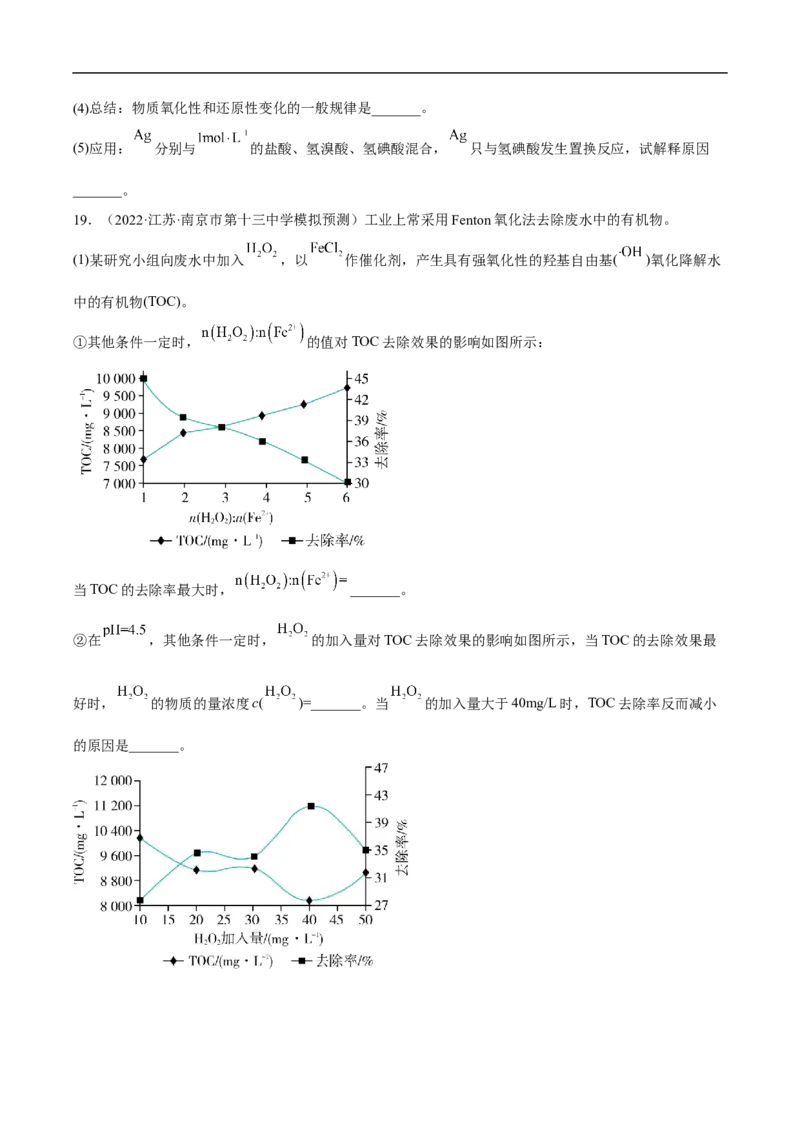
(3)对比实验i和iii,为探究氨水对 的还原性或 氧化性的影响,该同学利用如图装置继续实验。
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①利用电极反应解释该实验的结论:_______。
②利用该方法也可证明酸性增强可提高 的氧化性,与上述实验操作不同的是_______。(4)总结:物质氧化性和还原性变化的一般规律是_______。
(5)应用: 分别与 的盐酸、氢溴酸、氢碘酸混合, 只与氢碘酸发生置换反应,试解释原因
_______。
19.(2022·江苏·南京市第十三中学模拟预测)工业上常采用Fenton氧化法去除废水中的有机物。
(1)某研究小组向废水中加入 ,以 作催化剂,产生具有强氧化性的羟基自由基( )氧化降解水
中的有机物(TOC)。
①其他条件一定时, 的值对TOC去除效果的影响如图所示:
当TOC的去除率最大时, _______。
②在 ,其他条件一定时, 的加入量对TOC去除效果的影响如图所示,当TOC的去除效果最
好时, 的物质的量浓度c( )=_______。当 的加入量大于40mg/L时,TOC去除率反而减小
的原因是_______。(2)我国学者制备了一种介孔二氧化锰负载的 催化剂,并将其应用到苯并三唑( ,
BZA)的降解中,催化机理如下图:
①BZA可以与 或 结合的原因是_______。
②直接降解BZA的活性氧物种的化学式为_______。
③该过程中 分解的途径可用语言描述为_______。
20.(2022·辽宁·高考真题)工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得
诺贝尔奖,其反应为: 。回答下列问题:
(1)合成氨反应在常温下_______(填“能”或“不能”)自发。
(2)_______温(填“高”或“低”,下同)有利于提高反应速率,_______温有利于提高平衡转化率,综合考
虑催化剂(铁触媒)活性等因素,工业常采用 。
针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
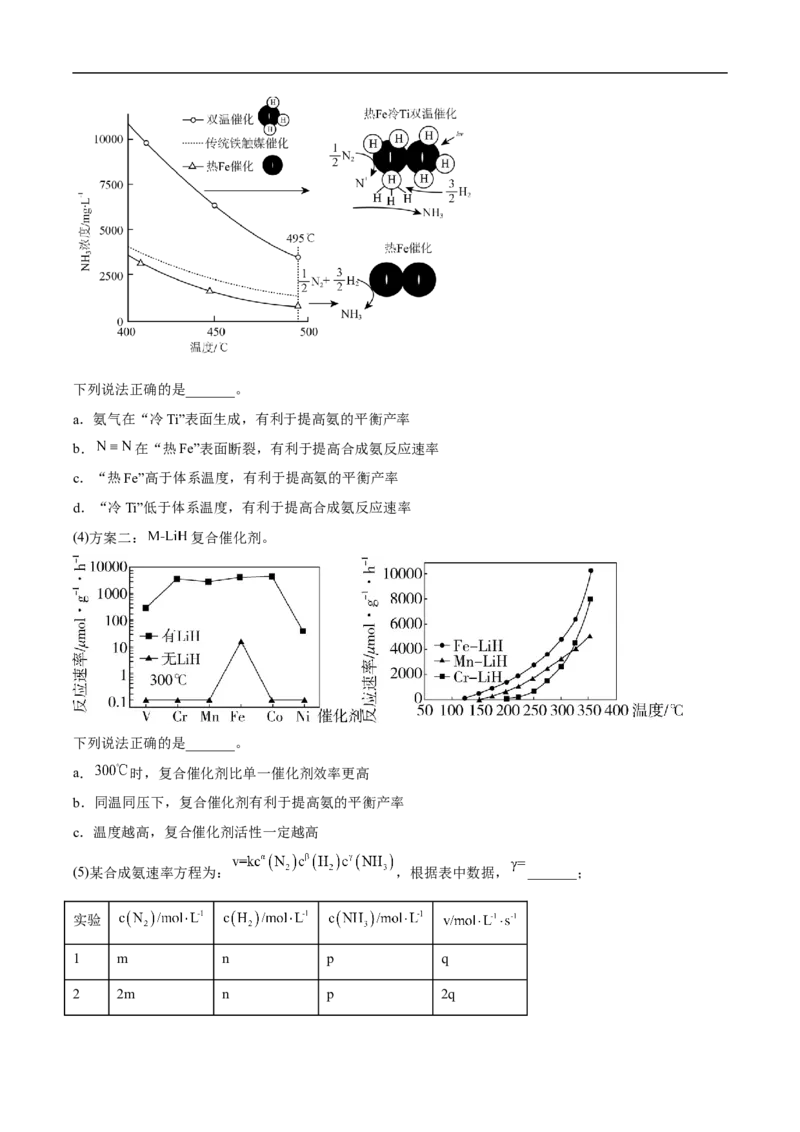
(3)方案一:双温-双控-双催化剂。使用 双催化剂,通过光辐射产生温差(如体系温度为 时,
的温度为 ,而 的温度为 )。下列说法正确的是_______。
a.氨气在“冷Ti”表面生成,有利于提高氨的平衡产率
b. 在“热Fe”表面断裂,有利于提高合成氨反应速率
c.“热Fe”高于体系温度,有利于提高氨的平衡产率
d.“冷Ti”低于体系温度,有利于提高合成氨反应速率
(4)方案二: 复合催化剂。
下列说法正确的是_______。
a. 时,复合催化剂比单一催化剂效率更高
b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高
(5)某合成氨速率方程为: ,根据表中数据, _______;
实验
1 m n p q
2 2m n p 2q3 m n 0.1p 10q
4 m 2n p 2.828q
在合成氨过程中,需要不断分离出氨的原因为_______。
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
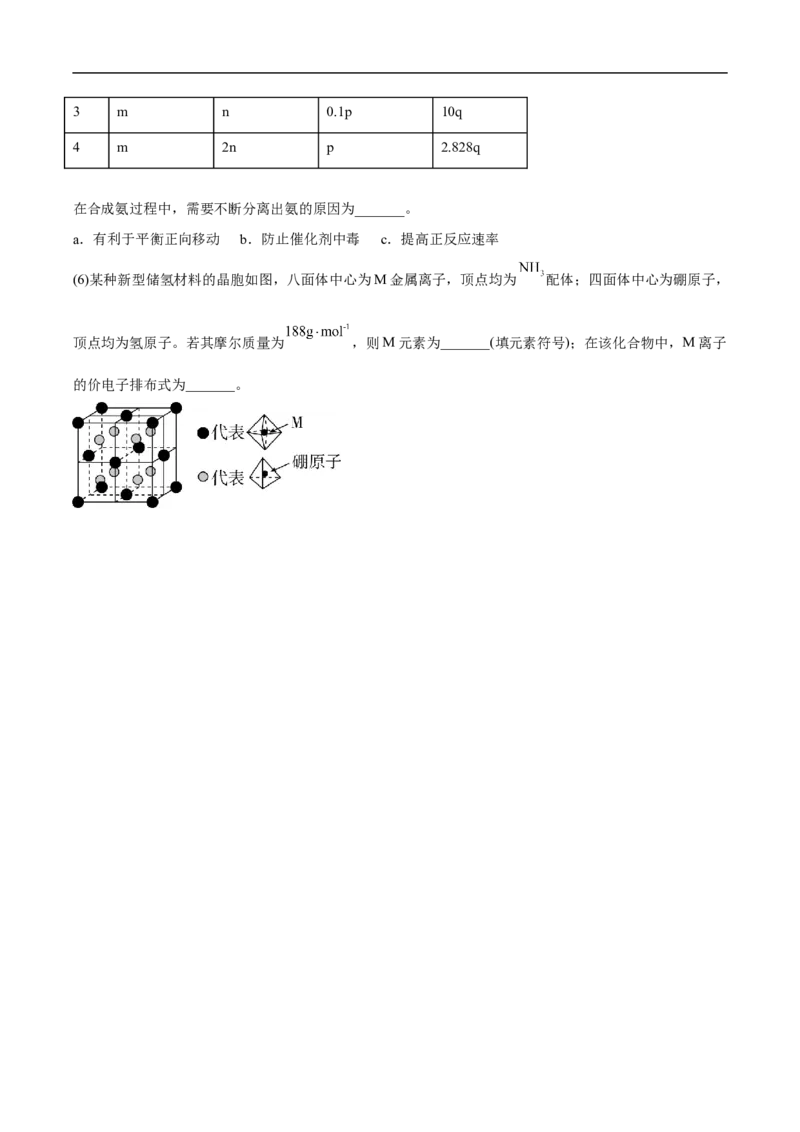
(6)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为 配体;四面体中心为硼原子,
顶点均为氢原子。若其摩尔质量为 ,则M元素为_______(填元素符号);在该化合物中,M离子
的价电子排布式为_______。