文档内容
易错点 23 弱电解质的电离平衡
易错题【01】弱电解质的判断
(1)弱电解质不能完全电离:一定浓度的HA溶液的pH不同;与同浓度盐酸比较导电性
不同;与同浓度的盐酸比较和锌反应的速率不同;
(2)溶液中存在电离平衡:弱酸HA溶液稀释前后pH的变化不同于强酸;同离子效应会
改变溶液的pH;改变温度,HA溶液的pH变化,等体积、等pH的HA溶液与盐酸分别与
过量的锌反应生成H 的量不同;
2
(3)盐类能水解:配制某浓度的醋酸钠溶液,向其中加入几滴酚酞溶液,溶液变为浅红色;
用玻璃棒蘸取一定浓度的醋酸钠溶液滴在pH试纸上,溶液pH >7。
易错题【02】电离平衡的判断
(1)应该深刻地理解勒夏特列原理——平衡向“减弱”这种改变的方向移动,移动的结果
不能“抵消”或“超越”这种改变从定量角度分析电离平衡。
(2)当改变影响电离平衡的条件后,分析两种微粒浓度之比的变化时,若通过平衡移动的方
向不能作出判断,可采用化学平衡常数进行定量分析。
易错题【03】电离常数的四大应用
①判断弱酸(或弱碱)的相对强弱,电离常数越大,酸性(或碱性)越强。
②判断盐溶液的酸性(或碱性)强弱
电离常数越大,对应盐的水解程度越小,盐溶液的碱性(或酸性)越弱。
③判断反应能否发生或者判断产物是否正确
通过强酸制弱酸来判断。如HCO :K =4.2×10-7,K =5.6×10-11,苯酚(C HOH):K=
2 3 a1 a2 6 5 a
1.3×10-10,向苯酚钠(C HONa)溶液中通入的CO 不论是少量还是过量,其化学方程式均为
6 5 2
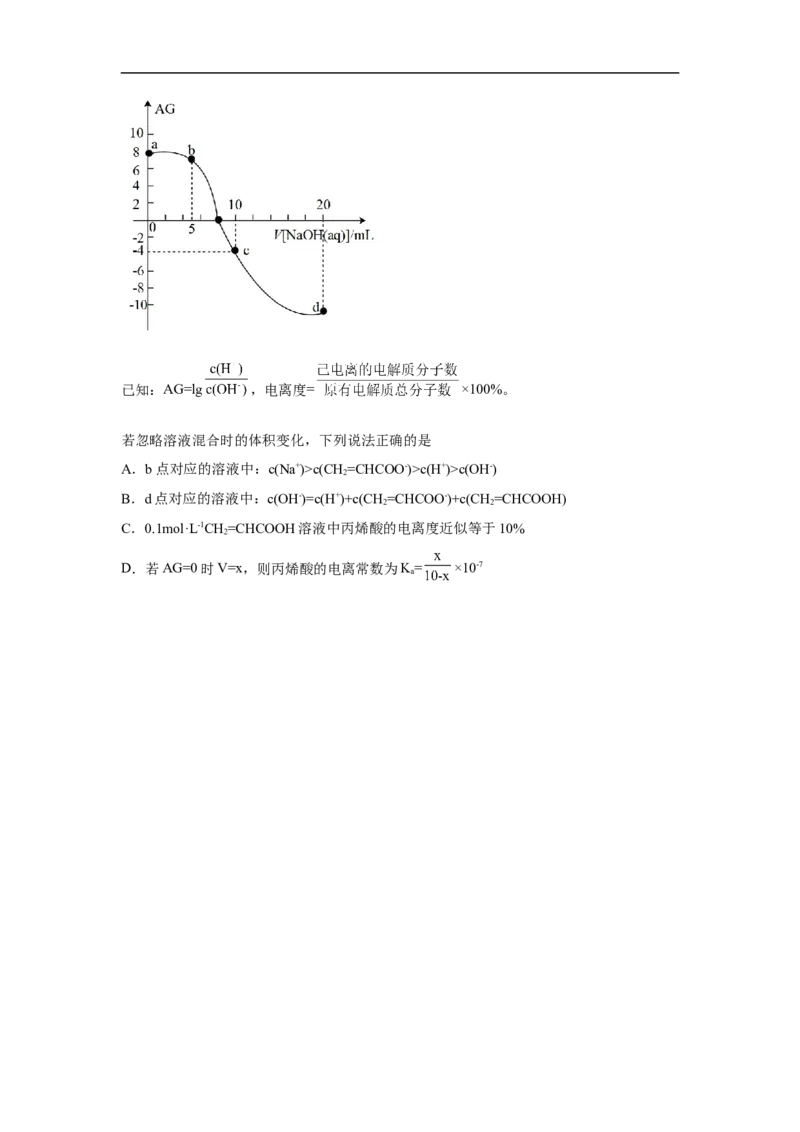
C HONa+CO+HO===C HOH+NaHCO 。
6 5 2 2 6 5 3
④判断溶液微粒浓度比值的变化
利用温度不变,电离常数不变来判断。
如把0.1 mol·L-1CHCOOH溶液加水稀释, ,
3
稀释时,c(H+)减小,K 不变,则 变。
a
易错题【04】酸性强弱的比的方法七种判断方法(1)根据化学方程式判断:较强酸制较弱酸是复分解反应发生的条件之一,它体现了酸性
的相对强弱.如CaCO +2CHCOOH=(CH COO) Ca + CO ↑+ HO,说明酸性:
3 3 3 2 2 2
CHCOOH > HCO。
3 2 3
(2)根据pH大小判断:相同浓度的酸电离出H+的程度不同,酸越弱c(H+)越小,pH越
大;与强碱生成的盐溶液的水解程度越大,碱性越强。
(3)根据pH变化判断:同pH的酸分别加水稀释相同的倍数,溶液的pH变化大的为较强
酸;同pH的酸的稀溶液分别加入少量该酸相应的无水钠盐或钾盐(正盐),pH 变化大的为
较弱酸。
(4)根据反应物消耗量判断:pH相同、体积相同的一元酸与碱中和,消耗碱最多的为较
弱酸;物质的最浓度相同、体积相同的一元酸与碱中和,消耗碱的量相同时,弱酸盐溶液
的 pH大于强酸盐溶液;若反应后溶液呈中性(pH=7),则强酸消耗碱的量大于弱酸。
(5)根据生成H 的速率判断:在相同条件下,同浓度的酸与较活泼金属反应(如Al、Zn
2
等)剧烈程度小的为较弱酸。
(6)根据导电性强弱判断:同温度、同物质的量浓度酸溶液,较强酸溶液的导电性强于较
弱酸溶液。
(7)根据电离常数判断:相同温度下,电离常数越大酸越强
典例分析
例题1、下列事实一定能说明HNO 为弱电解质的是( )
2
A.用HNO 溶液做导电实验灯泡很暗
2
B.常温下0.1 mol·L-1的HNO 溶液加水稀释c(H+)减小
2
C.1 L c(H+)=0.1 mol·L-1的HNO 和1 L c(H+)=0.1 mol·L-1的盐酸与足量的NaOH溶
2
液完全反应,最终HNO 消耗的NaOH溶液多
2
D.0.1 mol·L-1的HNO 溶液能使紫色石蕊试液变红色
2
【解析】如果强酸(如盐酸)的浓度很小灯泡也很暗,A错误;不论是强酸还是弱酸,加水
稀释,溶液中c(H+)均减小,B错误;依据HNO+NaOH===NaNO +HO、HCl+
2 2 2
NaOH===NaCl+HO可知,因溶液中c(H+)相同,分别与足量的NaOH溶液完全反应,最
2
终HNO 消耗的NaOH多,所以HNO 没有全部电离,C正确;HNO 溶液能使紫色石蕊试
2 2 2
液变红色,只说明溶液呈酸性,不能说明HNO 为弱酸,D错误。
2
例题2、室温下: 、 。NaCO 和NaHCO 混
2 3 3
合溶液具有控制酸碱平衡、供给细胞生存代谢所必需的能量和无机盐成分等作用。室温下,
通过下列实验探究一定浓度的NaCO 和NaHCO 混合溶液的性质。
2 3 3实验 实验操作和现象
1 用pH计测得混合溶液的pH为10.25
2 向混合溶液中滴几滴酚酞,加水稀释,溶液红色变浅
3 向混合溶液中通入过量的CO,无明显现象
2
4 向实验3所得溶液中滴加少量Ba(OH) 溶液,产生白色沉淀
2
下列有关说法正确的是
A. 实验1溶液中存在:
B. 实验2中随蒸馏水的不断加入,溶液中 的值逐渐变小
C. 实验3所得溶液中存在
D. 实验4反应的离子方程式为:
A【解析】 ,实验 1 溶液的 pH 为 10.25,
, 则 , 根 据 电 荷 守 恒 ,
,A正确;向混合溶液中滴几滴酚酞,加水稀释,溶液红
色变浅,说明pH减小,氢离子浓度增大, 不变,所以溶
液中 的值逐渐增大,B错误;向混合溶液中通入过量的 CO ,溶质变为碳酸氢
2
钠,根据电荷守恒,溶液中 ,C错误;
实验3所得溶液中的溶质是碳酸氢钠,滴加少量Ba(OH) 溶液生成碳酸钡沉淀、碳酸钠、
2水,反应的离子方程式为: ,D错误。
例题3、已知次磷酸(H PO )为一元酸,欲证明它是弱电解质,下列操作方法不正确的是(
3 2
)
A.用物质的量浓度相同的NaCl溶液和NaH PO 溶液进行导电性实验,比较灯泡的亮度
2 2
B.用一定浓度的NaOH溶液分别滴定等体积、等pH的盐酸和次磷酸溶液,比较消耗碱液
的体积
C.加热滴有酚酞试液的NaH PO 溶液,溶液颜色变深
2 2
D.常温下,稀释0.1 mol·L-1次磷酸溶液至原溶液体积的100倍,测得pH在4~5之间
【解析】NaCl和NaH PO 都属于强电解质,所以用物质的量浓度相同的NaCl溶液和
2 2
NaH PO 溶液进行导电性实验,比较灯泡的亮度,不能证明HPO 是弱电解质,故A错误;
2 2 3 2
因盐酸为强酸,若滴定时次磷酸溶液消耗NaOH溶液的体积大于等体积、等pH的盐酸消
耗的NaOH溶液的体积,则说明次磷酸为弱电解质,B正确;若次磷酸为弱电解质,则
NaH PO 溶液呈碱性,加热促进其水解,滴有酚酞试液的NaH PO 溶液颜色变深,C正确;
2 2 2 2
常温下,若次磷酸为一元强酸,则把0.1 mol·L-1次磷酸溶液稀释至原溶液体积的100倍,
pH应为3,而现测得pH在4~5之间,说明次磷酸没有完全电离,为弱电解质,D正确。
1.(2022·北京·高考真题)2022年3月神舟十三号航天员在中国空间站进行了“天宫课
堂”授课活动。其中太空“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象。下列说法不
正确的是
A.醋酸钠是强电解质
B.醋酸钠晶体与冰都是离子晶体
C.常温下,醋酸钠溶液的
D.该溶液中加入少量醋酸钠固体可以促进醋酸钠晶体析出
2.(2022·吉林四平·模拟预测)饱和二氧化硫水溶液中存在下列平衡体系:SO +H O
2 2
H++ , H++ ,若向此溶液中
A.加水, 浓度增大
B.通入少量Cl 气体,溶液pH增大
2
C.加少量CaSO 粉末, 浓度基本不变
3D.通入少量HCl气体,溶液中 浓度减小
3.(2022·湖北·高考真题)根据酸碱质子理论,给出质子 的物质是酸,给出质子的能
力越强,酸性越强。已知: , ,
下列酸性强弱顺序正确的是
A. B.
C. D.
4.(2022·浙江·高考真题) 时,苯酚 的 ,下列说法正确的是
A.相同温度下,等 的 和 溶液中,
B.将浓度均为 的 和 溶液加热,两种溶液的 均变大
C. 时, 溶液与 溶液混合,测得 ,则此时溶液中
D. 时, 的 溶液中加少量 固体,水的电离程度变小
5.(2022·浙江·高考真题)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说
2 a1 a2
法正确的是
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电
2 2
离度为0.013%
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
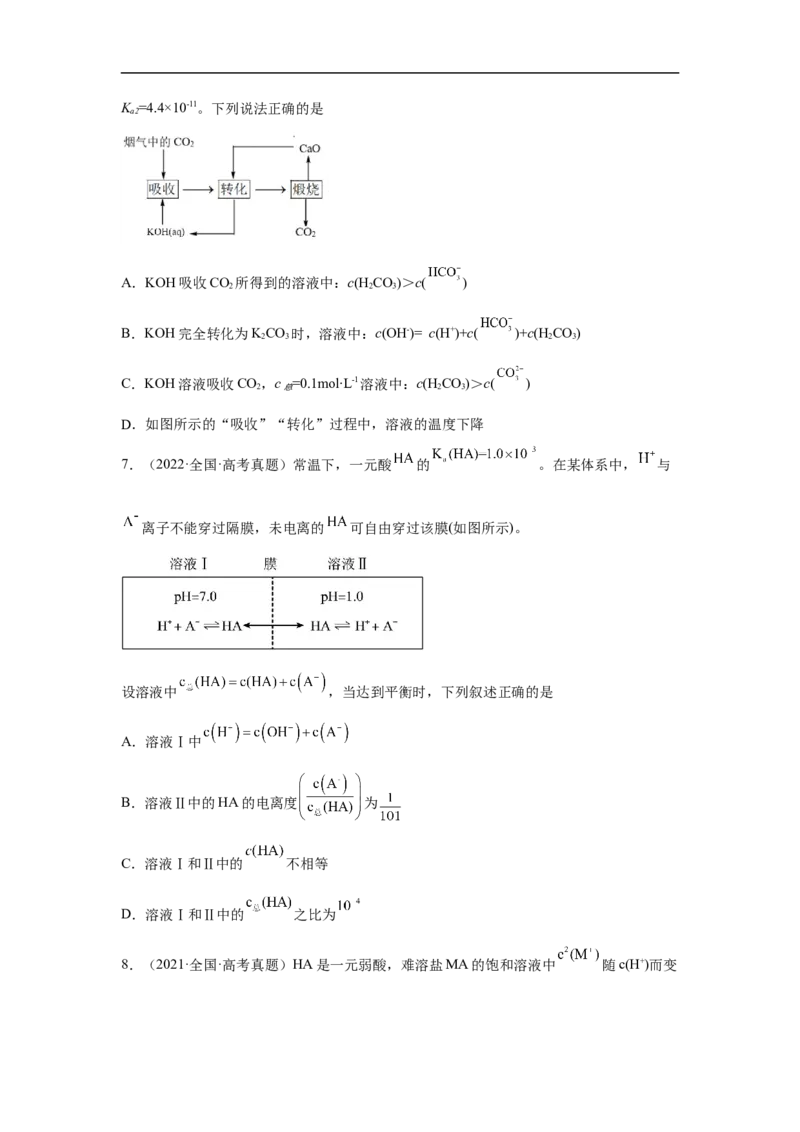
6.(2022·江苏·高考真题)一种捕集烟气中CO 的过程如图所示。室温下以
2
0.1mol∙L-1KOH溶液吸收CO,若通入CO 所引起的溶液体积变化和HO挥发可忽略,溶液
2 2 2
中含碳物种的浓度c =c(H CO)+c( )+c( )。HCO 电离常数分别为K =4.4×10-7、
总 2 3 2 3 a1K =4.4×10-11。下列说法正确的是
a2
A.KOH吸收CO 所得到的溶液中:c(H CO)>c( )
2 2 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c( )+c(H CO)
2 3 2 3
C.KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c( )
2 总 2 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
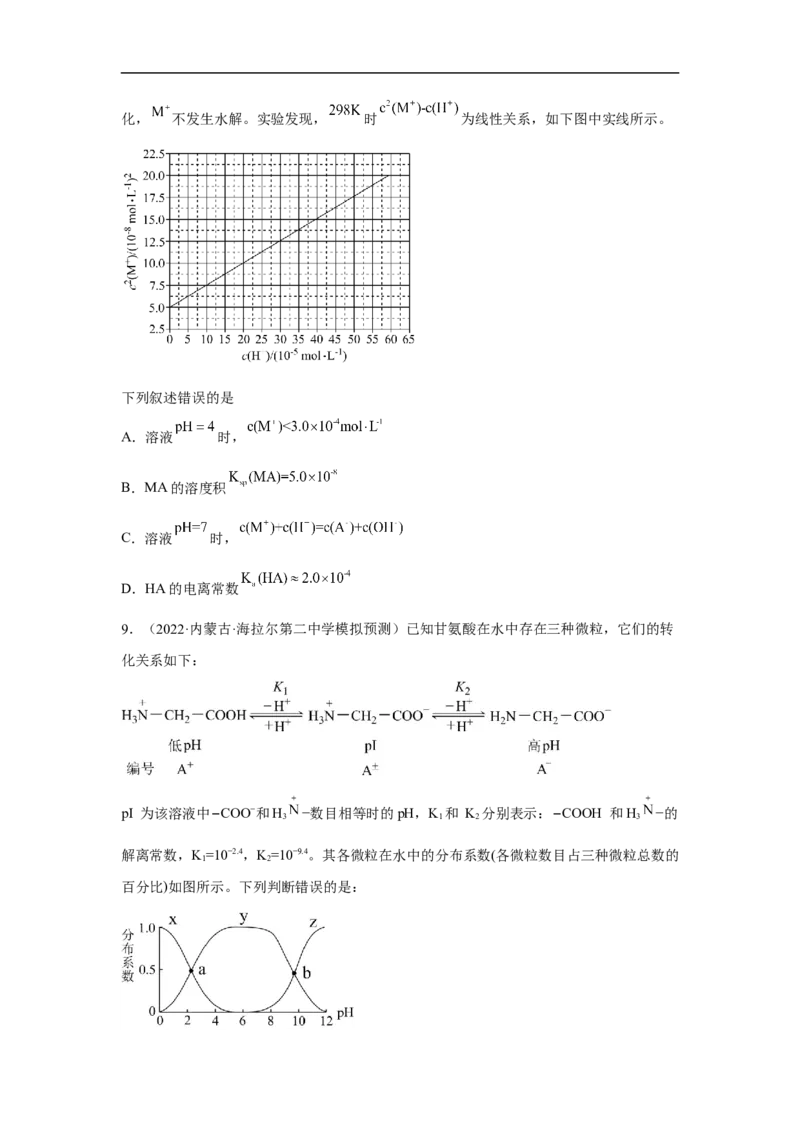
7.(2022·全国·高考真题)常温下,一元酸 的 。在某体系中, 与
离子不能穿过隔膜,未电离的 可自由穿过该膜(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
A.溶液Ⅰ中
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的 不相等
D.溶液Ⅰ和Ⅱ中的 之比为
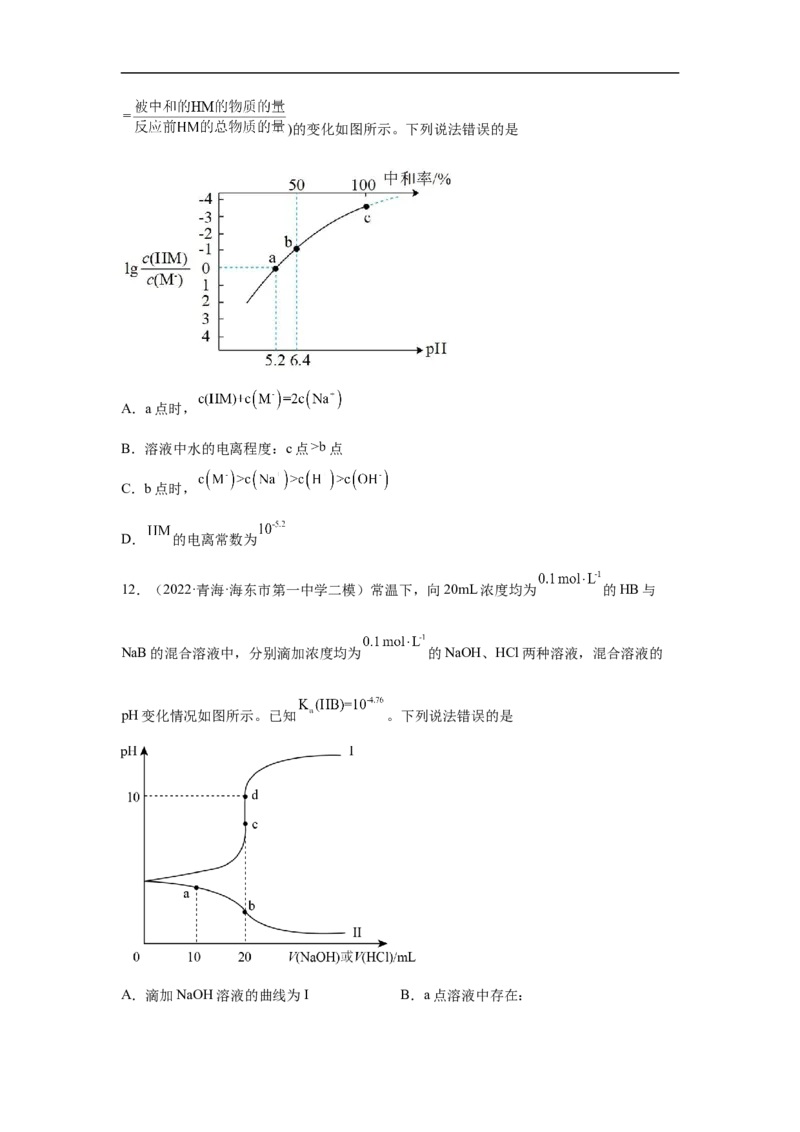
8.(2021·全国·高考真题)HA是一元弱酸,难溶盐MA的饱和溶液中 随c(H+)而变化, 不发生水解。实验发现, 时 为线性关系,如下图中实线所示。
下列叙述错误的是
A.溶液 时,
B.MA的溶度积
C.溶液 时,
D.HA的电离常数
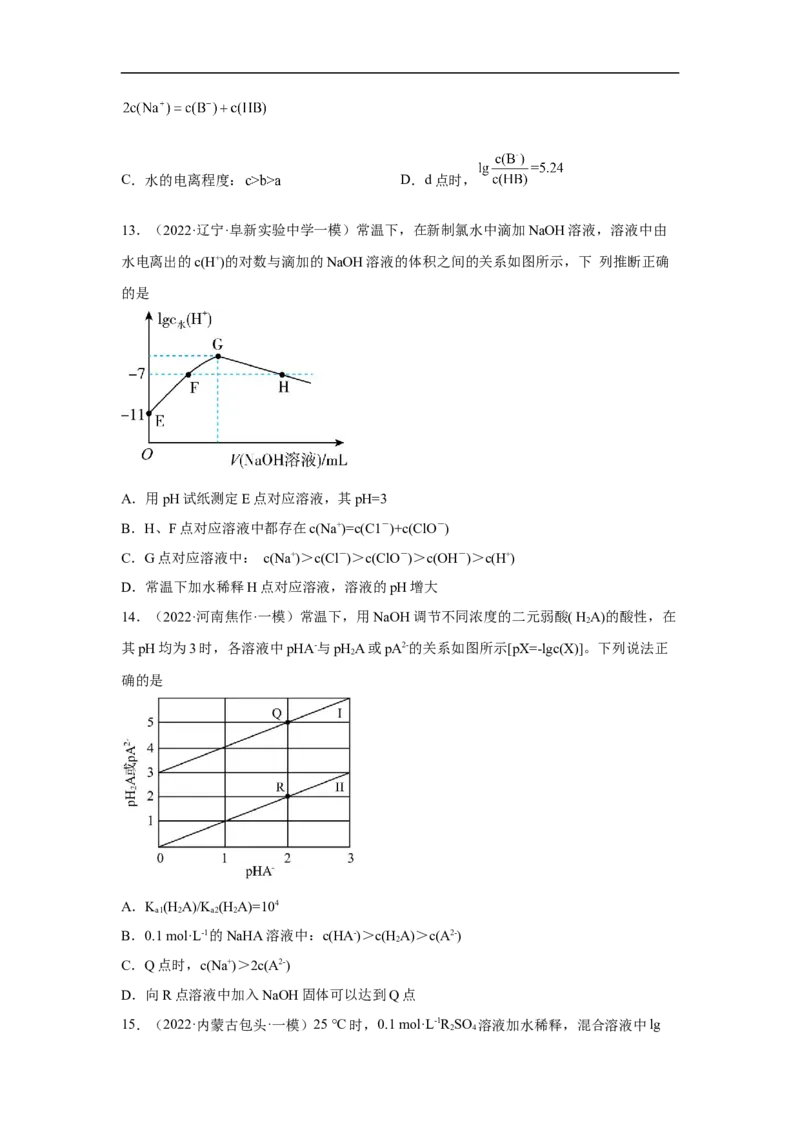
9.(2022·内蒙古·海拉尔第二中学模拟预测)已知甘氨酸在水中存在三种微粒,它们的转
化关系如下:
pI 为该溶液中−COO−和H −数目相等时的pH,K 和 K 分别表示:−COOH 和H −的
3 1 2 3
解离常数,K=10−2.4,K=10−9.4。其各微粒在水中的分布系数(各微粒数目占三种微粒总数的
1 2
百分比)如图所示。下列判断错误的是:A.a点对应的 pH=2.4
B.pH=4 时,c(A±)>c(A-)>c(A+)
C.甘氨酸溶液的 pI=6
D.甘氨酸溶于水后溶液显酸性
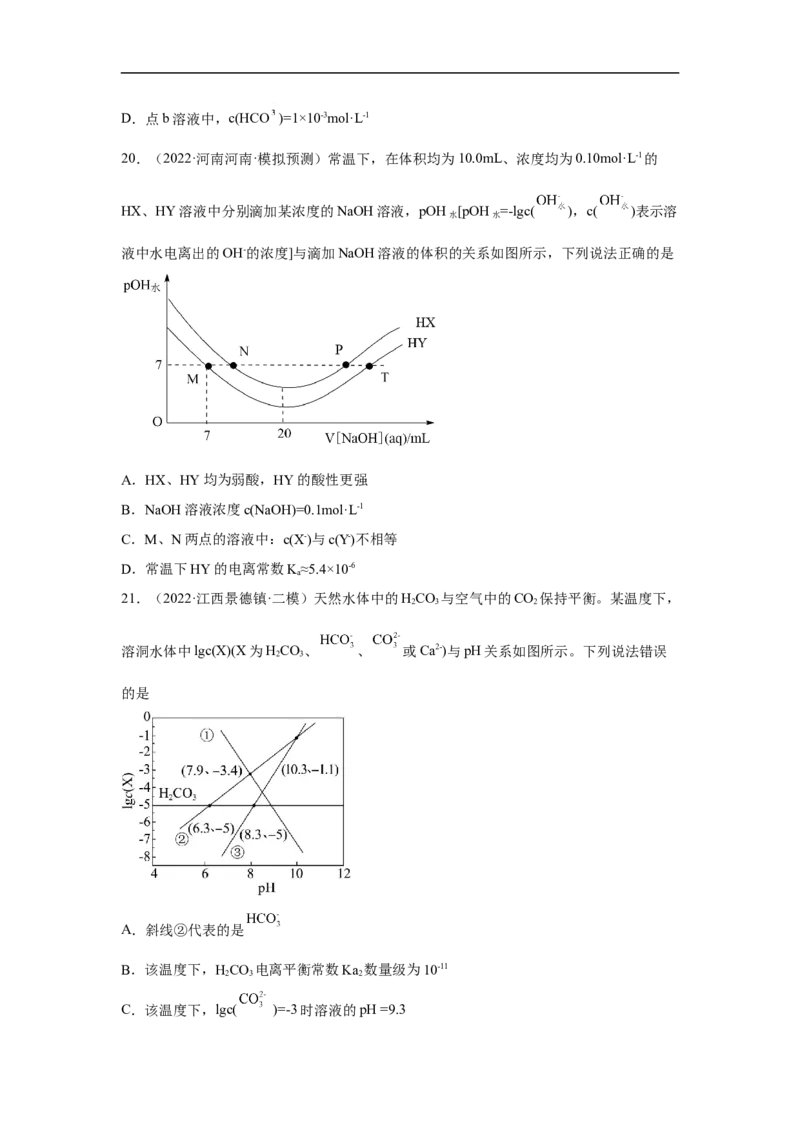
10.(2022·河南·模拟预测)25℃时,用0.1000 的 溶液分别滴定体积均为
50.00 、浓度均为0.0500 的 、 (邻苯二甲酸氢钾)及 溶液,其滴定
曲线如图所示:
下列说法正确的是
A.
B.V( 溶液) 时,②中
C.V( 溶液)均为0时,阴离子总数① ② ③
D.分别滴定至 时,
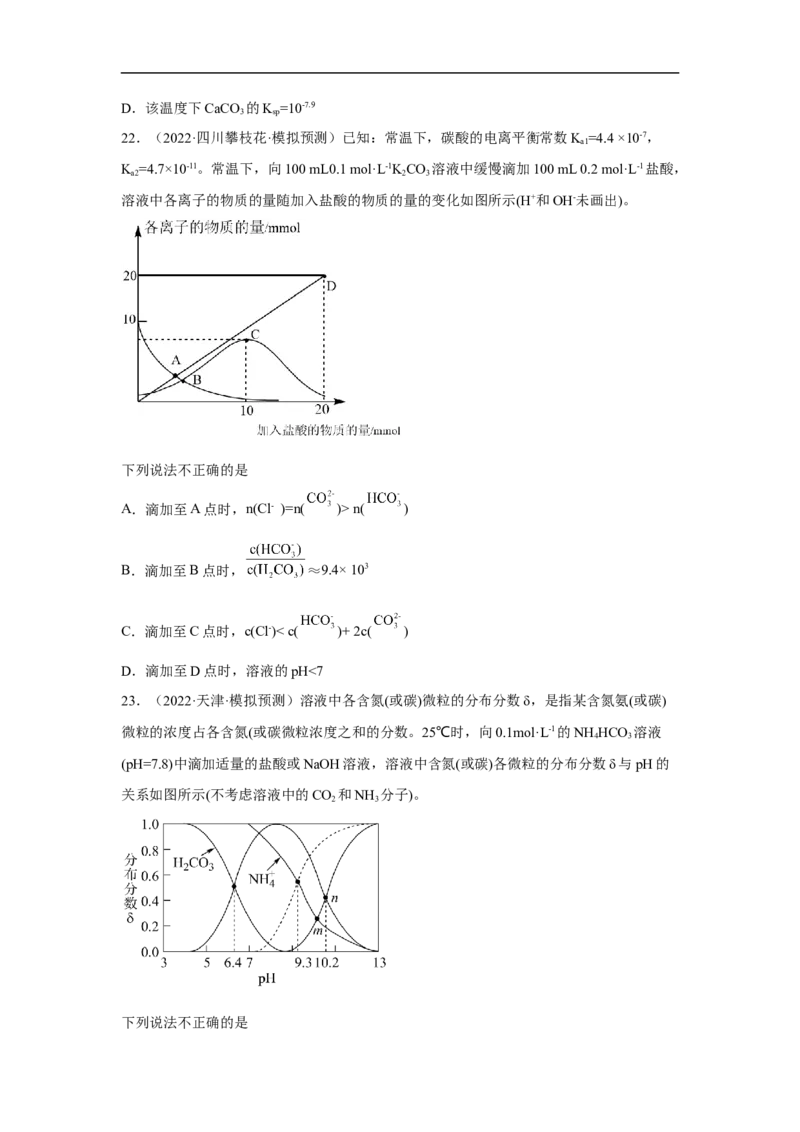
11.(2022·辽宁鞍山·一模) 是一种一元弱酸,常温下,向 溶液中
逐滴加入浓度为 的 溶液,溶液中 、 、中和率(中和率)的变化如图所示。下列说法错误的是
A.a点时,
B.溶液中水的电离程度:c点 点
C.b点时,
D. 的电离常数为
12.(2022·青海·海东市第一中学二模)常温下,向20mL浓度均为 的HB与
NaB的混合溶液中,分别滴加浓度均为 的NaOH、HCl两种溶液,混合溶液的
pH变化情况如图所示。已知 。下列说法错误的是
A.滴加NaOH溶液的曲线为I B.a点溶液中存在:C.水的电离程度: D.d点时,
13.(2022·辽宁·阜新实验中学一模)常温下,在新制氯水中滴加NaOH溶液,溶液中由
水电离出的c(H+)的对数与滴加的NaOH溶液的体积之间的关系如图所示,下 列推断正确
的是
A.用pH试纸测定E点对应溶液,其pH=3
B.H、F点对应溶液中都存在c(Na+)=c(C1-)+c(ClO-)
C.G点对应溶液中: c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+)
D.常温下加水稀释H点对应溶液,溶液的pH增大
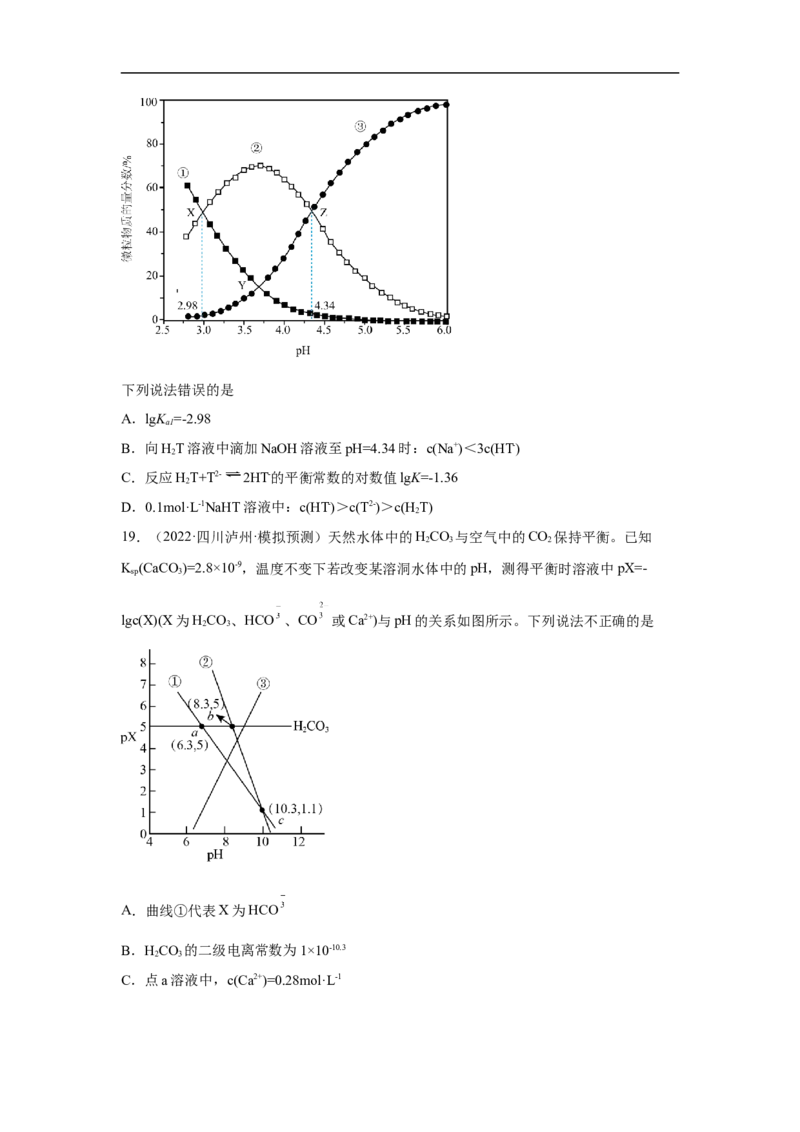
14.(2022·河南焦作·一模)常温下,用NaOH调节不同浓度的二元弱酸( H A)的酸性,在
2
其pH均为3时,各溶液中pHA-与pHA或pA2-的关系如图所示[pX=-lgc(X)]。下列说法正
2
确的是
A.K (H A)/K (H A)=104
a1 2 a2 2
B.0.1 mol·L-1的NaHA溶液中:c(HA-)>c(HA)>c(A2-)
2
C.Q点时,c(Na+)>2c(A2-)
D.向R点溶液中加入NaOH固体可以达到Q点
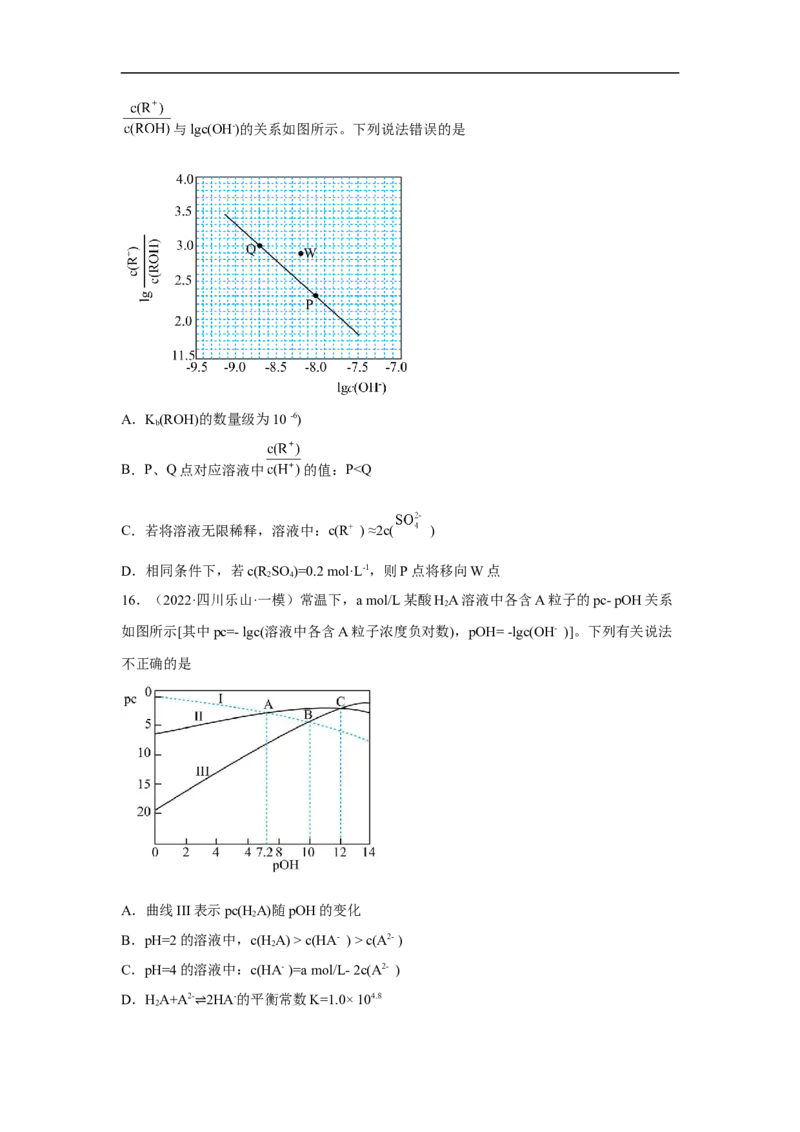
15.(2022·内蒙古包头·一模)25 °C时,0.1 mol·L-1R SO 溶液加水稀释,混合溶液中lg
2 4与lgc(OH-)的关系如图所示。下列说法错误的是
A.K(ROH)的数量级为10 -6)
b
B.P、Q点对应溶液中 的值:P
c(HA- ) > c(A2- ) 2 C.pH=4的溶液中:c(HA- )=a mol/L- 2c(A2- ) D.HA+A2- 2HA-的平衡常数K=1.0× 104.8 2 ⇌17.(2022·河南河南·二模)工业上可用氨水处理硫酸厂尾气中的SO 常温下,向一定浓 2. 度的氨水中通入SO 气体,溶液中lgx[x= 或 与溶液pH的关系如图所示。 2 下列说法错误的是 A.曲线II代表lg B.当溶液的pH由7.2降到1.9的过程中,溶液中 浓度呈增大趋势 C.当溶液中的c( ) =c(HSO )时,溶液的pH约为4 2 3 D.(NH )SO 溶液中存在离子浓度关系:c(NH ·H O) +c(OH-)>c(H+) +c( ) +c( H SO ) 4 2 3 3 2 2 3 18.(2022·河南·模拟预测)常温下,酒石酸(记作HT)中各含T微粒占所有含T微粒的物 2 质的量分数随pH的变化曲线如下图所示:下列说法错误的是 A.lgK =-2.98 a1 B.向HT溶液中滴加NaOH溶液至pH=4.34时:c(Na+)<3c(HT-) 2 C.反应HT+T2- 2HT-的平衡常数的对数值lgK=-1.36 2 D.0.1mol·L-1NaHT溶液中:c(HT-)>c(T2-)>c(HT) 2 19.(2022·四川泸州·模拟预测)天然水体中的HCO 与空气中的CO 保持平衡。已知 2 3 2 K (CaCO)=2.8×10-9,温度不变下若改变某溶洞水体中的pH,测得平衡时溶液中pX=- sp 3 lgc(X)(X为HCO、HCO 、CO 或Ca2+)与pH的关系如图所示。下列说法不正确的是 2 3 A.曲线①代表X为HCO B.HCO 的二级电离常数为1×10-10.3 2 3 C.点a溶液中,c(Ca2+)=0.28mol·L-1D.点b溶液中,c(HCO )=1×10-3mol·L-1 20.(2022·河南河南·模拟预测)常温下,在体积均为10.0mL、浓度均为0.10mol·L-1的 HX、HY溶液中分别滴加某浓度的NaOH溶液,pOH [pOH =-lgc( ),c( )表示溶 水 水 液中水电离出的OH-的浓度]与滴加NaOH溶液的体积的关系如图所示,下列说法正确的是 A.HX、HY均为弱酸,HY的酸性更强 B.NaOH溶液浓度c(NaOH)=0.1mol·L-1 C.M、N两点的溶液中:c(X-)与c(Y-)不相等 D.常温下HY的电离常数K≈5.4×10-6 a 21.(2022·江西景德镇·二模)天然水体中的HCO 与空气中的CO 保持平衡。某温度下, 2 3 2 溶洞水体中lgc(X)(X为HCO、 、 或Ca2-)与pH关系如图所示。下列说法错误 2 3 的是 A.斜线②代表的是 B.该温度下,HCO 电离平衡常数Ka 数量级为10-11 2 3 2 C.该温度下,lgc( )=-3时溶液的pH =9.3D.该温度下CaCO 的K =10-7.9 3 sp 22.(2022·四川攀枝花·模拟预测)已知:常温下,碳酸的电离平衡常数K =4.4 ×10-7, a1 K =4.7×10-11。常温下,向100 mL0.1 mol·L-1KCO 溶液中缓慢滴加100 mL 0.2 mol·L-1盐酸, a2 2 3 溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(H+和OH-未画出)。 下列说法不正确的是 A.滴加至A点时,n(Cl- )=n( )> n( ) B.滴加至B点时, ≈9.4× 103 C.滴加至C点时,c(Cl-)< c( )+ 2c( ) D.滴加至D点时,溶液的pH<7 23.(2022·天津·模拟预测)溶液中各含氮(或碳)微粒的分布分数δ,是指某含氮氨(或碳) 微粒的浓度占各含氮(或碳微粒浓度之和的分数。25℃时,向0.1mol·L-1的NH HCO 溶液 4 3 (pH=7.8)中滴加适量的盐酸或NaOH溶液,溶液中含氮(或碳)各微粒的分布分数δ与pH的 关系如图所示(不考虑溶液中的CO 和NH 分子)。 2 3 下列说法不正确的是A.K(NH ·H O)>K (H CO) b 3 2 al 2 3 B.n点时,溶液3c(HCO )+c(OH-)=c(NH )+c(H+) C.m点时,c(NH ·H O)>c(HCO ) 3 2 D.反应HCO +NH·H O NH +CO +H O的平衡常数为K,lgK=-0.9 3 2 2 24.(2022·湖南·模拟预测)草酸是一种二元弱酸,K =5.9 ×10-2,K =6.4 ×10-5,室温下, a1 a2 用0.1 000 mol· L-1的NaOH标准溶液滴定25 mL0.1 mol·L-1的HC O(草酸)溶液的滴定曲线 2 2 4 如图a所示。图b为在上述滴定过程中草酸溶液中草酸各种形态的分布系数与pH的关系。 下列说法错误的是 A.该温度下,将0.1 mol·L-1草酸溶液和0.1 mol· L-1草酸钠溶液等体积混合,溶液pH约为 2.6 B.X点附近滴定突跃不如Y点附近明显,是因为X点时形成缓冲溶液 C.X点对应图b中的M点,Y点对应图b中的N点 D.Y点时,溶液中c(Na+ )>c( )>c(OH- )>c( )>c(H+) 25.(2022·江西·上饶市第一中学模拟预测)常温下,向10mL0.1mol·L-1丙烯酸 (CH=CHCOOH)溶液中滴加pH=13的NaOH溶液,溶液的酸度(AG)与NaOH溶液体积的关 2 系如图所示。已知:AG=lg ,电离度= ×100%。 若忽略溶液混合时的体积变化,下列说法正确的是 A.b点对应的溶液中:c(Na+)>c(CH =CHCOO-)>c(H+)>c(OH-) 2 B.d点对应的溶液中:c(OH-)=c(H+)+c(CH =CHCOO-)+c(CH =CHCOOH) 2 2 C.0.1mol·L-1CH=CHCOOH溶液中丙烯酸的电离度近似等于10% 2 D.若AG=0时V=x,则丙烯酸的电离常数为K= ×10-7 a