文档内容
模板 01 四大平衡常数的综合应用
第一步:提取数据和 ①从题目已知条件中提取平衡常数、pH、粒子浓度等数据;
信息 ②对图像、表格、文字等进行分析,获取与平衡有关的信息。
第二步:确定计算过 ①根据题目要求,找出各个平衡之间的相互关系,确定需要的数据。
程 ②找出新的平衡与已知平衡之间的关系,写出新平衡的平衡表达式,确
定需要的数据。
第三步:进行转换计 根据目标反应平衡常数表达式,用已知平衡常数进行转换,并代入数据
算 进行计算。
技法01 四大平衡常数的关系
1.电离常数与水解常数、水的离子积常数的关系
(1)定量关系
①对于一元弱酸HA,K 与K 的关系
a hHA H++A-,K= ;A-+HO HA+OH-,K = 。
a 2 h
则K·K =c(H+)·c(OH-)=K ,故K = 。
a h w h
常温时,K·K =K =1.0×10-14,K = 。
a h w h
②对于二元弱酸HB,K (HB)、K (HB)与 K (HB-)、K (B2-)的关系
2 a1 2 a2 2 h h
HB-+HO HB+OH-,K (HB-)= = = 。
2 2 h
B2-+HO HB-+OH-,K (B2-)= = = 。
2 h
(2)大小关系:相同温度下,弱酸的电离常数越小,对应的弱酸根离子的水解常数越大。
【特别提醒】
常温时,对于一元弱酸HA,当K >1×10-7时,K <1×10-7,此时将等物质的量浓度的 HA溶液与
a h
NaA溶液等体积混合,HA的电离程度大于A-的水解程度,混合溶液呈酸性;同理,当K<1×10-7时,
a
K >1×10-7,A-的水解程度大于HA的电离程度,混合溶液呈碱性。
h
2.电离常数与溶度积常数的关系
根据电离常数计算出各离子浓度,进而计算K 。
sp
如汽车尾气中的SO 可用石灰水吸收,生成亚硫酸钙浊液。常温下,测得某 CaSO 与水形成的浊液的
2 3
pH为9,忽略S 的第二步水解,则K (CaSO )= (保留3位有效数字)。[已知:K
sp 3 a1
(HSO )=1.2×10-2,K (HSO )=5.6×10-8]
2 3 a2 2 3
分析:常温下,pH=9,c(OH-)=1×10-5 mol·L-1,由S +HO HS +OH-知,c(HS )
2
≈c(OH-)=1×10-5 mol·L-1。K (S )= = =
h
,则 = ,c(S )=5.6×10-4 mol·L-1。由物料守恒可知:c(Ca2
+)=c(S )+c(HS )=5.6×10-4 mol·L-1+1×10-5 mol·L-1=5.7×10-4 mol·L-1,则 K
sp
(CaSO)=c(Ca2+)·c(S )≈3.19×10-7。
3
3.电离常数、溶度积常数与平衡常数的关系
(1)建立K 与K的关系,一般是在K的表达式的分子、分母中同乘以c(H+)或c(OH-),转化为
a
K 与K 的关系。
a w
如常温下联氨的第一步电离方程式为NH +HO N +OH- K =8.7×10-7,反应NH +H+
2 4 2 2 b1 2 4
N 的K= 。
2
分析:K= = = =8.7×107。
(2)建立K 与K的关系,一般是在K的表达式的分子、分母中同乘以某个离子的浓度,将分子、分母
sp
转化为不同物质的K 。
sp
4.K 与溶解度(S)之间的计算关系
sp
对于AB型物质,其K = 。
sp
如60 时溴酸银(AgBrO )的溶解度为0.6 g,则K (AgBrO )约等于 。
3 sp 3
℃分析:60 时,c(Ag+)=c(Br )= ≈2.5×10-2 mol·L-1,则 K (AgBrO )=c
sp 3
(Ag+)·c(Br℃ )=6.25×10-4。
5.难溶碱的K 与pH之间的关系
sp
对于M(OH) ,K =c(Mn+)·cn(OH-),c(OH-)= ,进而计算溶液的pH。c(Mn
n sp
+)= <1.0×10-5 mol·L-1时,沉淀完全。
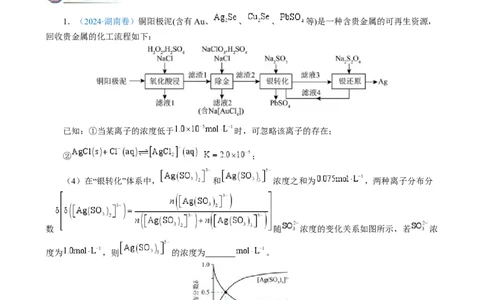
1.(2024·湖南卷)铜阳极泥(含有Au、 、 、 等)是一种含贵金属的可再生资源,
回收贵金属的化工流程如下:
已知:①当某离子的浓度低于 时,可忽略该离子的存在;
② ;
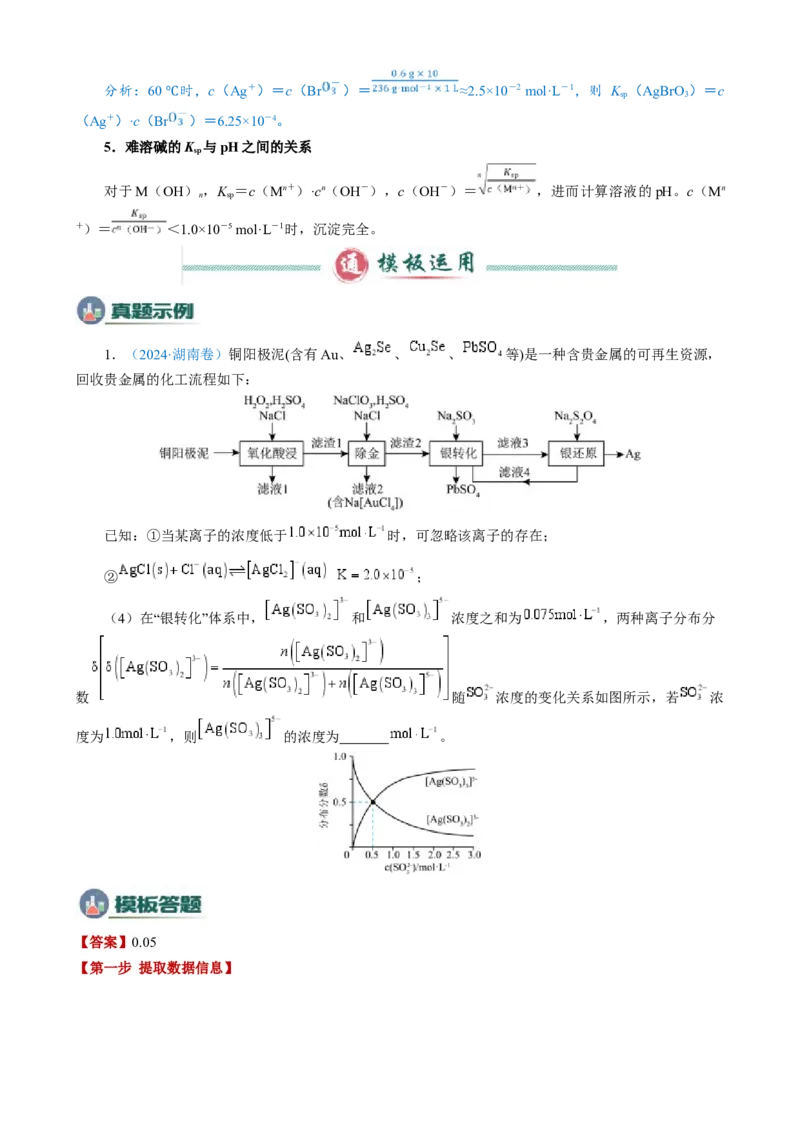
(4)在“银转化”体系中, 和 浓度之和为 ,两种离子分布分
数 随 浓度的变化关系如图所示,若 浓
度为 ,则 的浓度为 。
【答案】0.05
【第一步 提取数据信息】【第二步 确定计算过程】
①根据平衡写出平衡常数表达式:K = ;
②当 时,此时 ,代入数据求出K;
③根据K和c(SO32-)求 的浓度。
【第三步 进行计算】
在“银转化”体系中, 和 浓度之和为 ,溶液中存在平衡关系:
,当 时,此时
,则该平衡关系的平衡常数
,当 时,
,解得此时 。
1.(2024·全国甲卷)钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、
钴、锰的 价氧化物及锌和铜的单质。
注:加沉淀剂使一种金属离子浓度小于等于10-5mol·L-1 ,其他金属离子不沉淀,即认为完全分离。
已知:①Ksp(CuS)=6.5×10-36 ,Ksp(ZnS)=2.5×10-22 ,Ksp(CoS)=4.0×10-21 。
(3)假设“沉铜”后得到的滤液中c(Zn2+)和c(Co2+)均为0.10mol·L-1 ,向其中加入Na2S至Zn2+ 沉淀完
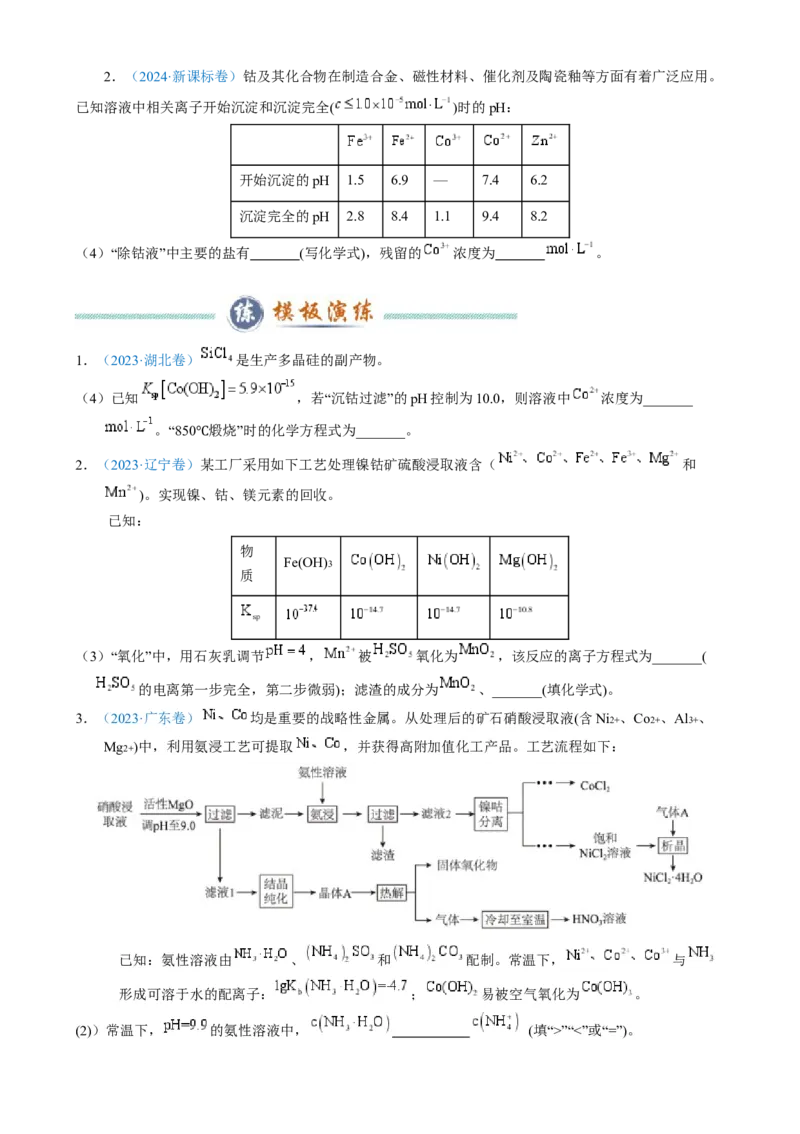
全,此时溶液中c(Co2+)= mol·L-1 ,据此判断能否实现Zn2+ 和Zn2+ 的完全分离 (填“能”或“不能”)。2.(2024·新课标卷)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着广泛应用。
已知溶液中相关离子开始沉淀和沉淀完全( )时的pH:
开始沉淀的pH 1.5 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
(4)“除钴液”中主要的盐有 (写化学式),残留的 浓度为 。
1.(2023·湖北卷) 是生产多晶硅的副产物。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为_______
。“850 煅烧”时的化学方程式为_______。
2.(2023·辽宁卷)℃某工厂采用如下工艺处理镍钴矿硫酸浸取液含( 和
)。实现镍、钴、镁元素的回收。
已知:
物
Fe(OH)3
质
(3)“氧化”中,用石灰乳调节 , 被 氧化为 ,该反应的离子方程式为_______(
的电离第一步完全,第二步微弱);滤渣的成分为 、_______(填化学式)。
3.(2023·广东卷) 均是重要的战略性金属。从处理后的矿石硝酸浸取液(含Ni2+ 、Co2+ 、Al3+ 、
Mg2+)中,利用氨浸工艺可提取 ,并获得高附加值化工产品。工艺流程如下:
已知:氨性溶液由 、 和 配制。常温下, 与
形成可溶于水的配离子: ; 易被空气氧化为 。
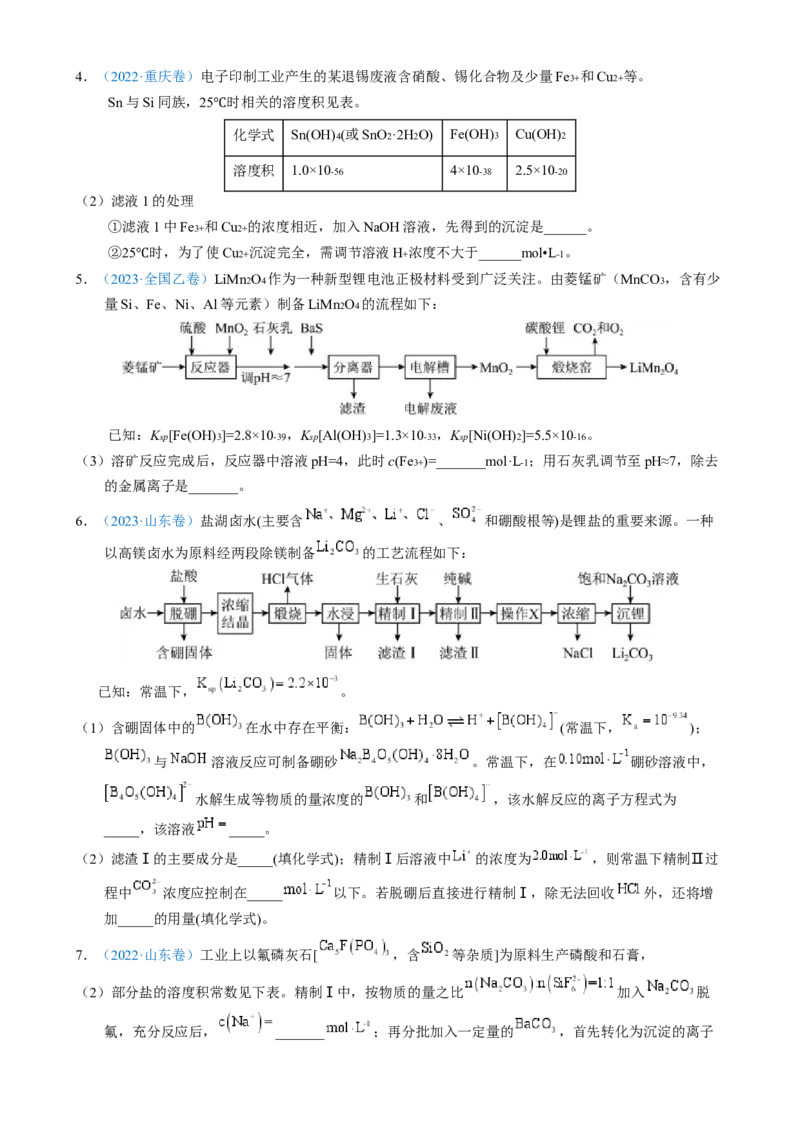
(2))常温下, 的氨性溶液中, (填“>”“<”或“=”)。4.(2022·重庆卷)电子印制工业产生的某退锡废液含硝酸、锡化合物及少量Fe3+ 和Cu2+ 等。
Sn与Si同族,25 时相关的溶度积见表。
℃ 化学式 Sn(OH)4(或SnO2·2H2O) Fe(OH)3 Cu(OH)2
溶度积 1.0×10-56 4×10-38 2.5×10-20
(2)滤液1的处理
①滤液1中Fe3+ 和Cu2+ 的浓度相近,加入NaOH溶液,先得到的沉淀是______。
②25 时,为了使Cu2+ 沉淀完全,需调节溶液H+ 浓度不大于______mol•L-1 。
5.(2023
℃
·全国乙卷)LiMn2O4 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3 ,含有少
量Si、Fe、Ni、Al等元素)制备LiMn2O4 的流程如下:
已知:Ksp[Fe(OH)3]=2.8×10-39 ,Ksp[Al(OH)3]=1.3×10-33 ,Ksp[Ni(OH)2]=5.5×10-16 。
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=_______mol·L-1 ;用石灰乳调节至pH≈7,除去
的金属离子是_______。
6.(2023·山东卷)盐湖卤水(主要含 、 和硼酸根等)是锂盐的重要来源。一种
以高镁卤水为原料经两段除镁制备 的工艺流程如下:
已知:常温下, 。
(1)含硼固体中的 在水中存在平衡: (常温下, );
与 溶液反应可制备硼砂 。常温下,在 硼砂溶液中,
水解生成等物质的量浓度的 和 ,该水解反应的离子方程式为
_____,该溶液 _____。
(2)滤渣Ⅰ的主要成分是_____(填化学式);精制Ⅰ后溶液中 的浓度为 ,则常温下精制Ⅱ过
程中 浓度应控制在_____ 以下。若脱硼后直接进行精制Ⅰ,除无法回收 外,还将增
加_____的用量(填化学式)。
7.(2022·山东卷)工业上以氟磷灰石[ ,含 等杂质]为原料生产磷酸和石膏,
(2)部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比 加入 脱
氟,充分反应后, _______ ;再分批加入一定量的 ,首先转化为沉淀的离子是_______。
8.(2022·广东卷)稀土( )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可
用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸 熔点为 ;月桂酸和 均难溶于水。该工艺条件下,
稀土离子保持 价不变; 的 , 开始溶解时的pH为8.8;有
关金属离子沉淀的相关pH见下表。
离子
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(2)“过滤1”前,用 溶液调pH至_______的范围内,该过程中 发生反应的离子方程式为
_______。
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提取 ,
可提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 低于_______ (保留两
位
有效数字)。
9.(2024届·湖北·三模)废旧铅蓄电池具有较高的回收利用价值。由废铅膏(含 、 、 和
以及少量的铁和铝的氧化物)制备 的流程如下:
② ,
(5)“脱硫”时 转化反应的离子方程式为 ;用沉淀溶解平衡原理解释选择
的原因 。
10.(2024·广东惠州一模)氯碱厂制备的原盐中含有的杂质主要为 及大分子有机物和
难溶性泥沙等物质。
已知: 的电离常数(3)用 溶液吸收一定量 气体形成 缓冲溶液, 时,溶液中
=__________。
11.(2024届·河北承德·三模)废旧手机的废线路板中富含Cu、Sn、Ni、Pb等金属和少量Ag、Au,具
有较高的回收价值,其中部分金属的回收工艺流程如下:
已知:①常温下, 微溶于水,可与 结合生成 配离子: 。
②25 时, , 。
(4) ℃的排放标准为 mg·L 。“沉锡”残余液排放前应调节溶液的pH范围为 。
12.(2024届·山东济宁·三模)一种以锌精矿(主要成分是ZnS,还含有铁、钴、铜等元素的氧化物)为原
料制备纯锌并将其它金属元素回收利用的工艺流程如下:
已知:③ ; ;
(1)常温下,“含尘烟气”中的 用氨水吸收至溶液的 时,
的平衡常数 。
13.(2024届·辽宁沈阳·三模)稀土元素铈及其化合物在生产生活中有重要用途,如汽车尾气用稀土/钯
三效催化剂处理,不仅可以降低催化剂的成本,还可以提高催化效能。以氟碳铈矿(主要成分为
)为原料制备 的一种工艺流程如图:已知:①滤渣1的主要成分是难溶于水的 ,滤渣2的主要成分是 ;
、 (a、b均大于0)。
(5)滤渣1经KCl溶液充分浸取后,测得反应体系中K+ 的物质的量浓度为 ,则 的物质的
量浓度为 (用含a、b的式子表示)。
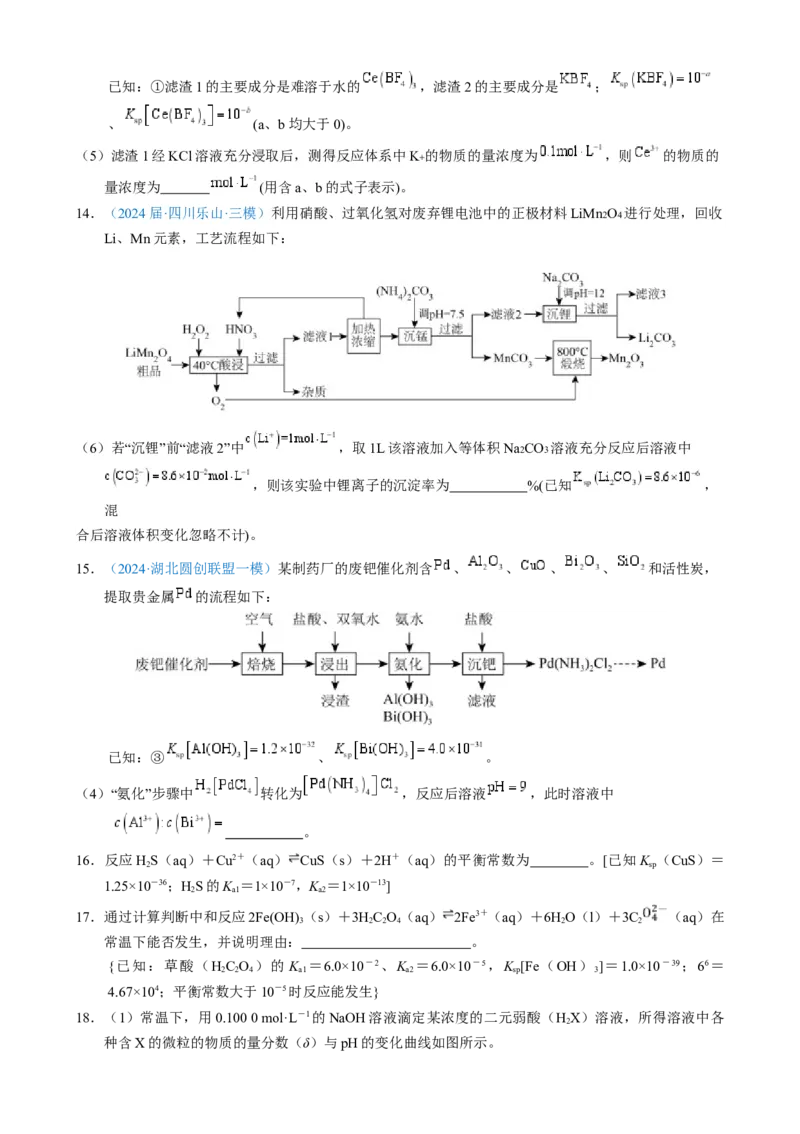
14.(2024届·四川乐山·三模)利用硝酸、过氧化氢对废弃锂电池中的正极材料LiMn2O4 进行处理,回收
Li、Mn元素,工艺流程如下:
(6)若“沉锂”前“滤液2”中 ,取1L该溶液加入等体积Na2CO3 溶液充分反应后溶液中
,则该实验中锂离子的沉淀率为 %(已知 ,
混
合后溶液体积变化忽略不计)。
15.(2024·湖北圆创联盟一模)某制药厂的废钯催化剂含 、 、 、 、 和活性炭,
提取贵金属 的流程如下:
已知:③ 、 。
(4)“氨化”步骤中 转化为 ,反应后溶液 ,此时溶液中
。
16.反应HS(aq)+Cu2+(aq) CuS(s)+2H+(aq)的平衡常数为 。[已知K (CuS)=
2 sp
1.25×10-36;HS的K =1×10-7,K =1×10-13]
2 a1 a2
17.通过计算判断中和反应2Fe(OH) (s)+3HC O (aq) 2Fe3+(aq)+6HO(l)+3C (aq)在
3 2 2 4 2 2
常温下能否发生,并说明理由: 。
{已知:草酸(HC O )的 K =6.0×10-2、K =6.0×10-5,K [Fe(OH) ]=1.0×10-39;66=
2 2 4 a1 a2 sp 3
4.67×104;平衡常数大于10-5时反应能发生}
18.(1)常温下,用0.100 0 mol·L-1的NaOH溶液滴定某浓度的二元弱酸(HX)溶液,所得溶液中各
2
种含X的微粒的物质的量分数(δ)与pH的变化曲线如图所示。则:HX的电离常数K = ,X2-的水解常数K = 。
2 a1 h
(2)已知常温下,K (AgCl)=1.76×10-10。
sp
银氨溶液中存在下列平衡:
Ag+(aq)+2NH ·H O(aq) [Ag(NH )]+(aq)+2HO(l) K =1.10×107。
3 2 3 2 2 1
常温下可逆反应AgCl(s)+2NH ·H O(aq) [Ag(NH ) ]+(aq)+Cl-(aq)+2HO(l)的化
3 2 3 2 2
学平衡常数K = 。
2