文档内容
江苏省南通市2023届高考模拟考试化学试题
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.下列反应是吸热反应,但不属于氧化还原反应的是( )
A.铝片与稀HSO 反应 B.Ba(OH) ·8H O与NH Cl反应
2 4 2 2 4
C.灼热的炭与CO 反应 D.甲烷在O 中的燃烧反应
2 2
2.下列有关化学用语的表述错误的是( )
A.醛基的结构简式:
B.丙烷分子的比例模型:
C.乙烯的电子式:
D.乙醇的比例模型:
3. 、 、 、 四种短周期元素原子序数依次增大,最外层电子数分别为4、1、x、7,已
知 原子的电子层数等于x。下列说法错误的是( )
A.元素 能与氢元素组成多种化合物
B.简单离子半径大小:
C.元素 的单质能与无水乙醇反应
D.元素 与元素 形成的化合物的水溶液显酸性
4.下列物质中既能跟稀HSO 反应,又能跟氢氧化钠溶液反应的是( )
2 4
①NaHCO ②Al O③Al(OH)④Al.
3 2 3 3
A.③④ B.②③④ C.①③④ D.全部
5.目前海水提溴的最主要方法之一是空气吹出法工艺,其流程图如下。下列说法错误的是( )
A.热空气能吹出溴是利用溴易挥发的性质B. 吸收溴的离子方程式为
C.不采用直接蒸馏含溴海水得到单质溴的主要原因是为了节能
D.蒸馏操作用到的主要仪器有蒸馏烧瓶和分液漏斗
6.实验小组同学探究NH 与Cl 的反应,装置如图所示。常温常压下,将氨气收集在薄膜保鲜袋(无
3 2
弹性)中,氯气收集在反应管中,关闭K,按图连接好装置;将氨气压入反应管,充分反应后打开
K。下列说法不正确的是( )
A.反应开始后,保鲜袋逐渐被吸入反应管
B.反应过程中,反应管中产生白烟
C.打开K后,水会倒吸入反应管
D.上述反应原理可用于检验输送氯气的管道是否泄漏
7.在硼酸[B(OH) ]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B
3
原子杂化轨道的类型及同层分子间的主要作用力分别是( )
A.sp,范德华力 B.sp2,范德华力
C.sp2,氢键 D.sp3,氢键
8.在一定温度下,将一定量的气体通入体积为2L的密闭容器中,使其发生反应,有关物质X、Y、
Z的物质的量的变化如图所示。则下列有关推断正确是( )
A.该反应的化学方程式为: 3Z = 3X+2Y
B.t 时,X、Y、Z的质量不再改变
0
C.t 时,Z的浓度为1.2 mol/L
0
D.t 时,反应停止,反应速率为0
0
9.在3L的密闭容器内充入2mol NO和2mol O ,一定温度下发生反应2NO(g)+O (g) 2NO (g),
2 2 2
达到化学平衡后测得NO 浓度为的0.60mol/L。则NO和O 的转化率之比为( )
2 2A.2:1 B.3:2 C.4:3 D.5:4
10.A~E是中学常见的5种化合物,A、B是氧化物,它们之间的转化关系如图所示。
则下列说法正确的是( )
A.单质X与A反应的化学方程式:Al O+2Fe Fe O+2Al
2 3 2 3
B.检验D溶液中金属阳离子的反应:Fe3++3SCN-=Fe(SCN) ↓
3
C.与D溶液反应时单质Y被氧化
D.由于化合物B和C均既能与酸反应,又能与碱反应
11.某燃料电池如图所示,两电极A、B材料都是石墨,下列说法错误的是()
A.氧气在正极发生还原反应
B.若电解质为氢氧化钠溶液,则负极反应式为 H-2e-+2OH-=2HO
2 2
C.电子由电极a流经电解液到电极b
D.若正极消耗的气体质量为4 g,则转移的电子的物质的量为0.5 mol
12.“人文奥运、科技奥运、绿色奥运”是2008年北京奥运会的重要特征.其中禁止运动员使用兴
奋剂是重要举措之一.如图两种兴奋剂的结构分别为:则关于它们的说法中正确的是( )
A.利尿酸乙酯分子中有三种含氧官能团,在核磁共振氢谱上共有七个峰
B.1 mol兴奋剂X与足量浓溴水反应,最多消耗4 mol Br
2
C.两种兴奋剂最多都能和含3molNaOH的溶液反应D.两种分子中的所有碳原子均不可能共平面
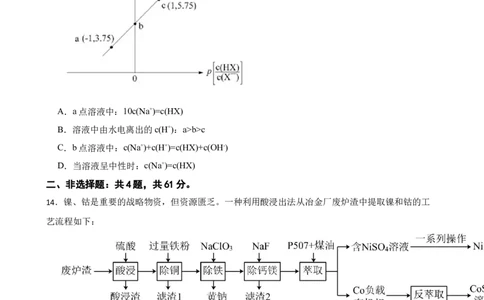
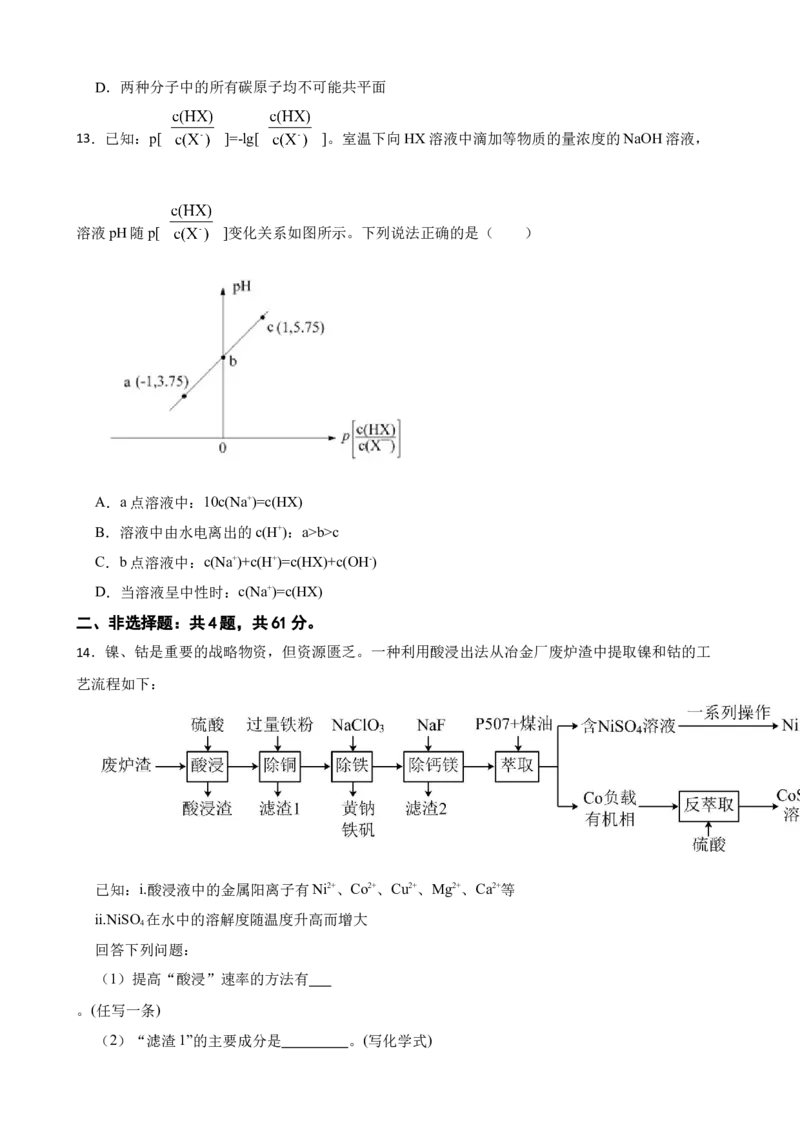
13.已知:p[ ]=-lg[ ]。室温下向HX溶液中滴加等物质的量浓度的NaOH溶液,
溶液pH随p[ ]变化关系如图所示。下列说法正确的是( )
A.a点溶液中:10c(Na+)=c(HX)
B.溶液中由水电离出的c(H+):a>b>c
C.b点溶液中:c(Na+)+c(H+)=c(HX)+c(OH-)
D.当溶液呈中性时:c(Na+)=c(HX)
二、非选择题:共4题,共61分。
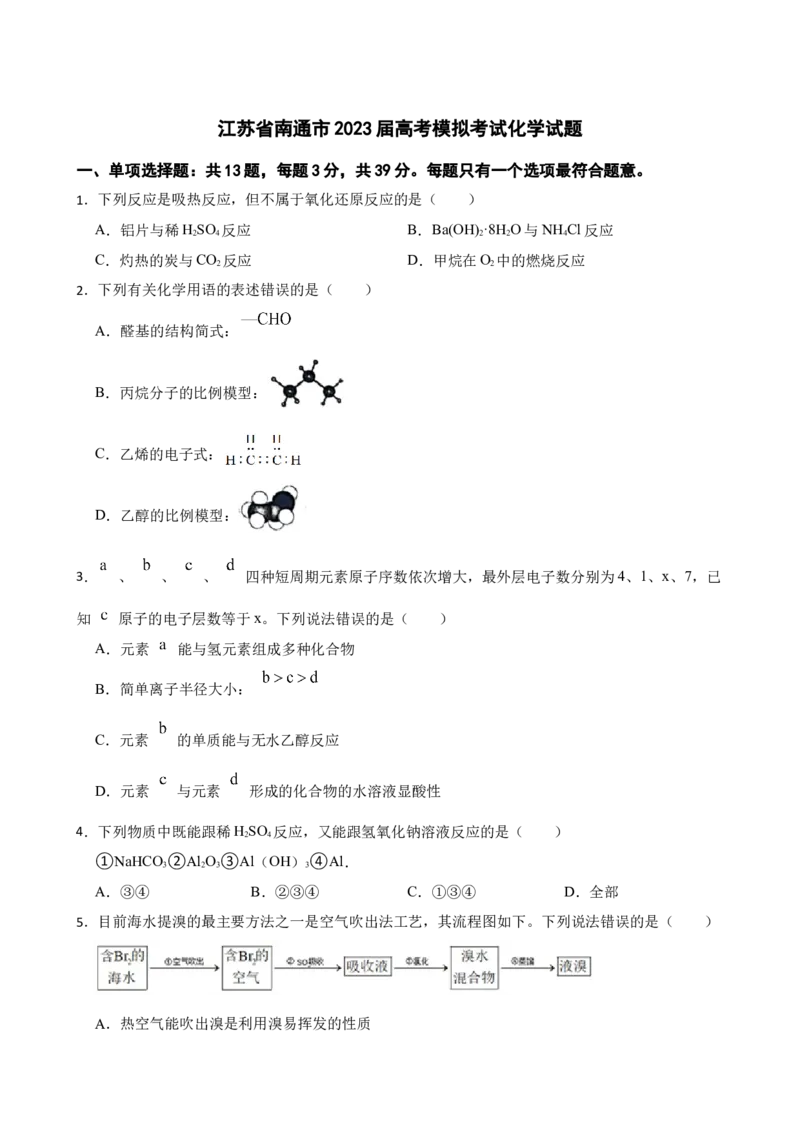
14.镍、钴是重要的战略物资,但资源匮乏。一种利用酸浸出法从冶金厂废炉渣中提取镍和钴的工
艺流程如下:
已知:i.酸浸液中的金属阳离子有Ni2+、Co2+、Cu2+、Mg2+、Ca2+等
ii.NiSO 在水中的溶解度随温度升高而增大
4
回答下列问题:
(1)提高“酸浸”速率的方法有
。(任写一条)
(2)“滤渣1”的主要成分是 。(写化学式)(3)黄钠铁矾的化学式为Na Fe (SO )(OH) ,“除铁”的离子方程式为
2 6 4 4 12
。
(4)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是
(结合平衡理论解释)。Ca2+和Mg2+沉淀完全时,溶液中F-的浓度c(F- )最小为 mol·L-1。(已知
离子浓度≤10-5 mol·L-1时,认为该离子沉淀完全,K (CaF )=1.0 ×10-10,K (MgF )=7.5×10-11)
sp 2 sp 2
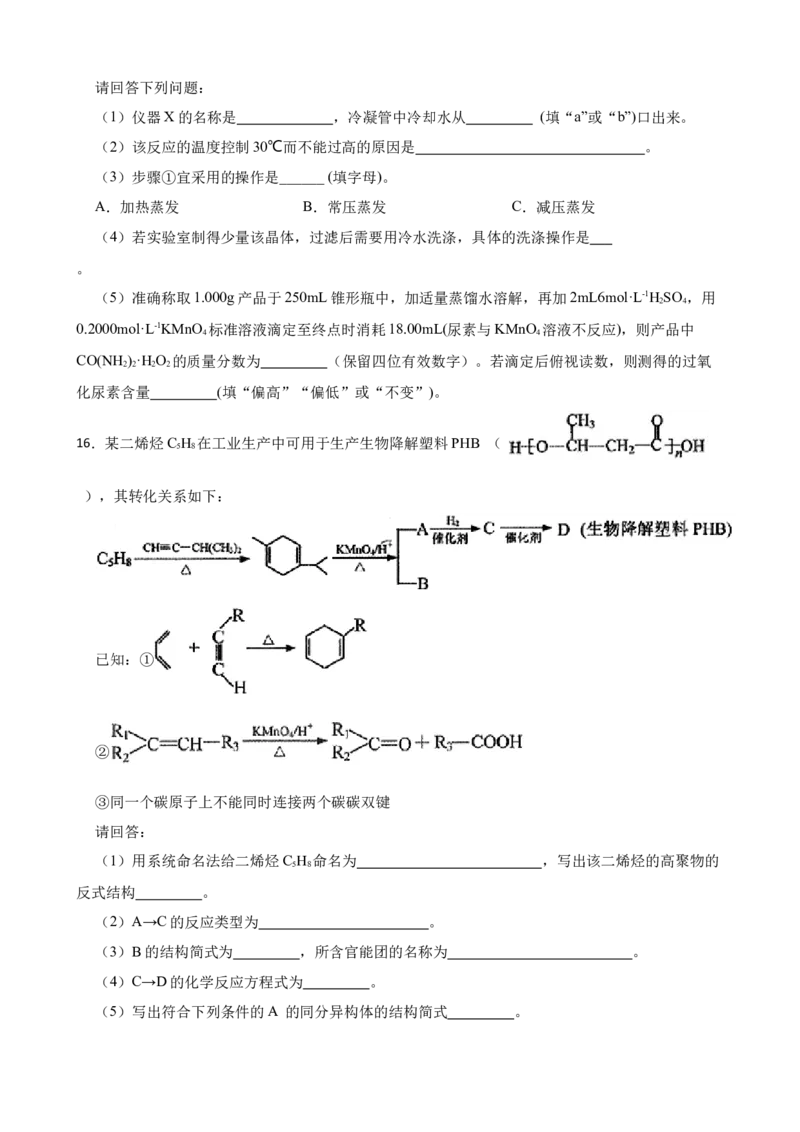
(5)镍、钴萃取率与料液pH、萃取剂体积与料液体积比V:V 的关系曲线如下图所示,则“萃
a 0
取”时应选择的pH和V:V 分别为 、 。
a 0
(6)获得NiSO (s)的“一系列操作”是 。
4
(7)工艺流程中,可循环利用的物质是 。
15.过氧化尿素是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域。用低浓度的
双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素。反应的方程式为:CO(NH )+HO
2 2 2 2
CO(NH )·H O。过氧化尿素的部分性质如下:
2 2 2 2
分子式 外观 热分解温度 熔点 溶解性
CO(NH )·H O 白色晶体 45℃ 75~85℃ 易溶于水、有机溶剂
2 2 2 2
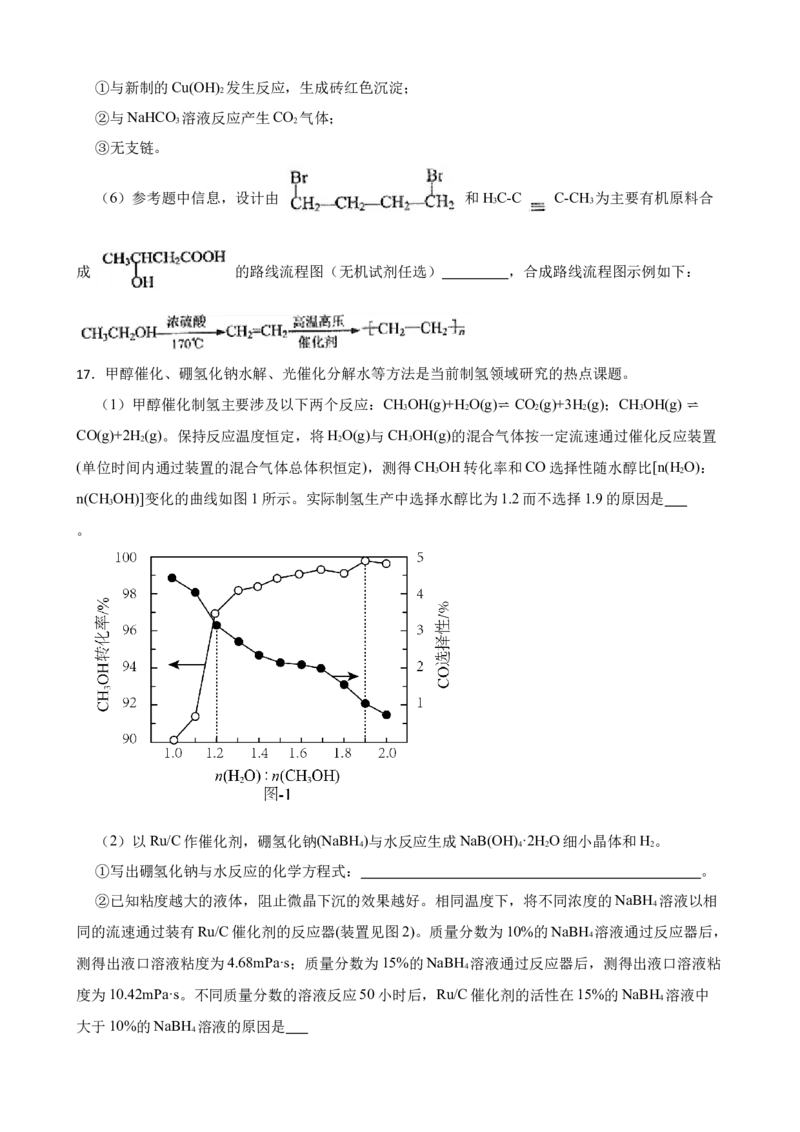
合成过氧化尿素的流程及反应装置图如图:请回答下列问题:
(1)仪器X的名称是 ,冷凝管中冷却水从 (填“a”或“b”)口出来。
(2)该反应的温度控制30℃而不能过高的原因是 。
(3)步骤①宜采用的操作是______ (填字母)。
A.加热蒸发 B.常压蒸发 C.减压蒸发
(4)若实验室制得少量该晶体,过滤后需要用冷水洗涤,具体的洗涤操作是
。
(5)准确称取1.000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加2mL6mol·L-1HSO ,用
2 4
0.2000mol·L-1KMnO 标准溶液滴定至终点时消耗18.00mL(尿素与KMnO 溶液不反应),则产品中
4 4
CO(NH )·H O 的质量分数为 (保留四位有效数字)。若滴定后俯视读数,则测得的过氧
2 2 2 2
化尿素含量 (填“偏高”“偏低”或“不变”)。
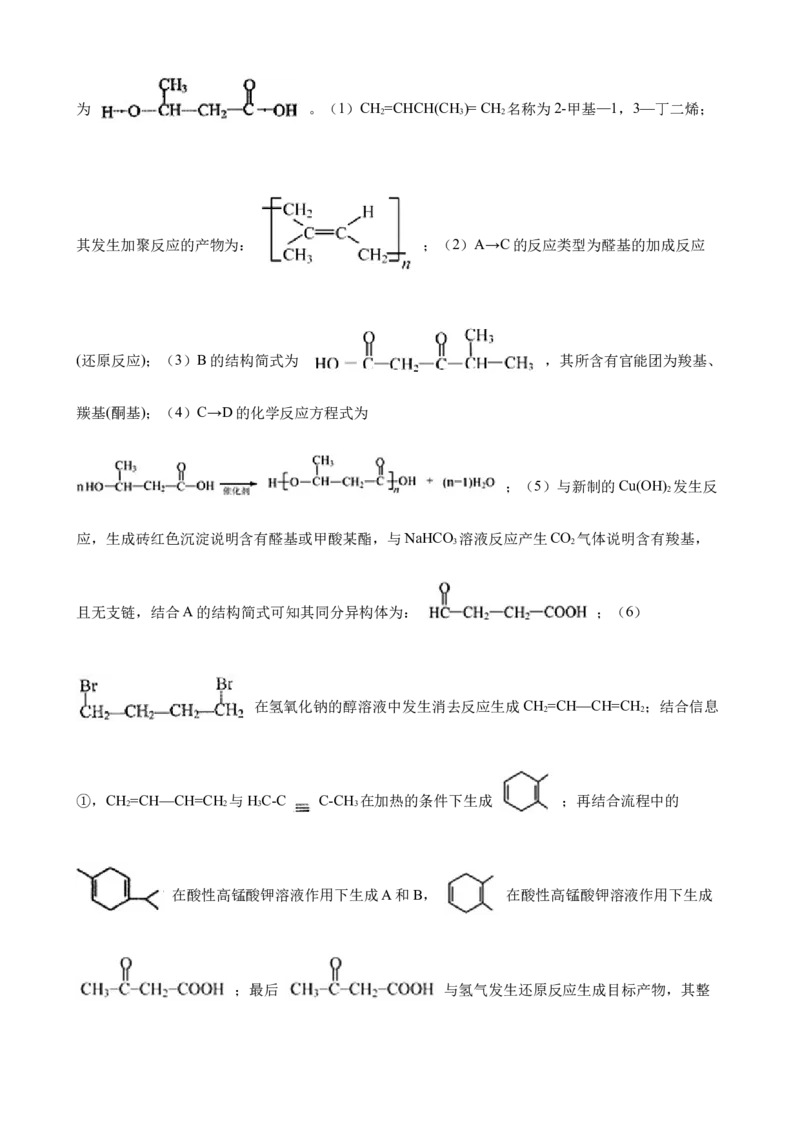
16.某二烯烃CH 在工业生产中可用于生产生物降解塑料PHB (
5 8
),其转化关系如下:
已知:①
②
③同一个碳原子上不能同时连接两个碳碳双键
请回答:
(1)用系统命名法给二烯烃CH 命名为 ,写出该二烯烃的高聚物的
5 8
反式结构 。
(2)A→C的反应类型为 。
(3)B的结构简式为 ,所含官能团的名称为 。
(4)C→D的化学反应方程式为 。
(5)写出符合下列条件的A 的同分异构体的结构简式 。①与新制的Cu(OH) 发生反应,生成砖红色沉淀;
2
②与NaHCO 溶液反应产生CO 气体;
3 2
③无支链。
(6)参考题中信息,设计由 和HC-C C-CH 为主要有机原料合
3 3
成 的路线流程图(无机试剂任选) ,合成路线流程图示例如下:
17.甲醇催化、硼氢化钠水解、光催化分解水等方法是当前制氢领域研究的热点课题。
(1)甲醇催化制氢主要涉及以下两个反应:CH 3 OH(g)+H 2 O(g)⇌ CO 2 (g)+3H 2 (g);CH 3 OH(g) ⇌
CO(g)+2H (g)。保持反应温度恒定,将HO(g)与CH OH(g)的混合气体按一定流速通过催化反应装置
2 2 3
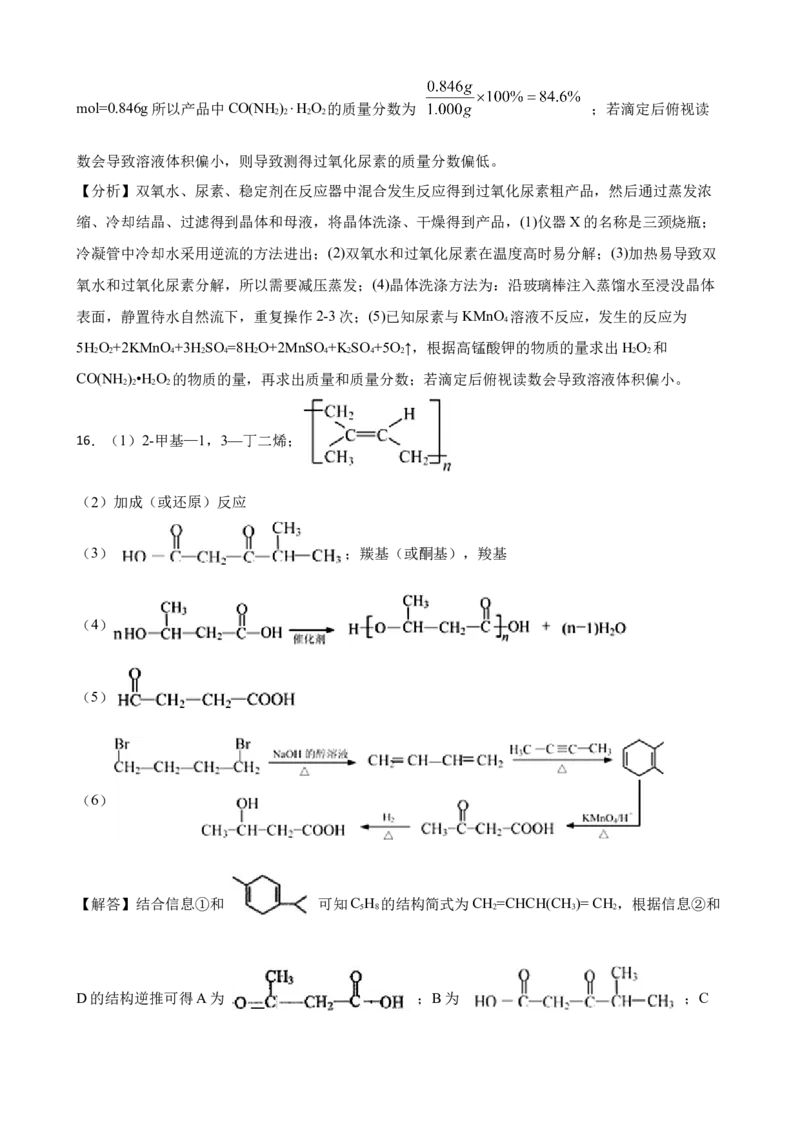
(单位时间内通过装置的混合气体总体积恒定),测得CH OH转化率和CO选择性随水醇比[n(H O):
3 2
n(CHOH)]变化的曲线如图1所示。实际制氢生产中选择水醇比为1.2而不选择1.9的原因是
3
。
(2)以Ru/C作催化剂,硼氢化钠(NaBH )与水反应生成NaB(OH) ·2H O细小晶体和H。
4 4 2 2
①写出硼氢化钠与水反应的化学方程式: 。
②已知粘度越大的液体,阻止微晶下沉的效果越好。相同温度下,将不同浓度的NaBH 溶液以相
4
同的流速通过装有Ru/C催化剂的反应器(装置见图2)。质量分数为10%的NaBH 溶液通过反应器后,
4
测得出液口溶液粘度为4.68mPa·s;质量分数为15%的NaBH 溶液通过反应器后,测得出液口溶液粘
4
度为10.42mPa·s。不同质量分数的溶液反应50小时后,Ru/C催化剂的活性在15%的NaBH 溶液中
4
大于10%的NaBH 溶液的原因是
4。
(3)基于TiO 材料光催化分解水制氢的可能机理如图3所示。
2
①若使用H18O代替HO分解制氢,则获得的氧气可能是 (填字母)。
2 2
a.O b.18O c.Ol8O
2 2
②补充完成TiO 材料光催化分解水制氢的过程描述:在紫外光的照射下,TiO 材料的VB端将电
2 2
子转移至CB端,
。答案
1.B
【解答】A.铝片与稀HSO 反应,是氧化还原反应,也是放热反应,故不选A项;
2 4
B. Ba(OH) ·8H O与NH Cl反应是吸热反应,该反应不是氧化还原反应,
2 2 4
故答案为:B项;
C.灼热的炭与CO 反应,该反应是吸热反应,同时碳的化合价发生变化,是氧化还原反应,故不选C
2
项。
D.甲烷在O 中的燃烧反应是氧化还原反应,也是放热反应,故不选D项;
2
故答案为B。
【分析】反应物的总能量小于生成物的总能量的反应叫做吸热反应;在反应中有化合价升降的叫做
氧化还原反应。
2.B
【解答】A.醛基是醛类(如CH CHO、HCHO)的官能团,醛基的结构简式为-CHO,A不符合题
3
意
B.丙烷分子的结构简式为CH CH CH ,它的球棍模型为 ,B符合题意;
3 2 3
C.乙烯的结构简式为CH =CH ,其电子式为 ,C不符合题意;
2 2
D.乙醇的结构简式为CH CH OH,它的比例模型为 ,D不符合题意;
3 2
故答案为:B。
【分析】注意区分比例模型、球棍模型;区分结构式、电子式和结构简式。
3.B
【解答】A.元素碳能与氢元素组成烷烃、烯烃、炔烃、芳香烃等多种化合物,A不符合题意;
B.b、c、d分别为Na、Al、Cl元素,简单离子半径大小:Cl->Na+>Al3+,B符合题意;
C.元素Na的单质能与无水乙醇反应,生成乙醇钠和氢气,C不符合题意;
D.元素 与元素 形成的化合物为AlCl ,其为强酸弱碱盐,水溶液显酸性,D不符合题意;
3
故答案为:B。【分析】A.烃的种类繁多;
B.电子层结构相同,序数越大越小;
C.Na能与醇反应;
D.强酸弱碱盐水解呈酸性。
4.D
【解答】解:Al、Al O、Al(OH)、弱酸的酸式盐、弱酸的铵盐、氨基酸、蛋白质等都既能和稀
2 3 3
硫酸反应又能和NaOH溶液反应,碳酸氢钠属于弱酸的酸式盐,所以能和稀硫酸、NaOH溶液反应
的物质有碳酸氢钠、氧化铝、氢氧化铝和铝,
故选D.
【分析】Al、Al O、Al(OH)、弱酸的酸式盐、弱酸的铵盐、氨基酸、蛋白质等都既能和稀硫酸
2 3 3
反应又能和NaOH溶液反应,据此分析解答.
5.D
【解答】A. 溴易挥发,所以热空气能吹出溴是利用溴易挥发的性质,故A不符合题意;
B. 二氧化硫具有还原性,溴具有强氧化性,二者能发生氧化还原反应,反应方程式为
SO +2HO+Br =HSO +2HBr,离子方程式是SO +2HO+Br =SO 2-+4H++2Br-,故B不符合题意;
2 2 2 2 4 2 2 2 4
C. 海水中溴的含量很低,如果直接采用直接蒸馏含溴海水得到单质溴浪费能源,将溴还原的目的是
富集溴,达到节能的目的,故C不符合题意;
D. 蒸馏操作用到的主要仪器有蒸馏烧瓶、冷凝管、尾接管、锥形瓶、温度计等,故D符合题意;
故答案为:D。
【分析】用空气从含Br 的海水将Br 吹出得到含Br 的空气,用二氧化硫吸收,得到吸收液,发生的
2 2 2
反应为SO +2HO+Br =HSO +2HBr,然后将吸收液氯化,发生的反应为2HBr+Cl =Br +2HCl,得到
2 2 2 2 4 2 2
溴水混合物,然后采用蒸馏的方法得到液溴,据此分析解答.
6.C
【解答】A.由上面分析可知,反应开始后,反应管内气体压强减小,保鲜袋逐渐被吸入反应管,A
不符合题意;
B.反应过程中,反应管中生成NH Cl固体,悬浮于气体中,从而产生白烟,B不符合题意;
4
C.打开K后,因反应管内气体的压强等于大气压强,所以水不会倒吸入反应管,C符合题意;
D.利用上述反应原理,可将蘸有浓氨水的玻璃棒靠近输送氯气管道中怀疑漏气的部位,从而根据有
无白烟产生,判断管道是否泄漏,D不符合题意;
故答案为:C。【分析】根据反应时,氨气和氯气发生反应,得到氯化铵白烟导致压强降低,保鲜袋逐渐被吸入反
应管,产物中海油气体,气压大于外界大气压,水不会流入反应管中,此反应的实验现象明显可以
用来检验氯气管道是否泄漏,结合选项进行判断即可
7.C
【解答】B原子最外层的3个电子都参与成键,故B原子可以形成sp2杂化轨道;B(OH) 分子中的—
3
OH可以与相邻分子中的H原子形成氢键。
【分析】本题考查元素轨道的杂化方式和氢键的判断,熟练掌握氢键的形成条件是解题的关键。
8.B
【解答】A.由图可知,X、Y的物质的量增大,X、Y为生成物,Z物质的量减小,Z为反应物,到
平衡后,X生成1.8mol,Y生成1.2mol,Z反应1.8mol,X、Y、Z的化学计量数之比=1.8:1.2:
1.8=3:2:3,此后任何物质的物质的量不变,则反应为可逆反应,因此该反应的化学方程式为:3Z
3X+2Y,A不符合题意;
B.化学平衡时各组分的浓度不再随时间变化而变化, X、Y、Z的质量也不再改变,B符合题意;
C.根据图象可知平衡时Z的浓度c(Z)= =0.6mol/L,C不符合题意;
D.根据可逆反应平衡的特征可知,反应处于平衡时正、逆反应速率相等,但不等于零,D不符合题
意;
故答案为:B。
【分析】A.根据X、Y、Z物质的量的变化判断反应物、产物,利用物质的量之比等于化学计量数之
比确定化学计量数,据此书写化学方程式;
B.化学平衡时的特征作判断;
C.根据物质的量与体积计算浓度;
D.根据可逆反应的特征判断。
9.A
【解答】设O 的转化率为α,由题意列三段式: ,化学平
2
衡后测得NO 浓度为的0.60mol/L,即平衡后n(NO )=2α=0.6×3=1.8,则α=0.9,故α(NO):
2 2
α(O )=2α:α=2:1,A符合题意;
2
故答案为:A。【分析】根据三段式计算。
10.C
【解答】A.由分析可知,单质X与A的反应为铝与氧化铁在高温下发生置换反应生成铁和氧化铝,
反应的化学方程式:Fe O+2Al Al O+2Fe,故A不符合题意;
2 3 2 3
B.检验D溶液中铁离子的反应为铁离子与硫氰酸根离子反应生成硫氰化铁,反应的离子方程式为Fe3
++3SCN-=Fe(SCN) ,故B不符合题意;
3
C.Y与D溶液的反应为铁与硫酸铁反应生成硫酸亚铁,反应中铁为还原剂被氧化,故C符合题意;
D.C为硫酸铝,硫酸铝不能与酸反应,故D不符合题意;
故答案为:C。
【分析】依据题给转化关系可知,A+X=B+Y是置换反应,单质X、Y都和稀硫酸反应说明是X、Y
是活泼金属单质,A、B是能与硫酸反应的金属氧化物,由氧化物A和硫酸反应生成的D能与单质Y
反应生成E可知, A为变价金属,则Y为铁,置换反应是氧化铁与铝发生的铝热反应,X为Al、A
为Fe O、B为Al O、C为Al (SO4)、D为Fe (SO )、E为FeSO 。
2 3 2 3 2 3 2 4 3 4
11.C
【解答】A.b电极上氧气得电子发生还原反应作电池的正极,选项A不符合题意;
B.若电解质为氢氧化钠溶液,则负极上氢气失电子产生的氢离子与氢氧根离子结合生成水,电极反
应式为:H-2e-+2OH-=2HO,选项B不符合题意;
2 2
C.根据以上分析,原电池中电子从负极流向正极,即从a电极流出经导线流向b电极,选项C符合题
意;
D.正极发生还原反应,电极方程式为O+2HO+4e-=4OH-,若正极消耗的气体质量为4克,即
2 2
0.125mol,则转移的电子的物质的量为0.125mol×4=0.5mol,选项D不符合题意。
故答案为:C。
【分析】在原电池中,负极失去电子,发生的是氧化反应;正极得到电子,发生的是还原反应;外
电路中,电子是由负极流向正极,而在电解液中,阴离子向负极附近移动,阳离子向正极附近移动。
12.B
【解答】解:A.利尿酸含C=C、C=O、﹣COC﹣、﹣COOH,含7种位置的H原子,则含四种含氧
官能团,在核磁共振氢谱上共有七个峰,故A错误;
B.兴奋剂X含酚﹣OH和C=C,酚﹣H的邻对位能发生取代反应,则1mol兴奋剂X与足量浓溴水反应,最多消耗4molBr ,故B正确;
2
C.Y中羧基和Cl原子,水解生成HCl和酚羟基,1mol水解产物共含有2mol酚羟基、1mol羧基和
2molHCl,则1 mol兴奋剂Y与足量NaOH溶液反应,最多消耗5 mol NaOH,故C错误;
D.苯环为平面结构,与苯环直接相连的原子一定在同一平面内,则兴奋剂X中所有碳原子可能共
平面,故D错误;
故选B.
【分析】对比两种兴奋剂的结构,兴奋剂X中含有酚羟基,兴奋剂Y中含有C=O、COOH等官能团,
二者都含有C=C,结合有机物的结构和性质解答该题.
13.C
【解答】A.a点溶液中存在电荷守恒:c(Na+)+c(H+)=c(X-)+c(OH-),此时p[ ]=-1,则
c(X-)=10c(HX),代入电荷守恒得c(Na+)+c(H+)=10c(HX)+c(OH-),由于溶液呈酸性c(H+)>c(OH-),
c(Na+)<10c(HX),选项A不符合题意;
B.根据图示可知,a、b、c均为酸性溶液,则溶质为HX和NaX,pH<7的溶液中,HX的电离程度
大于X-的水解程度,可只考虑H+对水的电离的抑制,溶液pH越大氢离子浓度越小,水的电离程度
越大,则溶液中水的电离程度:a