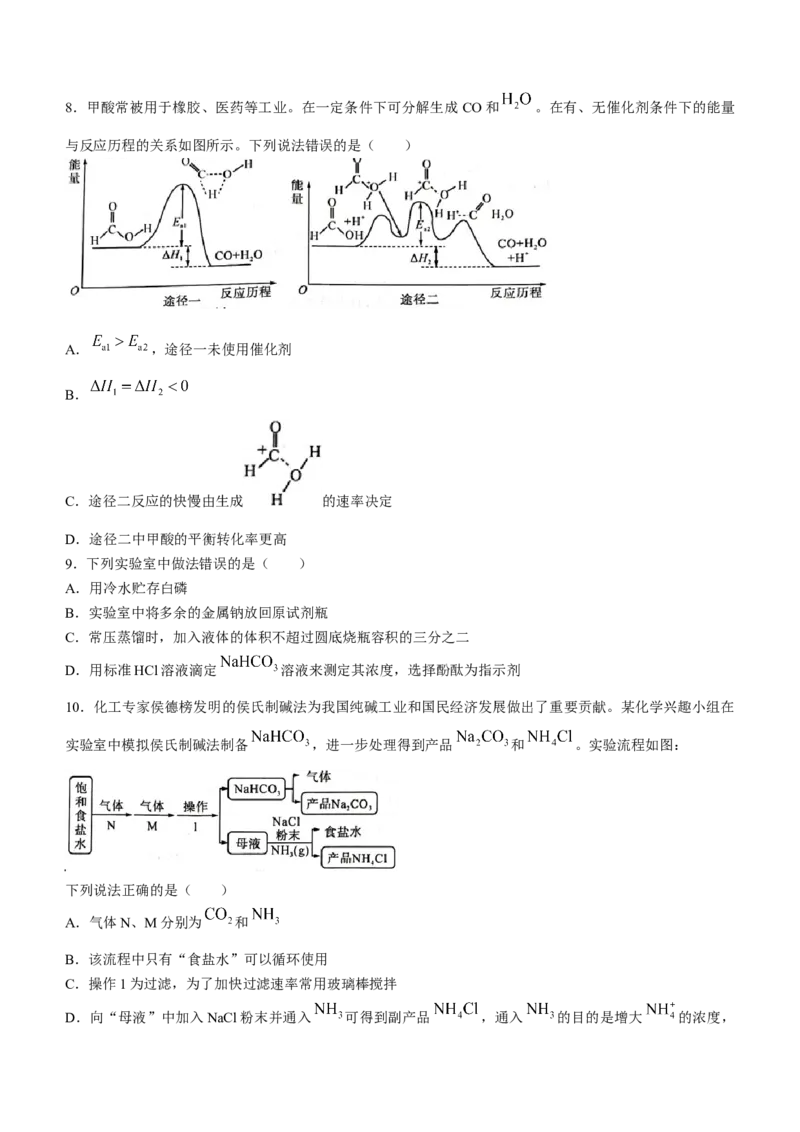
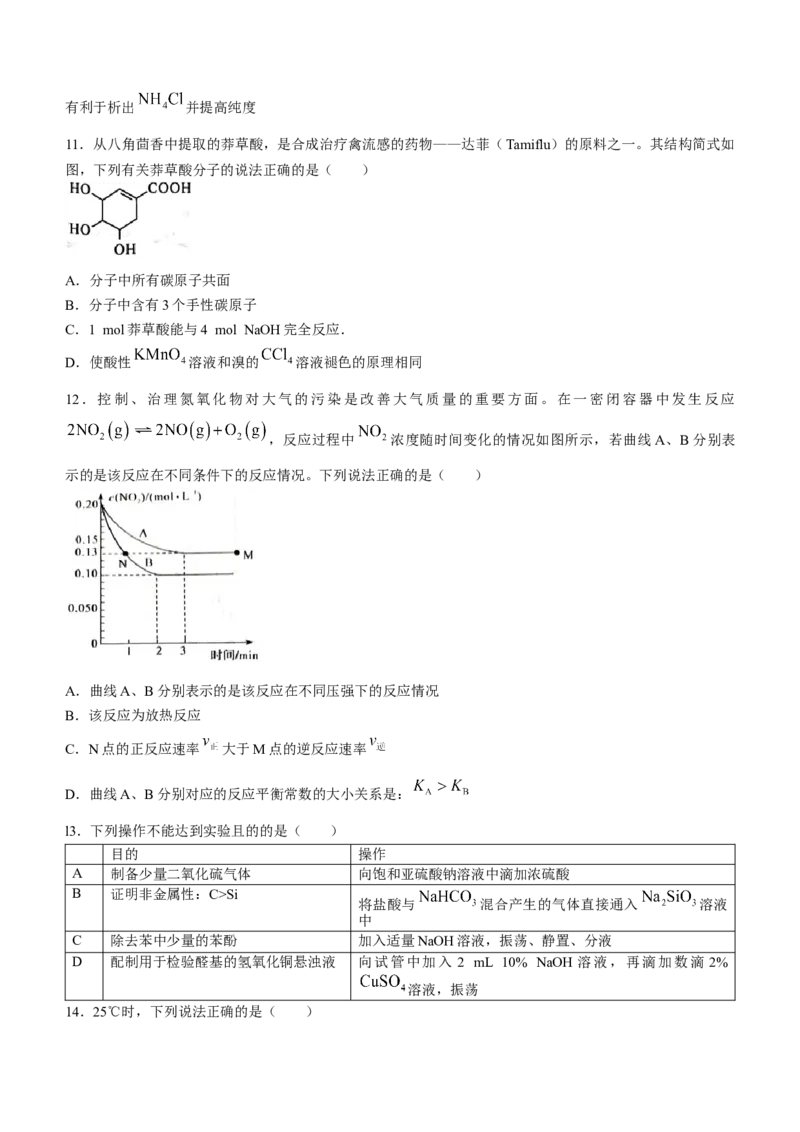
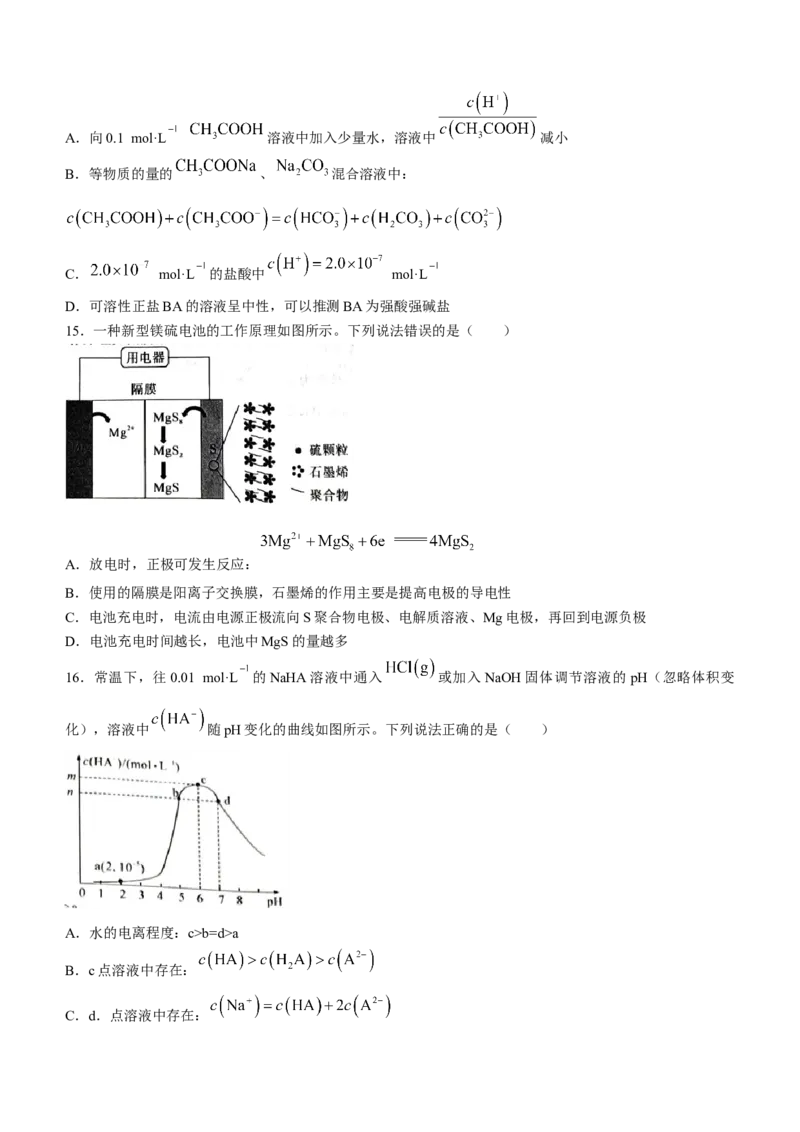
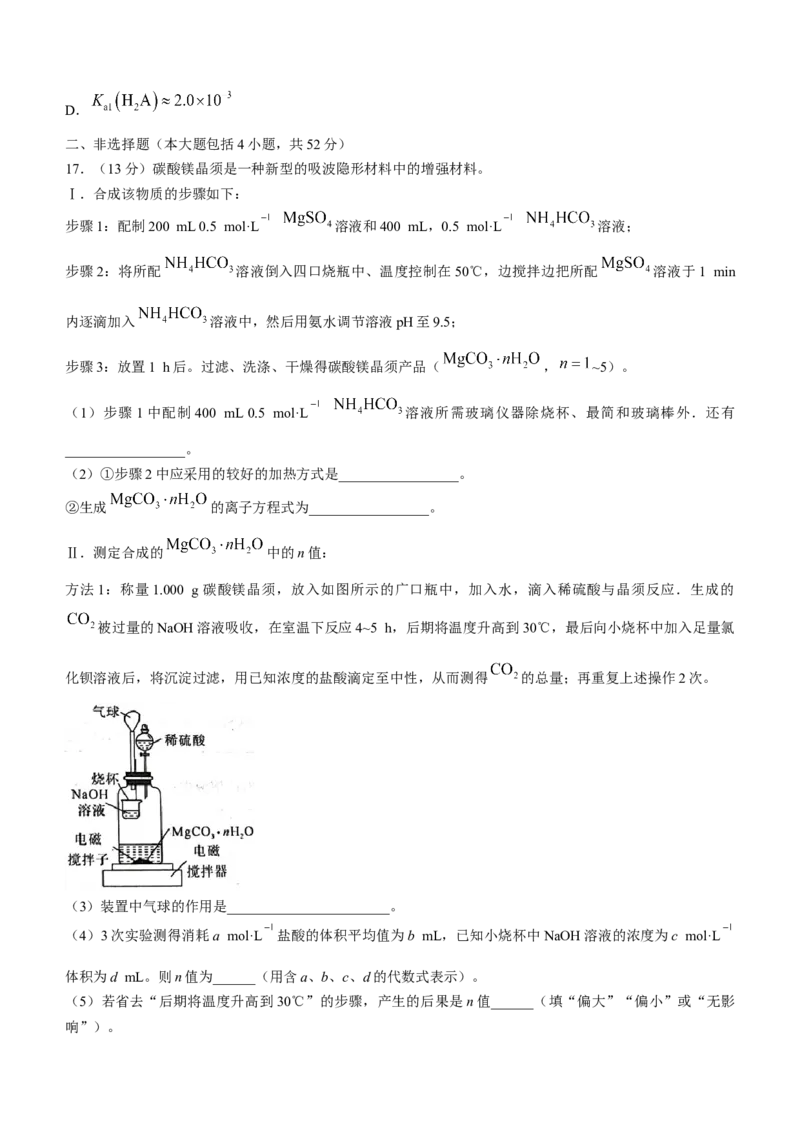
文档内容
吉安市高三上学期期末教学质量检测
2023.1
化学试题
(测试时间:100分钟 卷面总分,100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡|
2.回答选择题时,选出每小题答案后.用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干
净后,再选选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将答题卡交回。
可能用到的相对原于质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32
一、选择题(本大题共16个小题,每小题3分,共48分。在每小题给出的四个选项中,只有一项是符合题
目要求的)
1.化学与生活、环境和能源密切相关,下列过程没有涉及化学变化的是( )
A.葡萄酒中添加二氧化硫 B.对环境消毒杀菌,阻断病毒传播
C.稻草发酵肥田,发展绿色农业 D.蛋白质溶液中加入NaCl固体生成沉淀
2.九月.正是开学季.今年却因新冠肺炎疫情突发,给吉安市社会经济发展和生产生活带来了重大影响。化
学在新冠肺炎疫情防控中发挥着重要的作用,下列说法正确的是( )
A.医用消毒酒精中乙醇的体积分数为95%
B.医用酒精和84消毒液均可杀灭新型冠状病毒,二者消毒原理不同
C.酒精与84消毒液混合,可增强消毒效果
D.医用外科口罩和防护服所用的熔喷布是--种聚丙烯材料,属于纯净物
3.下列离子方程式书写正确的是( )
A.NaHS水解:
B.用惰性电极电解饱和 溶液:
C.用过量氨水吸收工业尾气中的 :
D.向 溶液中逐滴加入 溶液,使溶液呈中性:
4. 代表阿伏加德罗常数的值。下列说法正确的是( )A.1 mol 与3 mol 在一定条件下充分反应,转移的电子数为
B.11.2 L CO和 混合气体中含有的质子数为
C.1 L 1 mol·L 溴化铵水溶液中 与 的数量之和大于
D.25℃时, 的 溶液中含有 数为
5.碘元素在地壳中主要以 的形式存在,在海水中主要以 的形式存在,几种粒子之间的转化关系如
图所示。下列说法不正确的是( )
A.氧化性的强弱顺序为
B.一定条件下, 与 反应可能生成
C.向含 的溶液中通入 ,所得溶液中加入淀粉溶液一定变蓝
D.途径Ⅰ、途径Ⅱ中生成等量的 时转移电子数之比为1∶5
6.原子核的人工转变是利用 粒子(即氦核 )撞击原子核,使原子核转变为另一种原子核的过程。
1919年,卢瑟福利用 粒子轰击短周期非金属原子 ,发现了质子,使人类对原子核的认识更进一步,其
核反应原理为 ,其中元素X的最高价氧化物对应的水化物能与其气态氧化物反应生
成盐,下列说法正确的是( )
A.X、Y均可形成既含板性键又含非极性健的化合物
B. 的中子数为8
C.原子半径:XSi
将盐酸与 混合产生的气体直接通入 溶液
中
C 除去苯中少量的苯酚 加入适量NaOH溶液,振荡、静置、分液
D 配制用于检验醛基的氢氧化铜悬浊液 向试管中加入 2 mL 10% NaOH 溶液,再滴加数滴 2%
溶液,振荡
14.25℃时,下列说法正确的是( )A.向0.1 mol·L 溶液中加入少量水,溶液中 减小
B.等物质的量的 、 混合溶液中:
C. mol·L 的盐酸中 mol·L
D.可溶性正盐BA的溶液呈中性,可以推测BA为强酸强碱盐
15.一种新型镁硫电池的工作原理如图所示。下列说法错误的是( )
A.放电时,正极可发生反应:
B.使用的隔膜是阳离子交换膜,石墨烯的作用主要是提高电极的导电性
C.电池充电时,电流由电源正极流向S聚合物电极、电解质溶液、Mg电极,再回到电源负极
D.电池充电时间越长,电池中MgS的量越多
16.常温下,往0.01 mol·L 的NaHA溶液中通入 或加入NaOH固体调节溶液的pH(忽略体积变
化),溶液中 随pH变化的曲线如图所示。下列说法正确的是( )
A.水的电离程度:c>b=d>a
B.c点溶液中存在:
C.d.点溶液中存在:D.
二、非选择题(本大题包括4小题,共52分)
17.(13分)碳酸镁晶须是一种新型的吸波隐形材料中的增强材料。
Ⅰ.合成该物质的步骤如下:
步骤1:配制200 mL 0.5 mol·L 溶液和400 mL,0.5 mol·L 溶液;
步骤2:将所配 溶液倒入四口烧瓶中、温度控制在50℃,边搅拌边把所配 溶液于1 min
内逐滴加入 溶液中,然后用氨水调节溶液pH至9.5;
步骤3:放置1 h后。过滤、洗涤、干燥得碳酸镁晶须产品( , ~5)。
(1)步骤1中配制400 mL 0.5 mol·L 溶液所需玻璃仪器除烧杯、最简和玻璃棒外.还有
_________________。
(2)①步骤2中应采用的较好的加热方式是_________________。
②生成 的离子方程式为_________________。
Ⅱ.测定合成的 中的n值:
方法1:称量1.000 g碳酸镁晶须,放入如图所示的广口瓶中,加入水,滴入稀硫酸与晶须反应.生成的
被过量的NaOH溶液吸收,在室温下反应4~5 h,后期将温度升高到30℃,最后向小烧杯中加入足量氯
化钡溶液后,将沉淀过滤,用已知浓度的盐酸滴定至中性,从而测得 的总量;再重复上述操作2次。
(3)装置中气球的作用是_______________________。
(4)3次实验测得消耗a mol·L 盐酸的体积平均值为b mL,已知小烧杯中NaOH溶液的浓度为c mol·L
体积为d mL。则n值为______(用含a、b、c、d的代数式表示)。
(5)若省去“后期将温度升高到30℃”的步骤,产生的后果是n值______(填“偏大”“偏小”或“无影
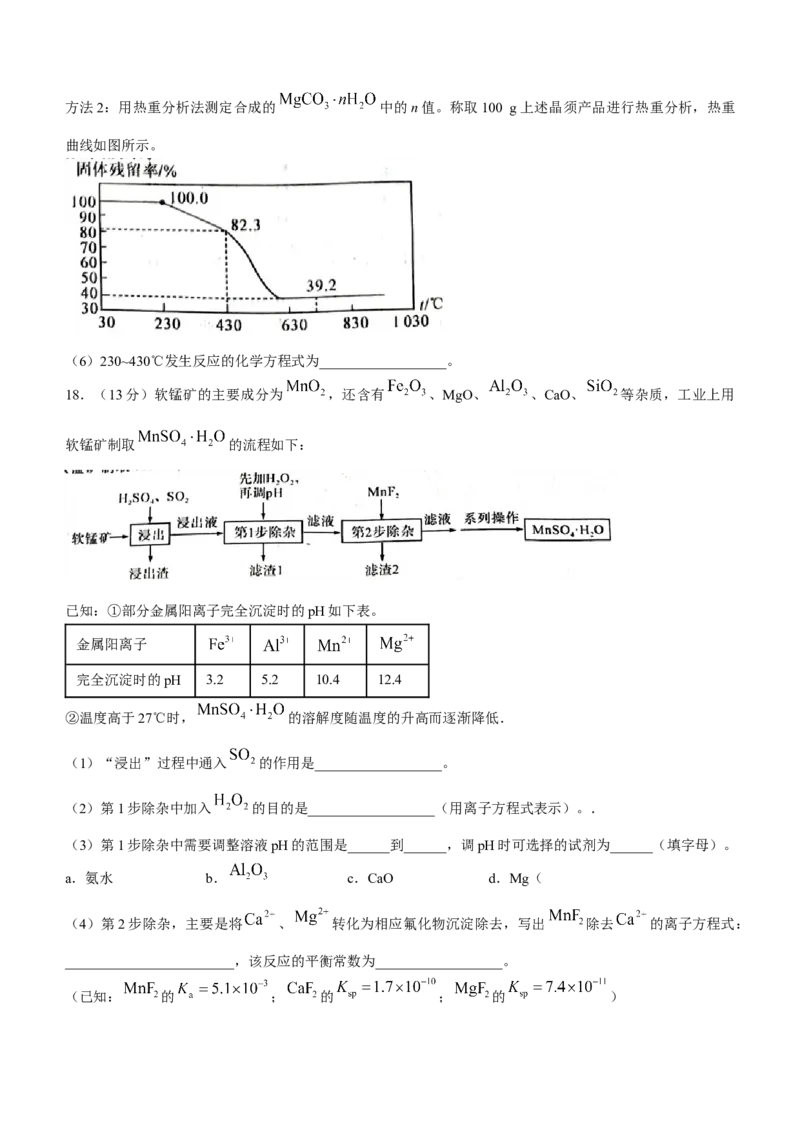
响”)。方法2:用热重分析法测定合成的 中的n值。称取100 g上述晶须产品进行热重分析,热重
曲线如图所示。
(6)230~430℃发生反应的化学方程式为__________________。
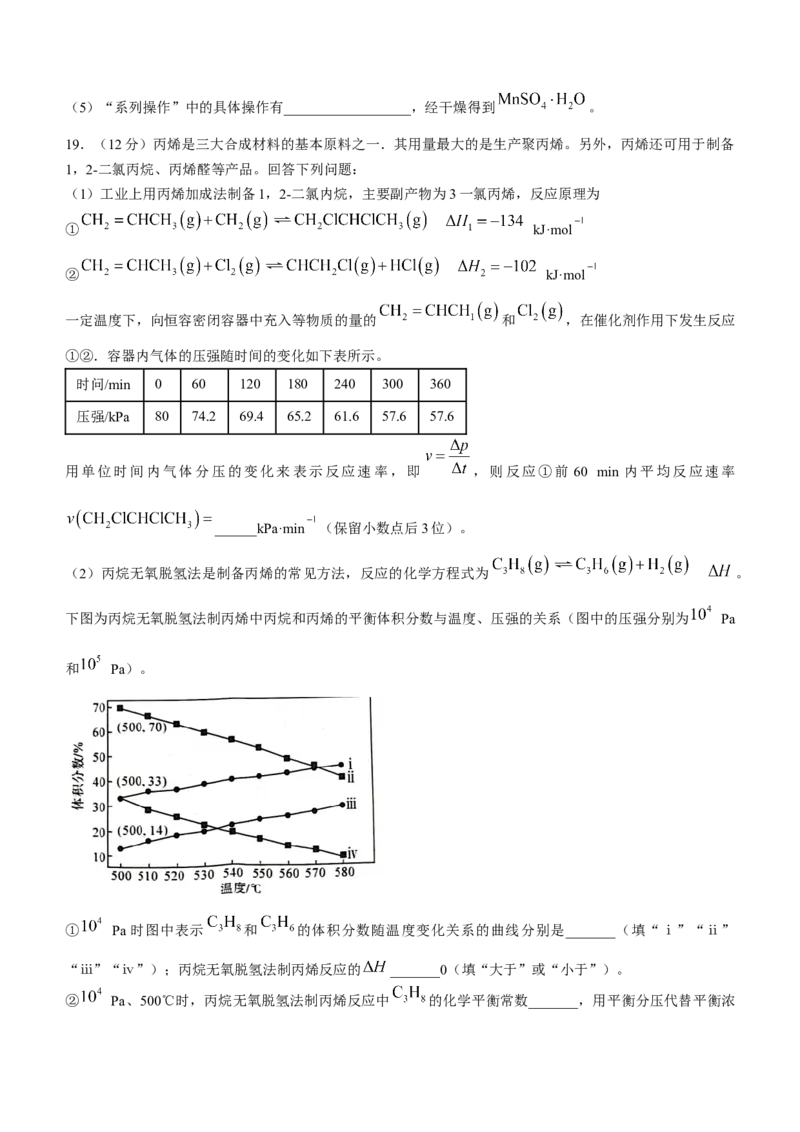
18.(13分)软锰矿的主要成分为 ,还含有 、MgO、 、CaO、 等杂质,工业上用
软锰矿制取 的流程如下:
已知:①部分金属阳离子完全沉淀时的pH如下表。
金属阳离子
完全沉淀时的pH 3.2 5.2 10.4 12.4
②温度高于27℃时, 的溶解度随温度的升高而逐渐降低.
(1)“浸出”过程中通入 的作用是__________________。
(2)第1步除杂中加入 的目的是__________________(用离子方程式表示)。.
(3)第1步除杂中需要调整溶液pH的范围是______到______,调pH时可选择的试剂为______(填字母)。
a.氨水 b. c.CaO d.Mg(
(4)第2步除杂,主要是将 、 转化为相应氟化物沉淀除去,写出 除去 的离子方程式:
________________________,该反应的平衡常数为__________________。
(已知: 的 ; 的 ; 的 )(5)“系列操作”中的具体操作有__________________,经干燥得到 。
19.(12分)丙烯是三大合成材料的基本原料之一.其用量最大的是生产聚丙烯。另外,丙烯还可用于制备
1,2-二氯丙烷、丙烯醛等产品。回答下列问题:
(1)工业上用丙烯加成法制备1,2-二氯内烷,主要副产物为3一氯丙烯,反应原理为
① kJ·mol
② kJ·mol
一定温度下,向恒容密闭容器中充入等物质的量的 和 ,在催化剂作用下发生反应
①②.容器内气体的压强随时间的变化如下表所示。
时问/min 0 60 120 180 240 300 360
压强/kPa 80 74.2 69.4 65.2 61.6 57.6 57.6
用单位时间内气体分压的变化来表示反应速率,即 ,则反应①前 60 min 内平均反应速率
______kPa·min (保留小数点后3位)。
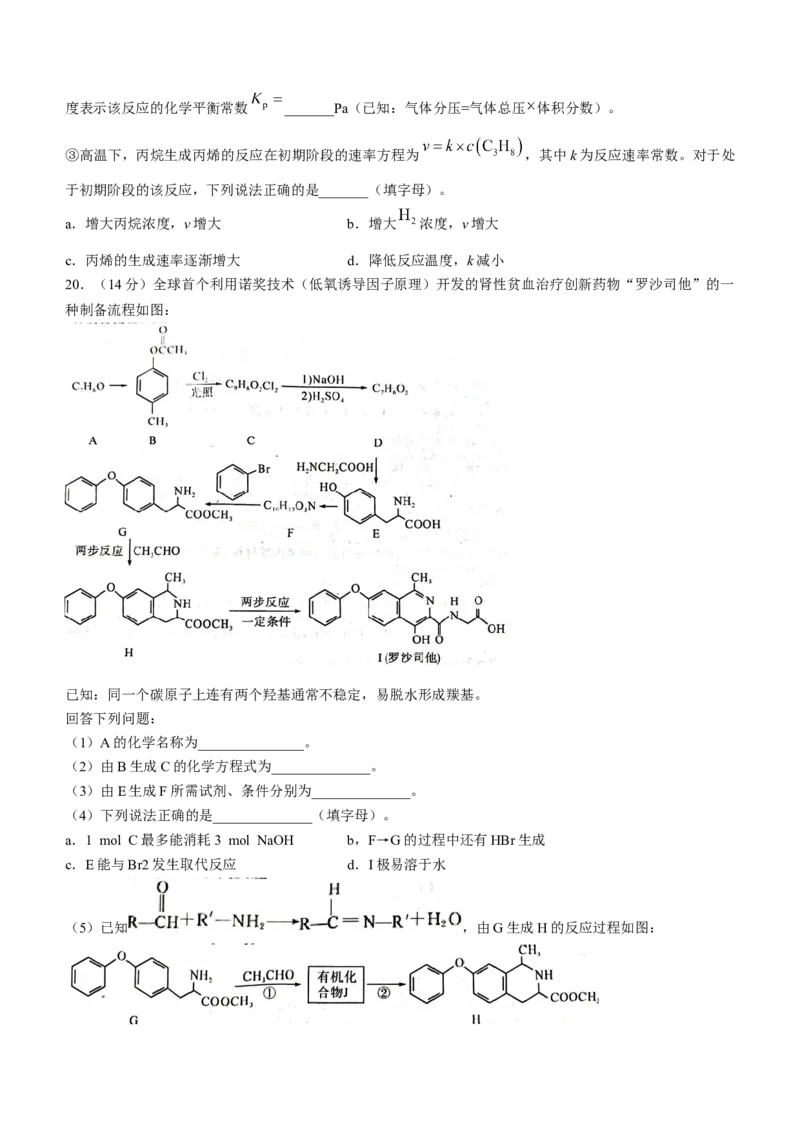
(2)丙烷无氧脱氢法是制备丙烯的常见方法,反应的化学方程式为 。
下图为丙烷无氧脱氢法制丙烯中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强分别为 Pa
和 Pa)。
① Pa时图中表示 和 的体积分数随温度变化关系的曲线分别是_______(填“ⅰ”“ⅱ”
“ⅲ”“ⅳ”);丙烷无氧脱氢法制丙烯反应的 _______0(填“大于”或“小于”)。
② Pa、500℃时,丙烷无氧脱氢法制丙烯反应中 的化学平衡常数_______,用平衡分压代替平衡浓度表示该反应的化学平衡常数 _______Pa(已知:气体分压=气体总压 体积分数)。
③高温下,丙烷生成丙烯的反应在初期阶段的速率方程为 ,其中k为反应速率常数。对于处
于初期阶段的该反应,下列说法正确的是_______(填字母)。
a.增大丙烷浓度,v增大 b.增大 浓度,v增大
c.丙烯的生成速率逐渐增大 d.降低反应温度,k减小
20.(14分)全球首个利用诺奖技术(低氧诱导因子原理)开发的肾性贫血治疗创新药物“罗沙司他”的一
种制备流程如图:
已知:同一个碳原子上连有两个羟基通常不稳定,易脱水形成羰基。
回答下列问题:
(1)A的化学名称为_______________。
(2)由B生成C的化学方程式为______________。
(3)由E生成F所需试剂、条件分别为______________。
(4)下列说法正确的是______________(填字母)。
a.1 mol C最多能消耗3 mol NaOH b,F→G的过程中还有HBr生成
c.E能与Br2发生取代反应 d.I极易溶于水
(5)已知 ,由G生成H的反应过程如图:有机化合物J的结构简式为_______________________;②的反应类型为____________。
(6)D的同分异构体中含有苯环的还有____________种,其中K、L是D的同分异构体:
①K既能发生银镜反应,又能发生水解反应,K在酸催化下发生水解反应的化学方程式为
_____________________________________________________________;
②L能够与饱和碳酸氢钠溶液反应放出 ,L的结构简式为_____________________。