文档内容
热点强化练 11 电解原理在工农业生产中的应用
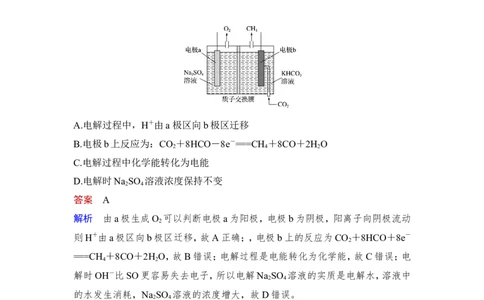
1.(2021·1月江苏省新高考适应性考试,9)利用电解法将CO 转化为CH 的原理如
2 4
图所示。下列说法正确的是( )
INCLUDEPICTURE "G:\\2021课件\\J4A.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\J4A.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\J4A.TIF" \* MERGEFORMATINET
A.电解过程中,H+由a极区向b极区迁移
B.电极b上反应为:CO +8HCO-8e-===CH +8CO+2H O
2 4 2
C.电解过程中化学能转化为电能
D.电解时Na SO 溶液浓度保持不变
2 4
答案 A
解析 由a极生成O 可以判断电极a为阳极,电极b为阴极,阳离子向阴极流动
2
则H+由a极区向b极区迁移,故A正确;,电极b上的反应为CO +8HCO+8e-
2
===CH +8CO+2H O,故B错误;电解过程是电能转化为化学能,故C错误;电
4 2
解时OH-比SO更容易失去电子,所以电解Na SO 溶液的实质是电解水,溶液中
2 4
的水发生消耗,Na SO 溶液的浓度增大,故D错误。
2 4
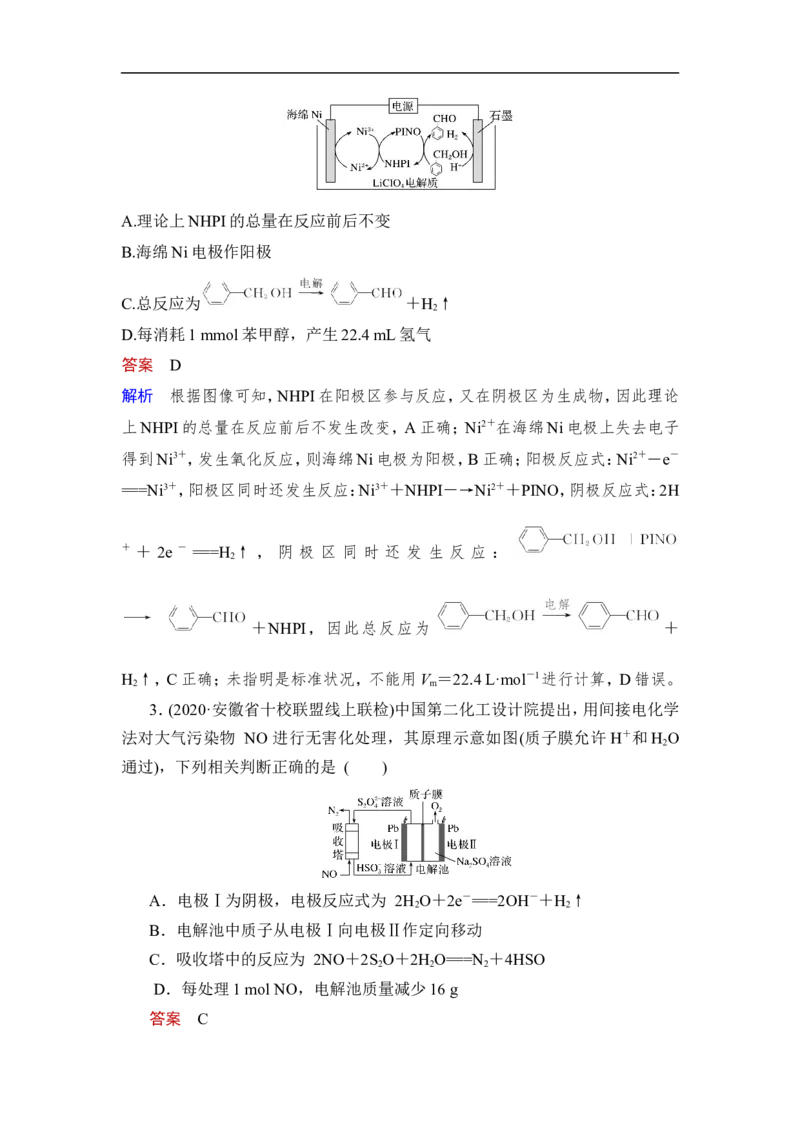
2.(2021·1 月辽宁普高校招生考试适应性测试,9)在 N-羟基邻苯二甲酰亚胺
(NHPI)介质中,可实现醇向醛的转化,原理如图。下列说法错误的是( )
INCLUDEPICTURE "G:\\2021课件\\D9.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\D9.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\D9.TIF" \* MERGEFORMATINETA.理论上NHPI的总量在反应前后不变
B.海绵Ni电极作阳极
C.总反应为 +H ↑
2
D.每消耗1 mmol苯甲醇,产生22.4 mL氢气
答案 D
解析 根据图像可知,NHPI在阳极区参与反应,又在阴极区为生成物,因此理论
上NHPI的总量在反应前后不发生改变,A正确;Ni2+在海绵Ni电极上失去电子
得到Ni3+,发生氧化反应,则海绵Ni电极为阳极,B正确;阳极反应式:Ni2+-e-
===Ni3+,阳极区同时还发生反应:Ni3++NHPI―→Ni2++PINO,阴极反应式:2H
+ + 2e - ===H ↑ , 阴 极 区 同 时 还 发 生 反 应 :
2
+NHPI,因此总反应为 +
H ↑,C正确;未指明是标准状况,不能用V =22.4 L·mol-1进行计算,D错误。
2 m
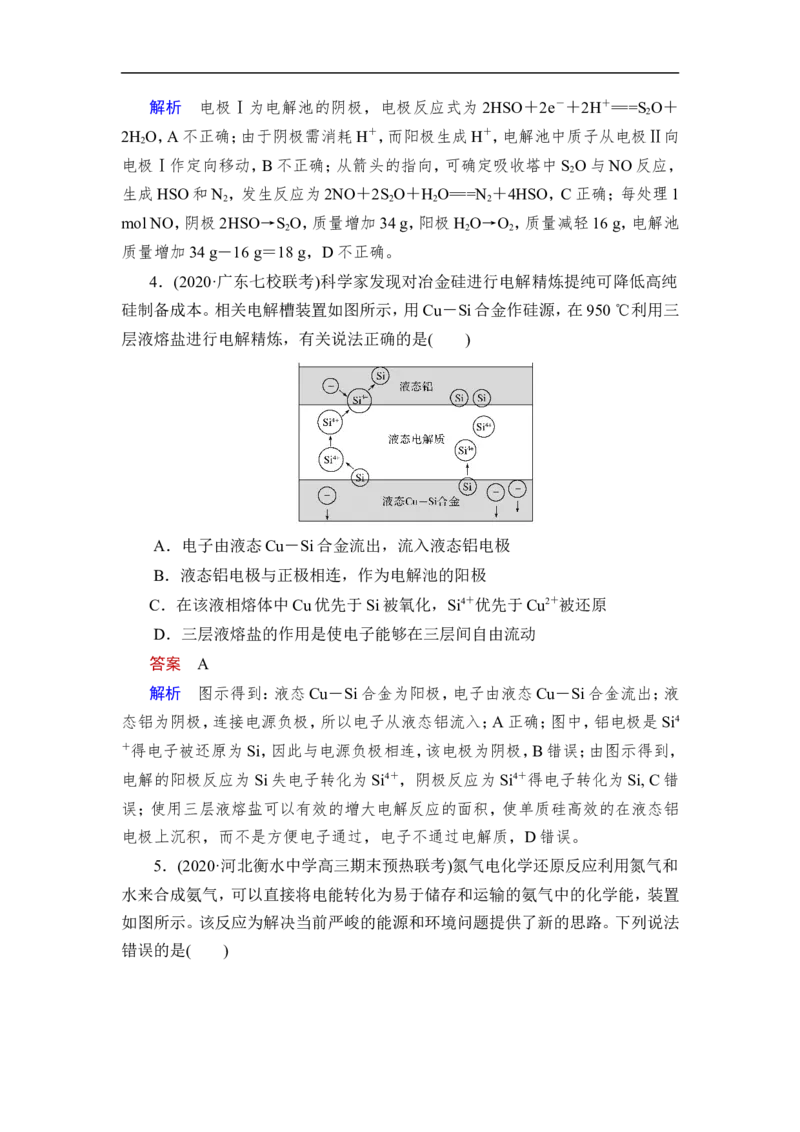
3.(2020·安徽省十校联盟线上联检)中国第二化工设计院提出,用间接电化学
法对大气污染物 NO 进行无害化处理,其原理示意如图(质子膜允许H+和H O
2
通过),下列相关判断正确的是 ( )
A.电极Ⅰ为阴极,电极反应式为 2H O+2e-===2OH-+H ↑
2 2
B.电解池中质子从电极Ⅰ向电极Ⅱ作定向移动
C.吸收塔中的反应为 2NO+2S O+2H O===N +4HSO
2 2 2
D.每处理1 mol NO,电解池质量减少16 g
答案 C解析 电极Ⅰ为电解池的阴极,电极反应式为 2HSO+2e-+2H+===S O+
2
2H O,A不正确;由于阴极需消耗H+,而阳极生成H+,电解池中质子从电极Ⅱ向
2
电极Ⅰ作定向移动,B不正确;从箭头的指向,可确定吸收塔中S O与NO反应,
2
生成HSO和N ,发生反应为2NO+2S O+H O===N +4HSO,C正确;每处理1
2 2 2 2
mol NO,阴极2HSO→S O,质量增加34 g,阳极H O→O ,质量减轻16 g,电解池
2 2 2
质量增加34 g-16 g=18 g,D不正确。
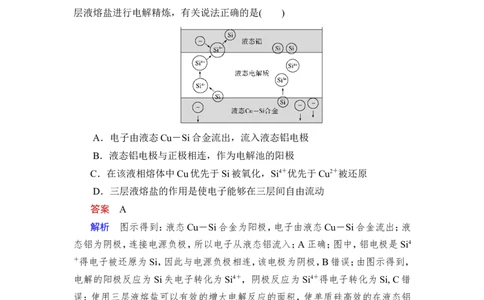
4.(2020·广东七校联考)科学家发现对冶金硅进行电解精炼提纯可降低高纯
硅制备成本。相关电解槽装置如图所示,用Cu-Si合金作硅源,在950 ℃利用三
层液熔盐进行电解精炼,有关说法正确的是( )
A.电子由液态Cu-Si合金流出,流入液态铝电极
B.液态铝电极与正极相连,作为电解池的阳极
C.在该液相熔体中Cu优先于Si被氧化,Si4+优先于Cu2+被还原
D.三层液熔盐的作用是使电子能够在三层间自由流动
答案 A
解析 图示得到:液态Cu-Si合金为阳极,电子由液态Cu-Si合金流出;液
态铝为阴极,连接电源负极,所以电子从液态铝流入;A正确;图中,铝电极是Si4
+得电子被还原为Si,因此与电源负极相连,该电极为阴极,B错误;由图示得到,
电解的阳极反应为Si失电子转化为Si4+,阴极反应为Si4+得电子转化为Si, C错
误;使用三层液熔盐可以有效的增大电解反应的面积,使单质硅高效的在液态铝
电极上沉积,而不是方便电子通过,电子不通过电解质,D错误。
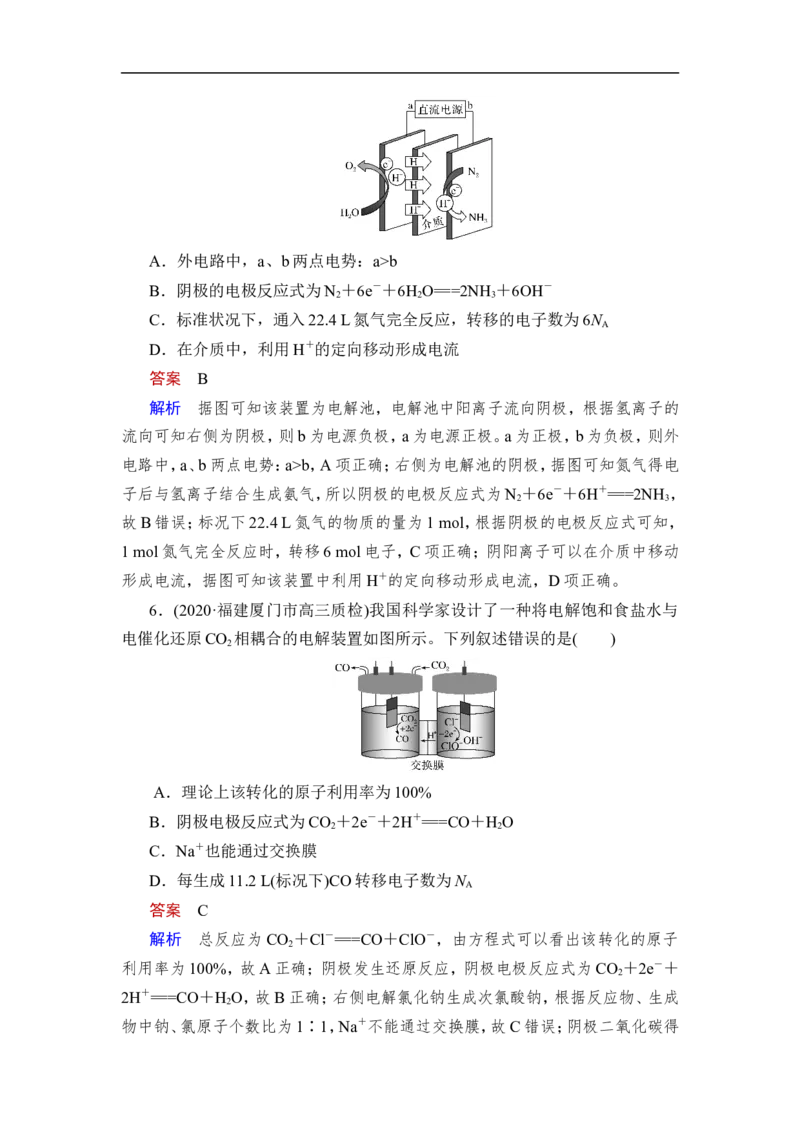
5.(2020·河北衡水中学高三期末预热联考)氮气电化学还原反应利用氮气和
水来合成氨气,可以直接将电能转化为易于储存和运输的氨气中的化学能,装置
如图所示。该反应为解决当前严峻的能源和环境问题提供了新的思路。下列说法
错误的是( )A.外电路中,a、b两点电势:a>b
B.阴极的电极反应式为N +6e-+6H O===2NH +6OH-
2 2 3
C.标准状况下,通入22.4 L氮气完全反应,转移的电子数为6N
A
D.在介质中,利用H+的定向移动形成电流
答案 B
解析 据图可知该装置为电解池,电解池中阳离子流向阴极,根据氢离子的
流向可知右侧为阴极,则b为电源负极,a为电源正极。a为正极,b为负极,则外
电路中,a、b两点电势:a>b,A项正确;右侧为电解池的阴极,据图可知氮气得电
子后与氢离子结合生成氨气,所以阴极的电极反应式为N +6e-+6H+===2NH ,
2 3
故B错误;标况下22.4 L氮气的物质的量为1 mol,根据阴极的电极反应式可知,
1 mol氮气完全反应时,转移6 mol电子,C项正确;阴阳离子可以在介质中移动
形成电流,据图可知该装置中利用H+的定向移动形成电流,D项正确。
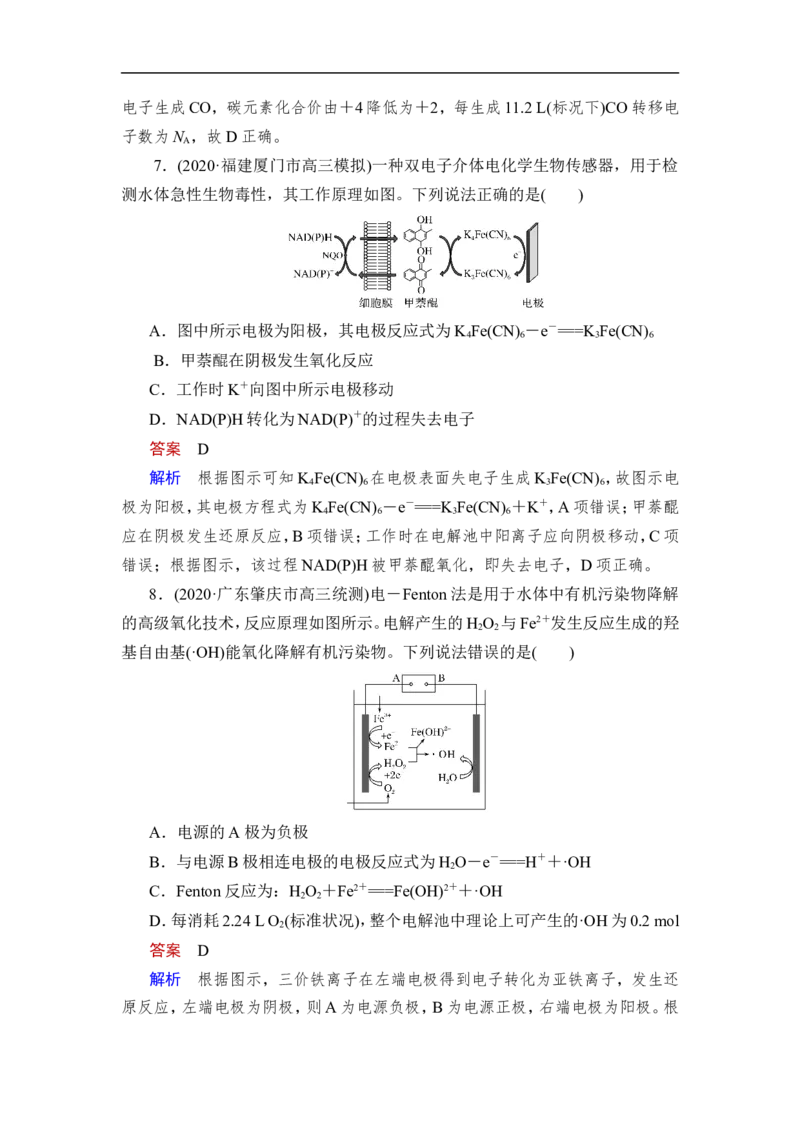
6.(2020·福建厦门市高三质检)我国科学家设计了一种将电解饱和食盐水与
电催化还原CO 相耦合的电解装置如图所示。下列叙述错误的是( )
2
A.理论上该转化的原子利用率为100%
B.阴极电极反应式为CO +2e-+2H+===CO+H O
2 2
C.Na+也能通过交换膜
D.每生成11.2 L(标况下)CO转移电子数为N
A
答案 C
解析 总反应为CO +Cl-===CO+ClO-,由方程式可以看出该转化的原子
2
利用率为100%,故A正确;阴极发生还原反应,阴极电极反应式为CO +2e-+
2
2H+===CO+H O,故B正确;右侧电解氯化钠生成次氯酸钠,根据反应物、生成
2
物中钠、氯原子个数比为1∶1,Na+不能通过交换膜,故C错误;阴极二氧化碳得电子生成CO,碳元素化合价由+4降低为+2,每生成11.2 L(标况下)CO转移电
子数为N ,故D正确。
A
7.(2020·福建厦门市高三模拟)一种双电子介体电化学生物传感器,用于检
测水体急性生物毒性,其工作原理如图。下列说法正确的是( )
A.图中所示电极为阳极,其电极反应式为K Fe(CN) -e-===K Fe(CN)
4 6 3 6
B.甲萘醌在阴极发生氧化反应
C.工作时K+向图中所示电极移动
D.NAD(P)H转化为NAD(P)+的过程失去电子
答案 D
解析 根据图示可知K Fe(CN) 在电极表面失电子生成K Fe(CN) ,故图示电
4 6 3 6
极为阳极,其电极方程式为K Fe(CN) -e-===K Fe(CN) +K+,A项错误;甲萘醌
4 6 3 6
应在阴极发生还原反应,B项错误;工作时在电解池中阳离子应向阴极移动,C项
错误;根据图示,该过程NAD(P)H被甲萘醌氧化,即失去电子,D项正确。
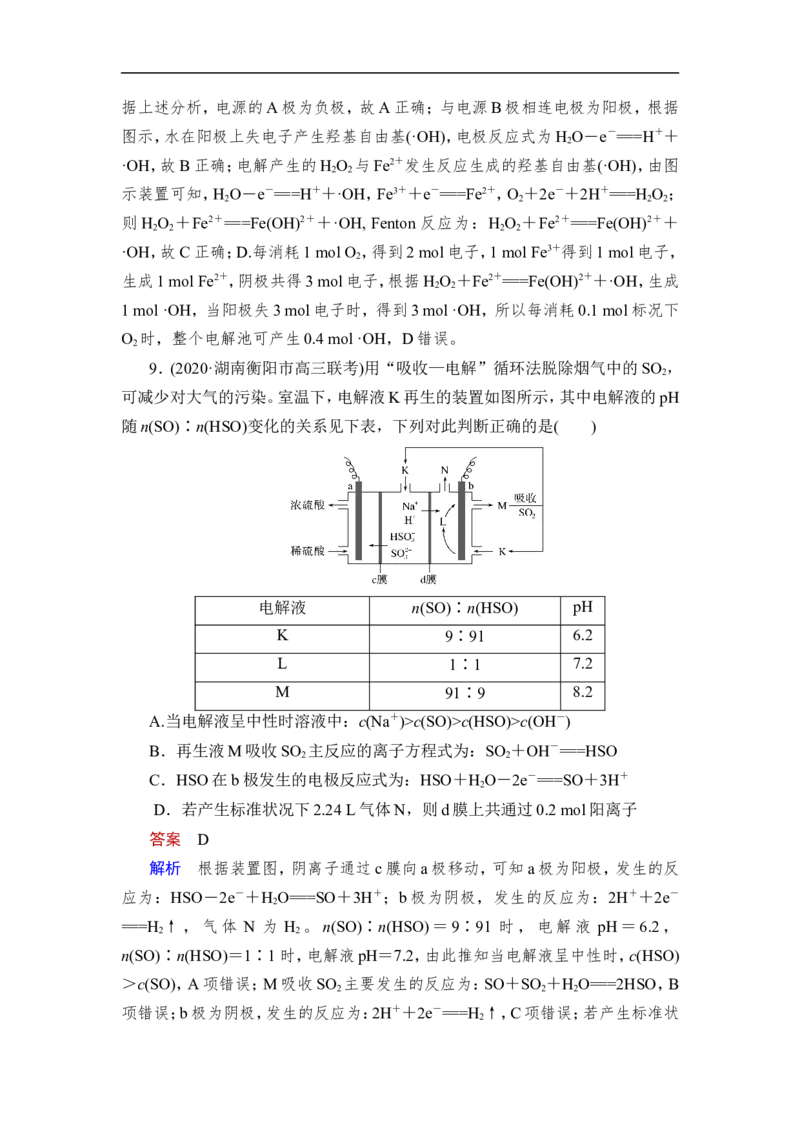
8.(2020·广东肇庆市高三统测)电-Fenton法是用于水体中有机污染物降解
的高级氧化技术,反应原理如图所示。电解产生的H O 与Fe2+发生反应生成的羟
2 2
基自由基(·OH)能氧化降解有机污染物。下列说法错误的是( )
A.电源的A极为负极
B.与电源B极相连电极的电极反应式为H O-e-===H++·OH
2
C.Fenton反应为:H O +Fe2+===Fe(OH)2++·OH
2 2
D.每消耗2.24 L O (标准状况),整个电解池中理论上可产生的·OH为0.2 mol
2
答案 D
解析 根据图示,三价铁离子在左端电极得到电子转化为亚铁离子,发生还
原反应,左端电极为阴极,则A为电源负极,B为电源正极,右端电极为阳极。根据上述分析,电源的A极为负极,故A正确;与电源B极相连电极为阳极,根据
图示,水在阳极上失电子产生羟基自由基(·OH),电极反应式为H O-e-===H++
2
·OH,故B正确;电解产生的H O 与Fe2+发生反应生成的羟基自由基(·OH),由图
2 2
示装置可知,H O-e-===H++·OH,Fe3++e-===Fe2+,O +2e-+2H+===H O ;
2 2 2 2
则 H O +Fe2+===Fe(OH)2++·OH, Fenton 反应为:H O +Fe2+===Fe(OH)2++
2 2 2 2
·OH,故C正确;D.每消耗1 mol O ,得到2 mol电子,1 mol Fe3+得到1 mol电子,
2
生成1 mol Fe2+,阴极共得3 mol电子,根据H O +Fe2+===Fe(OH)2++·OH,生成
2 2
1 mol ·OH,当阳极失3 mol电子时,得到3 mol ·OH,所以每消耗0.1 mol标况下
O 时,整个电解池可产生0.4 mol ·OH,D错误。
2
9.(2020·湖南衡阳市高三联考)用“吸收—电解”循环法脱除烟气中的SO ,
2
可减少对大气的污染。室温下,电解液K再生的装置如图所示,其中电解液的pH
随n(SO)∶n(HSO)变化的关系见下表,下列对此判断正确的是( )
电解液 n(SO)∶n(HSO) pH
K 9∶91 6.2
L 1∶1 7.2
M 91∶9 8.2
A.当电解液呈中性时溶液中:c(Na+)>c(SO)>c(HSO)>c(OH-)
B.再生液M吸收SO 主反应的离子方程式为:SO +OH-===HSO
2 2
C.HSO在b极发生的电极反应式为:HSO+H O-2e-===SO+3H+
2
D.若产生标准状况下2.24 L气体N,则d膜上共通过0.2 mol阳离子
答案 D
解析 根据装置图,阴离子通过c膜向a极移动,可知a极为阳极,发生的反
应为:HSO-2e-+H O===SO+3H+;b极为阴极,发生的反应为:2H++2e-
2
===H ↑,气体 N 为 H 。n(SO)∶n(HSO)=9∶91 时,电解液 pH=6.2,
2 2
n(SO)∶n(HSO)=1∶1时,电解液pH=7.2,由此推知当电解液呈中性时,c(HSO)
>c(SO),A项错误;M吸收SO 主要发生的反应为:SO+SO +H O===2HSO,B
2 2 2
项错误;b极为阴极,发生的反应为:2H++2e-===H ↑,C项错误;若产生标准状
2况下2.24 L气体N(0.1 mol H ),阴极消耗0.2 mol H+,减少0.2 mol正电荷,需要
2
补充0.2 mol正电荷以达到平衡,则d膜上会通过0.2 mol阳离子,D项正确。