文档内容
本章笔答题答题语言规范强化练
1.在80 ℃时,纯水的pH小于7,为什么?
答案 室温时,纯水中的c(H+)=c(OH-)=10-7 mol·L-1,又因水的电离(H O
2
H++OH-)是吸热过程,故温度升高到80 ℃,电离程度增大,致使c(H+)=c(OH
-)>10-7 mol·L-1,即pH<7。
2.甲、乙两瓶氨水的浓度分别为1 mol·L-1和0.1 mol·L-1,则甲、乙两瓶氨水中
c(OH-)之比小于(填“大于”“等于”或“小于”)10。请说明理由。甲瓶氨水浓
度是乙瓶氨水浓度的 1 0 倍,故甲瓶 NH ·H O 的电离程度比乙瓶 NH ·H O 的电离
3 2 3 2
程度小,所以甲、乙两瓶氨水中 c (OH - ) 之比小于 1 0 。
3.利用浓氨水分解制备NH ,应加入NaOH固体,试用化学平衡原理分析NaOH
3
的作用。
答案 NaOH固体溶于氨水后放热促使NH 挥发;增大OH-浓度,使平衡NH +
3 3
H ONH ·H ONH+OH-逆向移动,加快氨气逸出。
2 3 2
4.常温下,0.1 mol·L-1 NaHCO 溶液的pH大于8,则溶液中c(H CO )>(填“>”
3 2 3
“=”或“<”)c(CO),原因是: HCO CO + H + , HCO + H O H CO + OH - ,
2 2 3
HCO 的水解程度大于电离程度 (用离子方程式和必要的文字说明)。
5.(1)若在空气中加热MgCl ·6H O,生成的是Mg(OH)Cl或MgO,写出相应反应
2 2
的 化 学 方 程 式 : MgCl ·6H O ===== M g(OH)Cl + HCl ↑ + 5H O ↑ ,
2 2 2
MgCl ·6H O ===== M gO + 2HCl ↑ + 5H O ↑ 或 Mg(OH)Cl ===== M gO +
2 2 2
HCl ↑ 。
(2)在干燥的HCl气流中加热MgCl ·6H O时,能得到无水MgCl ,其原因是:在干
2 2 2
燥的 HC l 气流中,抑制了 MgC l 的水解,且带走 MgC l ·6H O 受热产生的水蒸气,
2 2 2
故能得到无水 MgC l 。
2
(3)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl 易发生水解,无水
3
CeCl 可用加热CeCl ·6H O和NH Cl固体混合物的方法来制备。其中NH Cl的作
3 3 2 4 4
用是: 分解出 HC l 气体,抑制 CeC l 水解。
3
6.用沉淀溶解平衡解答下列问题。
(1)Mg(OH) 沉淀中混有的Ca(OH) 应怎样除去?写出实验步骤。
2 2
答案 加入MgCl 溶液,充分搅拌,过滤,沉淀用水洗涤。
2
(2)Ba2+有很强的毒性,胃酸酸性很强(pH约为1),医学上进行消化系统的X射线
透视时,服用大量 BaSO 仍然是安全的,其原因是:对于沉淀溶解平衡:
4
BaSO (s) Ba 2 + (aq) + SO(aq) , H + 不会影响 Ba 2 + 或 SO 的浓度,平衡不移动 。
4(3)有一种工艺流程是通过将AgCl沉淀溶于氨水,从含金、银、铜的金属废料中来
提取银。已知在溶解后的溶液中测出含有[Ag(NH ) ]+,试从沉淀溶解平衡移动的
3 2
角度解释 AgCl 沉淀溶解的原因: AgCl 固体在溶液中存在沉淀溶解平衡
AgCl(s) Ag + (aq) + Cl - (aq) ,由于 Ag + 和 NH ·H O 结合成 [Ag(NH ) ] + ,使 Ag +
3 2 3 2
浓度降低,导致 AgC l 的沉淀溶解平衡向着溶解的方向移动 。
(4)几种离子完全沉淀的pH
物质(25 ℃) Fe(OH) Cu(OH) Fe(OH)
2 2 3
完全沉淀时的pH范围 ≥9.6 ≥6.4 ≥3
除去CuSO 酸性溶液中的FeSO ,方法是: 首先滴加 H O ,将 F e 2 + 完全转化为 F e 3
4 4 2 2
+ ,再慢慢加入 CuO [ 或 C u (OH) CO ] ,调至 pH>3 ,过滤 。
2 2 3
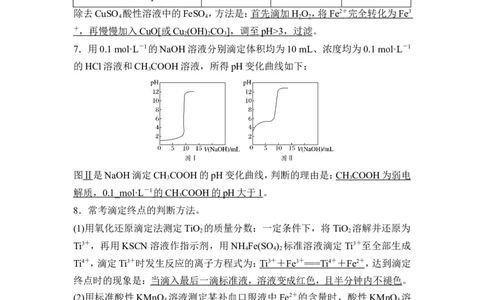
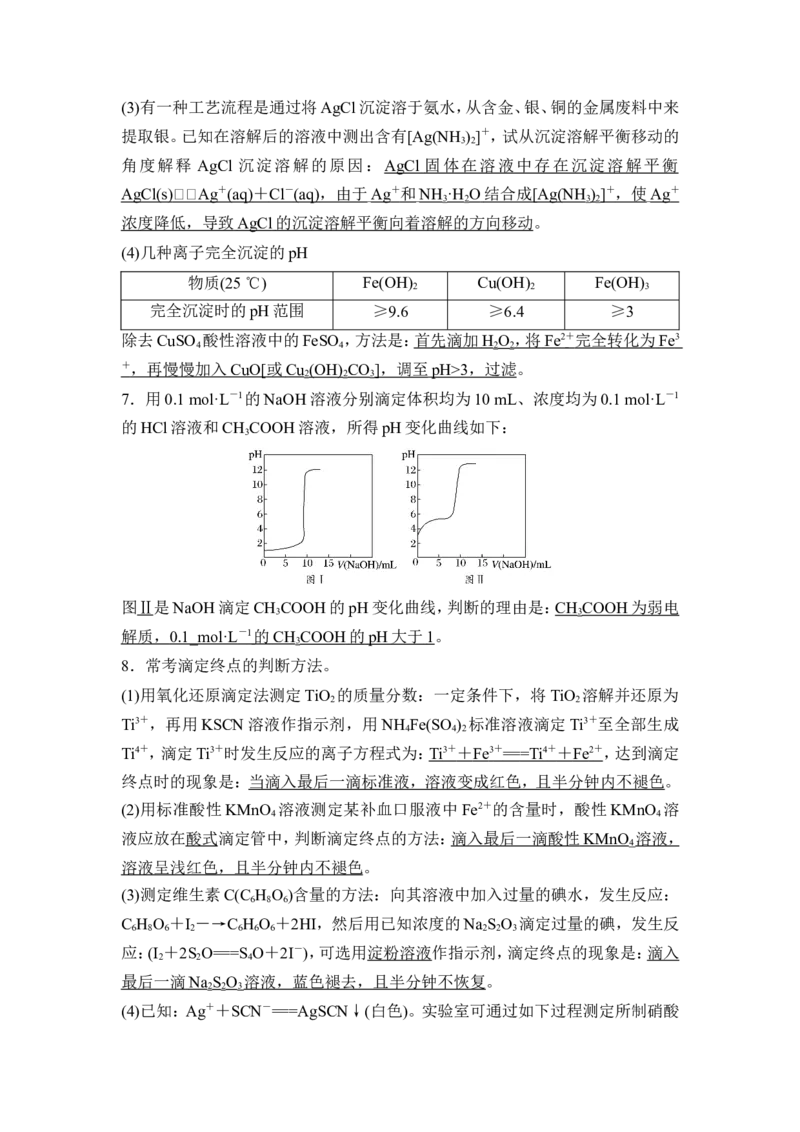
7.用0.1 mol·L-1的NaOH溶液分别滴定体积均为10 mL、浓度均为0.1 mol·L-1
的HCl溶液和CH COOH溶液,所得pH变化曲线如下:
3
图Ⅱ是NaOH滴定CH COOH的pH变化曲线,判断的理由是:CH COOH 为弱电
3 3
解质, 0.1_mol·L - 1 的 CH COOH 的 pH 大于 1 。
3
8.常考滴定终点的判断方法。
(1)用氧化还原滴定法测定TiO 的质量分数:一定条件下,将TiO 溶解并还原为
2 2
Ti3+,再用KSCN溶液作指示剂,用NH Fe(SO ) 标准溶液滴定Ti3+至全部生成
4 4 2
Ti4+,滴定Ti3+时发生反应的离子方程式为: Ti 3 + + Fe 3 + == =Ti 4 + + Fe 2 + ,达到滴定
终点时的现象是:当滴入最后一滴标准液,溶液变成红色,且半分钟内不褪色。
(2)用标准酸性KMnO 溶液测定某补血口服液中Fe2+的含量时,酸性KMnO 溶
4 4
液应放在酸式滴定管中,判断滴定终点的方法: 滴入最后一滴酸性 KMnO 溶液,
4
溶液呈浅红色,且半分钟内不褪色。
(3)测定维生素C(C H O )含量的方法:向其溶液中加入过量的碘水,发生反应:
6 8 6
C H O +I ―→C H O +2HI,然后用已知浓度的Na S O 滴定过量的碘,发生反
6 8 6 2 6 6 6 2 2 3
应:(I +2S O===S O+2I-),可选用淀粉溶液作指示剂,滴定终点的现象是:滴入
2 2 4
最后一滴 N a S O 溶液,蓝色褪去,且半分钟不恢复。
2 2 3
(4)已知:Ag++SCN-===AgSCN↓(白色)。实验室可通过如下过程测定所制硝酸银样品的纯度(杂质不参与反应)。
①称取2.000 g硝酸银样品,加水溶解,定容到100 mL。溶液配制过程中所用的玻
璃仪器除烧杯、玻璃棒外还有 100_mL 容量瓶、胶头滴管 。
②准确量取25.00 mL溶液,酸化后滴入几滴铁铵矾[NH Fe(SO ) ]溶液作指示剂,
4 4 2
再用0.100 mol·L-1 NH SCN标准溶液滴定。滴定终点的实验现象为:溶液变为红
4
色,且半分钟内不褪色。