文档内容
第 03 讲 物质的量在化学方程式计算中的应用
目录
01 模拟基础练
【题型一】根据方程式进行计算
【题型二】关系式法在化学计算中的应用
【题型三】差量法在化学计算中的应用
【题型四】守恒法在化学计算中的应用
02 重难创新练
03 真题实战练
题型一 根据化学方程式进行计算
1.向500 mL氢氧化钠溶液中投入10.8 g铝,二者恰好完全反应,计算回答:
(1)铝的物质的量是 。
(2)氢氧化钠溶液的物质的量浓度是 。
(3)在标准状况下生成氢气的体积是 。
【答案】(1) 0.4 mol (2)0.8 mol·L-1 (3) 13.44 L
【解析】(1)铝的摩尔质量是27 g·mol-1,n(Al)==0.4 mol。
(2)设参加反应的氢氧化钠的物质的量是n,
则2Al+2HO+2NaOH===2NaAlO+3H↑
2 2 2
2 mol 2 mol
0.4 mol n
则=,n=0.4 mol,c(NaOH)==0.8 mol·L-1。
(3)设生成标准状况下的氢气的体积是V,
2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
2 mol 3×22.4 L
0.4 mol V
所以V==13.44 L。
2.把10.2 g镁铝合金的粉末放入过量的烧碱溶液中,在标准状况下生成6.72 L氢气。试计算:
(1)该合金中铝的质量分数是 。(2)该合金中镁与铝的物质的量之比是 。
(3)该合金溶于足量的盐酸溶液中,标准状况下产生氢气的体积是 。
【答案】(1)52.9% (2)1∶1 (3)11.2 L
【解析】(1)把镁铝合金的粉末放入过量的烧碱溶液中,镁不反应,只有铝能与氢氧化钠溶液反应。设
铝的物质的量为n(Al),则:
2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
2 mol 3×22.4 L
n(Al) 6.72 L
解得:n(Al)=0.2 mol,m(Al)=0.2 mol×27 g·mol-1=5.4 g,铝的质量分数为×100%≈52.9%。
(2)m(Mg)=10.2 g-5.4 g=4.8 g,n(Mg)==0.2 mol,则n(Al)∶n(Mg)=1∶1。
(3)设由铝生成的氢气为V(H ),由镁生成的氢气为V(H ),由铝和镁与盐酸的反应可知:
1 2 2 2
2Al+6HCl===2AlCl +3H↑
3 2
2 mol 3×22.4 L
0.2 mol V(H )
1 2
解得:V(H )=6.72 L;
1 2
Mg+2HCl===MgCl +H↑
2 2
1 mol 22.4 L
0.2 mol V(H )
2 2
解得:V(H )=4.48 L,V (H )=V(H )+V(H )=6.72 L+4.48 L=11.2 L。
2 2 总 2 1 2 2 2
3.把1.1 g铁、铝混合物溶于200 mL 5 mol·L-1盐酸中,反应后盐酸的浓度变为4.6 mol·L-1(溶液体积
变化忽略不计)。求:
(1)反应中消耗HCl的物质的量。
(2)该混合物中铝、铁的物质的量。
【答案】(1)0.08 mol (2)0.02 mol 0.01 mol
【解析】(1)消耗HCl的物质的量:0.2 L×5 mol·L-1-0.2 L×4.6 mol·L-1=0.08 mol。
(2)设Al、Fe的物质的量分别为x、y。
2Al + 6HCl===2AlCl +3H↑
3 2
2 mol 6 mol
x 3x
Fe + 2HCl ===FeCl +H↑
2 2
1 mol 2 mol
y 2y
得x=0.02 mol,y=0.01 mol。
4.已知MnO 与浓盐酸反应的化学方程式为MnO + 4HCl(浓) MnCl +Cl↑+2H O,回答下列问题:
2 2 2 2 2
(1)该反应的离子方程式为___________________________。(2)被氧化的HCl占HCl总量的________。
(3)当标准状况下有11.2 L氯气生成时,该反应转移的电子数为________(设N 为阿伏加德罗常数的值)。
A
(4)1.74 g MnO 与100 mL 12 mol·L-1的过量浓盐酸完全反应(假设HCl无挥发),在反应后的溶液中加入
2
足量的AgNO 溶液,可生成________g沉淀。
3
【答案】(1)MnO +4H++2Cl- Mn2++Cl↑+2H O
2 2 2
(2) (3)N (4)166.46
A
【解析】(1)书写该反应的离子方程式时,HCl、MnCl 要拆写成离子形式,故反应的离子方程式为
2
MnO +4H++2Cl- Mn2++Cl↑+2H O(2)该反应中一半HCl作还原剂,一半HCl作酸(3)当标准状况下有11.2 L
2 2 2
氯气生成时,该反应转移的电子数为 N (4)n(MnO )= =0.02 mol,n(HCl)=12 mol·L-1×0.1 L=1.2
A 2
mol。反应中被氧化的n(HCl)=n(MnO )×2=0.04 mol,反应后溶液中n(Cl-)=1.2 mol-0.04 mol=1.16 mol,加入
2
足量的AgNO 溶液生成1.16 mol AgCl,m(AgCl)=1.16 mol×143.5 g·mol-1=166.46 g。
3
5.钢铁制品经常进行烤蓝处理,即在铁制品的表面生成一层致密的Fe O 。某学习小组为了研究烤蓝
3 4
铁片,分别进行了以下实验操作:
①把一定量烤蓝铁片加工成均匀粉末。
②取m g该粉末,放入28.00 mL 1 mol·L-1的盐酸中,恰好完全反应,生成标准状况下的气体134.4
mL,向溶液中滴入KSCN溶液,无明显现象。
完成下列各题:
(1)将反应后的溶液稀释至100 mL,则溶液中c(Fe2+) = 。
(2)样品中n(Fe)∶n(Fe O) = 。
3 4
【答案】(1)0.14 mol·L-1 (2)4∶1
【解析】(1)m g该粉末,与28.00 mL 1 mol·L-1的盐酸恰好完全反应,溶液中的溶质为FeCl ,n(HCl) =
2
0.028 mol,根据Cl守恒,可知FeCl 的物质的量为0.014 mol,溶液稀释至100 mL后, c(Fe2+) = 0.014 mol
2
÷ 0.1 = 0.14 mol·L-1;(2)生成H 的物质的量为0.006 mol,Fe和 Fe O 混合固体与HCl溶液发生如下三个反
2 3 4
应:Fe+ 2HCl = FeCl + H ↑;Fe O + 8HCl = 2FeCl + FeCl + 4H O;Fe + FeCl = 3FeCl 。先根据氢气的
2 2 3 4 3 2 2 3 2
物质的量算出与HCl反应的Fe的物质的量和消耗HCl的量:
Fe+ 2HCl = FeCl + H ↑
2 2
1 2 1
0.006 0.012 0.006
则剩余的HCl的物质的量为0.028-0.012=0.016mol,算出Fe O 的物质的量:
3 4
Fe O + 8HCl = 2FeCl + FeCl + 4H O
3 4 3 2 2
1 8 2
0.002 0.016 0.04根据生成的FeCl 的物质的量,算出与FeCl 反应的Fe的物质的量:
3 3
Fe + 2FeCl = 3FeCl
3 2
1 2
0.02 0.04
综上,n(Fe)=0.06 + 0.02=0.08 mol,n(Fe O)=0.02 mol,n(Fe)∶n(Fe O) =4∶1。
3 4 3 4
6.称取天然碱样品4份,溶于水后,分别逐滴加入相同浓度的盐酸溶液30mL,产生CO 的体积(标准
2
状况)如下表:
Ⅰ Ⅱ Ⅲ IV
盐酸体积/mL 30 30 30 30
样品/g 3.32 4.15 5.81 7.47
二氧化碳体积/mL 672 840 896 672
(1)若用2.49g样晶进行同样的实验时,产生CO___________mL(标准状况)。
2
(2)另取3.32g天然碱样品于300 ℃加热分解至完全,产生CO 112mL(标准状况)和水0.45g,确定该天
2
然碱的化学式___________。
(3)由上表中第Ⅳ组数据确定盐酸溶液的浓度___________mol·L-1.
【答案】(1)504 (2)2Na CO·NaHCO ·2H O (3)2.5
2 3 3 2
【解析】(1)盐酸的体积一定,实验Ⅰ、Ⅱ、Ⅲ中随样品质量增大,产生CO 的体积增大,而实验Ⅳ中
2
却减小,说明Ⅰ、Ⅱ中盐酸有剩余,若用2.49 g样品进行同样的实验时,则样品中碳元素全部转移到CO
2
中,根据定比关系,则产生CO 的体积为: ;(2)加热分解生成的二氧化碳,说
2
明该天然碱中含有NaHCO ,生成CO 的物质的量为 ,根据分解方程式:
3 2
2NaHCO NaCO+CO ↑+H O,可知3.32 g样品中NaHCO 的物质的量为 ,分解
3 2 3 2 2 3
生成的水为0.005 mol,3.32 g样品与盐酸反应生成二氧化碳为: ,根据碳原子守
恒,3.32 g样品中NaCO 的物质的量为: ,3.32 g样品中结晶水物质的量
2 3为: ,故3.32 g样品中n(Na CO):n(NaHCO ) :n(H O)=0.02 mol:0.01
2 3 3 2
mol:0.02 mol=2:1:2,则该天然碱的组成为:2NaCO·NaHCO ·2H O;(3)可知7.47 g样品中,NaCO
2 3 3 2 2 3
为物质的量为: ,根据NaCO+HCl=NaCl+NaHCO ,可知消耗HCl为0.045
2 3 3
mol,生成CO 的物质的量为: ,由NaHCO +HCl═NaCl+CO ↑+H O,可知消耗的
2 3 2 2
HCl为0.03 mol,故30mL溶液中HCl的总量为: ,则盐酸的物质的量浓
度为: 。
题型二 关系式法在化学计算中的应用
7.把氯气通入浓氨水中,会立即发生反应:3Cl+8NH·H O=6NH Cl+N +8H O。在标准状况下,把
2 3 2 4 2 2
1.12 L Cl 、N 的混合气体(90% Cl 和10% N ,均为体积分数)通入浓氨水,实验测得逸出标准状况下的气
2 2 2 2
体体积为0.672 L(其中有50% Cl 和50% N ),此反应中被氧化的NH 的质量为( )
2 2 3
A.3.4 g B.0.34 g C.1.36 g D.4.48 g
【答案】B
【解析】由反应方程式可得出每3 mol Cl (反应气)生成1 mol N (生成气)时,气体物质的量减少了2
2 2
mol,即体积减小44.8 L(标准状况下),这一量即为“理论差量”,而这一差量所对应的被氧化的氨的物质
的量为2 mol,再从题中所给的数据可以求出“实际差量”为(1.12-0.672) L=0.448 L。即:
3Cl~2NH ~ N ΔV
2 3 2
2 mol×17 g·mol-1 44.8 L
m(被氧化的NH ) 0.448 L
3
列出比例式:(2 mol×17 g·mol-1)∶m(被氧化的NH )=44.8 L∶0.448 L,则m(被氧化的NH )=0.34 g。
3 3
8. 用“间接碘量法”测定CuCl ·2H O样品的纯度,过程如下:取0.400 0 g试样溶于水,加入过量KI
2 2
固体,充分反应,生成白色CuI沉淀,滴入几滴淀粉溶液作指示剂,用0.100 0 mol·L-1 Na SO 标准溶液滴
2 2 3
定,到达滴定终点时,消耗Na
2
S
2
O
3
标准溶液20.00 mL。(滴定反应为I
2
+2S 2O2-=S 4O2-+2I-)
3 6
(1)写出生成白色CuI沉淀的离子方程式:____________________________。
(2)该样品中CuCl ·2H O的质量分数为______________。
2 2【答案】(1) 2Cu2++4I-=2CuI↓+I (2) 85.50%
2
【解析】(1)CuCl 与过量的KI发生氧化还原反应,产生CuI、I 、KCl,反应的离子方程式为2Cu2++4I-
2 2
=2CuI↓+I
2
。(2)根据反应方程式2Cu2++4I-=2CuI↓+I
2
、I
2
+2S 2O2-=S 4O2-+2I-可得关系式:2Cu2+~I
2
~2S 2O2-,
3 6 3
n(Na SO)=0.100 0 mol·L-1×0.02 L=0.002 00 mol,则 n(Cu2+)=0.002 00 mol,根据 Cu 元素守恒,可得
2 2 3
m(CuCl ·2HO)=0.002 00 mol×171 g·mol-1=0.342 0 g,所以该样品中 CuCl ·2HO 的质量分数为(0.342 0
2 2 2 2
g÷0.400 0 g)×100%=85.50%。
9.化学需氧量(COD)是衡量水质的重要指标之一,COD 是指在特定条件下用一种强氧化剂(如
KMnO )定量地氧化水体中的还原性物质所消耗的氧化剂的量(折算为氧化能力相当的O 质量,单位:
4 2
mg·L-1)。某水样的COD测定过程如下:取100.0 mL水样,用硫酸酸化,加入10.00 mL 0.002 000 mol·L-1
KMnO 溶液,充分作用后,再加入10.00 mL 0.005 000 mol·L-1 Na C O 溶液。用0.002 000 mol·L-1 KMnO
4 2 2 4 4
溶液滴定,滴定终点时消耗6.50 mL。
已知:2Mn O-+5C 2O2-+16H+=2Mn2++10CO
2
↑+8H
2
O。
4 4
(1)1 mol KMnO 的氧化能力与_____________g O 的氧化能力相当(作氧化剂时转移的电子数相同)。
4 2
(2)该水样的COD值是_____________mg·L-1。(写出计算过程,结果保留小数点后一位)
【答案】(1)40 (2)5.2
【解析】由最后KMnO 溶液滴定多余的NaC O 溶液,可求出剩余NaC O 的量与水样消耗KMnO 溶
4 2 2 4 2 2 4 4
液后剩余KMnO 的量,从而求出水样消耗KMnO 的量,再转化为O 的量即可算出该水样中的COD。 (1)
4 4 2
5
由得失电子守恒可知,5O~4KMnO ,则1 mol KMnO 的氧化能力与1 mol× =1.25 mol O 的氧化能力相当,
2 4 4 4 2
即与1.25 mol×32 g·mol-1=40 g O 的氧化能力相当。(2)根据方程式可知2KMnO ~5Na C O ,剩余KMnO 的
2 4 2 2 4 4
2
物质的量为0.005 mol·L-1×10×10-3 L× -6.5×10-3 L×0.002 mol·L-1=7×10-6 mol,则水样中消耗KMnO 的物质
5 4
的量为 0.01 L×0.002 mol·L-1-7×10-6 mol=1.3×10-5 mol,又由得失电子守恒可知,5O~4KMnO ,则
2 4
5
n(O )=1.3×10-5 mol× =1.625×10-5 mol,m(O )=1.625×10-5 mol×32 g·mol-1=5.2×10-4 g=0.52 mg,则该水样的
2 4 2
0.52 mg
COD值为 =5.2 mg·L-1。
0.1 L
10.金属锡的纯度可以通过下述方法分析:将试样溶于盐酸,反应的化学方程式为
Sn+2HCl=SnCl +H ↑,再加入过量的FeCl 溶液,发生反应SnCl +2FeCl =SnCl +2FeCl ,最后用已知浓度的
2 2 3 2 3 4 2
KCr O 溶液滴定生成的Fe2+,反应的化学方程式为6FeCl +K Cr O+14HCl=6FeCl +2KCl+2CrCl +7H O。现
2 2 7 2 2 2 7 3 3 2
有金属锡试样0.613 g,经上述反应后,共用去0.100 mol·L-1 KCr O 溶液16.00 mL。求试样中锡的质量分
2 2 7数_____________ (假定杂质不参加反应,锡的相对原子质量为119)。
【答案】93.2%
【解析】Sn与KCr O 物质的量的关系:
2 2 7
3Sn~3SnCl ~6FeCl ~K Cr O
2 2 2 2 7
3×119 g 1 mol
m(Sn) 0.100 mol·L-1×0.016 L
m(Sn)=3×119 g×0.100mol·L-1×0.016 L=0.571 2 g,w(Sn)=0.571 2 g×100%≈93.2%。
1mol 0.613 g
11.一定条件下,将TiO 溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH Fe(SO ) 标准溶液滴定
2 4 4 2
Ti3+至全部生成Ti4+。称取TiO 样品0.60 g,消耗0.20 mol·L-1的NH Fe(SO ) 溶液36.75 mL,则样品中TiO
2 4 4 2 2
的质量分数是 98% 。
【答案】8%
【解析】根据得失电子守恒,将TiO 溶解并还原为Ti3+,Ti3+与NH Fe(SO ) 溶液反应,有关系式
2 4 4 2
TiO~Ti3+~NHFe(SO ) ,消耗 0.20 mol·L-1的 NH Fe(SO ) 溶液 36.75 mL,即 NH Fe(SO ) 的物质的量为
2 4 4 2 4 4 2 4 4 2
36.75×10-3 L×0.20 mol·L-1=7.35×10-3 mol,则TiO 的物质的量为7.35×10-3 mol,所以样品中TiO 的质量分
2 2
数是7.35×10-3mol×80 g·mol-1
×100%=98%。
0.60 g
题型三 差量法在化学计算中的应用
12.工业纯碱中常含有少量的NaCl杂质,某化学兴趣小组取m g纯碱样品与足量稀盐酸充分反应,加
热、蒸干、灼烧,得n g固体.则该样品中纯碱的质量分数为 ( A)
106(n-m) 168(m-n) 84(n-m)
A. ×100% B. ×100% C. ×100% D.
11m 56m 11m
n-m
×100%
m
【答案】A
【解析】设碳酸钠的质量为x,则:
NaCO+2HCl=2NaCl+CO ↑+H O 固体质量增加
2 3 2 2
106 117 11
106(n-m)
x(n-m) g,106= 11 ,解得x=106(n-m) g,故该样品中纯碱的质量分数为 g
11
x (n-m) g 11
mg106(n-m)
×100%= ×100%。
11m
13.200℃时将 16.0g NaOH 和 NaHCO 的混合物放在密闭容器中加热到质量不再减少为止,称得剩
3
余固体质量为 14.8g,试回答:
(1)剩余固体的化学式是__________。
(2)原混合物中 NaOH 的质量分数__________。
【答案】(1)NaOH 、NaCO (2)65%
2 3
【解析】在密闭容器中进行反应,可能的反应有:NaOH+NaHCO NaCO+HO、2NaHCO
3 2 3 2 3
NaCO+CO↑+HO,假设NaOH与NaHCO 恰好完全反应,则:
2 3 2 2 3
NaOH+NaHCO NaCO+HO m
3 2 3 2
40 84 18
△
x y 16g-14.8g=1.2g
解得:x=2.67g、y=5.6g,因x+y<16g,故16gNaOH和NaHCO 固体混合物不能恰好反应,所以存在
3
过量问题,由于NaHCO 受热能分解,NaOH不能,因而过量物质为NaOH。(1)由上述分析可知剩余固体
3
物质是NaOH、NaCO ;(2)原混合物中m(NaOH)=16g-5.6g=10.4g,因此原混合物中NaOH的质量分数为
2 3
10.4g/16g×100%=65%。
14.臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来
制取臭氧:3O 2O。
2 3
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为_____________g·mol-1(保留
一位小数)。
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为_____________L。
【答案】(1)35.6 (2)3
【解析】(1)设原有1 mol O ,则有
2
3O 2O Δn
2 3
3 mol 2 mol 1 mol
0.3 mol 0.1 mol
则
M
= m 总= 32 g ≈35.6 g·mol-1。
n 0.9mol
总
(2)3O 2O ΔV
2 3
3体积 2体积 1体积
V 8 L-6.5 L=1.5 L解得V=3 L。
题型四 守恒法在化学计算中的应用
15.(2024•云南省大理市期末)有200mlMgCl 和AlCl 的混合物,其中c(Mg2+)为0.2mol/L,c(C1-)为
2 3
1.3mol/L。为使Mg2+全部转化为沉淀分离出来,至少需加4mol/L溶液的NaOH体积为( )
A.40ml B.72ml C.80ml D.128ml
【答案】C
【解析】MgCl 和AlCl 的混合溶液,其中Mg2+浓度为0.2mol•L-1,Cl-浓度为1.3mol•L-1,设Al3+的浓度
2 3
为x,由电荷守恒可知,0.2mol/L×2+x×3=1.3mol/L×1,解得x=0.3mol/L,则Mg2+、Al3+的物质的量分别为
0.2L×0.2mol/L=0.04mol、0.2L×0.3mol/L=0.06mol,欲使Mg2+全部沉淀分离出来,Mg2++2OH-=Mg(OH) ↓,
2
Al3++4OH-=AlO -+2H O,则需n(NaOH)=0.04mol×2+0.06mol×4=0.32mol, V(NaOH)=
2 2
=0.08L=80.0mL,故选C。
16.14 g铜金合金与足量的某浓度硝酸反应,将产生的气体与 2.24 L(标准状况)O 混合,通入水中,
2
气体恰好被完全吸收,则合金中铜的质量为( )
A.9.6 g B.6.4 g C.12.8 g D.1.6 g
【答案】C
【解析】根据守恒法计算,金不与硝酸反应,铜金合金中只有铜与硝酸反应,据整个过程中转移电子
守恒可知,Cu失去电子总数等于 O 得到电子总数,则有 n(Cu)×2=n(O )×4,解得n(Cu)=2×2.24 L÷22.4
2 2
L·mol-1=0.2 mol,故合金中铜的质量为m(Cu)=0.2 mol×64 g·mol-1=12.8 g。
17.碳酸铜和碱式碳酸铜[Cu (OH) CO]均可溶于盐酸,转化为氯化铜。在高温下这两种化合物均能分
2 2 3
解成氧化铜。溶解28.4 g上述混合物,消耗1 mol·L-1盐酸500 mL。煅烧等质量的上述混合物,得到氧化铜
的质量是 ( )
A.35 g B.30 g C.20 g D.15 g
【答案】C
【解析】碳酸铜和碱式碳酸铜均可溶于盐酸,转化为氯化铜,溶解28.4 g混合物,消耗1 mol·L-1盐酸
500 mL,HCl的物质的量为0.5 mol,根据氯原子守恒则CuCl 的物质的量为0.25 mol。根据铜原子守恒可
2
知,原混合物中含有Cu的物质的量为0.25 mol,灼烧等质量的上述混合物,得到氧化铜的物质的量为 0.25
mol,则m(CuO)=0.25 mol×80 g·mol-1=20 g。
18.向500 mL稀硝酸中加入一定量的铁粉,铁粉完全溶解后,放出NO 6.272 L(标准状况下),同时溶
液质量增加11.2 g。下列判断不正确的是 ( )
A.原HNO 的物质的量浓度为2.24 mol·L-1
3
B.原溶液中投入铁粉的物质的量是0.2 molC.反应后溶液中c(Fe3+)∶c(Fe2+)=2∶3
D.反应后的溶液还可以溶解铜粉4.48 g
【答案】B
【解析】标准状况下6.272 L NO为0.28 mol,假设反应后生成Fe2+、Fe3+的物质的量分别为x、y,据得
失电子守恒可得0.28 mol×(5-2)=2x+3y;反应后溶液质量增加 11.2 g,则有56 g·mol-1 (x+y)-0.28 mol×30
g·mol-1=11.2 g , 联 立 上 述 两 式 解 得 : x=0.21 mol , y=0.14 mol , 则 反 应 后 溶 液 中
c(Fe3+)∶c(Fe2+)=n(Fe3+)∶n(Fe2+)=0.14 mol∶0.21 mol=2∶3,C项正确。据铁原子守恒可知,原溶液中投入
铁粉的物质的量为 0.21 mol+0.14 mol=0.35 mol,B 项错误。据 N 原子守恒可知,原 HNO 溶液中
3
1.12mol
n(HNO)=0.21 mol×2+0.14 mol×3+0.28 mol=1.12 mol,则有c(HNO)= =2.24 mol·L-1,A项正确。
3 3 0.5 L
反应后的溶液为 Fe(NO ) 和Fe(NO ) 混合液,加入铜粉,发生反应:2Fe3++Cu=2Fe2++Cu2+,则0.14 mol
3 2 3 3
Fe3+可溶解0.07 mol Cu,可溶解铜粉的质量为0.07 mol×64 g·mol-1=4.48 g,D项正确。
19.将13.6 g Fe、Fe O 和CuO的混合粉末加入100 mL一定物质的量浓度的盐酸中,充分反应,生成
2 3
标准状况下的氢气896 mL,过滤,滤渣经洗涤、干燥后得到1.28 g固体纯净物,经检验滤液中只含有一种
溶质。请回答:
(1)固体混合物中CuO的质量为_____________。
(2)盐酸的浓度为_____________。
【答案】(1)1.60 (2) 3.60 mol·L-1
【解析】[解析] (1)因反应后滤液中只含有一种溶质,应为 FeCl ,得到的1.28 g固体纯净物为Cu,
2
n(Cu)=0.02 mol,由 CuO~Cu,得 CuO 的质量为 1.60 g;(2)生成标准状况下的氢气 896 mL,则 n(H )=
2
896 mL =0.04 mol,设Fe、Fe O 物质的量分别为x、y,可得56 g·mol-1 x+160 g·mol-1 y+1.60
2 3
22.4 L·mol-1
g=13.6 g,根据电子得失守恒得:2x=2y+2×0.02 mol+0.04 mol×2,解得x=0.1 mol、y=0.04 mol,反应后滤液
0.36mol
中n(FeCl )=x+2y=0.18 mol,根据FeCl ~2HCl得,n(HCl)=0.36 mol,所以c(HCl)= =3.60 mol·L-1。
2 2 0.10 L
20. 取1.77 g镁铝合金投入100 mL 2.00 mol·L-1的盐酸中,合金完全溶解,放出氢气1.904 L(已折算
成标准状况)。请计算:
(1)镁铝合金中镁的质量分数=_____________%(保留三位有效数字)。
(2)上述溶液中继续滴加 V mL 1.00 mol·L-1的 NaOH 溶液,得到沉淀 3.10 g。则 V 的最大值
=____________。
【答案】(1)54.2 (2)220
【解析】 (1)根据题意得出24 g·mol-1 n(Mg)+27 g·mol-1 n(Al)=1.77 g,镁、铝与盐酸反应生成氢气,根据得失电子数目守恒得出 2n(Mg)+3n(Al)= 1.904 L ×2,两式联立解得,n(Mg)=0.04 mol,
22.4 L·mol-1
n(Al)=0.03 mol。合金中镁的质量分数为0.04mol×24 g·mol-1 ×100%≈54.2%。(2)根据上述计算,得
1.77 g
出n(Mg)=0.04 mol,n(Al)=0.03 mol,假设镁、铝全部生成沉淀,则沉淀质量为 0.04 mol×58 g·mol-1+0.03
mol×78 g·mol-1=4.66 g>3.10 g,氢氧化铝为两性氢氧化物,因此沉淀达到3.10 g,消耗氢氧化钠的最大量应
是让部分氢氧化铝转化成偏铝酸钠,3.10 g沉淀中含氢氧化镁沉淀的质量为0.04 mol×58 g·mol-1=2.32 g,含
氢氧化铝的质量为3.10 g-2.32 g=0.78 g,反应后溶液中的溶质为NaCl和NaAlO ,根据铝原子守恒,溶液
2
中 n(NaAlO )=0.02 mol , 根 据 钠 原 子 守 恒 , 消 耗 氢 氧 化 钠 溶 液 最 大 体 积 为
2
100×10-3L×2 mol·L-1+0.02 mol =0.22 L,即220 mL。
1mol·L-1
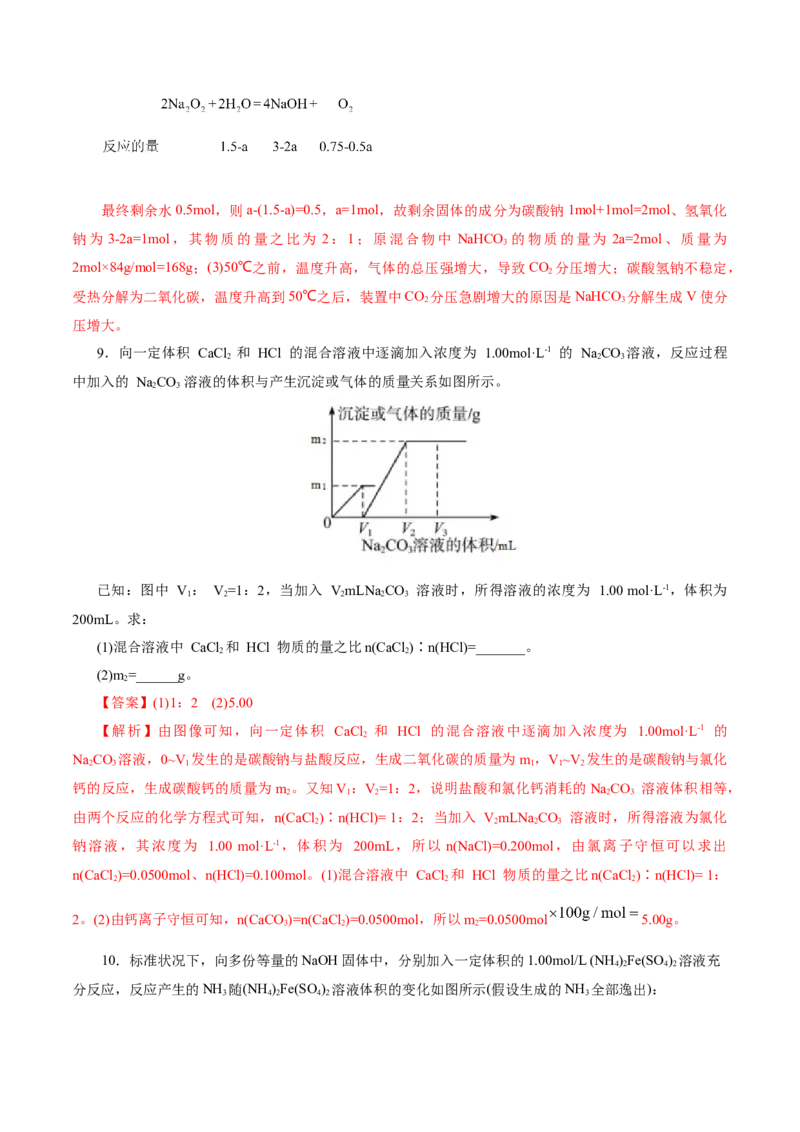
21.已知一定量的氢气在氯气中燃饶,所得混合物用 500mL 6.0 mol·L-1的KOH溶液恰好完全吸收,测
得溶液中含有ClO- 0.20 mol、ClO -0.30 mol(忽略氯气与水反应、盐类水解及溶液体积变化)。回答下列问题。
3
(1)所得溶液中c(Cl-)为________mol·L-1。
(2)所用氯气和参加反应的氢气的物质的量之比n(Cl )∶n(H )=________。
2 2
【答案】(1)5.0 (2)15∶4或3.75∶ 1
【解析】(1)因为KOH与混合物恰好完全反应,溶质为 KCl、KClO、KClO ,根据电荷守恒,n(K
3
+)=n(Cl-)+n(ClO-)+n(ClO -),代入数值,500×10-3×6=n(Cl-)+0.20+0.30,解得n(Cl-)=2.5mol,则c(Cl
3
-)=2.5/500×10-3mol·L-1=5.0mol·L-1;(2)Cl 与KOH反应发生氧化还原反应,根据得失电子数目守恒,n(Cl
2
-)=n(ClO-)×1+n(ClO -)×5,解得n(Cl-)=1.7mol,有HCl与KOH反应生成n(Cl-)=(2.5-1.7)mol=0.8mol,
3
因此参加反应氢气的物质的量0.8/2mol=0.4mol,根据氯元素守恒,所用氯气的总物质的量为n(Cl )=(2.5+
2
0.2+0.3)/2mol=1.5mol,因此所用氯气和参加反应氢气物质的量之比为1.5:0.4=15:4。
1.(2024•安徽省合肥市期中)某稀溶液中含有4mol KNO 和2mol HSO ,向其中加入1.2mol Fe,充分
3 2 4
反应(已知NO -被还原为NO),最终溶液体积为1L,下列说法正确的是( )
3
A.所得溶液中c(NO -)=2.75mol·L-1 B.所得溶液中c(Fe2+):c(Fe3+)=1:1
3
C.反应后生成NO的体积为28L(标准状况下) D.所得溶液中的溶质只有FeSO
4
【答案】B【解析】铁与稀硝酸完全反应生成硝酸铁、一氧化氮和水,反应的离子方程式为
,由方程式可知,4mol氢离子完全反应消耗1mol硝酸根离子,生成1mol
铁离子、一氧化氮的物质的量为1mol;则过量的铁与反应生成的铁离子反应生成亚铁离子,反应的离子方
程式为Fe+2Fe3+=3Fe2+,由方程式可知,过量的0.2mol铁,消耗0.4mol铁离子、生成0.6mol亚铁离子,则
反应后溶液中钾离子的物质的量为4mol、铁离子的物质的量为0.6mol、亚铁离子的物质的量为0.6mol、硝
酸根离子的物质的量为3mol、硫酸根离子的物质的量为2mol。A项,反应后硝酸根离子的物质的量为
3mol,浓度为 =3mol/L,故A错误;B项,反应后溶液中铁离子的物质的量为0.6mol、亚铁离子的物
质的量为0.6mol,则溶液中铁离子和亚铁离子的浓度之比为1:1,故B正确;C项,反应生成一氧化氮的
物质的量为1mol,则标准状况下一氧化氮的体积为 ,故C错误;D项,反应所
得溶液中含有铁离子、亚铁离子、钾离子、硫酸根离子和硝酸根离子,则所得溶液中的溶质不可能只含有
硫酸亚铁,故D错误;故选B。
2.(2024•湖南省名校联考期中)将2.56 gCu投入12mL10mol·L-1硝酸中,恰好完全反应,向反应后的溶
液中加入40mLamol·L-1NaOH溶液,Cu2+恰好完全沉淀,将生成的气体与bmol O 一起通入足量NaOH溶液
2
中,气体恰好被完全吸收生成c mol NaNO 。下列判断正确的是( )
3
A.生成的气体中只有NO B.
C. D.
【答案】C
【解析】A项, 2.56 gCu的物质的量为 =0.04mol,若生成的气体中只含有NO,由方程式
3Cu+8HNO =3Cu(NO)+2NO↑+4HO可知,0.04molCu需要消耗 HNO,而12mL10mol·L-1硝酸中
3 3 2 2 3
n(HNO)=0.12mol, <0.12mol,说明还会发生反应Cu+4HNO =Cu(NO)+2NO↑+2H O,生成的气
3 3 3 2 2 2
体有NO和NO ,A错误;B项,2.56 gCu的物质的量为 =0.04mol,投入12mL10mol·L-1硝酸中,
2恰好完全反应,向反应后的溶液中加入40mLamol·L-1NaOH溶液,Cu2+恰好完全沉淀,则
n[Cu(OH) ]=0.04mol,则n(NaOH)=0.08mol,NaOH溶液的浓度为 =amol/L=2mol/L,a=2,B错误;
2
C项,将生成的气体与bmol O 一起通入足量NaOH溶液中,气体恰好被完全吸收生成c mol NaNO ,由得
2 3
失电子守恒可知,O 得到的电子数和Cu失去的电子数相等,则bmol×4=0.04mol×2,则b=0.02,C正确;
2
D项,Cu和HNO 溶液反应完全后,生成NO、NO 的混合气体,加入NaOH溶液后溶液中存在NaNO ,
3 2 3
则NO、NO 的总物质的量为0.12mol-0.08mol=0.04mol,由N元素守恒可知,气体恰好被完全吸收生成
2
n(NaNO )=0.04mol,c=0.04,D错误;故选C。
3
3.(2024•湖北省云学名校新高考联盟期中联考)将13.6g Cu和Cu O组成的混合物加入250 mL一定浓
2
度的稀硝酸中,固体完全溶解生成Cu(NO ) 和NO,向所得溶液中加入1.0 L 0.5 mol/LNaOH溶液时,金属
3 2
离子恰好沉淀完全,生成沉淀的质量为19.6 g,下列说法错误的是( )
A.原稀硝酸的浓度为2 mol/L
B.Cu和Cu O的物质的量之比为2:1
2
C.反应后剩余硝酸的物质的量为0.1 mol
D.产生的NO在标准状况下的体积为2.24L
【答案】A
【解析】铜和氧化亚铜和硝酸反应生成硝酸铜,和一氧化氮,溶液中加入氢氧化钠,反应生成氢氧化
铜沉淀19.6g,即 =0.2mol,说明铜离子物质的量为0.2mol,则原混合物中氧元素的质量为
13.6g-64g/mol×0.2mol=0.8g,物质的量为 =0.05mol,则氧化亚铜的物质的量为0.05mol,铜的物质
的量为0.1mol。A项,所得溶液中加入1.0L0.5mol•L-1的NaOH溶液,生成沉淀的质量为19.6g,此时溶液
呈中性,且金属离子沉淀完全,说明溶液为硝酸钠,即硝酸根离子物质的量等于钠离子物质的量,则溶液
中硝酸根离子物质的量为0.5mol,原硝酸的物质的量=硝酸根离子物质的量+一氧化氮物质的量,根据电子
守恒分析,铜元素失去电子数=0.1×2mol+0.05×2×1mol=0.3mol则一氧化氮的物质的量为0.1mol,则原稀硝
酸的浓度为 =2.4mol·L-1,A错误;B项,原固体混合物中,Cu和Cu O的物质的量之比为
2
0.1:0.05=2:1,B正确;C项,硝酸的物质的量为0.6mol,反应后生成的硝酸铜的物质的量为0.2mol则
硝酸根离子物质的量为0.4mol,一氧化氮的物质的量为0.1mol,则说明反应后剩余硝酸的物质的量为0.6mol-0.4mol-0.1mol=0.1mol,C正确;D项,由B 中计算一氧化氮物质的量为0.1mol,则标准状况下的
体积为2.24L,D正确;故选A。
4.(2024•安徽省淮北市期中)将1.76g镁铜合金投入20mL一定浓度的硝酸中,合金完全溶解,产生
NO和NO 混合气体896mL(不考虑其他气体,体积折算为标准状况下),反应结束后向溶液中加入
2
120mL1mol·L-1NaOH溶液,恰好使溶液中的金属阳离子全部转化为沉淀3.12g。若将盛有896mL该混合气
体的容器倒扣在水中,通入一定体积的氧气,恰好可将该混合气体完全转化。下列说法错误的是( )
A.Mg与Cu的物质的量比值为3:1 B.NO和NO 的体积比为1:1
2
C.原硝酸的浓度为8mol·L-1 D.通入的O 的体积(标准状况下)V=448Ml
2
【答案】A
【解析】A项,根据电子转移守恒可知,镁铜失去电子总和等于硝酸生成NO和NO 得到电子总和,
2
而镁铜失去电子与Mg2+、Cu2+生成沉淀结合的OH-的物质的量相等,且氢氧根物质的量是镁铜物质的量总
和的两倍,最终沉淀比开始合金的增重即为氢氧根的质量,故氢氧根物质的量为 ,
Mg与Cu的物质的量之和为0.04mol,设镁物质的量为a mol,铜物质的量为(0.04-a)mol,则24a+64(0.04-
a)=1.76,解得a=0.02,即Mg与Cu的物质的量都是0.02mol,物质的量比值为1:1,A错误;B项,NO
和NO 混合气体共896mL,标准状况下混合气体总物质的量为0.04mol,设混合气体中NO的物质的量为x
2
mol,NO 的物质的量为(0.04-x)mol,根据电子转移守恒可知,镁铜失去电子总和等于硝酸生成NO和NO
2 2
得到电子总和,而镁铜失去电子与Mg2+、Cu2+生成沉淀结合的OH-的物质的量相等,则:3x+0.04-x=
0.08,解得x=0.02,故NO和NO 的物质的量都为0.02mol,体积比为1:1,B正确;C项,金属离子恰好
2
完全沉淀时,溶液的溶质为NaNO ,则未被还原的HNO 的物质的量等于n(NaOH)=1mol/
3 3
L×0.12L=0.12mol,因此根据N原子守恒,原硝酸的物质的量为n(气体)+ 未被还原的
n(HNO)=0.04+0.12=0.16mol,原硝酸的浓度为 ,C正确;D项,NO、NO 与氧气、水反
3 2
应又转化为HNO,反应方程式为4NO +O +2H O=4HNO 、4NO+3O +2H O=4HNO ,NO、NO 物质的量
3 2 2 2 3 2 2 3 2
都是0.02mol 因此根据方程式n(O )= =0.02mol,标准状况下通入氧气的体积为:
, 2
0.02mol×22.4L/mol=0.448L,即448mL,D正确;本题选A。
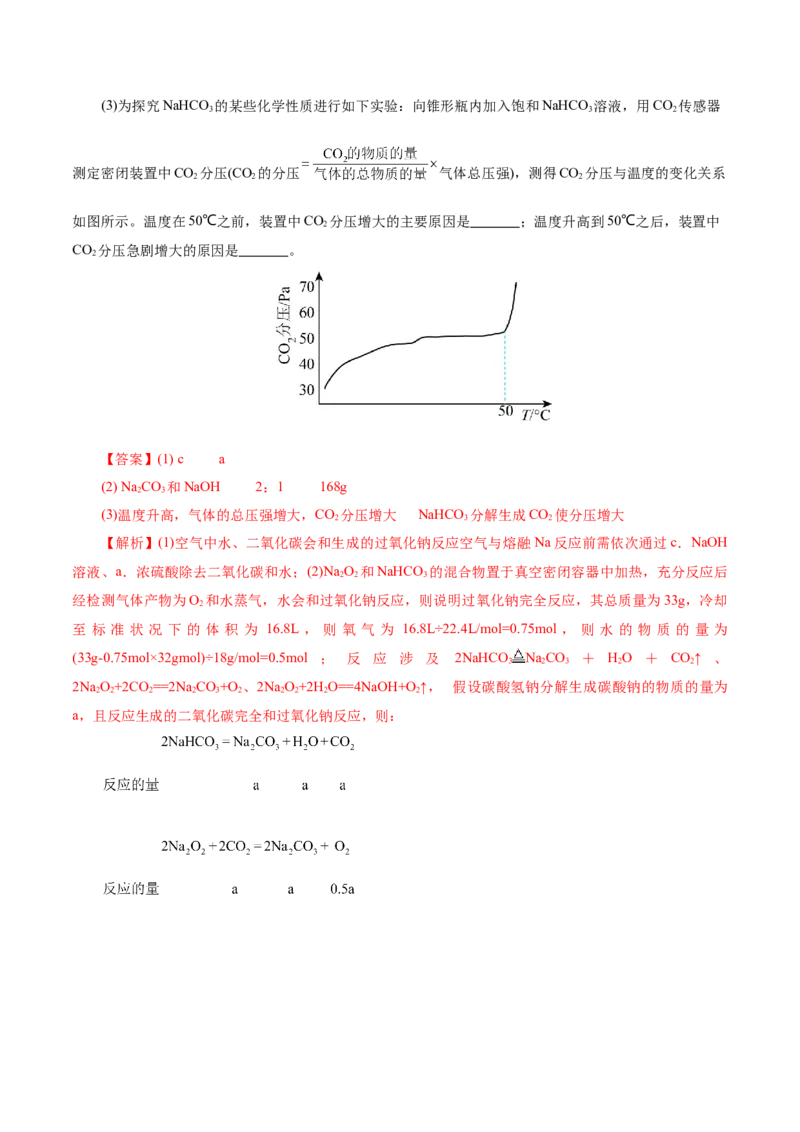
5.(2024•上海省浦东新区期中)某学生用 NaHCO 和 KHCO 组成的某混合物与盐酸进行实验,测得下
3 3
表数据(盐酸的物质的量浓度相等,体积均为 50 mL)。实验编号 I II III
盐酸的体积 50.0mL 50.0mL 50.0mL
m(混合物) 13.56g 21.88g 25.36g
V(CO )(标准状况) 3.36L 5.04L 5.04L
2
(1)则该学生所用盐酸的物质的量浓度是 mol/L;
(2)50 mL 该盐酸恰好能溶解上述组成的混合物的质量是 g;
(3)上述固体混合物中 KHCO 的质量分数是 (用小数表示,保留 2 位小数)。
3
【答案】(1)4.5 (2)20.34 (3)44.25%
【解析】混合物发生反应:H++HCO-═CO ↑+H O,由①②数据可知,继续增大混合物的质量,气体的
3 2 2
体积增大,说明实验①中盐酸有剩余、固体混合物完全反应.若②中盐酸有剩余,继续增大混合物的质量,
气体的体积会增大,由②③数据可知,实验中气体的体积不变,说明实验②中盐酸完全反应,根据实验①
的数据可知,生成5.04L二氧化碳需要固体混合物的质量为13.56g× =20.34 g<21.88g,故实验②中盐
酸完全反应、固体混合物有剩余。(1)求盐酸浓度需选择盐酸不足量的数据进行,如随着混合物质量增加,
二氧化碳气体量不再增加,表明盐酸全部反应完,由表中数据可知,盐酸完全反应生成二氧化碳5.04L,
结合H++HCO-=H O+CO↑可知n(HCl)= ,盐酸的浓度为
3 2 2
;(2)由表中数据可知,由于固体混合物从13.56g→21.88g,二氧化碳气体的体
积还在增加,故加入13.56g混合物时盐酸过量,而固体混合物从21.88g→25.36g,二氧化碳气体的体积不
再变化,说明加入25.36g混合物时盐酸不足,50 mL 该盐酸恰好能溶解上述组成的混合物的质量是
13.56g× =20.34 g;(3)加入13.56g混合物时,盐酸有剩余,混合物完全反应,根据H++HCO
═CO ↑+H O,可知n(混合物)=n(CO )= ,设13.56g混合物中NaHCO 、KHCO 的
2 2 2 3 3
物质的量分别为x和y,则有:x+y=0.15mol、84x+100y=13.56g,解得y=0.06mol、x=0.09mol,KHCO 的
3质量分数是 。
6.(2024•浙江省浙南名校联盟开学考试)为确定某一铁铜样品中各成份的含量,某同学进行了如下实
验:准确称取一份质量为 铁铜样品,逐渐加入一定体积某浓度的稀硝酸,每次实验充分反应后,测
得生成 气体的体积为 (已换成标准状况,假设生成的 全部逸出),并测得剩余固体质量为 。
各次实验的数据如下表:
稀硝酸体积 0 80 160 240 320 400
体积V(L) 0 0.896 1.792 2.688 3.584 4.48
剩余固体质量m(g) 12.24 8.88 5.52 1.92 0 0
根据以上实验数据,请回答:
(1)上述实验当加入 稀硝酸后,所发生反应的离子方程式为 。
(2)稀硝酸的物质的量浓度为 。
(3)样品中Fe、Cu的物质的量之比为 。
【答案】(1) 3Fe2++4H++NO===3Fe3++2HO+NO↑
2
(2)2
(3)5∶2
【解析】(1)根据表格数据,硝酸体积从320mL到400mL,固体质量都是0,但是生成NO,说明是硝
酸与Fe2+反应生成的,离子方程式为:3Fe2++4H++NO===3 Fe3++2HO+NO↑;(2)根据前2阶段数据,
2
硝酸的体积、NO的体积、金属减少的质量均成比例,可以判断开始为Fe反应生成Fe2+,有关系式:
3Fe~8HNO ~2NO,第1阶段生成的NO的物质的量为0.04mol,则消耗的HNO 为0.16mol,体积为
3 3
80mL,硝酸的物质的量浓度为 =2mol/L;(3)分析表格的数据:前2阶段数据,硝酸的体积每增加
80mL,NO的体积增加0.896L、金属减少的质量均成3.36g,可以判断为Fe反应生成Fe2+,当硝酸体积从
160mL到240mL,NO的体积增加0.896L、而金属的质量减少3.6g,说明这一阶段是把剩余的铁反应成
Fe2+,铜反应了一部分,剩余铜1.92g;设这3.6g的金属中Fe的物质的量为x,铜的物质的量为y,有方程
组:2x+2y= =0.12;56x+64y=3.6;解得x=0.03mol,y=0.03mol,则原样品中铜的总质量为0.03mol =3.84g,铜的总物质的量为0.06mol;铁的总质量为12.24g-3.84g=8.4g,物质的量为
=0.15mol;样品中Fe、Cu的物质的量之比为0.15mol:0.06mol=5∶2。
7.(2024•海南省海口市期末)已知Fe O 在高炉中有下列反应:Fe O+CO→2FeO+CO。反应形成的
2 3 2 3 2
固体混合物(含Fe O 和FeO)中,元素铁和氧的质量比用m(Fe)∶m(O)表示。
2 3
(1)上述固体混合物中,m(Fe)∶m(O)不可能是 (选填a、b、c)。
a.21∶9 b.21∶7.5 c.21∶6
(2)若m(Fe)∶m(O)=21∶8,计算Fe O 被CO还原的百分率 。
2 3
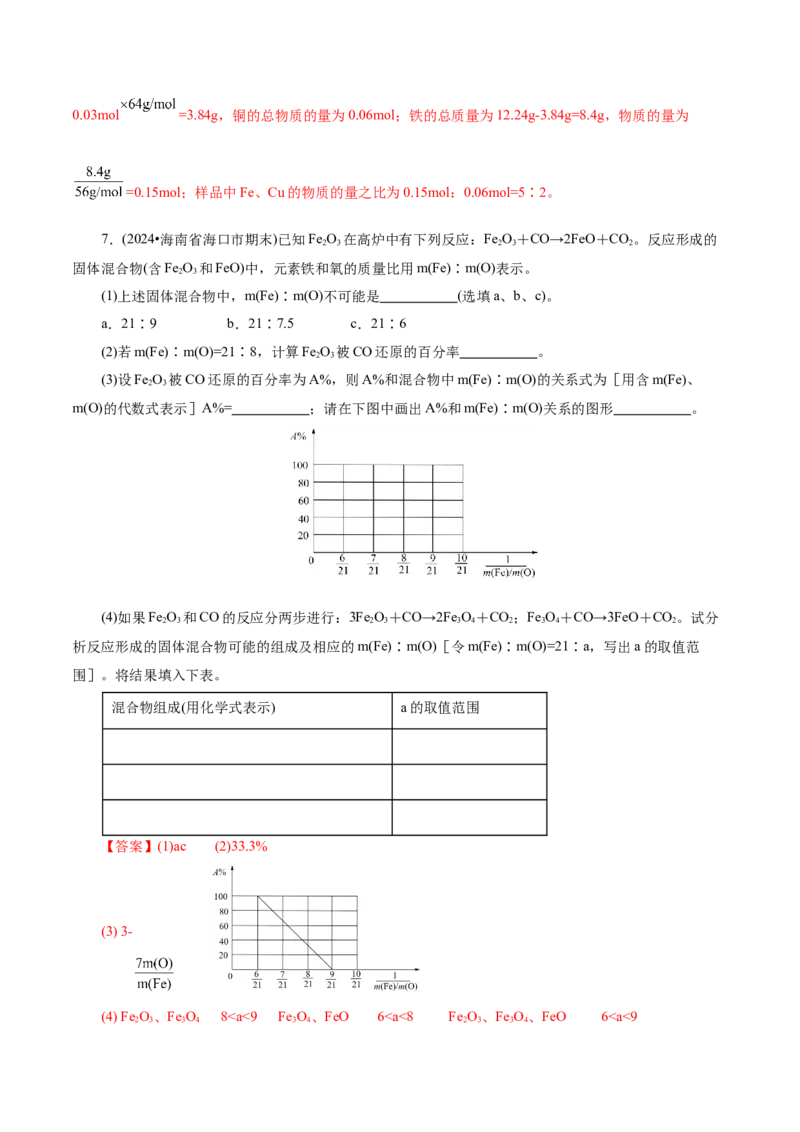
(3)设Fe O 被CO还原的百分率为A%,则A%和混合物中m(Fe)∶m(O)的关系式为[用含m(Fe)、
2 3
m(O)的代数式表示]A%= ;请在下图中画出A%和m(Fe)∶m(O)关系的图形 。
(4)如果Fe O 和CO的反应分两步进行:3Fe O+CO→2Fe O+CO;Fe O+CO→3FeO+CO。试分
2 3 2 3 3 4 2 3 4 2
析反应形成的固体混合物可能的组成及相应的m(Fe)∶m(O)[令m(Fe)∶m(O)=21∶a,写出a的取值范
围]。将结果填入下表。
混合物组成(用化学式表示) a的取值范围
【答案】(1)ac (2)33.3%
(3) 3-
(4) Fe O、Fe O 82,且为整数),则n(X)= mol= mol, n(X) 0.06mol 34m
m m
m
g/mol。当m=3,M(X)=102g/mol, 羟基数目大于羧基数目,说明含有2个羟基和1个羧基,说明X分子
式有4个O,碳和氢的摩尔质量=102-16×4=38g/mol,分子式为C HO, 2个羟基和1个羧基就占了3个H
3 2 4
原子,可知这个分子式不合理,m=3不成立;当m=4,M(X)=136g/mol,说明含有3个羟基和1个羧基,
同上分析可知分子式为C HO,该分子式合理,例如可能的结构简式为 。故答案是:
4 8 5
含有3个羟基和1个羧基,相对分子质量为136。