文档内容
第四章 非金属及其化合物
第13讲 硫及其化合物(精练)
完卷时间:50分钟
可能用到的相对原子质量:H1 O16 Na23 S32 Mn55 Fe56
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·四川攀枝花市·高三二模)化学与生产、生活密切相关,下列叙述错误的是
A.石灰石可用作燃煤的脱硫剂 B.过氧化氢溶液可用作医用消毒剂
C.碳酸钡可用作胃肠X射线透视的造影剂 D.硫化钠可用作去除废水中Pb2+的沉淀剂
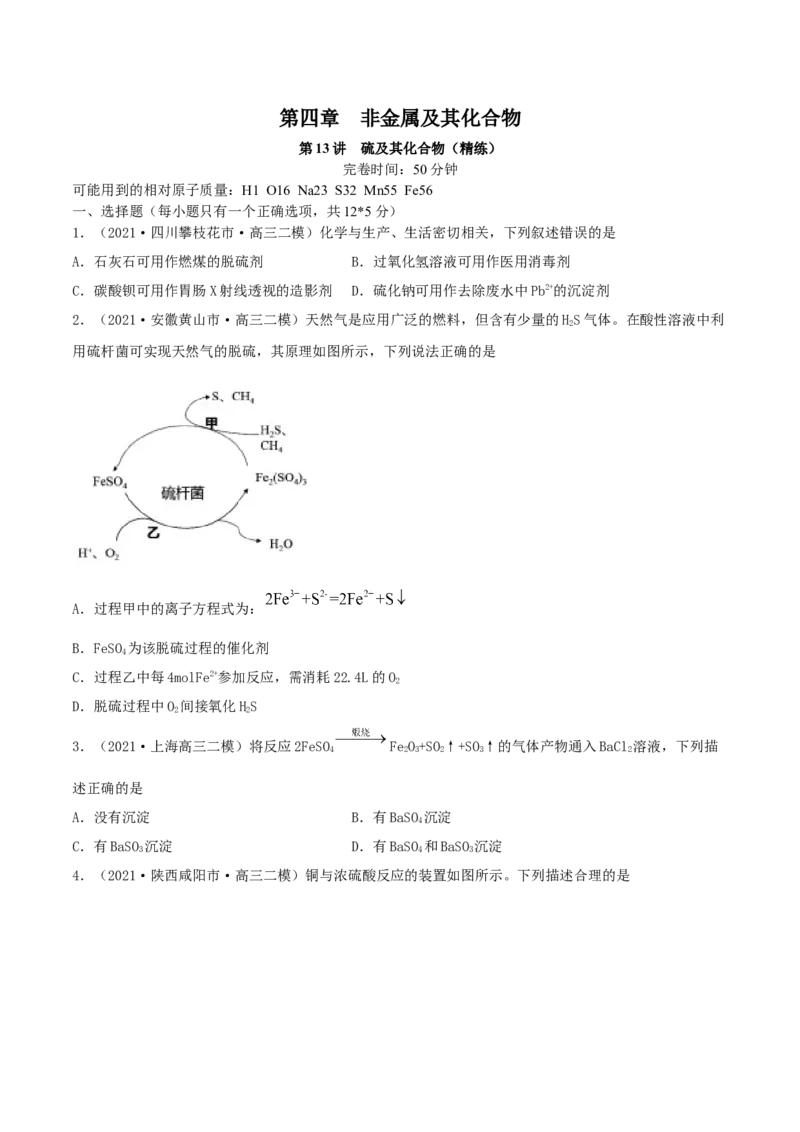
2.(2021·安徽黄山市·高三二模)天然气是应用广泛的燃料,但含有少量的HS气体。在酸性溶液中利
2
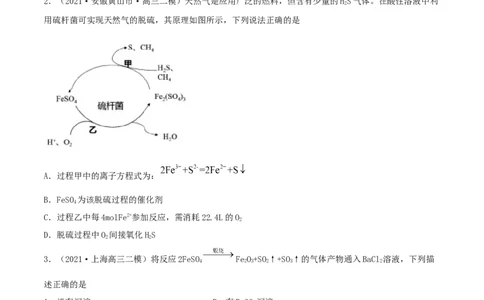
用硫杆菌可实现天然气的脱硫,其原理如图所示,下列说法正确的是
A.过程甲中的离子方程式为:
B.FeSO 为该脱硫过程的催化剂
4
C.过程乙中每4molFe2+参加反应,需消耗22.4L的O
2
D.脱硫过程中O 间接氧化HS
2 2
3.(2021·上海高三二模)将反应2FeSO FeO+SO↑+SO↑的气体产物通入BaCl 溶液,下列描
4 2 3 2 3 2
述正确的是
A.没有沉淀 B.有BaSO 沉淀
4
C.有BaSO 沉淀 D.有BaSO 和BaSO 沉淀
3 4 3
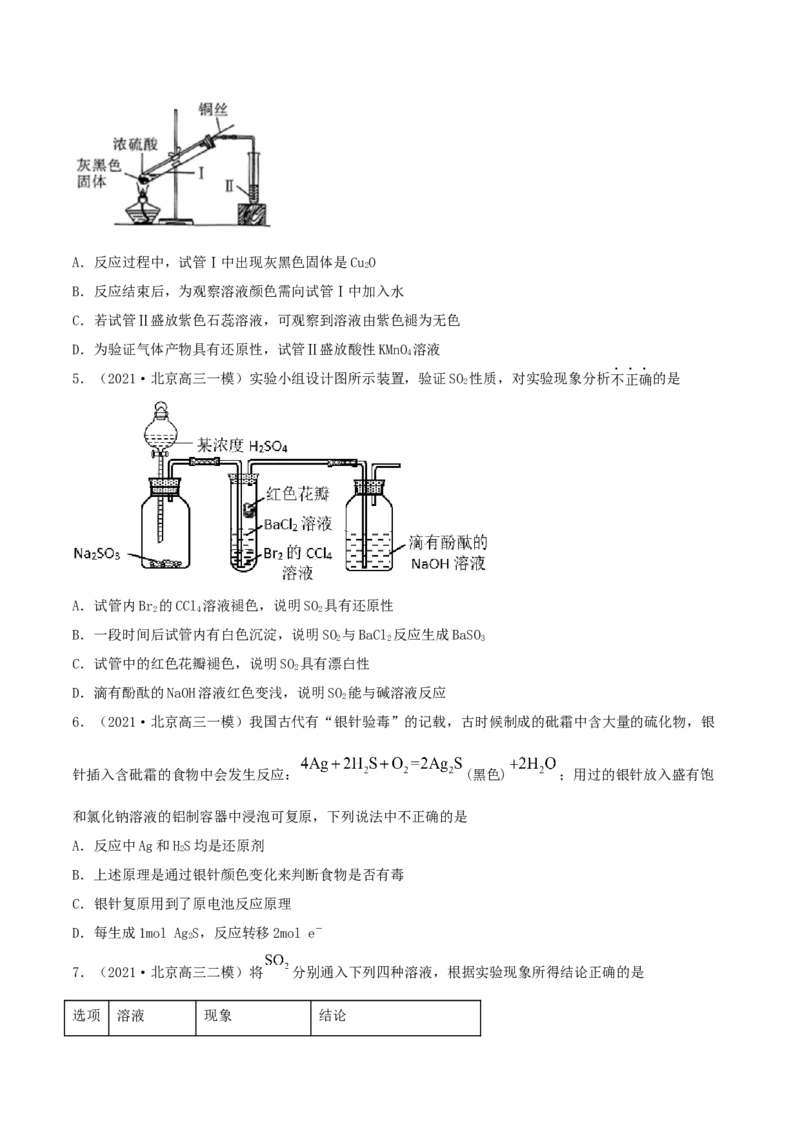
4.(2021·陕西咸阳市·高三二模)铜与浓硫酸反应的装置如图所示。下列描述合理的是A.反应过程中,试管Ⅰ中出现灰黑色固体是CuO
2
B.反应结束后,为观察溶液颜色需向试管Ⅰ中加入水
C.若试管Ⅱ盛放紫色石蕊溶液,可观察到溶液由紫色褪为无色
D.为验证气体产物具有还原性,试管Ⅱ盛放酸性KMnO 溶液
4
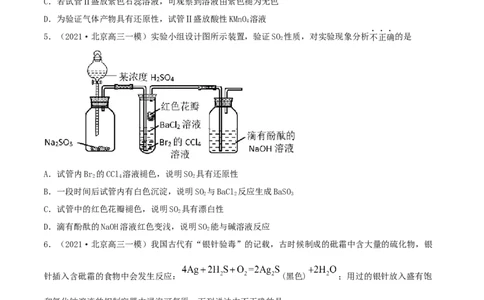
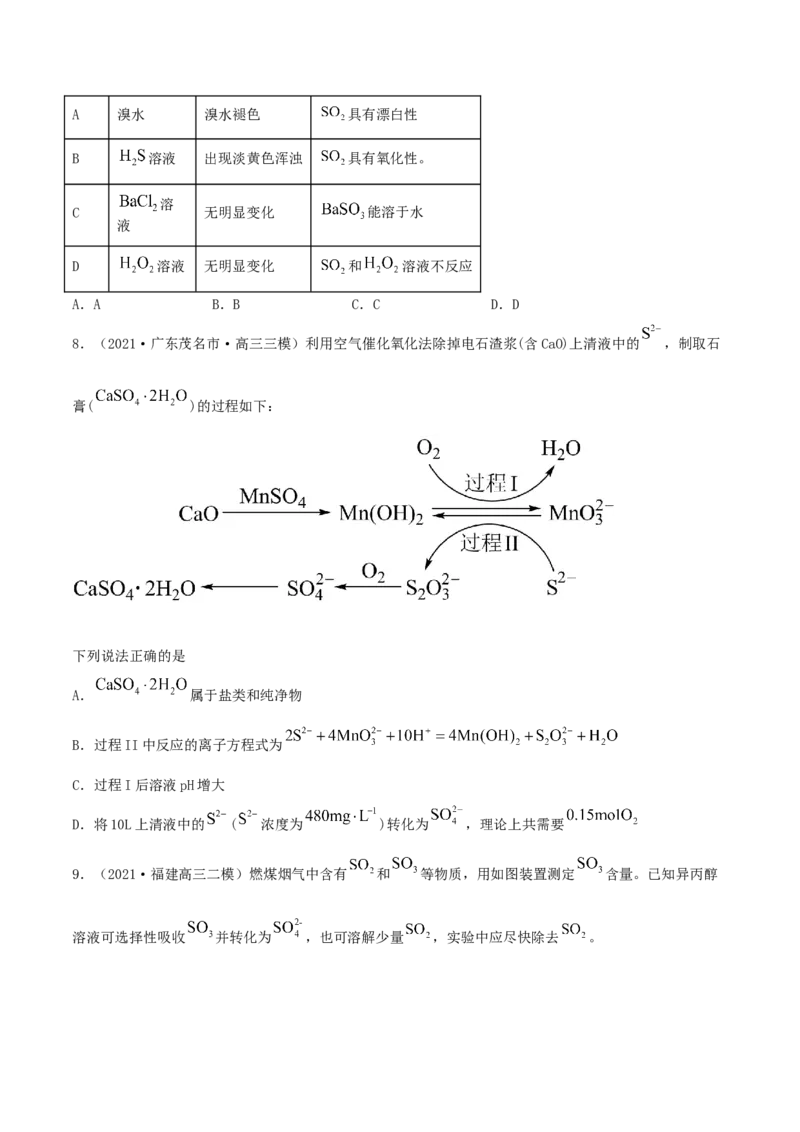
5.(2021·北京高三一模)实验小组设计图所示装置,验证SO 性质,对实验现象分析不正确的是
2
A.试管内Br 的CCl 溶液褪色,说明SO 具有还原性
2 4 2
B.一段时间后试管内有白色沉淀,说明SO 与BaCl 反应生成BaSO
2 2 3
C.试管中的红色花瓣褪色,说明SO 具有漂白性
2
D.滴有酚酞的NaOH溶液红色变浅,说明SO 能与碱溶液反应
2
6.(2021·北京高三一模)我国古代有“银针验毒”的记载,古时候制成的砒霜中含大量的硫化物,银
针插入含砒霜的食物中会发生反应: (黑色) ;用过的银针放入盛有饱
和氯化钠溶液的铝制容器中浸泡可复原,下列说法中不正确的是
A.反应中Ag和HS均是还原剂
2
B.上述原理是通过银针颜色变化来判断食物是否有毒
C.银针复原用到了原电池反应原理
D.每生成1mol AgS,反应转移2mol e-
2
7.(2021·北京高三二模)将 分别通入下列四种溶液,根据实验现象所得结论正确的是
选项 溶液 现象 结论A 溴水 溴水褪色 具有漂白性
B 溶液 出现淡黄色浑浊 具有氧化性。
溶
C 无明显变化 能溶于水
液
D 溶液 无明显变化 和 溶液不反应
A.A B.B C.C D.D
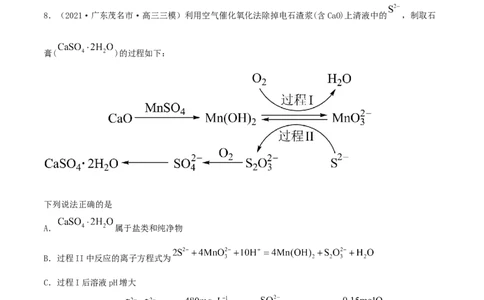
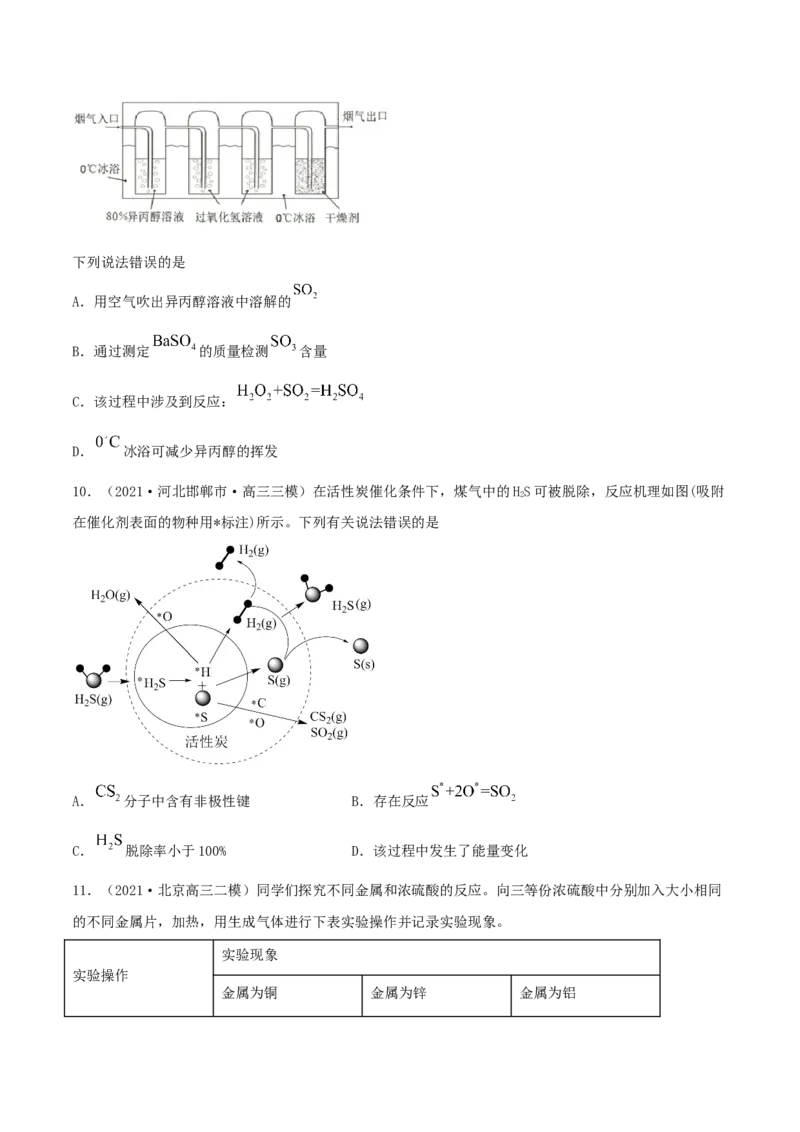
8.(2021·广东茂名市·高三三模)利用空气催化氧化法除掉电石渣浆(含CaO)上清液中的 ,制取石
膏( )的过程如下:
下列说法正确的是
A. 属于盐类和纯净物
B.过程II中反应的离子方程式为
C.过程I后溶液pH增大
D.将10L上清液中的 ( 浓度为 )转化为 ,理论上共需要
9.(2021·福建高三二模)燃煤烟气中含有 和 等物质,用如图装置测定 含量。已知异丙醇
溶液可选择性吸收 并转化为 ,也可溶解少量 ,实验中应尽快除去 。下列说法错误的是
A.用空气吹出异丙醇溶液中溶解的
B.通过测定 的质量检测 含量
C.该过程中涉及到反应:
D. 冰浴可减少异丙醇的挥发
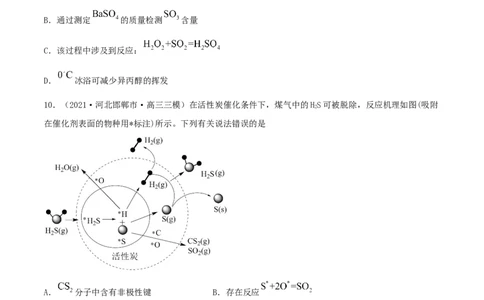
10.(2021·河北邯郸市·高三三模)在活性炭催化条件下,煤气中的HS可被脱除,反应机理如图(吸附
2
在催化剂表面的物种用*标注)所示。下列有关说法错误的是
A. 分子中含有非极性键 B.存在反应
C. 脱除率小于100% D.该过程中发生了能量变化
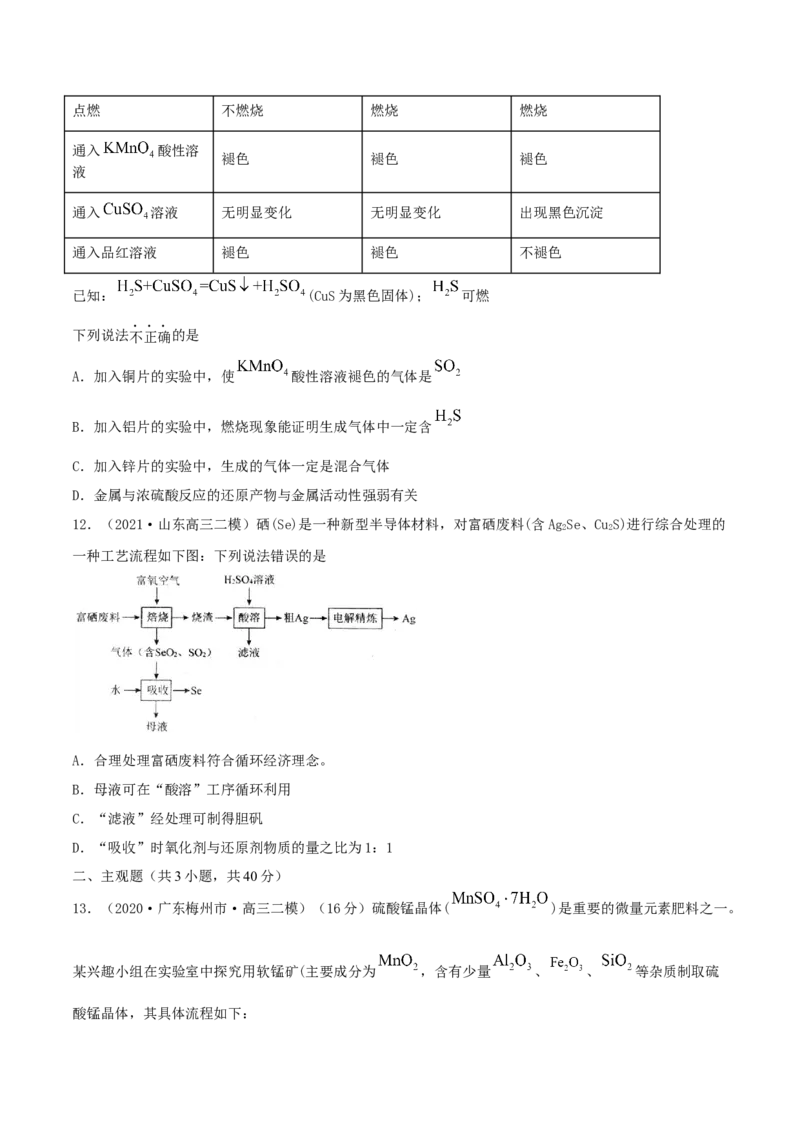
11.(2021·北京高三二模)同学们探究不同金属和浓硫酸的反应。向三等份浓硫酸中分别加入大小相同
的不同金属片,加热,用生成气体进行下表实验操作并记录实验现象。
实验现象
实验操作
金属为铜 金属为锌 金属为铝点燃 不燃烧 燃烧 燃烧
通入 酸性溶
褪色 褪色 褪色
液
通入 溶液 无明显变化 无明显变化 出现黑色沉淀
通入品红溶液 褪色 褪色 不褪色
已知: (CuS为黑色固体); 可燃
下列说法不正确的是
A.加入铜片的实验中,使 酸性溶液褪色的气体是
B.加入铝片的实验中,燃烧现象能证明生成气体中一定含
C.加入锌片的实验中,生成的气体一定是混合气体
D.金属与浓硫酸反应的还原产物与金属活动性强弱有关
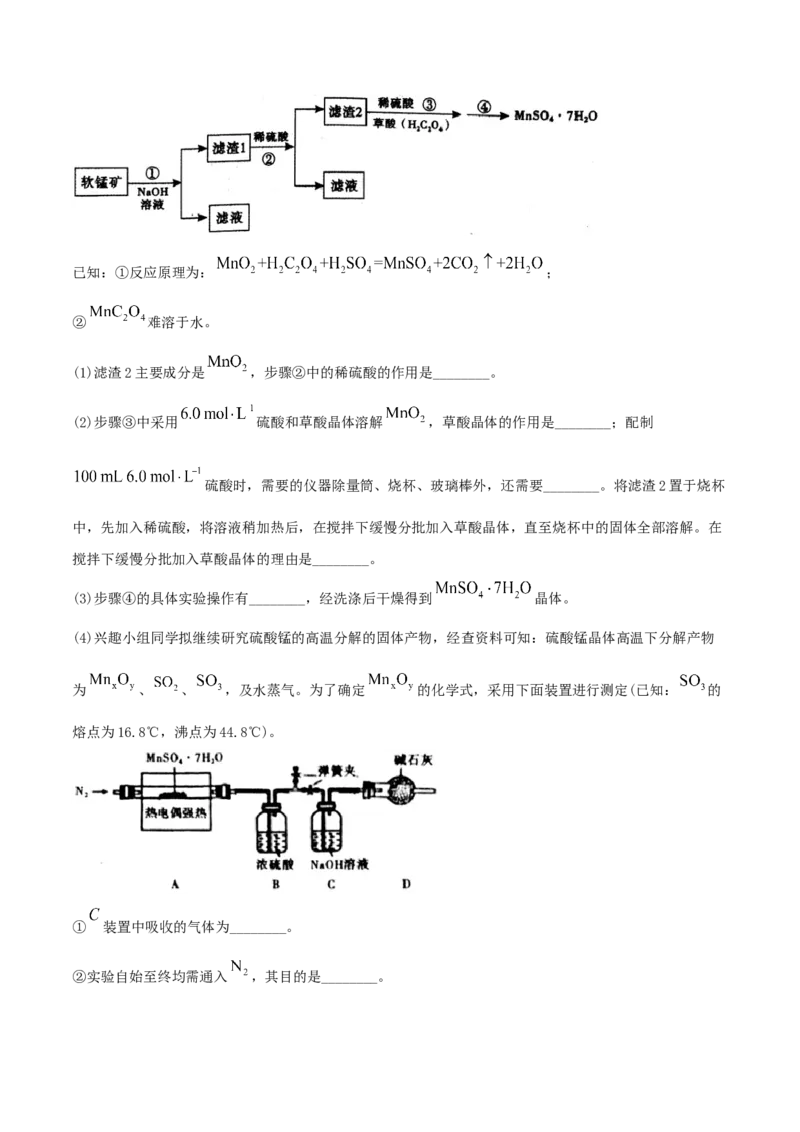
12.(2021·山东高三二模)硒(Se)是一种新型半导体材料,对富硒废料(含AgSe、CuS)进行综合处理的
2 2
一种工艺流程如下图:下列说法错误的是
A.合理处理富硒废料符合循环经济理念。
B.母液可在“酸溶”工序循环利用
C.“滤液”经处理可制得胆矾
D.“吸收”时氧化剂与还原剂物质的量之比为1:1
二、主观题(共3小题,共40分)
13.(2020·广东梅州市·高三二模)(16分)硫酸锰晶体( )是重要的微量元素肥料之一。
某兴趣小组在实验室中探究用软锰矿(主要成分为 ,含有少量 、 、 等杂质制取硫
酸锰晶体,其具体流程如下:已知:①反应原理为: ;
② 难溶于水。
(1)滤渣2主要成分是 ,步骤②中的稀硫酸的作用是________。
(2)步骤③中采用 硫酸和草酸晶体溶解 ,草酸晶体的作用是________;配制
硫酸时,需要的仪器除量筒、烧杯、玻璃棒外,还需要________。将滤渣2置于烧杯
中,先加入稀硫酸,将溶液稍加热后,在搅拌下缓慢分批加入草酸晶体,直至烧杯中的固体全部溶解。在
搅拌下缓慢分批加入草酸晶体的理由是________。
(3)步骤④的具体实验操作有________,经洗涤后干燥得到 晶体。
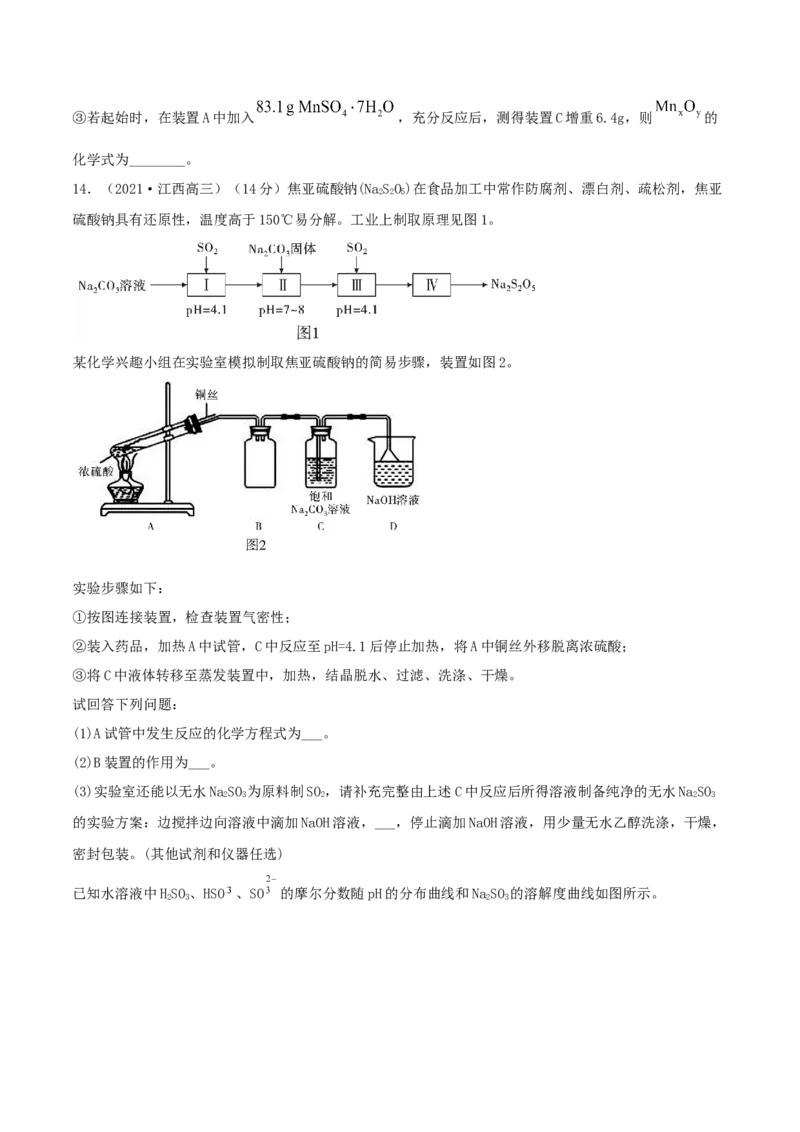
(4)兴趣小组同学拟继续研究硫酸锰的高温分解的固体产物,经查资料可知:硫酸锰晶体高温下分解产物
为 、 、 ,及水蒸气。为了确定 的化学式,采用下面装置进行测定(已知: 的
熔点为16.8℃,沸点为44.8℃)。
① 装置中吸收的气体为________。
②实验自始至终均需通入 ,其目的是________。③若起始时,在装置A中加入 ,充分反应后,测得装置C增重6.4g,则 的
化学式为________。
14.(2021·江西高三)(14分)焦亚硫酸钠(NaSO)在食品加工中常作防腐剂、漂白剂、疏松剂,焦亚
2 2 5
硫酸钠具有还原性,温度高于150℃易分解。工业上制取原理见图1。
某化学兴趣小组在实验室模拟制取焦亚硫酸钠的简易步骤,装置如图2。
实验步骤如下:
①按图连接装置,检查装置气密性;
②装入药品,加热A中试管,C中反应至pH=4.1后停止加热,将A中铜丝外移脱离浓硫酸;
③将C中液体转移至蒸发装置中,加热,结晶脱水、过滤、洗涤、干燥。
试回答下列问题:
(1)A试管中发生反应的化学方程式为___。
(2)B装置的作用为___。
(3)实验室还能以无水NaSO 为原料制SO,请补充完整由上述C中反应后所得溶液制备纯净的无水NaSO
2 3 2 2 3
的实验方案:边搅拌边向溶液中滴加NaOH溶液,___,停止滴加NaOH溶液,用少量无水乙醇洗涤,干燥,
密封包装。(其他试剂和仪器任选)
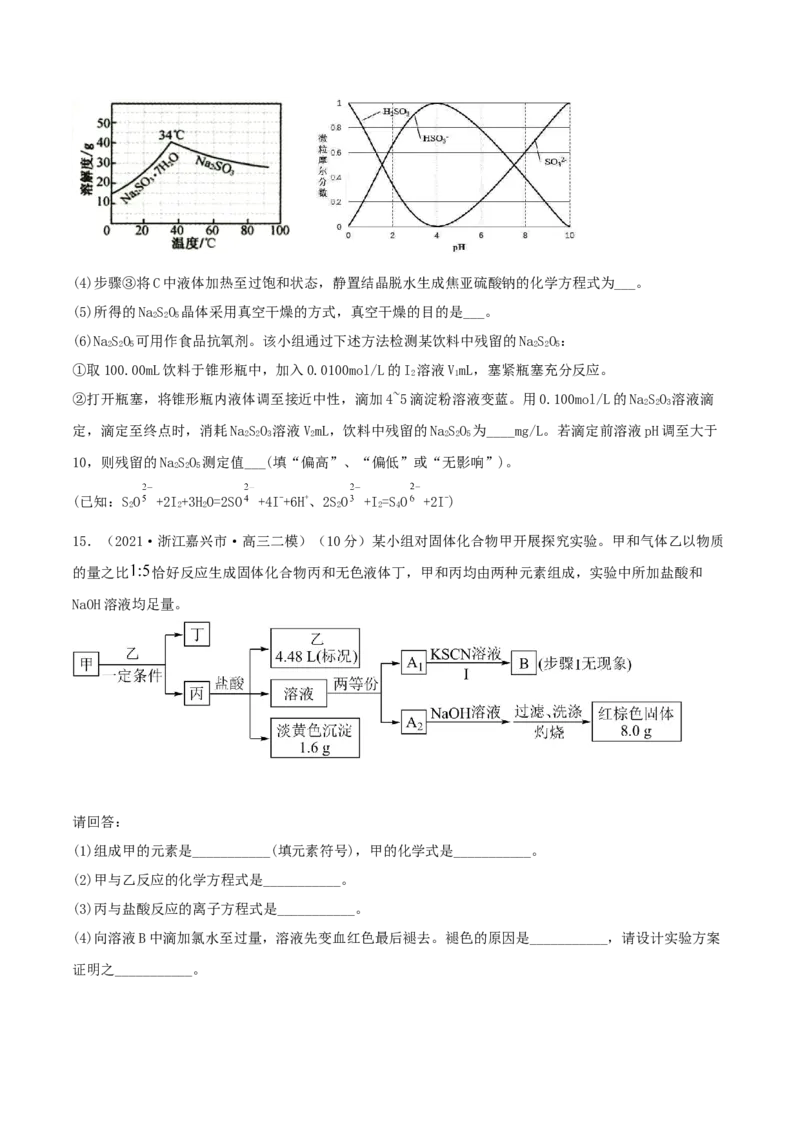
已知水溶液中HSO、HSO 、SO 的摩尔分数随pH的分布曲线和NaSO 的溶解度曲线如图所示。
2 3 2 3(4)步骤③将C中液体加热至过饱和状态,静置结晶脱水生成焦亚硫酸钠的化学方程式为___。
(5)所得的NaSO 晶体采用真空干燥的方式,真空干燥的目的是___。
2 2 5
(6)NaSO 可用作食品抗氧剂。该小组通过下述方法检测某饮料中残留的NaSO:
2 2 5 2 2 5
①取100.00mL饮料于锥形瓶中,加入0.0100mol/L的I 溶液VmL,塞紧瓶塞充分反应。
2 1
②打开瓶塞,将锥形瓶内液体调至接近中性,滴加4~5滴淀粉溶液变蓝。用0.100mol/L的NaSO 溶液滴
2 2 3
定,滴定至终点时,消耗NaSO 溶液VmL,饮料中残留的NaSO 为____mg/L。若滴定前溶液pH调至大于
2 2 3 2 2 2 5
10,则残留的NaSO 测定值___(填“偏高”、“偏低”或“无影响”)。
2 2 5
(已知:SO +2I+3HO=2SO +4I-+6H+、2SO +I=SO +2I-)
2 2 2 2 2 4
15.(2021·浙江嘉兴市·高三二模)(10分)某小组对固体化合物甲开展探究实验。甲和气体乙以物质
的量之比 恰好反应生成固体化合物丙和无色液体丁,甲和丙均由两种元素组成,实验中所加盐酸和
NaOH溶液均足量。
请回答:
(1)组成甲的元素是___________(填元素符号),甲的化学式是___________。
(2)甲与乙反应的化学方程式是___________。
(3)丙与盐酸反应的离子方程式是___________。
(4)向溶液B中滴加氯水至过量,溶液先变血红色最后褪去。褪色的原因是___________,请设计实验方案
证明之___________。