文档内容
训练(三十八) 弱电解质的电离平衡
1.(2021·湖南益阳调研)将浓度为0.05 mol/L的HClO溶液加水不断稀释,下列各量始终
保持增大的是( )
A.c(H+) B.
C.K(HClO) D.
a
B [HClO溶液加水稀释,HClO的电离平衡正向移动,c(H+)、c(ClO-)均减小,A错误;
n(H+)增大,n(HClO)减小,由于溶液体积相同,则增大,B正确;由于温度不变,则K(HClO)
a
不变,C错误,若忽略水的电离,则c(H+)始终等于c(ClO-),随稀释的进行,由水电离出的H+
不断增多,故不断减小,D错误。]
2.(2021·广州荔湾区检测)常温下,一元弱碱MOH溶液中存在电离平衡MOH⇌M++
OH-,下列说法正确的是( )
A.加入MCl固体,MOH电离平衡逆向移动,M+浓度减小
B.加水稀释,溶液中MOH的电离程度和M+浓度均增大
C.升高温度,MOH电离平衡正向移动,MOH的电离程度和M+浓度均增大
D.滴加少量稀盐酸,MOH的电离程度和OH-浓度均增大
C [加入MCl固体,溶液中c(M+)增大,MOH电离平衡逆向移动,A错误;加水稀释,溶
液中MOH的电离程度增大,但M+浓度减小,B错误;升高温度,MOH电离平衡正向移动,
MOH的电离程度增大,由于溶液体积不变,则M+浓度增大,C正确;滴加少量稀盐酸,H+和
OH-反应生成HO,MOH电离平衡正向移动,MOH的电离程度增大,但OH-浓度减小,D错
2
误。]
3.(2021·天津部分区联考)已知某温度下,四种弱酸的电离常数:K(HCN)=4.9×10-10,
a
K(HF)=6.3×10-4,K(CHCOOH)=1.8×10-5 ,K(HNO)=5.6×10-4。物质的量浓度都为
a a 3 a 2
0.1 mol/L的下列溶液中,c(H+)最大的是( )
A.HCN B.CHCOOH
3
C.HF D.HNO
2
C [相同温度下,弱酸的电离常数越大,其酸性越强,物质的量浓度都为0.1 mol/L,电离
产生c(H+)也越大,故0.1 mol/L HF溶液中c(H+)最大。]
4.(2021·河南南阳调研)下列实验事实能说明HNO 是弱电解质的是( )
2
①HNO 溶液能与NaHCO 溶液混合,放出气泡
2 3②用HNO 溶液做导电性实验,灯泡很暗
2
③HNO 溶液不与NaSO 溶液反应
2 2 4
④0.1 mol·L-1HNO 溶液中,c(H+)=0.015 mol·L-1
2
⑤相同浓度时,HNO 溶液的导电能力比盐酸弱
2
⑥取0.1 mol·L-1HNO 溶液200 mL,加水至体积为2 L,pH<2
2
A.①②③ B.④⑤⑥
C.①③④ D.①④⑤⑥
B [HNO 溶液能与NaHCO 溶液反应,放出气体,说明HNO 的酸性强于HCO,不能
2 3 2 2 3
判断HNO 是否为弱电解质,①错误;HNO 溶液导电能力与溶液中离子浓度有关,灯泡很暗,
2 2
不能判断HNO 是否为弱电解质,②错误;由于HSO 是稳定的可溶性强酸,HNO 溶液不与
2 2 4 2
NaSO 溶液反应不能判断HNO 是否为弱电解质,③错误;0.1 mol·L-1 HNO 溶液中,c(H+)
2 4 2 2
=0.015 mol·L-1,说明HNO 未完全电离,则HNO 是弱电解质,④正确;相同浓度时,HNO
2 2 2
溶液的导电能力比盐酸弱,说明HNO 并未完全电离,则HNO 是弱电解质,⑤正确;取0.1
2 2
mol·L-1 HNO 溶液200 mL,加水至体积为2 L,pH<2,说明加水稀释时,HNO 电离产生H
2 2
+,则HNO 是弱电解质,⑥正确。]
2
5.(2021·山东日照实验中学检测)下列说法中正确的是( )
A.HCOOH溶于水,当HCOOH电离出的c(H+)=c(HCOO-)时,表明HCOOH处于电离
平衡状态
B.常温下,将1 moL/L醋酸用蒸馏水稀释,稀释过程中,电离程度增大,c(H+)减小
C.常温下,由 1 mol·L-1AOH 溶液的 pH=13,可推知 AOH 溶液电离方程式为
AOH===A++OH-
D.稀释氨水时,所有粒子浓度都一定会减小
B [HCOOH电离出的c(H+)和c(HCOO-)永远相等,不能表明HCOOH处于电离平衡
状态,A项错误。醋酸溶液中存在CHCOOHCHCOO-+H+,加水稀释促进电离,n(H+)
3 3
增大,但体积增大大于电离程度的倍数,c(H+)减小,B项正确;由1 mol·L-1AOH溶液中的
c(OH-)=10-1mol·L-1知,AOH为弱碱,故电离方程式为AOHA++OH-,C项错误;稀释
氨水时,c(OH-)减小,c(H+)增大,D项错误。]
6.(2021·东北育才中学检测)25 ℃时,向盛有50 mL pH=2的HA溶液的绝热容器中加
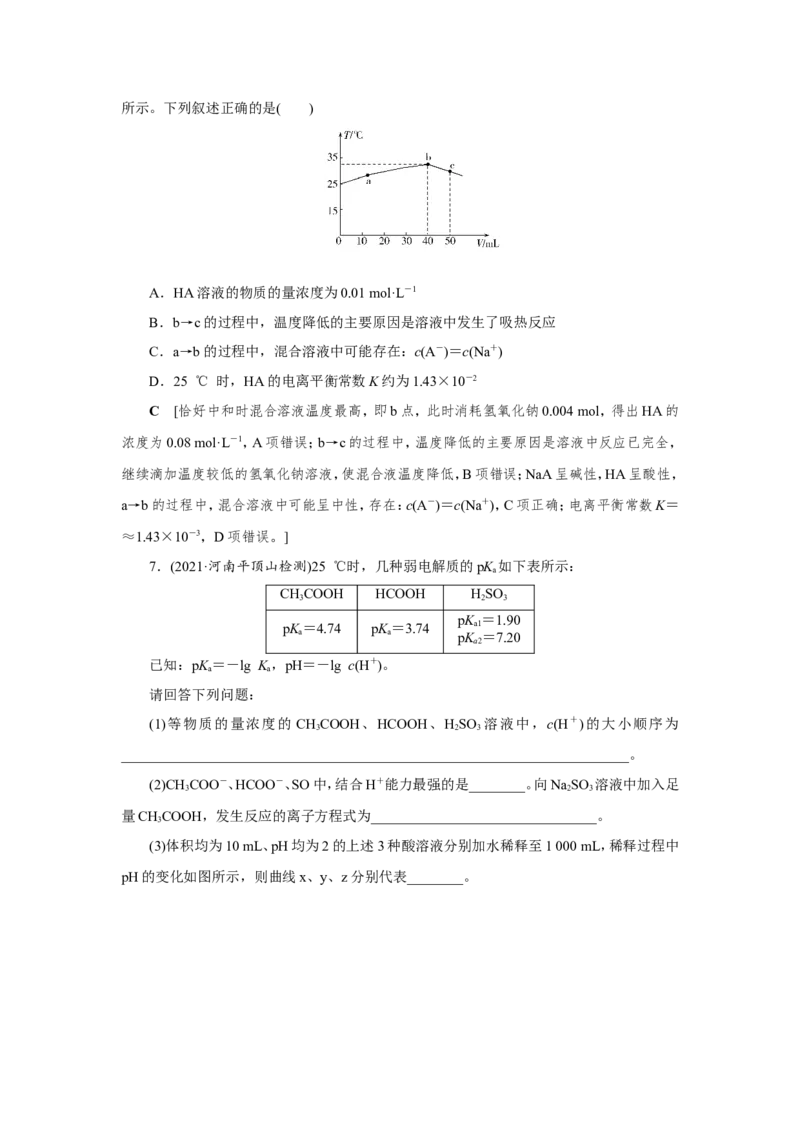
入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。下列叙述正确的是( )
A.HA溶液的物质的量浓度为0.01 mol·L-1
B.b→c的过程中,温度降低的主要原因是溶液中发生了吸热反应
C.a→b的过程中,混合溶液中可能存在:c(A-)=c(Na+)
D.25 ℃ 时,HA的电离平衡常数K约为1.43×10-2
C [恰好中和时混合溶液温度最高,即b点,此时消耗氢氧化钠0.004 mol,得出HA的
浓度为0.08 mol·L-1,A项错误;b→c的过程中,温度降低的主要原因是溶液中反应已完全,
继续滴加温度较低的氢氧化钠溶液,使混合液温度降低,B项错误;NaA呈碱性,HA呈酸性,
a→b的过程中,混合溶液中可能呈中性,存在:c(A-)=c(Na+),C项正确;电离平衡常数K=
≈1.43×10-3,D项错误。]
7.(2021·河南平顶山检测)25 ℃时,几种弱电解质的pK 如下表所示:
a
CHCOOH HCOOH HSO
3 2 3
pK =1.90
pK=4.74 pK=3.74 a1
a a pK =7.20
a2
已知:pK=-lg K,pH=-lg c(H+)。
a a
请回答下列问题:
(1)等物质的量浓度的 CHCOOH、HCOOH、HSO 溶液中,c(H+)的大小顺序为
3 2 3
________________________________________________________________________。
(2)CH COO-、HCOO-、SO中,结合H+能力最强的是________。向NaSO 溶液中加入足
3 2 3
量CHCOOH,发生反应的离子方程式为________________________________。
3
(3)体积均为10 mL、pH均为2的上述3种酸溶液分别加水稀释至1 000 mL,稀释过程中
pH的变化如图所示,则曲线x、y、z分别代表________。解析 (1)由于pK=-lg K,则pK 的值越小,K 越大,对应酸的酸性越强,则酸性:
a a a a
HSO >HCOOH>CH COOH>HSO,故等物质的量浓度的三种溶液中 c(H+)的大小顺序:
2 3 3
HSO >HCOOH>CH COOH。
2 3 3
(2) 酸 性 越 强 , 对 应 酸 根 结 合 H + 的 能 力 就 越 弱 , 由 于 酸 性 :
HSO >HCOOH>CH COOH>HSO,则结合H+的能力:SO>CH COO->HCOO->HSO。由于酸
2 3 3 3
性:HSO > CHCOOH>HSO,NaSO 溶液中加入足量CHCOOH,反应生成NaHSO 和
2 3 3 2 3 3 3
CHCOONa,离子方程式为SO+CHCOOH===HSO+CHCOO-。
3 3 3
(3)由于pH=-lg c(H+),pH越大,溶液中c(H+)越小,由三种溶液稀释相同倍数时pH的
变化快慢可知,酸性:x>y>z,由于酸性:HSO >HCOOH>CH COOH,故x是HSO ,y是
2 3 3 2 3
HCOOH,z是CHCOOH。
3
答案 (1)H SO >HCOOH>CH COOH
2 3 3
(2)SO SO+CHCOOH===HSO+CHCOO-
3 3
(3)H SO HCOOH CHCOOH
2 3 3