文档内容
大题突破 2 综合实验题题型研究
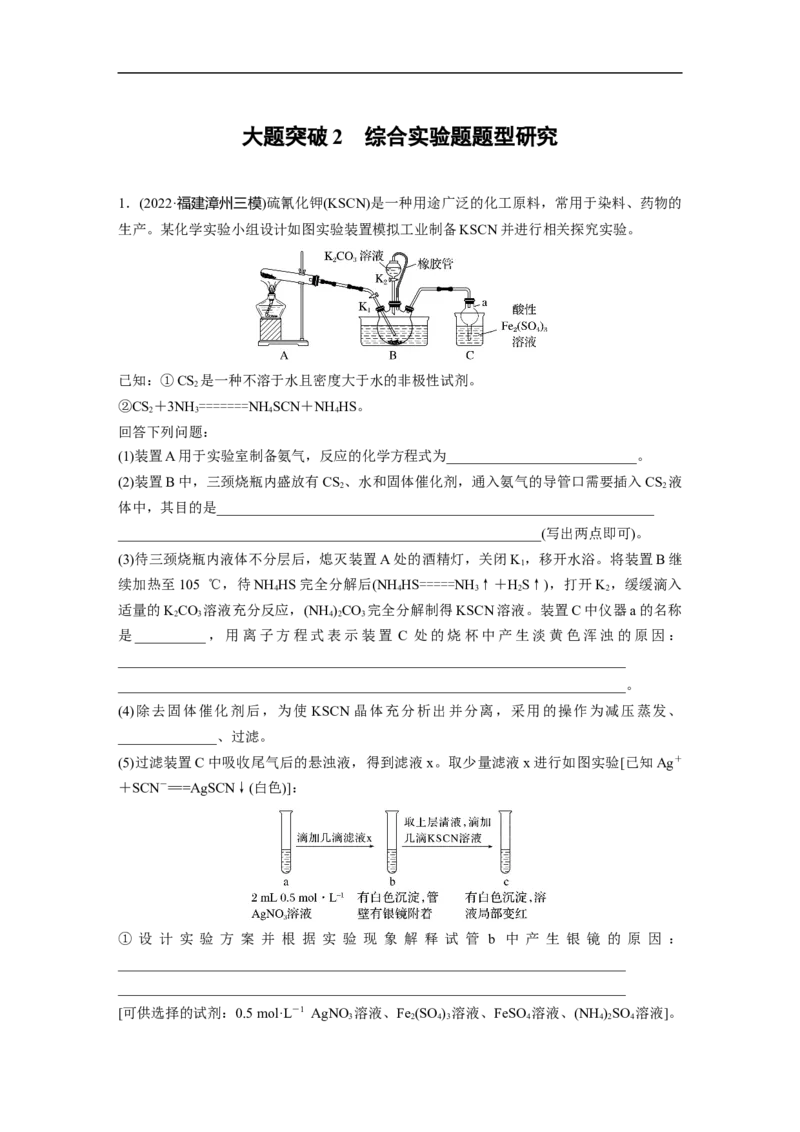
1.(2022·福建漳州三模)硫氰化钾(KSCN)是一种用途广泛的化工原料,常用于染料、药物的
生产。某化学实验小组设计如图实验装置模拟工业制备KSCN并进行相关探究实验。
已知:①CS 是一种不溶于水且密度大于水的非极性试剂。
2
②CS+3NH =======NH SCN+NH HS。
2 3 4 4
回答下列问题:
(1)装置A用于实验室制备氨气,反应的化学方程式为___________________________。
(2)装置B中,三颈烧瓶内盛放有CS 、水和固体催化剂,通入氨气的导管口需要插入CS 液
2 2
体中,其目的是______________________________________________________________
____________________________________________________________(写出两点即可)。
(3)待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K ,移开水浴。将装置B继
1
续加热至105 ℃,待NH HS完全分解后(NH HS=====NH ↑+HS↑),打开K ,缓缓滴入
4 4 3 2 2
适量的KCO 溶液充分反应,(NH )CO 完全分解制得KSCN溶液。装置C中仪器a的名称
2 3 4 2 3
是__________,用离子方程式表示装置 C 处的烧杯中产生淡黄色浑浊的原因:
________________________________________________________________________
________________________________________________________________________。
(4)除去固体催化剂后,为使 KSCN 晶体充分析出并分离,采用的操作为减压蒸发、
______________、过滤。
(5)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液х进行如图实验[已知Ag+
+SCN-===AgSCN↓(白色)]:
① 设 计 实 验 方 案 并 根 据 实 验 现 象 解 释 试 管 b 中 产 生 银 镜 的 原 因 :
________________________________________________________________________
________________________________________________________________________
[可供选择的试剂:0.5 mol·L-1 AgNO 溶液、Fe (SO ) 溶液、FeSO 溶液、(NH )SO 溶液]。
3 2 4 3 4 4 2 4②小组同学观察到试管c中实验现象后,用力振荡试管,又观察到红色褪去且白色沉淀增多,
结合平衡移动的知识解释其原因:____________________________________________
________________________________________________________________________。
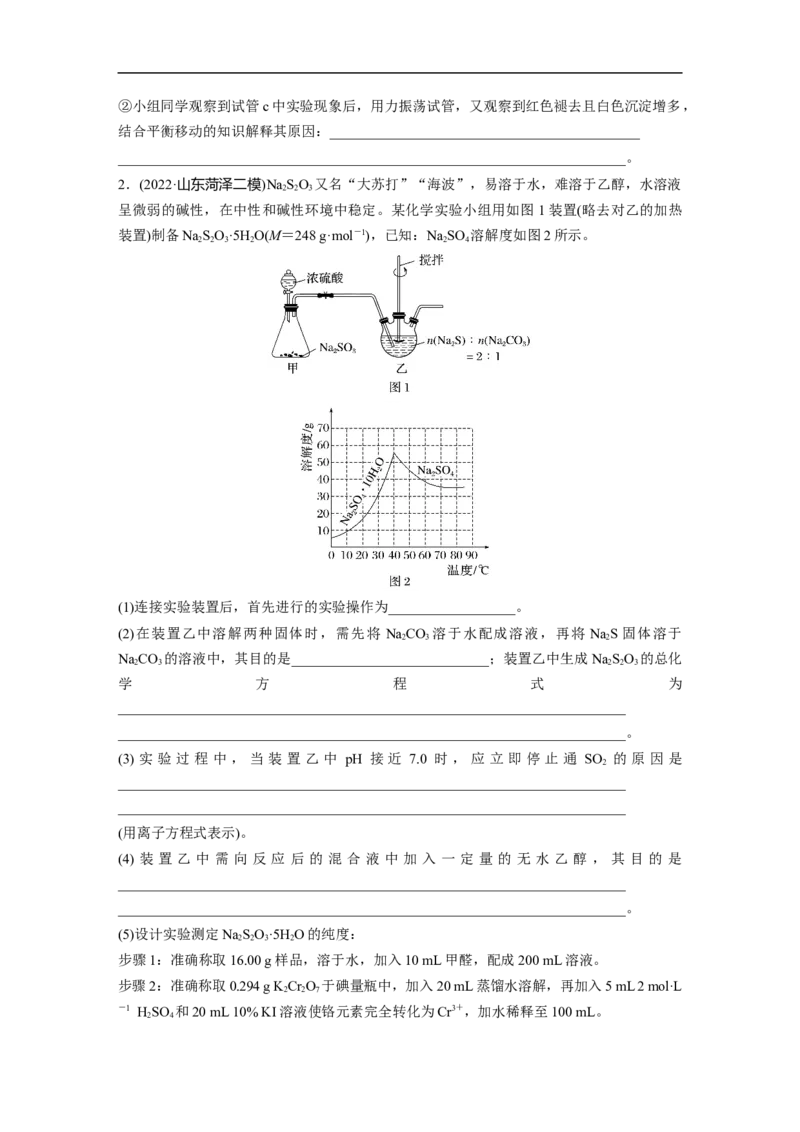
2.(2022·山东菏泽二模)NaSO 又名“大苏打”“海波”,易溶于水,难溶于乙醇,水溶液
2 2 3
呈微弱的碱性,在中性和碱性环境中稳定。某化学实验小组用如图1装置(略去对乙的加热
装置)制备NaSO·5H O(M=248 g·mol-1),已知:NaSO 溶解度如图2所示。
2 2 3 2 2 4
(1)连接实验装置后,首先进行的实验操作为__________________。
(2)在装置乙中溶解两种固体时,需先将 NaCO 溶于水配成溶液,再将 NaS 固体溶于
2 3 2
NaCO 的溶液中,其目的是____________________________;装置乙中生成NaSO 的总化
2 3 2 2 3
学 方 程 式 为
________________________________________________________________________
________________________________________________________________________。
(3) 实 验 过 程 中 , 当 装 置 乙 中 pH 接 近 7.0 时 , 应 立 即 停 止 通 SO 的 原 因 是
2
________________________________________________________________________
________________________________________________________________________
(用离子方程式表示)。
(4) 装 置 乙 中 需 向 反 应 后 的 混 合 液 中 加 入 一 定 量 的 无 水 乙 醇 , 其 目 的 是
________________________________________________________________________
________________________________________________________________________。
(5)设计实验测定NaSO·5H O的纯度:
2 2 3 2
步骤1:准确称取16.00 g样品,溶于水,加入10 mL甲醛,配成200 mL溶液。
步骤2:准确称取0.294 g K CrO 于碘量瓶中,加入20 mL蒸馏水溶解,再加入5 mL 2 mol·L
2 2 7
-1 HSO 和20 mL 10% KI溶液使铬元素完全转化为Cr3+,加水稀释至100 mL。
2 4步骤3:向碘量瓶中加入1 mL 1%淀粉溶液,用待测NaSO 溶液滴定碘量瓶中溶液至终点,
2 2 3
消耗NaSO 溶液20.00 mL(已知:I+2SO===2I-+SO)。
2 2 3 2 2 4
试计算NaSO·5H O的纯度为______________(结果保留三位有效数字)。
2 2 3 2
(6)利用甲装置中的残渣(Na SO 和NaSO 的混合物)制备NaSO ·10H O晶体,将下列实验方
2 4 2 3 2 4 2
案补充完整:将固体混合物溶于水配成溶液,________________________________
________________________________________________________________________
________________________________________________________________________,
洗涤、干燥得NaSO ·10H O晶体(实验中须使用氧气、pH计)。
2 4 2
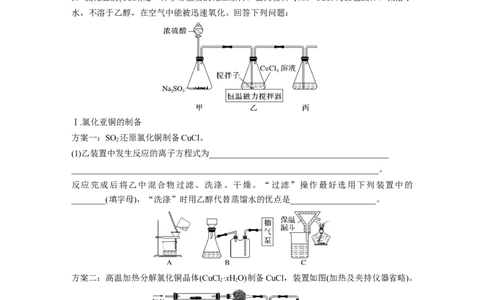
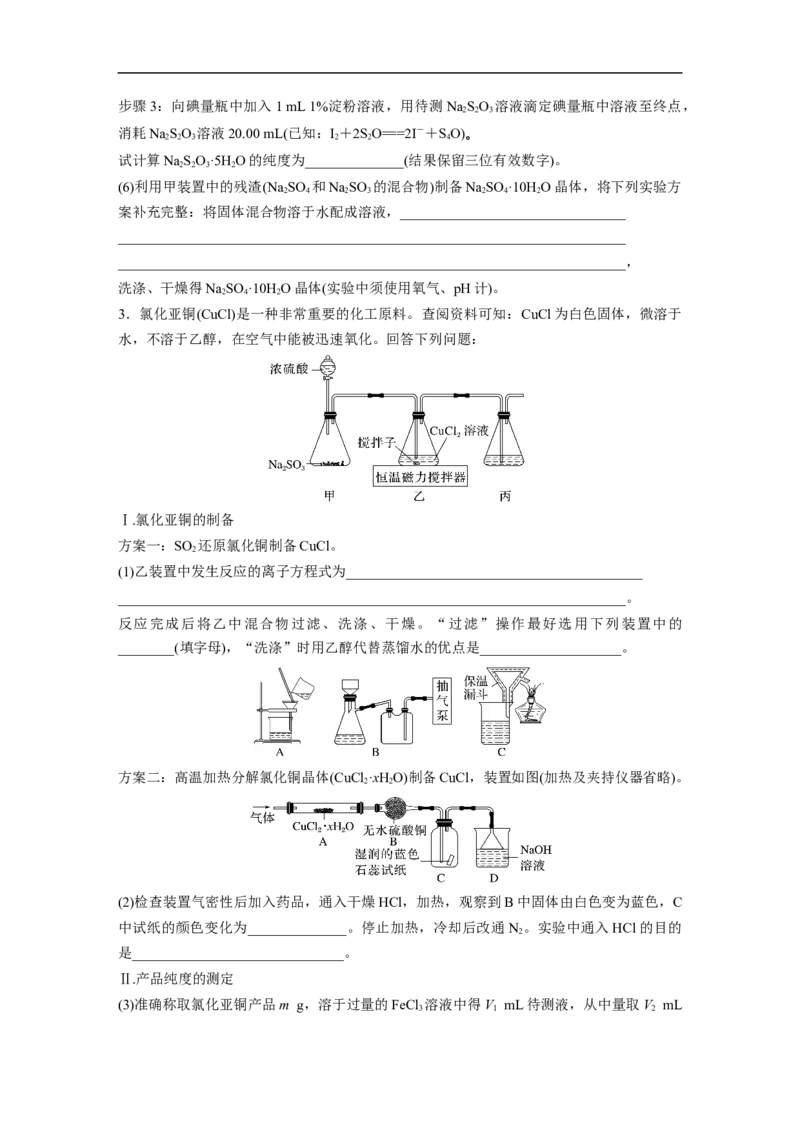
3.氯化亚铜(CuCl)是一种非常重要的化工原料。查阅资料可知:CuCl为白色固体,微溶于
水,不溶于乙醇,在空气中能被迅速氧化。回答下列问题:
Ⅰ.氯化亚铜的制备
方案一:SO 还原氯化铜制备CuCl。
2
(1)乙装置中发生反应的离子方程式为__________________________________________
________________________________________________________________________。
反应完成后将乙中混合物过滤、洗涤、干燥。“过滤”操作最好选用下列装置中的
________(填字母),“洗涤”时用乙醇代替蒸馏水的优点是____________________。
方案二:高温加热分解氯化铜晶体(CuCl ·xHO)制备CuCl,装置如图(加热及夹持仪器省略)。
2 2
(2)检查装置气密性后加入药品,通入干燥HCl,加热,观察到B中固体由白色变为蓝色,C
中试纸的颜色变化为______________。停止加热,冷却后改通N 。实验中通入HCl的目的
2
是______________________________。
Ⅱ.产品纯度的测定
(3)准确称取氯化亚铜产品m g,溶于过量的FeCl 溶液中得V mL待测液,从中量取V mL
3 1 2于锥形瓶中,加入2滴邻菲罗啉指示剂,立即用a mol·L-1硫酸铈[Ce(SO )]标准溶液滴定至
4 2
终点,消耗Ce(SO) 溶液b mL。产品中CuCl的质量分数为_______%。(已知:CuCl+Fe3+
4 2
===Cu2++Fe2++Cl-,Fe2++Ce4+===Fe3++Ce3+)
下列有关滴定的说法错误的是______(填字母)。
A.未用标准溶液润洗滴定管会使测定结果偏低
B.滴定时要适当控制滴定速度
C.在接近终点时,使用“半滴操作”可提高滴定的准确度
D.滴定前滴定管尖嘴部分有气泡,滴定后无气泡会使测定结果偏低
4.(2022·福建省惠安第一中学三模)某学习小组为了探究SO 的还原性,按图示设计并进行
2
实验(部分装置省略)。回答下列问题:
(1)仪器a的名称为______________,装置B的作用是____________________________
________________________________________________________________________。
(2)预测SO 与FeCl 溶液发生氧化还原反应的离子方程式为______________________
2 3
________________________________________________________________________。
(3)往C中持续通入SO 至饱和,观察到溶液先变红色,5分钟后变黄,约9小时后变为浅绿
2
色。
经查资料:红色物质可能是Fe3+与HSO、SO形成的配合物,配合物可表示为[Fe(A) (H O) ]3-
n 2 m
xn(A为HSO或SO,x为1或2,n+m=6,n越大配合物越稳定,溶液颜色越深)。室温下进
行以下实验。
序号 操作 现象
溶液先变红,随后产生沉淀和刺
向1 mL 1 mol·L-1 FeCl 溶液中滴
3
实验1 激性气味气体。抽滤得到橙黄色
加3 mL 1 mol·L-1 NaHSO 溶液
3
沉淀
溶液先变红,析出少量沉淀,加
向1 mL 1 mol·L-1 FeCl 溶液中滴
3
实验2 至2 mL析出大量沉淀,加至3
加3 mL 1 mol·L-1 Na SO 溶液
2 3
mL沉淀溶解,溶液颜色加深
实验3[略,判断实验1抽滤得到的沉淀不是Fe(OH) ]
3
① 通 过 计 算 说 明 实 验 1 得 到 的 沉 淀 为 Fe (SO ) , 而 非 Fe(HSO ) :
2 3 3 3 3
________________________________________________________________________。
已知:K [Fe(OH) ]=2.6×10-39、K (H SO )=1.2×10-2、K (H SO )=5.6×10-8。
sp 3 a1 2 3 a2 2 3
②实验1生成沉淀和气体的离子方程式为______________________________________________________________________________________________________________。
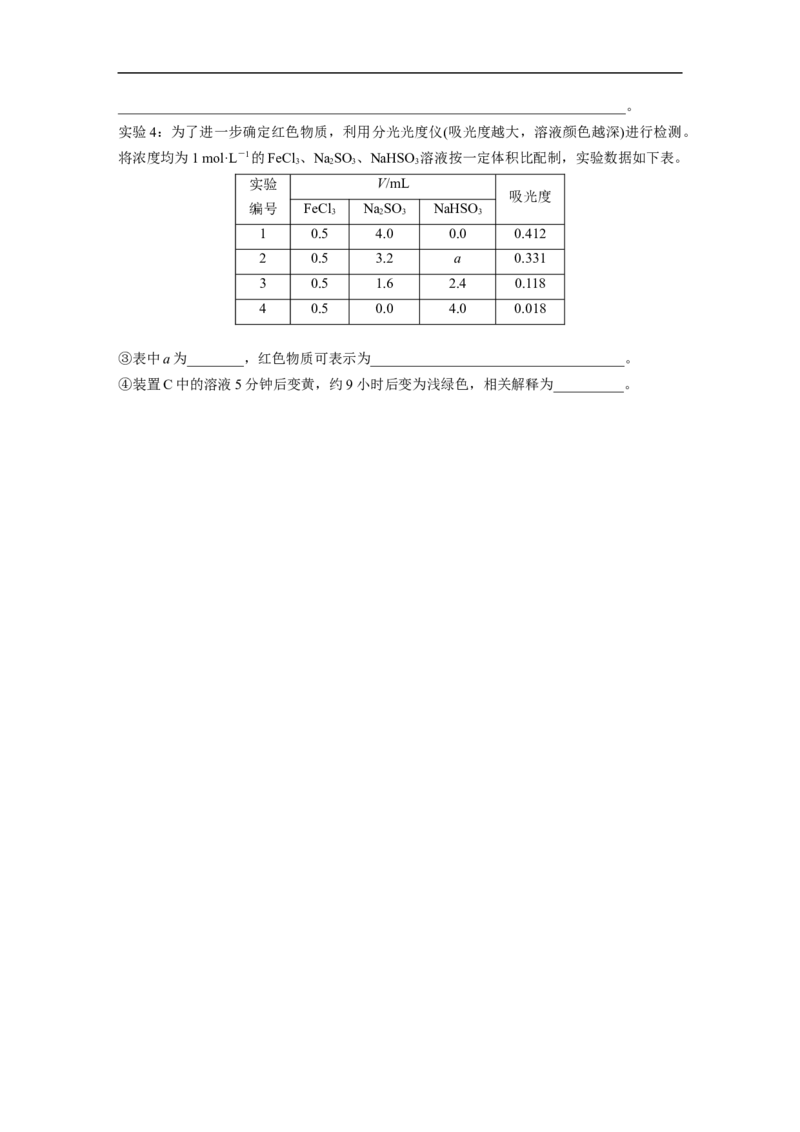
实验4:为了进一步确定红色物质,利用分光光度仪(吸光度越大,溶液颜色越深)进行检测。
将浓度均为1 mol·L-1的FeCl 、NaSO 、NaHSO 溶液按一定体积比配制,实验数据如下表。
3 2 3 3
实验 V/mL
吸光度
编号 FeCl NaSO NaHSO
3 2 3 3
1 0.5 4.0 0.0 0.412
2 0.5 3.2 a 0.331
3 0.5 1.6 2.4 0.118
4 0.5 0.0 4.0 0.018
③表中a为________,红色物质可表示为____________________________________。
④装置C中的溶液5分钟后变黄,约9小时后变为浅绿色,相关解释为__________。