文档内容
1.下列所得溶液的物质的量浓度为0.1 mol·L-1的是( )
A.将0.1 mol氨充分溶解在1 L水中
B.将10 g质量分数为98%的硫酸与990 g水混合
C.将25.0 g胆矾溶于水配成1 L溶液
D.将10 mL 1 mol·L-1的盐酸与90 mL水充分混合
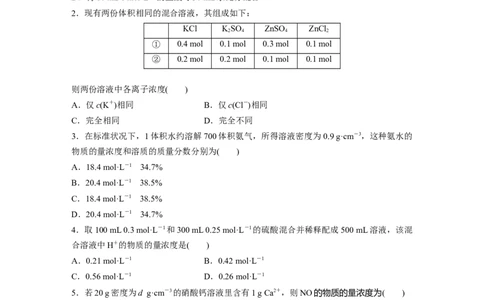
2.现有两份体积相同的混合溶液,其组成如下:
KCl KSO ZnSO ZnCl
2 4 4 2
① 0.4 mol 0.1 mol 0.3 mol 0.1 mol
② 0.2 mol 0.2 mol 0.1 mol 0.1 mol
则两份溶液中各离子浓度( )
A.仅c(K+)相同 B.仅c(Cl-)相同
C.完全相同 D.完全不同
3.在标准状况下,1体积水约溶解700体积氨气,所得溶液密度为0.9 g·cm-3,这种氨水的
物质的量浓度和溶质的质量分数分别为( )
A.18.4 mol·L-1 34.7%
B.20.4 mol·L-1 38.5%
C.18.4 mol·L-1 38.5%
D.20.4 mol·L-1 34.7%
4.取100 mL 0.3 mol·L-1和300 mL 0.25 mol·L-1的硫酸混合并稀释配成500 mL溶液,该混
合溶液中H+的物质的量浓度是( )
A.0.21 mol·L-1 B.0.42 mol·L-1
C.0.56 mol·L-1 D.0.26 mol·L-1
5.若20 g密度为d g·cm-3的硝酸钙溶液里含有1 g Ca2+,则NO的物质的量浓度为( )
A. mol·L-1 B. mol·L-1
C.2.5d mol·L-1 D.1.25d mol·L-1
6.(2022·天津滨海七校联考)将物质的量均为a mol的Na和Al一同投入m g足量水中,所
得溶液的密度为ρ g·cm-3,则此溶液的物质的量浓度为( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
7.下列说法正确的是( )
A.把100 mL 3 mol·L-1的HSO 跟100 mL H O混合,硫酸的物质的量浓度为1.5 mol·L-1
2 4 2B.把100 g 20%的NaCl溶液跟100 g HO混合后,NaCl溶液的溶质质量分数是10%
2
C.把200 mL 3 mol·L-1的BaCl 溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)
2
仍然是3 mol·L-1
D.把100 mL 20%的NaOH溶液跟100 mL H O混合后,NaOH溶液的溶质质量分数是10%
2
8.若以w 和w 分别表示浓度为c mol·L-1和c mol·L-1的氨水的质量分数,且知 2c =
1 2 1 2 1
c,则下列推断正确的是( )
2
A.2w=w B.2w=w
1 2 2 1
C.w>2w D.w<w<2w
2 1 1 2 1
9.配制250 mL 0.5 mol·L-1的NaOH溶液,在下列仪器中:①量筒、②250 mL容量瓶、③
托盘天平和砝码、④500 mL容量瓶、⑤烧杯、⑥玻璃棒、⑦漏斗、⑧药匙、⑨胶头滴管、
⑩250 mL烧瓶,需要用到的仪器按使用先后顺序排列正确的是( )
A.⑧③⑤⑥②⑨ B.②③⑦⑤⑥
C.②⑤⑦⑥① D.④③⑦⑤⑥
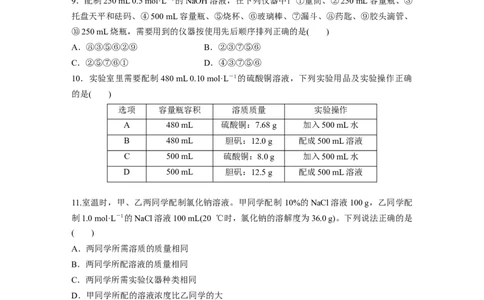
10.实验室里需要配制480 mL 0.10 mol·L-1的硫酸铜溶液,下列实验用品及实验操作正确
的是( )
选项 容量瓶容积 溶质质量 实验操作
A 480 mL 硫酸铜:7.68 g 加入500 mL水
B 480 mL 胆矾:12.0 g 配成500 mL溶液
C 500 mL 硫酸铜:8.0 g 加入500 mL水
D 500 mL 胆矾:12.5 g 配成500 mL溶液
11.室温时,甲、乙两同学配制氯化钠溶液。甲同学配制 10%的NaCl溶液100 g,乙同学配
制1.0 mol·L-1的NaCl溶液100 mL(20 ℃时,氯化钠的溶解度为36.0 g)。下列说法正确的是
( )
A.两同学所需溶质的质量相同
B.两同学所配溶液的质量相同
C.两同学所需实验仪器种类相同
D.甲同学所配的溶液浓度比乙同学的大
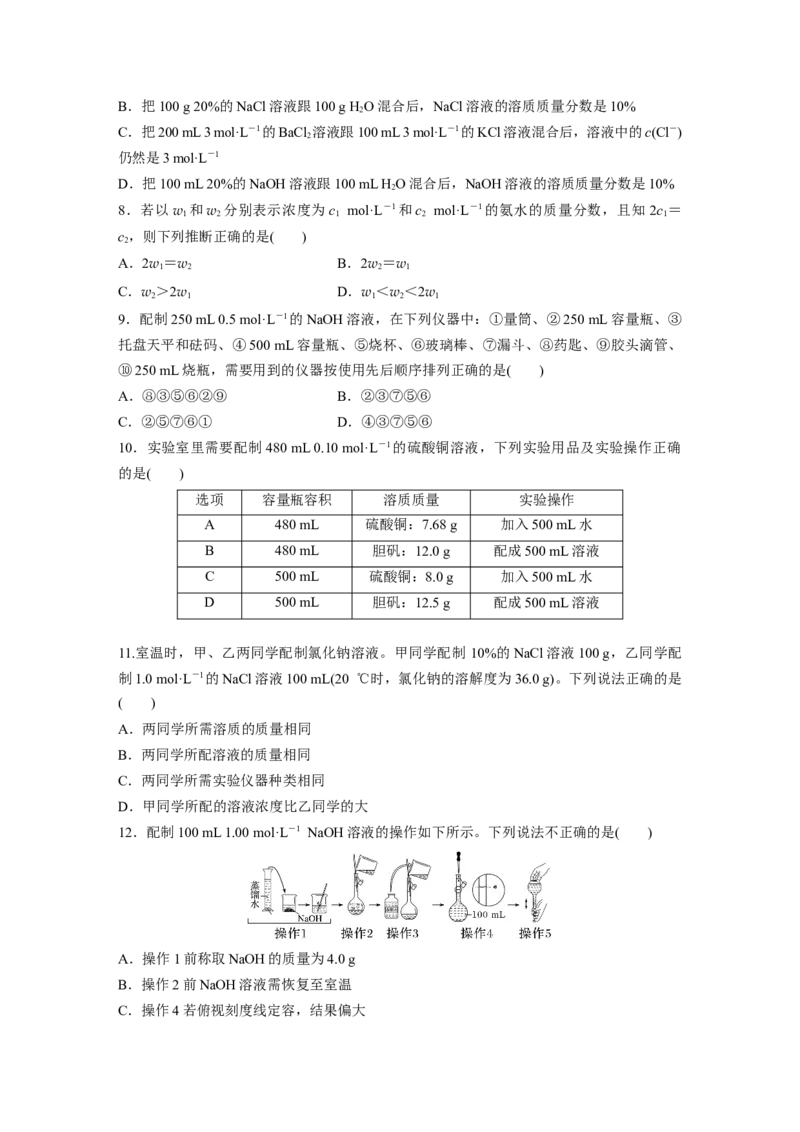
12.配制100 mL 1.00 mol·L-1 NaOH溶液的操作如下所示。下列说法不正确的是( )
A.操作1前称取NaOH的质量为4.0 g
B.操作2前NaOH溶液需恢复至室温
C.操作4若俯视刻度线定容,结果偏大D.操作5后液面下降,需补充少量水至刻度线
13.现有由硝酸钾、硝酸铵、硝酸镁组成的无土栽培液0.2 L,部分离子的浓度如下表所示:
离子种类 NH Mg2+ NO
物质的量浓度/(mol·L-1) 0.2 0.1 0.6
(1)混合液中,硝酸铵的物质的量为________,硝酸钾的质量为________________。
(2)该混合溶液中硝酸镁的物质的量浓度为___________________________,将该混合溶液加
水稀释至体积为1 L,稀释后溶液中NO的物质的量浓度为___________________________。
(3)向该稀释后的溶液中通入标准状况下的NH ________L可使Mg2+沉淀完全,写出Mg2+沉
3
淀过程中的离子方程式: __________________________________________________。
14.绿矾(FeSO ·7H O)在化学合成上用作还原剂及催化剂。工业上常用废铁屑溶于一定浓度
4 2
的硫酸溶液制备绿矾。
(1)98% 1.84 g·cm-3的浓硫酸在稀释过程中,密度下降,当稀释至50%时,密度为1.4 g·cm-
3,50%的硫酸物质的量浓度为__________(结果保留两位小数),50%的硫酸与30%的硫酸等体
积混合,混合酸的质量分数________(填“>”“<”或“=”)40%。
(2)将111.2 g绿矾(FeSO ·7H O,式量为278)在高温下加热,充分反应后生成Fe O 固体和
4 2 2 3
SO 、SO 、水的混合气体,则生成Fe O 的质量为________g;SO 为________mol。
2 3 2 3 2
实验室可用以下方法制备莫尔盐晶体[(NH )SO ·FeSO ·6H O,式量为392]。
4 2 4 4 2
(3)将4.88 g铁屑(含Fe O)与25 mL 3 mol·L-1 HSO 充分反应后,得到FeSO 和HSO 的混
2 3 2 4 4 2 4
合溶液,稀释溶液至100 mL,测得其pH=1。铁屑中Fe O 的质量分数是________(结果保
2 3
留两位小数)。
(4)向上述100 mL溶液中加入与该溶液中FeSO 等物质的量的(NH )SO 晶体,待晶体完全溶
4 4 2 4
解后蒸发掉部分水,冷却至t ℃,析出莫尔盐晶体12.360 g,剩余溶液的质量为82.560 g。t
℃时,计算(NH )SO ·FeSO ·6H O的溶解度为________(结果保留两位小数)。
4 2 4 4 2
15.人体血液里Ca2+的浓度一般采用m g·cm-3来表示。抽取一定体积的血样,加适量的草
酸铵[(NH )C O]溶液,可析出草酸钙(CaC O)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得
4 2 2 4 2 4
草酸(H C O),再用酸性KMnO 溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习
2 2 4 4
小组设计如下实验步骤测定血液样品中Ca2+的浓度。
Ⅰ.配制酸性KMnO 标准溶液:如图是配制50 mL酸性KMnO 标准溶液的过程示意图。
4 4(1)请你观察图示并判断其中不正确的操作有________(填序号)。
(2)其中确定50 mL溶液体积的容器是________(填名称)。
(3)如果按照图示的操作配制溶液,在其他操作均正确的情况下,配制溶液的浓度将
________(填“偏大”或“偏小”)。
Ⅱ.测定血液样品中Ca2+的浓度:取血液样品20.00 mL,经过上述处理后得到草酸,再用
0.020 mol·L-1酸性KMnO 溶液滴定,使草酸转化成CO 逸出,这时共消耗12.00 mL酸性
4 2
KMnO 溶液。
4
(4)已知草酸与酸性KMnO 溶液反应的离子方程式为 5HC O +2MnO+6H+===2Mnx++
4 2 2 4
10CO↑+8HO,则式中的x=________。
2 2
(5)滴定时,根据现象_________________________________________________,
即可确定反应达到终点。
(6)经过计算,血液样品中Ca2+的浓度为______mg·cm-3。