文档内容
第 30 讲 晶体结构与性质
1.实验室制取HF的原理为 ,氢氟酸可用来刻蚀玻璃,发生反应:
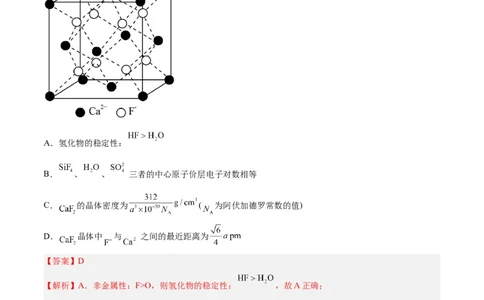
。 的立方晶胞如图所示,其晶胞参数为a pm。下列说法错误的是
A.氢化物的稳定性:
B. 、 、 三者的中心原子价层电子对数相等
C. 的晶体密度为 ( 为阿伏加德罗常数的值)
D. 晶体中 与 之间的最近距离为
【答案】D
【解析】A.非金属性:F>O,则氢化物的稳定性: ,故A正确;
B. 、 和 的中心原子的价层电子时数均为4,故B正确;
C.由氟化钙晶胞可知每个晶胞中含有4个 ,8个 ,由晶胞结构可知其密度为 故
C正确;
D. 晶体中 为面心立方最密堆积, 位于 围成的正四面体的空隙中, 与 之间的最近距离为立方晶胞体对角线长的 ,即为 ,故D错误;
答案选D。
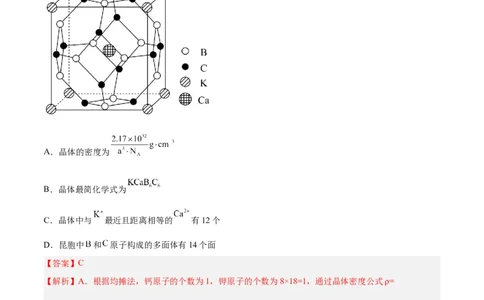
2.科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为 。阿伏加德罗常数的
值为 。下列说法错误的是
A.晶体的密度为
B.晶体最简化学式为
C.晶体中与 最近且距离相等的 有12个
D.昆胞中 和 原子构成的多面体有14个面
【答案】C
【解析】A.根据均摊法,钙原子的个数为1,钾原子的个数为8×18=1,通过晶体密度公式ρ=
= ,故A正确;
B.根据均摊法,钙原子的个数为1,钾原子的个数为8×18=1,硼原子、碳原子个数均为12× =6,晶体
最简化学式为KCaB C ,故B正确;
6 6
C.晶体最简化学式为KCaB C ,根据与Ca2+最近且距离相等的K+有8个,可判断与K+最近且距离相等的
6 6
Ca2+的个数也为8个,故C错误;D.通过欧拉定理:顶点数+面数-棱数=2,则面数=棱数-顶点数+2=36-24+2=14,故D正确;
故选C。
3.CaC 晶体的晶胞结构与 NaCl 晶体的晶胞结构相似(如图所示),但CaC 晶体中含有哑铃形的 ,使晶
2 2
胞沿一个方向拉长,下列关于CaC 晶体的说法正确的是
2
A.每个 Ca2+ 周围距离最近且相等的 的数目为 6
B.CaC 晶体,每个晶胞中含有 4 个 Ca2+ 和 4 个
2
C.6.4 gCaC 晶体中含有 0.2 mol 阴离子
2
D.每个 Ca2+周围距离最近且相等的 Ca2+有 12 个
【答案】B
【解析】A.根据题意可知,存在C 使沿一个方向拉长,根据晶胞图可知,每个Ca2+周围距离最近且相
等的C 的数目为4,故A错误;
B.CaC 晶体中,每个晶胞中含有Ca2+数目为 =4个,C 的数目为 =4,故B正确;
2
C.6.4gCaC 物质的量为0.1mol,CaC 中的阴离子为C ,则含阴离子物质的量为0.1mol,故C错误;
2 2
D.该晶胞中沿一个方向拉长,导致晶胞的一个平面的长与宽不等,与每个Ca2+距离相等且最近的Ca2+应
为4个,故D错误;
答案为B。
4.氮化硼(BN)晶体有多种结构。六方相氨化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作
高温润滑剂;立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示,关于这两种晶体的
说法正确的是A.两种晶体中B原子的杂化方式均为sp2
B.两种晶体中B-N键键长相等
C.六方相氮化硼层间共价键键能较小,所以可做高温润滑剂
D.每个立方氮化硼晶胞中含有4个B原子和4个N原子
【答案】D
【解析】A.立方氮化硼中硼原子形成4个共价键,所以立方氮化硼中硼原子采用的是sp3杂化,选项A错
误;
B.六方相氨化硼具有层状结构,立方相氮化硼形成正四面体结构,两种晶体中B-N键键长不相等,选项
B错误;
C.六方相氮化硼层间作用力为范德华力,相对较小,所以可做高温润滑剂,选项C错误;
D.根据立方氨化硼的晶胞示意图,每个晶胞中B原子个数是8 +6 =4,N原子个数为4,选项D正
确;
答案选D。
5.汞钡铜氧晶体的晶胞如图A所示,通过掺杂Ca2+获得的具有更高临界温度的超导材料如图B所示。下
列说法正确的是A.掺杂后晶体密度增大是因为晶胞中增加了1个Ca2+
B.汞钡铜氧晶体中的Hg和Cu个数比为1∶2
C.图A晶胞中一个Ba的分数坐标为( , , ),则另一个( , , )
D.图B晶胞中Ca周围距离最近的Hg数目和Hg周围距离最近的Ca的数目不同
【答案】C
【解析】A.由图A可知,汞钡铜氧晶体的晶胞中含 个Hg,2个Ba, 个Cu,
个O,掺杂Ca2+后,晶胞中含 个Hg,2个Ba, 个Cu, 个
O,1个Ca2+,所以掺杂后晶体密度增大不是因为晶胞中增加了1个Ca2+,故A错误;
B.由汞钡铜氧晶体的晶胞可知,Hg位于晶胞的顶点,则一个晶胞中含 个Hg,Cu位于晶胞的棱
上,则则一个晶胞中含 个Cu,汞钡铜氧晶体中的Hg和Cu个数比为1∶1,故B错误;
C.图A晶胞中两个Ba位于同一轴上,若一个Ba的分数坐标为( , , ),则另一个Ba的分数坐标
为( , , ),故C正确;
D.图B晶胞中Ca周围距离最近的Hg数目为8,Hg周围距离最近的Ca的数目也为8,则图B晶胞中Ca
周围距离最近的Hg数目和Hg周围距离最近的Ca的数目相同,故D错误;
答案选C。
6.铅磷青铜具有很高的耐腐蚀性和耐磨性,常用于制作耐磨零件和滑动轴承。如图为铅磷青铜的一种晶胞结构,已知A点原子的分数坐标为(0,0,0),B点原子的分数坐标为(1,1,0);下列说法不正确的是
A.该晶胞的化学式为PbCu P
3
B.C点原子的分数坐标为(0.5,0.5,1)
C.晶胞中,Pb位于第六周期第ⅣA族,Cu属于第ⅠB位于d区
D.晶体中基态磷原子的核外电子共有9种空间运动状态
【答案】C
【解析】A.由题干晶胞图可知,一个晶胞中含有1个P,含有Cu的个数为: =3个,含有Pb的个数
为: =1个,故该晶胞的化学式为PbCu P,A正确;
3
B.已知A点原子的分数坐标为(0,0,0),B点原子的分数坐标为(1,1,0),结合题干晶胞图可知C点原
子的分数坐标为(0.5,0.5,1),B正确;
C.已知Pb和C、Si、Ge、Sn同一主族,故Pb位于第六周期第ⅣA族,Cu是29号元素,其价电子排布
式为:3d104s1,属于第ⅠB位于ds区,C错误;
D.已知P是15号元素,其核外电子排布式为:1s22s22p63s23p3,故P原子核外占据9个不同的原子轨道,
即晶体中基态磷原子的核外电子共有9种空间运动状态,D正确;
故答案为:C。
7.砷化镓是一种立方晶系如图甲所示,将Mn掺杂到晶体中得到稀磁性半导体材料如图乙所示,砷化镓的
晶胞密度为gcm-3。下列说法错误的是
A.1mol砷化镓中配位键的数目是4N
AB.掺入Mn的晶体中Mn、Ga、As的原子个数比为5:26:32
C.沿体对角线a→b方向投影图如丙,若c在11处,则As的位置为7、9、11、13
D.该晶体中距离最近的两个镓原子之间的距离为 pm
【答案】B
【解析】A.由图甲知,1个As与4个Ga形成As-Ga共价键,即砷化镓中As的配位数为4,则1mol砷化
镓中配位键的数目是4N ,A正确;
A
B.掺入Mn的晶体中Ga有7个位于顶点,5个位于面心,个数为: ;As有4个位于体
内,Mn有1个位于顶点,1个位于面心,个数为: ;Mn、Ga、As的原子个数比为 :
:4=5:27:32,B错误;
C.由砷化镓晶胞结构可知,c位于侧面的面心,沿体对角线a→b方向投影图如丙,则As的位置为7、9、
11、13,C正确;
D.由晶胞结构可知,距离最近的两个镓原子之间的距离为面对角线的一半,晶胞中含4个Ga和4个As,
晶胞质量为 ,晶胞体积为 ,则晶胞边长为: pm,两个镓原子之间的最近距离为
pm,D正确;
故选:B。
8. 纳米晶体作为新一代光电半导体材料,已被广泛应用于光电子器件领域。 的晶胞为
立方型,其结构如下图所示。容忍因子 ( 、 和 分别代表着A、B、C位的离子半
径),其数值越接近1,晶体结构越稳定。已知 。下列说法错误的是A. 晶体中 和 的配位数均为6
B. 晶体中 填充在 构成的正八面体空隙中
C.若要提高 晶体的稳定性,可用离子半径略小于 的离子取代
D.若某 型晶体的容忍因子 ,则A、B位的离子均恰好与C位的离子相切
【答案】A
【解析】A.根据晶胞结构可知 晶体中 的配位数为12, 的配位数均为6,A错误;
B.根据晶胞结构 晶体中 填充在 构成的正八面体空隙中,B正确;
C.根据题干可知容忍因子其数值越接近1,晶体结构越稳定, 处于B位, ,若用
离子半径略小于 的离子取代 ,容忍因子的分母减小、容忍因子增大,越来越接近1,会提高晶体
的稳定性,C正确;
D. 说明 ,则A、B位的离子均恰好与C位的离子相切,D正确;
故选A。
9.实验室制取HF的原理为 ,氢氟酸可用来刻蚀玻璃,发生反应:
。 的立方晶胞如图所示,其晶胞参数为 。下列说法错误的是A.简单氢化物的稳定性:
B. 、 、 三者的VSEPR模型均为四面体形
C. 晶体与Si晶体的晶体类型相同,二者均为良好的半导体
D. 晶体中 与 之间的最近距离为
【答案】C
【解析】A.非金属性: ,则简单氢化物的稳定性: ,A正确;
B. 、 和 的中心原子的价层电子对数均为4,故VSEPR模型均为四面体形,B正确;
C.二氧化硅晶体和硅晶体均为共价晶体,共同点为熔点高、硬度大,不同点是二氧化硅晶体不导电,硅
晶体是良好的半导体材料,C错误;
D. 晶体中 为面心立方最密堆积, 位于 围成的正四面体的空隙中, 与 之间的最近
距离为立方晶胞体对角线长的 ,即为 ,D正确;
故答案为:C。
10.锌晶胞如图1所示,锌一二氧化锰电池如图2所示。下列叙述中正确的是已知:锌晶胞的底边长为apm,高为bpm;N 为阿伏加德罗常数的值;2M表示2mol•L-1。
A
A.放电过程中,Mn2+向负极区迁移
B.正极质量减少5.22g时,减少的锌晶胞数为0.01N
A
C.锌晶体的密度为ρ= g•cm-3
D.Zn的价电子排布式为1s22s22p63s23p63d104s2
【答案】B
【分析】锌一二氧化锰电池中Zn发生失电子的氧化反应,作负极,MnO 作正极。
2
【解析】A.根据图2,交换膜为阴离子交换膜,硫酸根离子向负极区迁移,A项错误;
B.正极的电极反应式为 ,5.22g 的物质的量为0.06mol,负极的
电极反应式为 ,根据电子守恒,溶解的锌为0.06mol,而1个锌晶胞含6个锌原子,故减
少的锌晶胞数为0.01N ,B项正确;
A
C.根据六棱柱体积计算方法以及密度公式直接计算锌密度,
cm ,故密度为ρ= g•cm-3,C项错误;
D.Zn的价电子排布式为 ,D项错误。故选B。
11.某水性钠离子电池电极材料由 、 、 、 组成,其立方晶胞嵌入和嵌出 过程中,
与 含量发生变化,依次变为格林绿、普鲁士蓝、普鲁士白三种物质,其过程如图所示。下列说法
错误的是
A.普鲁士蓝中 与 个数比为1:2
B.格林绿晶体中 周围等距且最近的 数为6
C.每个 晶胞完全转化为 晶胞,转移8个
D.若普鲁士白的晶胞棱长为a pm,则其晶体的密度为
【答案】A
【解析】A.根据均摊原则,普鲁士蓝晶胞中含Fe: 、CN-数为
、Na+数为4,根据化合价代数和等于0,可知Fe2+ 与Fe3+个数比为1:1,A错误;
B.根据晶胞图,格林绿晶体中 周围等距且最近的 数为6,B正确;
C.每个 晶胞有8个 完全转化为 晶胞,转移8个 ,C正确;
D.根据均摊原则,普鲁士白晶胞中含Fe: 、CN-数为 、
Na+数为8,若普鲁士白的晶胞棱长为a pm ,则其晶体的密度为= ,D正确;
故选A。
12. 晶体的晶胞结构如图所示。下列说法不正确的是
A.阴、阳离子个数比为
B. 晶体中距离 最近的 的数目为12
C.若晶胞边长均为 ,则 和 之间的最短距离为
D.阳离子位于由阴离子构成的正八面体空隙中
【答案】C
【解析】A. 位于顶点和面心,个数为 , 位于棱心和体心,个数为 ,阴、
阳离子个数比为 ,A项正确;
B. 晶体的晶胞中,该晶体中距离 最近的 的数目为12,B项正确;
C. 与 之间的最短距离等于晶胞面对角线的一半,即 和 之间的最短距离为 ,C项错
误;
D.由晶胞结构可知,晶胞中心的阳离子位于由阴离子构成的正八面体的中心,D项正确;
故选C。
13.下列有关说法不正确的是A.MgO的离子键的键能大于CaO的
B.干冰和 的晶体类型相同
C.如图所示的晶胞的化学式为
D.DNA双螺旋的两个螺旋链通过氢键相互结合
【答案】B
【解析】A. 的半径小于 ,所以 的离子键的键能大于 的,A正确;
B.干冰 为分子晶体, 为共价晶体,二者的晶体类型不相同,B错误;
C.如图所示的晶胞, 在体心,个数为1, 在顶点,个数为 , 在棱上,个数为 ,
所以该晶胞的化学式为 ,C正确;
D.DNA双螺旋含有N、H原子,两个螺旋链通过氢键相互结合,D正确;
故选B。
14.冰晶石( )常用作电解铝的助熔剂和研磨产品的耐磨添加剂,其晶胞结构如图所示,已知该晶胞
参数为a pm, 表示阿伏加德罗常数的值。下列说法错误的是
A. 中Al的配位数为6B.图中△位置填充的是Na
C.晶胞中 形成的全部四面体空隙和 的比值为1∶1
D.该晶体的密度为 g⋅cm-3
【答案】C
【解析】A. 中Al的配位数为6,A正确;
B.图中△位置填充的是 ,B正确;
C. 形成的全部四面体空隙和 的比值为2∶1,C错误;
D.该晶体的密度为 g⋅cm ,D正确;
故选C。
15.已知:2NO (g)+NaCl(s) NaNO3(s)+ClNO(g) ,下列说法正确的是
2
A.该反应的平衡常数可表达为
B.该反应一定能自发进行
C.降温有利于提高 的平衡转化率
D.NaCl晶胞(如图所示)中每个 周围与其距离最近的 有6个
【答案】C
【解析】A.该反应的平衡常数可表达为 ,故A错误;B.由题干信息可知,该反应的 , ,当 时,反应能自发进行,故该反应在低温
条件下易自发进行,故B错误;
C.该反应为放热反应,降温平衡正向移动,有利于提高 的平衡转化率,故C正确;
D.NaCl晶胞(如图所示)中每个 周围与其距离最近的 有12个,故D错误。
答案为:C。
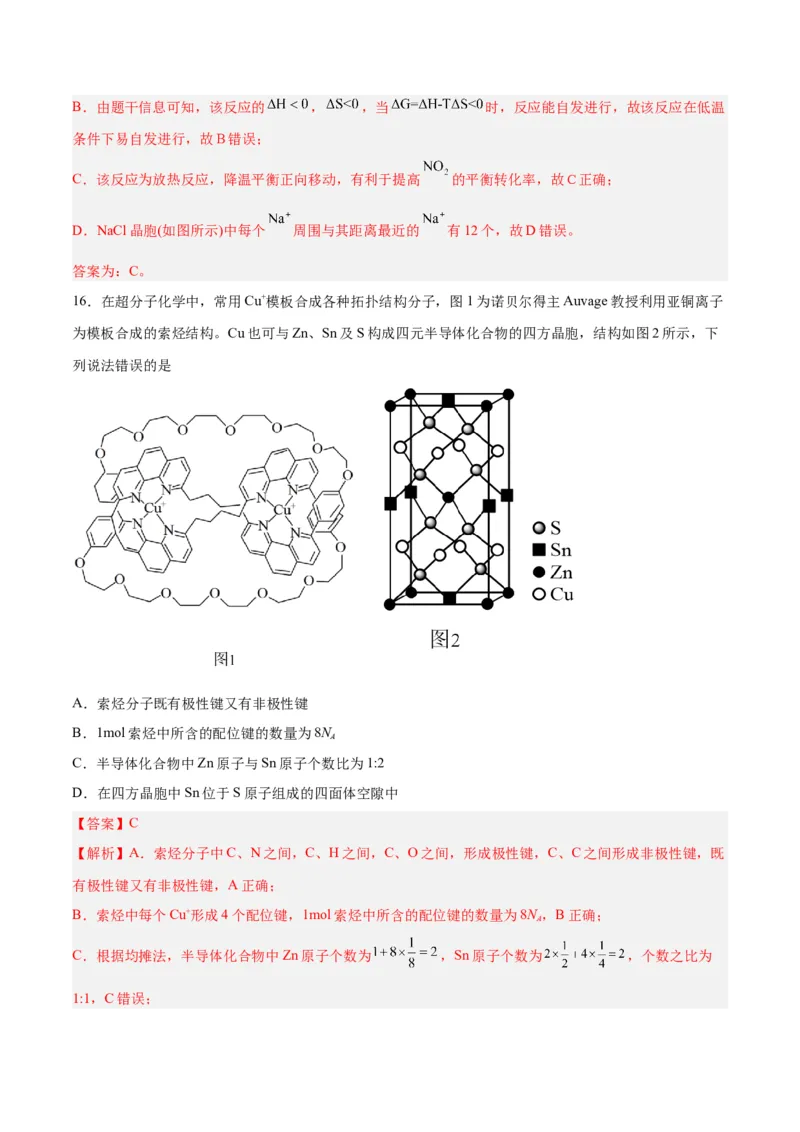
16.在超分子化学中,常用Cu+模板合成各种拓扑结构分子,图1为诺贝尔得主Auvage教授利用亚铜离子
为模板合成的索烃结构。Cu也可与Zn、Sn及S构成四元半导体化合物的四方晶胞,结构如图2所示,下
列说法错误的是
A.索烃分子既有极性键又有非极性键
B.1mol索烃中所含的配位键的数量为8N
A
C.半导体化合物中Zn原子与Sn原子个数比为1:2
D.在四方晶胞中Sn位于S原子组成的四面体空隙中
【答案】C
【解析】A.索烃分子中C、N之间,C、H之间,C、O之间,形成极性键,C、C之间形成非极性键,既
有极性键又有非极性键,A正确;
B.索烃中每个Cu+形成4个配位键,1mol索烃中所含的配位键的数量为8N ,B正确;
A
C.根据均摊法,半导体化合物中Zn原子个数为 ,Sn原子个数为 ,个数之比为
1:1,C错误;D.根据晶胞结构,在四方晶胞中Sn位于S原子组成的四面体空隙中,D正确;
故选C。
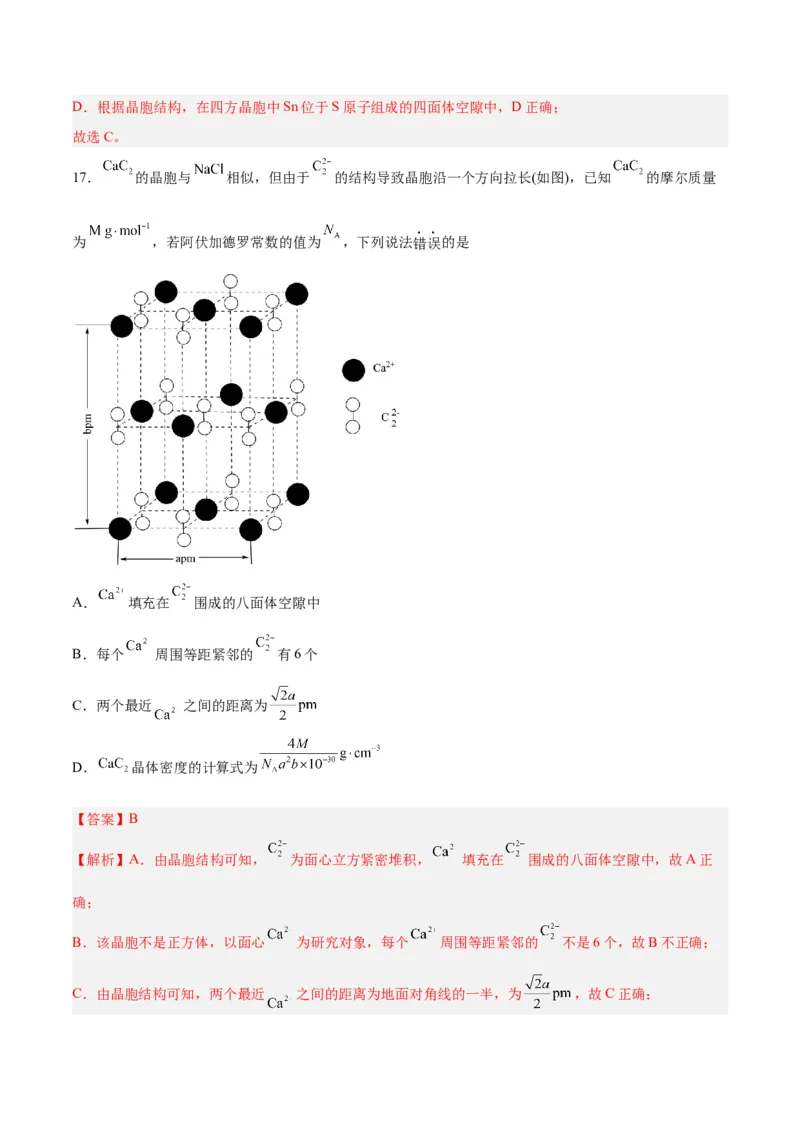
17. 的晶胞与 相似,但由于 的结构导致晶胞沿一个方向拉长(如图),已知 的摩尔质量
为 ,若阿伏加德罗常数的值为 ,下列说法错误的是
A. 填充在 围成的八面体空隙中
B.每个 周围等距紧邻的 有6个
C.两个最近 之间的距离为
D. 晶体密度的计算式为
【答案】B
【解析】A.由晶胞结构可知, 为面心立方紧密堆积, 填充在 围成的八面体空隙中,故A正
确;
B.该晶胞不是正方体,以面心 为研究对象,每个 周围等距紧邻的 不是6个,故B不正确;
C.由晶胞结构可知,两个最近 之间的距离为地面对角线的一半,为 ,故C正确;D. 晶体中Ca2+的个数为8 +6 =4, 的个数为1+12 =4,密度的计算式为
,故D正确;
故选B。
18.砷化镓(GaAs)是优良的半导体材料,熔点为1238℃,用于制作太阳能电池的材料,其结构如图所示,
其中以原子1为原点,原子2的坐标为(1,1,1)。下列有关说法中错误的是
A.原子3的坐标为( , , ) B.Ga的配位数为4
C.GaAs为共价晶体 D.若将Ga换成Al,则晶胞参数将变小
【答案】A
【解析】A.由图可知,原子3在x、y、z轴上的投影分别为 ,坐标为 ,A错误;
B.根据晶胞结构可知,Ga的配位数为4,B正确;
C.GaAs的熔点为1238℃,硬度大,熔点高硬度大,故晶体类型为共价晶体,C正确;
D.Ga原子半径比Al小,则若将Ga换成Al,则晶胞参数将变小,D正确;
故选A。
19.快离子导体是一类具有优良导电能力的固体电解质。图1(Li SBF )和图2是潜在的快离子导体材料的
3 4
结构示意图。温度升高时,NaCl晶体出现缺陷,晶体的导电性增强。该晶体导电时,③迁移的途径有两
条:
途径1:在平面内挤过2、3号氯离子之间的狭缝(距离为x)迁移到空位。
途径2:挤过由1、2、3号氯离子形成的三角形通道(如图3,小圆的半径为y)迁移到空位。
已知:氯化钠晶胞参数a=564pm,r(Na+)=95pm,r(Cl-)=185pm, =1.4, =1.7。
下列说法不正确的是A.第二周期元素中第一电离能介于B和F之间的元素有4种
B.图1所示晶体中,每个Li+与4个呈四面体结构的离子相邻
C.氯化钠晶体中,Na+填充在氯离子形成的正八面体空隙中
D.温度升高时,NaCl晶体出现缺陷,晶体的导电性增强,该晶体导电时,③迁移的途径可能性更大的是
途径1
【答案】D
【解析】A.第二周期元素第一电离能从左向右呈增大趋势,由于Be的2s轨道全满,N的2p轨道半满,
结构稳定,造成Be和N比同周期相邻元素的第一电离能高,因此第一电离能介于B和F之间的有Be、
C、N、O共4种,A正确;
B.由图1所示晶体结构可知,Li+位于棱心,正四面体结构的离子在体心,则每个Li+与4个呈四面体结构
的离子相邻,B正确;
C. NaCl晶胞中Na+周围有3个Cl-,则在NaCl晶体中,Na+周围等距离最近有6个C1-,6个C1-构成正
八面体结构,即Na+填充在C1-堆积而成的八面体空隙中,C正确;
D.该三角形为等边三角形,边长等于图2中面对角线长度,故三角形边长=
,即 ,r(Cl-)=185pm,解得x=24.8pm;内部虚线部分
三角形的顶角为120°、两腰长为r(Cl )+y、底长为282 pm,边角关系有 [ r(Cl )+y]=282 pm,解得
y= 47.2pm;由于挤过由1、2、 3号氯离子形成的三角形通道y的值大于挤过2、3号氯离子之间的狭缝x
值,所以Na+如果能挤过,那么挤过由1、2、 3号氯离子形成的三角形通道相对容易些,即迁移可能性更
大的途径是途径2,D错误;
故选D。20.化学式为 的笼形包合物四方晶胞结构如图所示(H原子未画出),晶胞中N
原子均参与形成配位键,每个苯环只有一半属于该晶胞。晶胞参数为a=b≠c, 则下列叙述正确
的是
A.Zn在元素周期表d区 B.设晶体中 原于的杂化方式为
C. D.Ni2+与Zn2+的配位数之比为2:3
【答案】D
【解析】A.Zn在元素周期表中位置为第4周期第IIB族,即位于ds区,A错误;
B.晶胞中镍离子配位数为4,即晶体中 原于的杂化方式为 ,B错误;
C.由晶胞示意图可知,一个晶胞中含有Ni2+个数为2 =1,Zn2+个数为8 =1,含有CN-为8 =4,
NH 个数为8 =2,苯环个数为4 =2,则该晶胞的化学式为 ,则
3
x:y:z=4:2:2=2:1:1,C错误;
D.晶胞中每个N原子均参与形成配位键,Ni2+周围形成的配位键数目为4,Zn2+周围形成的配位键数目为
6,则Ni2+与Zn2+的配位数之比为4:6=2:3,D正确;
故选D。