文档内容
第 31 讲 乙醇和乙酸
第一部分:高考真题感悟
1.(2022·海南·高考真题)化学与日常生活息息相关。下列说法错误的是
A.使用含氟牙膏能预防龋齿 B.小苏打的主要成分是
C.可用食醋除去水垢中的碳酸钙 D.使用食品添加剂不应降低食品本身营养价值
【答案】B
【解析】A.人体缺氟会导致龋齿,因此使用含氟牙膏可预防龋齿,A正确;B.小苏打的主要成分是
NaHCO ,B错误;C.食醋的主要成分为CHCOOH,可与碳酸钙反应生成可溶的醋酸钙、二氧化碳和水,
3 3
因此食醋可除去水垢中的碳酸钙,C正确;D.食品添加剂加入到食品中的目的是为改善食品品质和色、
香、味以及为防腐、保鲜和加工工艺的需要,所以合理使用有助于改善食品品质、丰富食品营养成分,不
应降低食品本身营养价值,D正确;答案选B。
2.(2021·山东·高考真题)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH- +CH O-能量变化如图
3
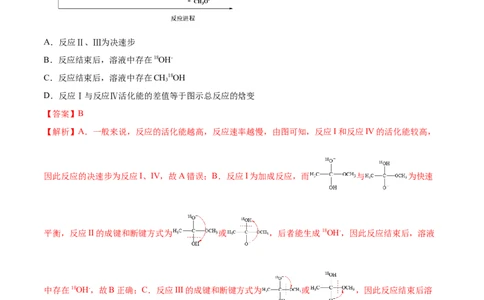
所示。已知 为快速平衡,下列说法正确的是A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
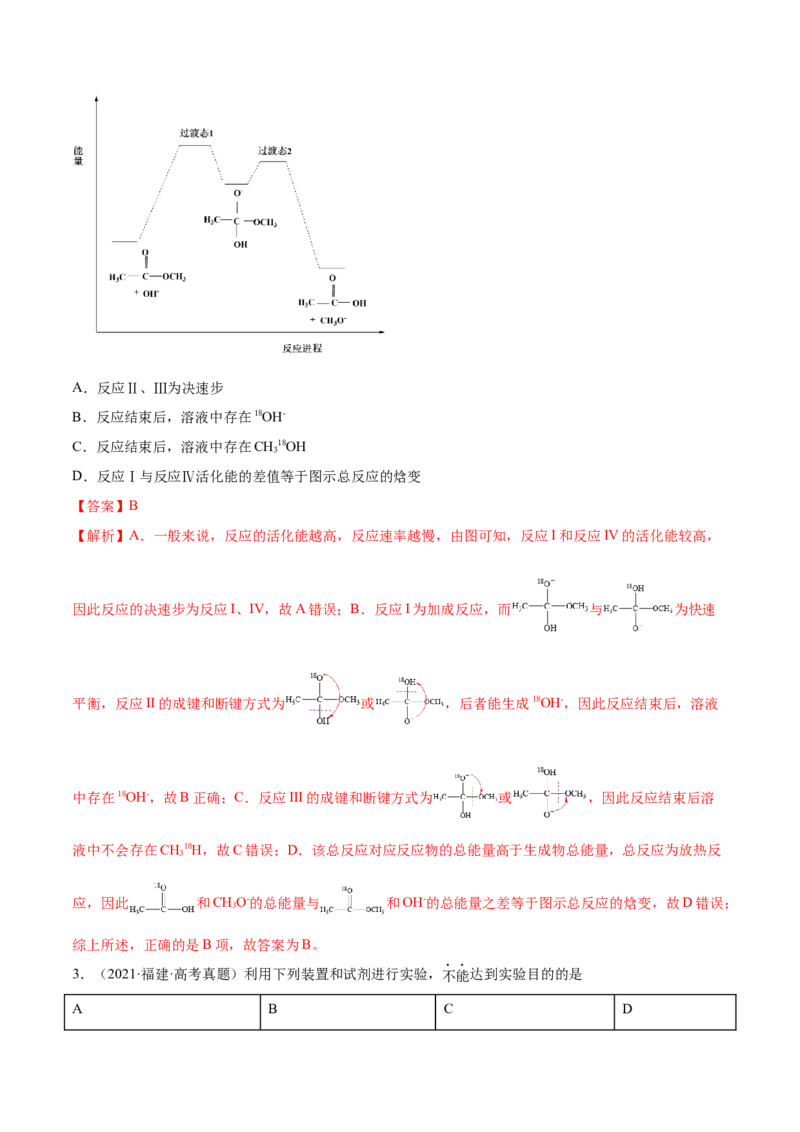
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
【答案】B
【解析】A.一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应IV的活化能较高,
因此反应的决速步为反应I、IV,故A错误;B.反应I为加成反应,而 与 为快速
平衡,反应II的成键和断键方式为 或 ,后者能生成18OH-,因此反应结束后,溶液
中存在18OH-,故B正确;C.反应III的成键和断键方式为 或 ,因此反应结束后溶
液中不会存在CH18H,故C错误;D.该总反应对应反应物的总能量高于生成物总能量,总反应为放热反
3
应,因此 和CHO-的总能量与 和OH-的总能量之差等于图示总反应的焓变,故D错误;
3
综上所述,正确的是B项,故答案为B。
3.(2021·福建·高考真题)利用下列装置和试剂进行实验,不能达到实验目的的是
A B C D制取乙酸乙酯(必要时可加
比较Zn与Cu的金属性强弱 除去Cl 中的HCl并干燥 实验室制取氯气
2 沸石)
【答案】D
【解析】A.该装置中,若Zn比Cu活泼,则总反应为Zn与硫酸的反应,此时Zn为负极,Cu为正极;若
Cu比Zn活泼,则总反应为Cu与硫酸锌的反应,此时Cu为负极,Zn为正极,所以可以比较Zn与Cu的金
属性强弱,A正确;B.稀硫酸中含有大量氢离子,可以抑制氯气的溶解,而稀硫酸中的水可以吸收
HCl,洗气后再用浓硫酸干燥,B正确;C.乙酸、乙醇和浓硫酸混合加热可以制取乙酸乙酯,饱和碳酸钠
溶液可以降低乙酸乙酯的溶解度,同时吸收乙酸和乙醇,便于分液分离得到乙酸乙酯,沸石可以防止暴沸,
C正确;D.制取氯气应用浓盐酸和二氧化锰共热,稀盐酸不与二氧化锰反应,D错误;综上所述答案为
D。
4.(2021·浙江·高考真题)下列说法正确的是
A. C 和C 互为同位素 B. C H 和C H 互为同系物
60 70 2 6 6 14
C. CO和CO 互为同素异形体 D.CHCOOH和CHOOCH是同一种物质
2 3 3
【答案】B
【解析】A.同种元素的不同种核素互称同位素,C 和C 为C元素的两种不同单质,不能互称同位素,A
60 70
错误;B.C H 和C H 均为烷烃,二者结构类似,分子组成上相差4个CH 基团,二者互为同系物,B正
2 6 6 14 2
确;C.同种元素的不同种单质互称同素异形体,CO和CO 为C元素的两种不同氧化物,二者不是单质,
2
不能互称同素异形体,C错误;D.两种物质的结构不同,不是同一种物质,二者互称同分异构体,D错
误;故答案选B。
5.(2013·海南·高考真题)下列鉴别方法不可行的是
A.用水鉴别乙醇、甲苯和溴苯
B.用燃烧法鉴别乙醇、苯和四氯化碳
C.用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
D.用酸性高锰酸钾溶液鉴别苯、环己烯和环己烷
【答案】D【解析】A.乙醇与水混溶,甲苯密度比水小,溴苯密度比水大,可加入水鉴别,故A可行;B.乙醇燃
烧,火焰明亮,无浓烟,苯燃烧有浓烟,四氯化碳不燃烧,现象各不相同,可鉴别,故B可行;C.乙醇
易溶于水,碳酸钠与乙酸反应生成二氧化碳气体,乙酸乙酯不溶于饱和碳酸钠溶液,溶液分层,可鉴别,
故C可行;D.甲苯、环己烯都可被酸性高锰酸钾氧化,故D不可行;故选D。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·广东·五华县教育教学研究室一模)从2020年1月开始,新型冠状病毒肺炎疫情全面爆发,关
于新型冠状病毒肺炎至今还没有研发出特效药,75%乙醇溶液是一种常见的杀灭病毒的消毒剂,关于乙醇,
下列说法不正确的是:
A.它的结构简式为CHCHOH B.100%乙醇消毒效果更好
3 2
C.它的官能团为羟基 D.它与水能以任意比互溶
【答案】B
【解析】乙醇是能与水以任意比互溶、有特殊香味的无色液体,分子式为C HO,结构简式为
2 6
CHCHOH,官能团为羟基,75%乙醇溶液的消毒效果比100%乙醇的消毒效果好,故选B。
3 2
2.(2022·上海·模拟预测)用分液漏斗可以分离的一组混合物是
A.乙酸乙酯和乙酸 B.溴苯和水
C.溴乙烷和乙醇 D.乙醇和水
【答案】B
【解析】A.乙酸乙酯和乙酸互溶,不分层,不能用分液漏斗分离,故A错误;B.溴苯是密度大于水的
液体,且不溶于水,能用分液漏斗分离,故B正确;C.乙醇是良好有机溶剂,乙醇和溴乙烷互溶,不能
用分液漏斗分离,故C错误;D.乙醇和水互溶,不能用分液漏斗分离,故D错误;故选B。
3.(2021·浙江·模拟预测)醋酸是常用的调味品。下列关于醋酸化学用语表述不正确的是
A.键线式: B.结构式:
C.最简式:CHO D.比例模型:
2
【答案】B【解析】A.醋酸的键线式为 ,故A正确;B.结构是共用电子对用短线表示,醋酸的结构式为
,故B错误;C.最简式是化合物分子中各元素的原子个数比的最简关系式,醋酸的最简
式是CHO,故C正确;D.比例模型体现的是组成该分子的原子间的大小、分子的空间结构、原子间的连
2
接顺序等,图示为醋酸的比例模型,故D正确;故答案为B。
4.(2022·云南·一模)下列叙述正确的
A.环丙烷的一氯代物有3种
B.可用溴水鉴别苯、苯乙烯和乙酸
C.乙醇和丙三醇都含羟基,互为同系物
D.乙烯使高锰酸钾溶液褪色发生加成反应
【答案】B
【解析】A.环丙烷的结构简式为 ,只有一种氢原子,一氯代物只有一种,故A错误;B.溴水加入苯
中,苯萃取溴单质,苯不溶于水,溶液出现分层;苯乙烯中含有碳碳双键,能使溴水褪色;溴水溶于乙酸,
溶液不分层;现象不同,可以鉴别,故B正确;C.乙醇为CHCHOH,丙三醇为CHOHCHOHCH OH,
3 2 2 2
含有羟基的数目不同,因此两者不互为同系物,故C错误;D.乙烯能使酸性高锰酸钾溶液褪色,发生氧
化反应,不是加成反应,故D错误;答案为B。
5.(2021·辽宁朝阳·模拟预测)乙醇和乙酸是生活中常见的两种有机物,下列说法正确的是
A.乙醇与乙醚互为同分异构体
B.乙醇能一步转化成乙酸
C.1mol乙酸能电离出4molH+
D.等物质的量的乙醇、乙酸中含有的C—H键数目一样多
【答案】B
【解析】A. 乙醇的结构简式为CHCHOH,乙醚的结构简式为CHCHOCH CH,故二者分子式不相同,
3 2 3 2 2 3
不互为同分异构体,故A错误;B. 乙醇可被强氧化剂高锰酸钾等直接氧化,一步转化成乙酸,故B正确;
C. 乙酸结构简式为CHCOOH,只有羧基上的氢原子能电离下来,故1mol乙酸只能电离出1molH+,故
3
C错误;D. 乙醇的结构简式为CHCHOH,1个乙醇分子中有5个C-H键,乙酸结构简式为
3 2
CHCOOH,1个乙酸分子中有3个C-H键,故等物质的量的乙醇、乙酸中含有的C—H键数目不一样多,
3故D错误;故选B。
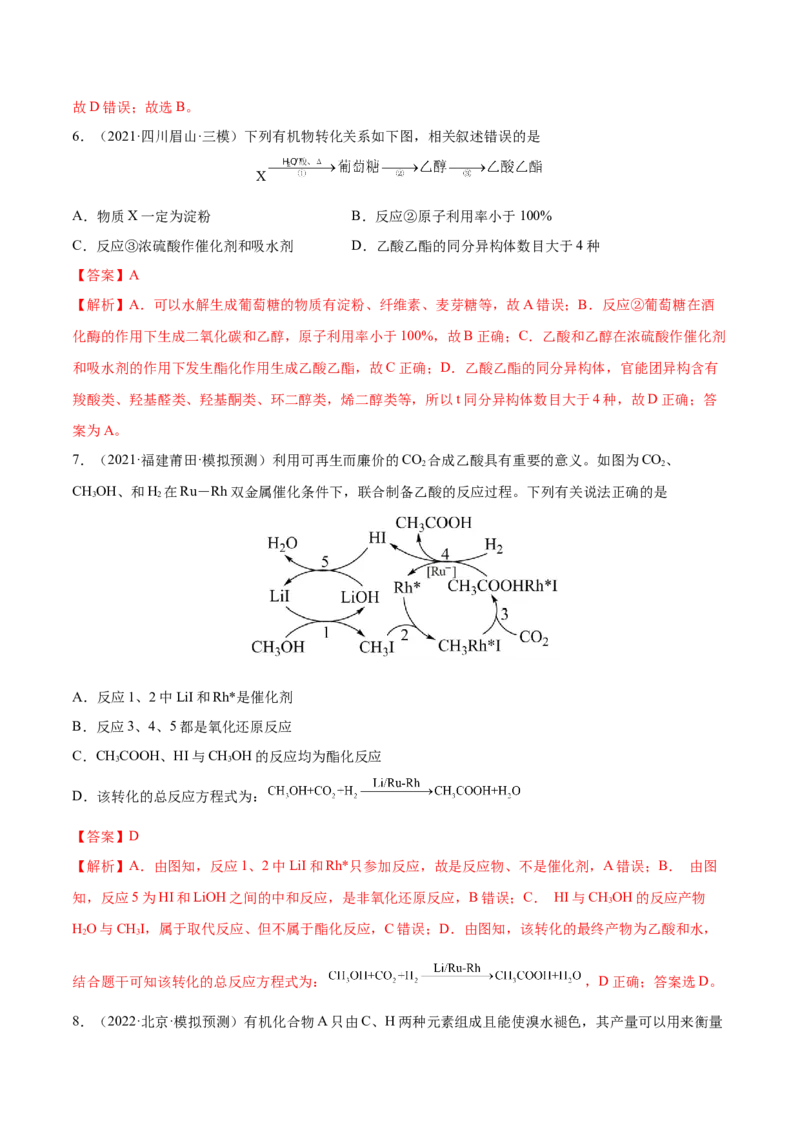
6.(2021·四川眉山·三模)下列有机物转化关系如下图,相关叙述错误的是
X
A.物质X一定为淀粉 B.反应②原子利用率小于100%
C.反应③浓硫酸作催化剂和吸水剂 D.乙酸乙酯的同分异构体数目大于4种
【答案】A
【解析】A.可以水解生成葡萄糖的物质有淀粉、纤维素、麦芽糖等,故A错误;B.反应②葡萄糖在酒
化酶的作用下生成二氧化碳和乙醇,原子利用率小于100%,故B正确;C.乙酸和乙醇在浓硫酸作催化剂
和吸水剂的作用下发生酯化作用生成乙酸乙酯,故C正确;D.乙酸乙酯的同分异构体,官能团异构含有
羧酸类、羟基醛类、羟基酮类、环二醇类,烯二醇类等,所以t同分异构体数目大于4种,故D正确;答
案为A。
7.(2021·福建莆田·模拟预测)利用可再生而廉价的CO 合成乙酸具有重要的意义。如图为CO、
2 2
CHOH、和H 在Ru-Rh双金属催化条件下,联合制备乙酸的反应过程。下列有关说法正确的是
3 2
A.反应1、2中LiI和Rh*是催化剂
B.反应3、4、5都是氧化还原反应
C.CHCOOH、HI与CHOH的反应均为酯化反应
3 3
D.该转化的总反应方程式为:
【答案】D
【解析】A.由图知,反应1、2中LiI和Rh*只参加反应,故是反应物、不是催化剂,A错误;B. 由图
知,反应5为HI和LiOH之间的中和反应,是非氧化还原反应,B错误;C. HI与CHOH的反应产物
3
HO与CHI,属于取代反应、但不属于酯化反应,C错误;D.由图知,该转化的最终产物为乙酸和水,
2 3
结合题干可知该转化的总反应方程式为: ,D正确;答案选D。
8.(2022·北京·模拟预测)有机化合物A只由C、H两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化学工业的发展水平。A、B、C、D、E有如图所示的关系。
则下列推断不正确的是
A.鉴别A和甲烷可选择酸性高锰酸钾溶液
B.B、D均能与金属钠反应
C.物质C的结构简式为CHCHO
3
D.B+D→E的化学方程式为:CHCHOH+CHCOOH CHCOOC H
3 2 3 3 2 5
【答案】D
【解析】由A的产量可以用来衡量一个国家石油化学工业的发展水平,可知A是乙烯,则B为
CHCHOH,C为CHCHO,D为CHCOOH,E为CHCOOC H。A.乙烯可使酸性高锰酸钾溶液褪色,
3 2 3 3 3 2 5
甲烷不能,A正确;B.乙醇,乙酸都可以和钠反应生成氢气,B正确;C.由分析可知物质C的结构简式
为CHCHO,C正确;D.B与D反应的化学方程式为CHCHOH+CHCOOH CHCOOC H+
3 3 2 3 3 2 5
HO,D错误;故选D。
2
9.(2022·湖南常德·模拟预测)乙酸乙酯是一种重要的有机化工原料和工业溶剂,以正丁烷为原料合成乙
酸乙酯的合成路线如下。
下列有关说法正确的是
A.正丁烷的沸点低于异丁烷的沸点 B.乙酸分子结构中所有原子可能共平面
C.乙酸与乙烯发生加成反应得到乙酸乙酯 D.乙烯发生聚合反应得到纯净物聚乙烯
【答案】C
【解析】A.碳原子数相同,支链越多,沸点越低,故正丁烷沸点高于异丁烷,选项A错误;B.
CHCOOH分子中含有羧羰基,但甲基中的氢原子一定不共平面,选项B错误;C.根据上述合成路线可知,
3
乙酸与乙烯发生加成反应得到乙酸乙酯,选项C正确;D.乙烯发生聚合反应得到的聚乙烯中聚合度n不
同,为混合物,选项D错误;答案选C。
10.(2022·江苏南通·模拟预测)下列制取乙酸乙酯的实验原理与装置能达到实验目的的是A.装置甲混合乙醇和浓硫酸 B.装置乙制取乙酸乙酯
C.装置丙分离乙酸乙酯和水层 D.装置丁蒸出水层中的乙醇
【答案】C
【解析】A.混合乙醇和浓硫酸时应该将浓硫酸加入到乙醇溶液中,A项错误;B.乙酸乙酯在氢氧化钠溶
液中会发生水解,B项错误;C.分离乙酸乙酯和水的溶液可采用分液的方法,有机层在上层,水层在下
层,C项正确;D.温度计水银球不能伸到液面以下,D项错误;故答案为C。
11.(2022·湖北·黄冈中学三模)某化学兴趣小组设计用如图所示装置进行C HOH的氧化实验,并验证产
2 5
物。沿箭头所示方向通入O,反应结束后取Ⅳ中所得产物滴入酸性KMnO 溶液。下列说法中错误的是
2 4
A.装置Ⅰ盛有浓硫酸,用于干燥氧气
B.装置Ⅱ、Ⅳ中的水浴方式分别为冰水浴、热水浴
C.滴入产物后酸性KMnO 溶液褪色,不能说明产物含有乙醛
4
D.向Ⅳ中小试管内滴入含酚酞的NaOH溶液,若红色褪去说明产物含有乙酸
【答案】B
【解析】氧气经干燥后进入盛有乙醇的圆底烧瓶中,和热的乙醇一起进入硬质玻璃管中,在铜的催化作用
下发生乙醇的催化氧化反应生成乙醛。生成的乙醛进入试管中,被冷凝收集。A.参与反应的氧气应该是
干燥的,则装置Ⅰ盛有浓硫酸,用于干燥氧气,A正确;B.需要乙醇蒸汽进入装置Ⅲ中,生成的乙醛需
要冷凝收集,所以装置Ⅱ、Ⅳ中的水浴方式分别为热水浴、冰水浴,B错误;C.由于乙醇易挥发,且能
使酸性高锰酸钾溶液褪色,所以滴入产物后酸性KMnO 溶液褪色,不能说明产物含有乙醛,C正确;D.
4
向Ⅳ中小试管内滴入含酚酞的NaOH溶液,若红色褪去说明碱性减弱,氢氧化钠被中和,因此可证明产物
中含有乙酸,D正确;答案选B。
12.(2022·上海普陀·二模)关于实验室制备乙酸丁酯的实验,下列叙述错误的是A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.加入过量乙酸可以提高1-丁醇的转化率
D.提纯乙酸丁酯需要用水、氢氧化钠溶液洗涤
【答案】D
【解析】A.制备乙酸丁酯的温度为120℃左右,故不能使用水浴加热,A正确;B.长玻璃导管其冷凝回
流作用,增大反应物的转化率,B正确;C.加入过量的乙酸可以使反应正向进行,提高丁醇的转化率,C
正确;D.乙酸丁酯能与氢氧化钠反应,不能用氢氧化钠洗涤,D错误;故选D。
二、主观题(共3小题,共40分)
13.(2021·浙江·模拟预测)(12分)乙烯是来自石油的重要的化工原料,乙烯的产量通常用来衡量一个
国家的石油化工发展水平。
完成下列填空:
(1) 和乙烷互为___________。
(2)反应①、②、③的反应类型分别为___________、___________、___________。
(3)反应④和反应⑥的反应方程式分别为___________、___________。
【答案】(每空2分)(1)同系物
(2)加成反应 氧化反应 取代反应(或酯化反应)
(3)
【解析】(1) 和乙烷均属于烷烃,结构相似,二者互为同系物。
(2)反应①是乙烯和水发生加成反应生成乙醇: ;反应②是乙醇的催
化氧化: ;反应③是乙醇和乙酸发生酯化反应生成乙酸乙酯:。
(3)反应④是乙烯发生加聚反应生成聚乙烯,反应方程式为 ,反应
⑥是乙烷和氯气发生取代反应生成一氯乙烷,反应方程式为 。
14.(2021·四川资阳·一模)(10分)化学工业为疫情防控提供了强有力的物质支撑。常用的消毒剂产品
按成分可以分为含氯消毒剂、醇类消毒剂、含碘消毒剂等9种。回答下列问题:
(1)①碘酊又称碘酒,常见配制方法是将一定质量的单质碘溶于适量酒精,再加水稀释。碘酒属于
___________。(选填:溶液、胶体、悬浊液、乳浊液)
②IO 是碘元素最稳定的氧化物之一,已知其中碘元素的化合价为+3、+5价,则IO 中+3价和+5价
4 9 4 9
的碘原子数目之比为___________,若IO 溶于水会生成两种含氧酸,写出该过程的化学方程式
4 9
___________。
(2)乙醇是生活中最常见的醇类消毒剂。
①下列关于乙醇的说法正确的是___________。
a.将日常饮用的白酒直接蒸馏即可得到无水乙醇
b.95%的酒精消毒杀菌效果比浓度为75%的酒精好
c.表面氧化的铜丝在酒精灯内焰加热时会恢复红色,说明酒精具有挥发性和还原性
d.平时生活中,可以采用大面积喷洒酒精的方式对室内等封闭空间消毒
②酒驾的检测原理是乙醇使酸化的KCr O 橙色溶液迅速还原成绿色的Cr O,同时生成无色无味气体,写
2 2 7 2 3
出该反应的离子方程式___________。
【答案】(每空2分)(1)①溶液 ②1:3 IO+2H O=HIO +3HIO
4 9 2 2 3
(2)①c ②2 +CH CHOH+4H+= 2CrO+2CO ↑+5H O
3 2 2 3 2 2
【解析】(1)①从常见配制方法可知,碘酒是碘的酒精溶液,碘酒属于溶液。②IO 中碘元素的化合价为+
4 9
3、+5价,碘酸根中I的化合价为+5价,碘酸根为−1价,则IO 可写成I (IO ) 形式,所以前面的I的化
4 9 m 3 n
合价为+3价,则IO 化学式为I(IO ), IO+3价和+5价的碘原子数目之比为1:3,若IO 溶于水会生成
4 9 3 3 4 9 4 9
两种含氧酸,则元素化合价不变,故生成的酸为HIO 和HIO ,该过程的化学方程式为:
2 3
IO+2H O=HIO +3HIO。
4 9 2 2 3
(2)①a. 将日常饮用的白酒直接蒸馏,会有少量水随酒精一起蒸馏出来,无法得到无水乙醇,加入新制的
生石灰吸水再蒸馏可得到无水乙醇,故a错误;b. 医用酒精是75%的酒精,95%的酒精消毒杀菌效果比浓
度为75%的酒精差,b错误;c. 表面氧化的铜丝在酒精灯内焰加热时会恢复红色,是因为氧化铜和焰心、内焰处乙醇发生氧化还原反应重新生成了铜,说明酒精具有挥发性和还原性,c正确;d.酒精是易燃物,封
闭空间大面积喷洒酒精有易燃易爆的可能,这种做法极其危险,d错误;则说法正确的是c。
②酒驾的检测原理是:乙醇具有还原性,使酸化的KCr O 橙色溶液迅速还原成绿色的Cr O,同时生成无
2 2 7 2 3
色无味气体二氧化碳,该反应的离子方程式为:2 +CH CHOH+4H+= 2CrO+2CO ↑+5H O。
3 2 2 3 2 2
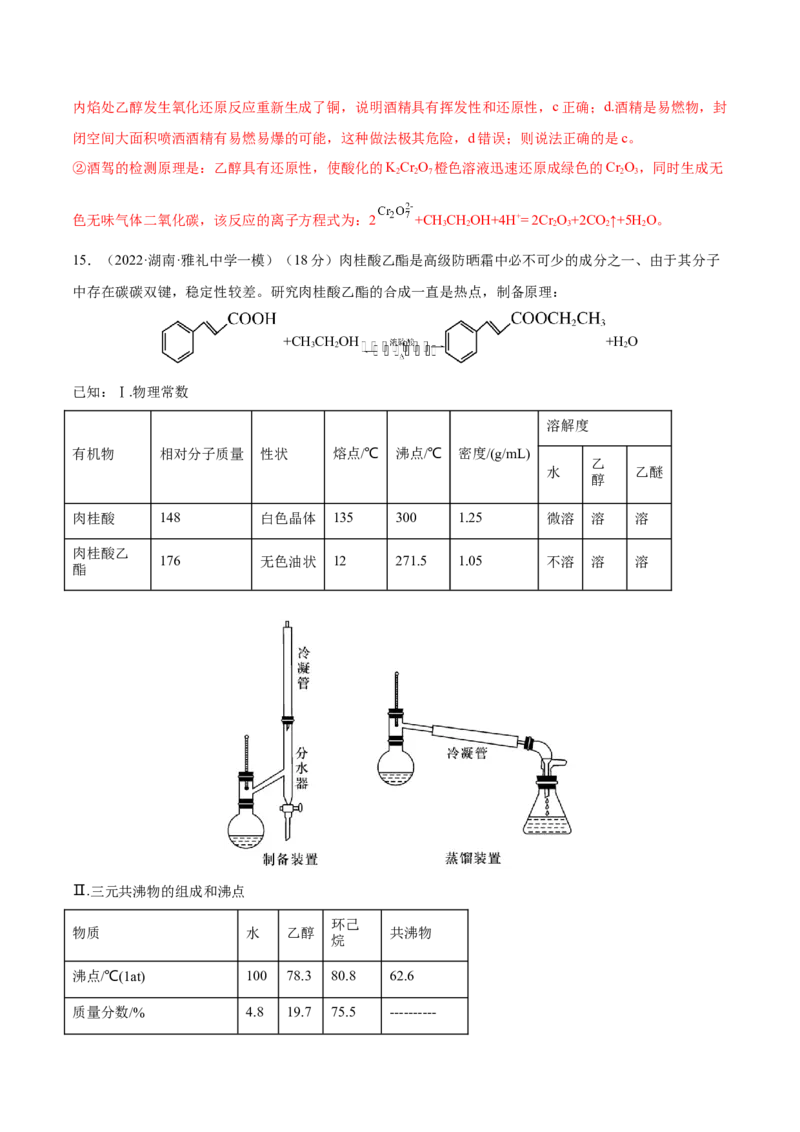
15.(2022·湖南·雅礼中学一模)(18分)肉桂酸乙酯是高级防晒霜中必不可少的成分之一、由于其分子
中存在碳碳双键,稳定性较差。研究肉桂酸乙酯的合成一直是热点,制备原理:
+CH CHOH +H O
3 2 2
已知:Ⅰ.物理常数
溶解度
有机物 相对分子质量 性状 熔点/℃ 沸点/℃ 密度/(g/mL)
乙
水 乙醚
醇
肉桂酸 148 白色晶体 135 300 1.25 微溶 溶 溶
肉桂酸乙
176 无色油状 12 271.5 1.05 不溶 溶 溶
酯
Ⅱ.三元共沸物的组成和沸点
环己
物质 水 乙醇 共沸物
烷
沸点/℃(1at) 100 78.3 80.8 62.6
质量分数/% 4.8 19.7 75.5 ----------上层 0.2 5.2 94.6
分水器内液体组
---------------
成
下层 10.4 18.4 71.2
Ⅲ.实验步骤:
①向圆底烧瓶中加入44.4g肉桂酸、25mL无水乙醇和25mL环己烷,在不断振摇下将3mL浓硫酸分多次加
入其中,加完后充分摇匀并加入几粒沸石;
②按照图示组装好仪器(安装分水器),加热圆底烧瓶,开始回流,分水器中出现上下两层,过程中不断将
上层液体流回圆底烧瓶,将下层液体放出;
③停止加热后,将圆底烧瓶中的物质倒入盛有80mL水的烧杯中,分批加入碳酸钠粉末;
④用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层;
⑤干燥,过滤;
⑥首先低温蒸出乙醚,再改用减压蒸馏(水浴加热即可)得到产品肉桂酸乙酯的体积为35.2mL。回答下列问
题:
(1)蒸馏装置中,选用的冷凝管为_______(填标号)。
A.空气冷凝管 B.球形冷凝管 C.直形冷凝管 D.蛇形冷凝管
(2)本实验中,分水器的作用是_______。
(3)步骤③加入碳酸钠粉末的作用是_______。
(4)步骤⑤合适的干燥剂为_______(填标号);
A.浓硫酸 B.无水氯化钙 C.氧化钙 D.氢氧化钠
采用减压蒸馏的原因是_______。
(5)已知无水乙醇的密度为0.79 g·mL−1,该实验中肉桂酸乙酯的产率为_______。
(6)产品纯度的分析,取amL所得样品,用乙醇作溶剂,准确配制成250.00mL溶液,量取25.00mL所配溶
液转移至锥形瓶中,加入mg氢氧化钠(过量),充分反应后,用浓度为c mol·L−1的盐酸滴定,消耗盐酸的
体积为V mL,该样品的纯度为_______(用代数式表示,无需化简)。
【答案】(除标注外,每空2分)(1)C
(2)分离出反应生成的水,促使平衡正向移动,提高产率
(3)除去过量的肉桂酸、硫酸,降低肉桂酸乙酯的溶解度
(4)B 碳碳双键的稳定性较差,高温下肉桂酸乙酯易发生副反应,采用减压蒸馏可以降低沸点,减小副反应
的发生
(5)70%(4分)(6) (4分)
【解析】44.4g肉桂酸、25mL无水乙醇和25mL环己烷,3mL浓硫酸混合加热,肉桂酸乙酯沸点较高,在
有碳碳双键的存在的情况下,高温易发生副反应,采用减压蒸馏可以降低沸点,在较低的温度下进行蒸馏,
减少副反应的发生,提高产率,反应中乙醇过量,按44.4g肉桂酸计算理论产量,计算产率;肉桂酸乙酯
与氢氧化钠发生水解反应,反应比例为1:1,过量的氢氧化钠与盐酸1:1反应,则n(肉桂酸乙酯)=
,求解n(肉桂酸乙酯)后继续计算产率,滴定重点溶液变为碱性,使用酚酞作为指示
剂。
(1)蒸馏装置中,选用的冷凝管为直形冷凝管。故选C;故答案为:C;
(2)本实验中,分水器的作用是分离出反应生成的水,促使平衡正向移动,提高产率。故答案为:分离出反
应生成的水,促使平衡正向移动,提高产率;
(3)步骤③加入碳酸钠粉末的作用是除去过量的肉桂酸、硫酸,降低肉桂酸乙酯的溶解度。故答案为:除去
过量的肉桂酸、硫酸,降低肉桂酸乙酯的溶解度;
(4)A.除去有机层中的水,使用浓硫酸不能过滤分离,故A不选;B.无水氯化钙,能干燥,可通过过滤分离,
故B选; C.氧化钙与水反应生成氢氧化钙,促进酯水解,故C不选; D.氢氧化钠是碱能促进酯水解,故
D不选;故选B。采用减压蒸馏的原因是碳碳双键的稳定性较差,高温下肉桂酸乙酯易发生副反应,采用
减压蒸馏可以降低沸点,减小副反应的发生。故答案为:B;碳碳双键的稳定性较差,高温下肉桂酸乙酯
易发生副反应,采用减压蒸馏可以降低沸点,减小副反应的发生;
(5)m(乙醇)=0.79g/mL×25mL=19.5g,
+CH CHOH +H O 根据方程式知,如果148g
3 2 2
肉桂酸反应需要46g乙醇,如果44.4g肉桂酸反应需要 =13.8g乙醇,所以乙醇过量,设生成肉
桂酸乙酯的质量为x,148g:176g=44.4g:x,x=52.8g,实际生成的肉桂酸乙酯的质量为35.2mL×1.05g/
mL=36.96g,其产率= ×100%=70%,故答案为:70%;
(6)产品纯度的分析,取amL所得样品,用乙醇作溶剂,准确配制成250.00mL溶液,量取25.00mL所配溶液转移至锥形瓶中,加入mg氢氧化钠(过量),充分反应后,用浓度为c mol·L−1的盐酸滴定,消耗盐酸的
体积为V mL,肉桂酸乙酯的物质的量为 , =
该样品的纯度为 (用代数式表示,无需化简)。故答案为:
。