文档内容
第 35 讲 化学综合实验
(模拟精练+真题演练)
完卷时间:50分钟
一、选择题(12×5分)
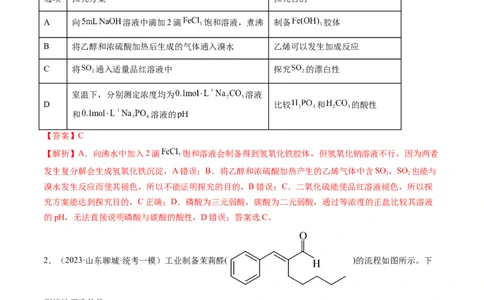
1.(2023·辽宁大连·大连八中校考模拟预测)下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
A 向 溶液中滴加2滴 饱和溶液,煮沸 制备 胶体
B 将乙醇和浓硫酸加热后生成的气体通入溴水 乙烯可以发生加成反应
C 将 通入适量品红溶液中 探究 的漂白性
室温下,分别测定浓度均为 溶液
D 比较 和 的酸性
和 溶液的
【答案】C
【解析】A.向沸水中加入2滴 饱和溶液会制备得到氢氧化铁胶体,但氢氧化钠溶液不行,因为两者
发生复分解会生成氢氧化铁沉淀,A错误;B.将乙醇和浓硫酸加热产生的乙烯气体中含SO ,SO 也能与
2 2
溴水发生反应而使其褪色,所以不能证明探究的目的,B错误;C.二氧化硫能使品红溶液褪色,所以探
究方案能达到探究目的,C正确;D.磷酸为三元弱酸,碳酸为二元弱酸,通过等浓度的正盐比较其溶液
的pH,无法直接说明磷酸与碳酸的酸性,D错误;答案选C。
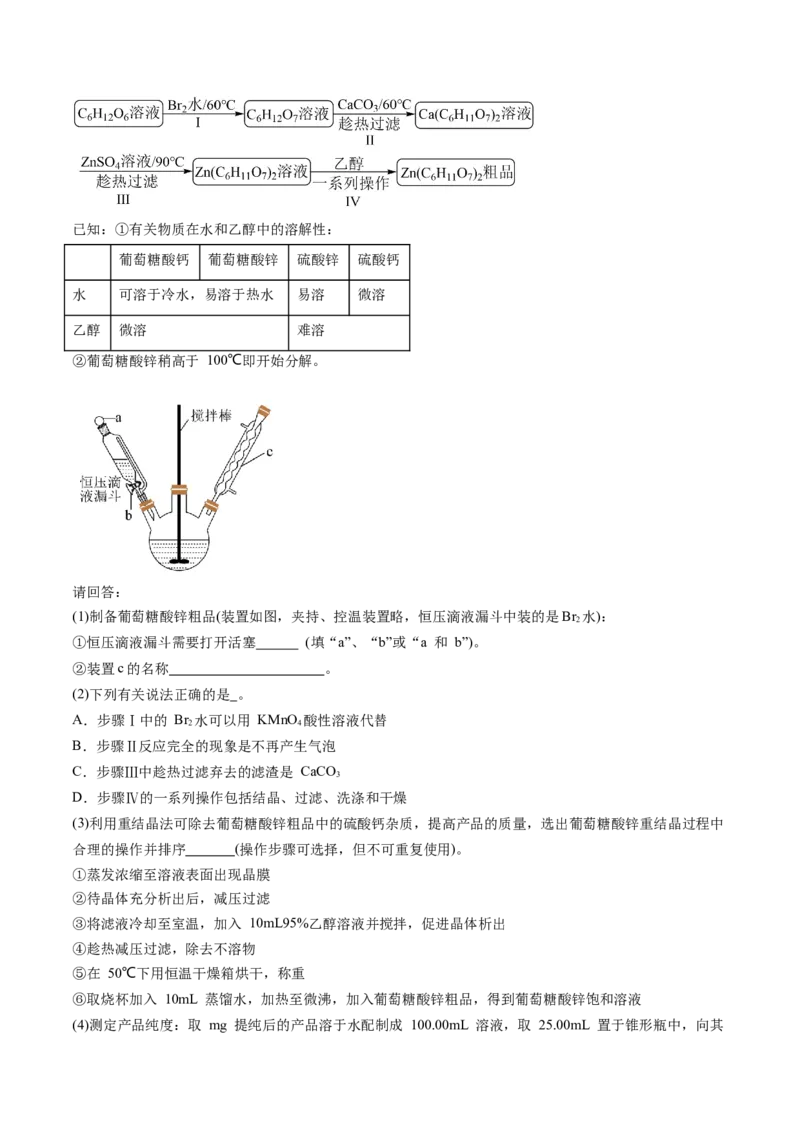
2.(2023·山东聊城·统考一模)工业制备茉莉醛( )的流程如图所示。下
列说法正确的是
已知:①庚醛易自身缩合生成与茉莉醛沸点接近的产物
②茉莉醛易被浓硫酸氧化
A.乙醇的主要作用是提供反应物B.干燥剂可选用无水
C.可将最后两步“蒸馏”和“柱色谱法分离”合并替换为“真空减压蒸馏”
D.可采用与浓硫酸共热的方法来除去产品中少量的庚醛自缩物
【答案】B
【分析】苯甲醛和庚醛在氢氧化钾乙醇溶液中发生羟醛缩合反应生成茉莉醛,乙醇做溶剂不参与反应,经
过冷却、萃取分液,用固体干燥剂干燥,可以选用无水硫酸钠做干燥剂,最后蒸馏、柱色谱法分离得到产
品。
【解析】A.据题意和分析,苯甲醛与庚醛反应生成水和茉莉醛,乙醇不参与反应,乙醇的主要作用是助
溶剂,故A错误;B.干燥剂的作用是吸收有机相中的残留水分,无水NaSO 吸收水形成结晶水合物,通
2 4
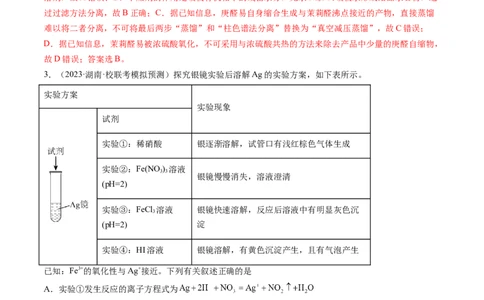
过过滤方法分离,故B正确;C.据已知信息,庚醛易自身缩合生成与茉莉醛沸点接近的产物,直接蒸馏
难以将二者分离,不可将最后两步“蒸馏”和“柱色谱法分离”替换为“真空减压蒸馏”,故C错误;
D.据已知信息,茉莉醛易被浓硫酸氧化,不可采用与浓硫酸共热的方法来除去产品中少量的庚醛自缩物,
故D错误;答案选B。
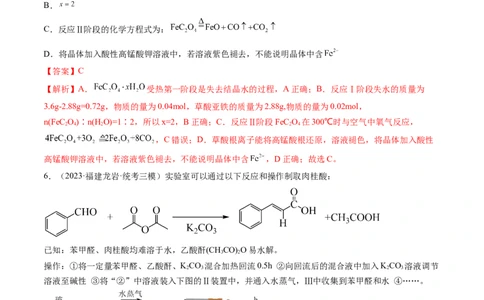
3.(2023·湖南·校联考模拟预测)探究银镜实验后溶解Ag的实验方案,如下表所示。
实验方案
实验现象
试剂
实验①:稀硝酸 银逐渐溶解,试管口有浅红棕色气体生成
实验②:Fe(NO ) 溶液
3 3
银镜慢慢消失,溶液澄清
(pH=2)
实验③:FeCl 溶液 银镜快速溶解,反应后溶液中有明显灰色沉
3
(pH=2) 淀
实验④:HI溶液 银镜溶解,有黄色沉淀产生,且有气泡产生
已知:Fe3+的氧化性与Ag+接近。下列有关叙述正确的是
A.实验①发生反应的离子方程式为
B.对比分析实验②和③表明:Cl-具有催化作用
C.实验④发生反应的类型为置换反应,说明氧化性;
D.综合上述实验说明溶解银的关键在于试剂的氧化性和能否生成银盐沉淀
【答案】D
【解析】A.Ag与稀硝酸反应产生NO,NO在瓶口与O 反应转化为红棕色的NO ,即实验①发生反应的
2 2
离子方程式为 ,A错误;B.对比分析实验②和③表明,实验③中
产生白色沉淀AgCl,能够加快Ag的溶解速率,Cl-参与沉淀反应不是催化剂,即不能证明Cl-具有催化作
用,B错误;C.实验④能够发生的原理是Ag溶解产生的Ag+与I-生成了难溶性的AgI,使得Ag溶解正向进行,致使Ag逐渐溶解,但不能说明氧化性: ,C错误;D.由实验②③可知由于实验③产生了
AgCl沉淀,Ag的溶解速度加快,实验①说明HNO 的氧化性强于Ag+,实验④是由于生成了AgI沉淀,故
3
综合上述实验说明溶解银的关键在于试剂的氧化性和能否生成银盐沉淀,D正确;故答案为:D。
4.(2023·全国·模拟预测)经处理后的工业废水中含有少量的苯酚,实验室测定其含量的步骤如下:
Ⅰ.取VmLamol•L-1KBrO 溶液,加入稍过量的KBr溶液并用HSO 酸化;Ⅱ.向Ⅰ所得溶液中加入VmL废
1 3 2 4 2
水,充分反应后再加入稍过量的KI溶液;Ⅲ.用bmol•L-1NaSO 标准溶液滴定Ⅱ中溶液至浅黄色时,滴加
2 2 3
2滴淀粉溶液,继续滴定至终点,共消耗VmLNa SO 溶液。
3 2 2 3
已知:①废水中不含干扰测定的物质;② +3Br → ↓+3HBr;
2
③I+Na SO=2NaI+Na SO,NaSO 溶液和NaSO 溶液均为无色。
2 2 2 3 2 4 6 2 2 3 2 4 6
下列说法正确的是
A.步骤Ⅰ中被氧化与被还原的溴元素质量之比为5:1B.步骤Ⅱ中Br 与苯酚发生加成反应
2
C.步骤Ⅲ中滴定至终点时溶液变为蓝色 D.废水中苯酚的含量为 g•L-1
【答案】A
【解析】A.步骤Ⅰ中反应为 ,被氧化与被还原的溴元素质量之比为5:
1,A正确;B.步骤Ⅱ中 与苯酚发生取代反应,是苯酚中的氢原子被溴原子取代的反应,B错误;C.
步骤Ⅲ中滴定至终点时溶液由蓝色褪为无色,C错误;D. ,根据反应
,可知 ;溴分别与苯酚和KI反应,先计算KI消耗
的溴的物质的量,设为 ,根据滴定原理可知 , ,
再计算苯酚消耗的溴的物质的量,设为 ,则
; (苯酚),则
,故废水中苯酚的含量为
,D错误;故选A。
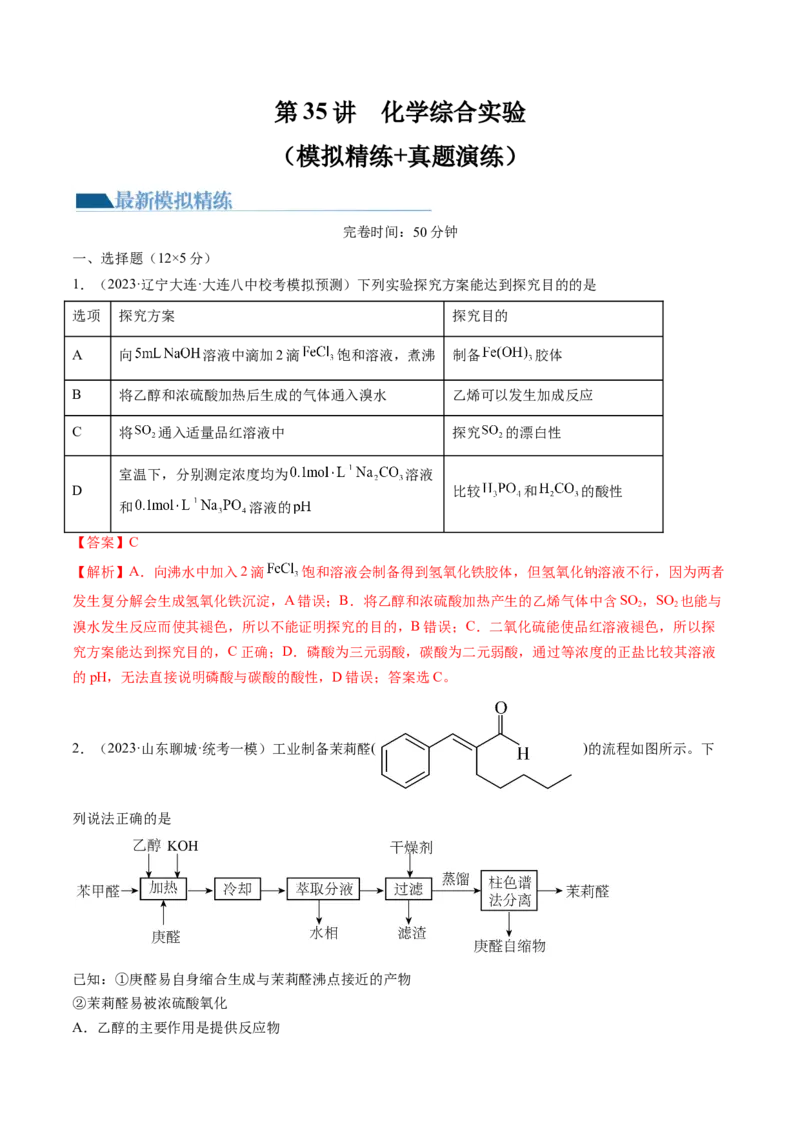
5.(2023·浙江温州·乐清市知临中学校考二模)某化学兴趣小组称取 晶体,在空气中
用热重法对其进行分析,得到剩余固体的质量随温度变化的曲线如图所示。下列说法不正确的是A.反应Ⅰ阶段是晶体失去结晶水
B.
C.反应Ⅱ阶段的化学方程式为:
D.将晶体加入酸性高锰酸钾溶液中,若溶液紫色褪去,不能说明晶体中含
【答案】C
【解析】A. 受热第一阶段是失去结晶水的过程,A正确;B.反应Ⅰ阶段失水的质量为
3.6g-2.88g=0.72g,物质的量为0.04mol,草酸亚铁的质量为2.88g,物质的量为0.02mol,
n(FeC O)∶n(H O)=1∶2,所以x=2,B正确;C.反应Ⅱ阶段FeC O 在300℃时与空气中氧气反应,
2 4 2 2 4
,C错误;D.草酸根离子能将高锰酸根还原,溶液褪色,将晶体加入酸性
高锰酸钾溶液中,若溶液紫色褪去,不能说明晶体中含 ,D正确;故选C。
6.(2023·福建龙岩·统考三模)实验室可以通过以下反应和操作制取肉桂酸:
已知:苯甲醛、肉桂酸均难溶于水,乙酸酐(CHCO) O易水解。
3 2
操作:①将一定量苯甲醛、乙酸酐、KCO 混合加热回流0.5h ②向回流后的混合液中加入KCO 溶液调节
2 3 2 3
溶液至碱性 ③将“②”中溶液装入下图的Ⅱ装置中,并通入水蒸气,Ⅲ中收集到苯甲醛和水 ④……。
下列有关说法错误的是A.回流过程中可能有气泡产生
B.当馏出液无油珠时,即可停止通入水蒸气
C.操作③结束时,应先移去热源再打开弹簧夹
D.向Ⅱ中残余溶液中加入盐酸酸化,再过滤、洗涤、干燥可以获得肉桂酸粗品
【答案】C
【分析】将一定量苯甲醛、乙酸酐、KCO 在圆底烧瓶中混合均匀,然后加热回流0.5h,发生题中反应生
2 3
成肉桂酸和乙酸,向回流后的混合液中加入KCO 溶液调节溶液至碱性,此时肉桂酸转化为肉桂酸钾,该
2 3
过程中生成二氧化碳气体,将反应后溶液转移到圆底烧瓶中组装成图中装置,加热盛水的圆底烧瓶,利用
水蒸气将苯甲醛蒸出,经冷凝后在III中收集未反应完的苯甲醛。
【解析】A.回流过程中生成的乙酸与碳酸钾可能反应生成二氧化碳气体,因此可能产生气泡,故A正确;
B.当馏出液无油珠时说明未反应的苯甲醛已完全除去,此时可停止通入水蒸气,故B正确;C.操作③结
束时,如先移去热源再打开弹簧夹,II中的液体会倒吸到I中,因此应先打开弹簧夹使系统与大气相通后
再移去热源,故C错误;D.向Ⅱ中残余溶液中加入盐酸酸化,使肉桂酸钾转化为肉桂酸,肉桂酸难溶于
水,经再滤、洗涤、干燥可以获得肉桂酸粗品,故D正确;故选:C。
7.(2023·山东枣庄·统考三模)实验室以甲苯和 为原料制备苯甲醛的主要流程如下图,下列说法错
误的是
A.“氧化”反应中氧化剂与还原剂的物质的量之比为2:1
B.“氧化”时间过长,部分苯甲醛会转化为苯甲酸
C.分液时,上层液体从分液漏斗上口倒出
D.蒸馏时,温度计水银球应插入液面以下
【答案】D
【分析】由题给流程可知,甲苯与稀硫酸和三氧化二锰、稀硫酸反应苯甲醛,分液得到含有硫酸锰的水相
和含有苯甲醛的有机相;有机相经蒸馏得到甲苯和苯甲醛。
【解析】A.由分析可知,“氧化”发生的反应为甲苯与稀硫酸和三氧化二锰、稀硫酸反应苯甲醛,由得
失电子数目守恒可知,反应中氧化剂三氧化二锰与还原剂甲苯的物质的量之比为2:1,故A正确;B.苯
甲醛检验还原性,可能被氧化为苯甲酸,所以若“氧化”时间过长,部分苯甲醛会转化为苯甲酸,故B正
确;C.分液时,为防止所得溶液中混有杂质,下层液体从下口流出,上层液体从分液漏斗上口倒出,故
C正确;D.蒸馏时,温度计水银球应放在蒸馏烧瓶的支管口处,不能插入液面以下,故D错误;故选
D。
8.(2023·湖南·校联考模拟预测)纯磷酸可通过市售85%磷酸溶液减压蒸馏除水、结晶除杂得到。制备纯
磷酸的实验装置如图(夹持装置略),下列说法错误的是已知:纯磷酸熔点为42℃,磷酸纯化过程需要严格控制温度和水分,温度低于21℃易形成杂质
(熔点为30℃),高于100℃,则发生分子间脱水生成焦磷酸等。
A.毛细管的作用是防止暴沸,还具有搅拌和加速水逸出的作用
B.磷酸过滤时需要控制温度低于20℃
C.实验选用水浴加热的目的是使溶液受热均匀
D.磷酸中少量的水极难除去的原因是磷酸与水分子形成氢键
【答案】B
【解析】A.空气流入毛细管可以对烧瓶中的溶液进行搅拌,能防止暴沸,同时还具有加速水逸出和防止
溶液沿毛细管上升的作用,A正确;B.过滤温度低于20℃时,磷酸和 杂质均为固体,无法
通过过滤去除杂质,B错误;C.水浴加热可避免直接加热造成的过度剧烈与温度不可控,还可使溶液受
热均匀,此外,水浴加热能最大限度保证温度低于100℃,避免磷酸分子间脱水生成焦磷酸等,C正确;
D.磷酸结构简式为 ,其中的羟基可以与水形成氢键,从而提高除水难度,D正确;故
选B。
9.(2023·河北保定·定州一中校考模拟预测)氢溴酸在医药和石化工业上有广泛用途,模拟工业制备氢溴
酸的流程如图所示。下列说法不正确的是
A.混合①使用冰水的目的是防止Br 和HBr挥发
2
B.为充分除去粗品中的Br ,需加入过量的NaSO
2 2 3
C.蒸馏时,加完“滤液”后,先通冷凝水,再点燃酒精灯加热
D.工业氢溴酸常带有淡淡的黄色,可能是因为含有Br
2
【答案】B
【解析】A.混合①使用冰水降低温度,防止Br 和HBr挥发,,A正确;B.加入NaSO ,的目的是除去
2 2 3
粗品中的Br ,但不需加入过量的NaSO ,因为过量的NaSO 能与HBr反应,会导致氢溴酸的产量降低,B
2 2 3 2 3
错误;C.蒸馏时,先通入冷凝水,再点燃酒精灯加热,C正确;D.溴单质具有挥发性,工业氢溴酸常带有淡淡的黄色,可能含有挥发出的 Br ,D正确;故选B。
2
10.(2023·福建·校联考二模)利用 转化制取连二亚硫酸钠(
)的装置如图。下列说法不正确的是
A.单向阀的作用是防倒吸
B.先通入 至悬浊液变澄清,再打开滴液漏斗旋塞
C.NaOH溶液不宜加入过多的原因是防止 水解
D.上述反应液经过滤,在冷却搅拌下加入一定量NaCl的作用是提高产率
【答案】C
【分析】SO 通入三颈烧瓶中与Zn的悬浊液反应生成ZnS O,Zn+2SO =ZnS O,再滴加氢氧化钠溶液转
2 2 4 2 2 4
化制取连二亚硫酸钠,
【解析】A.单向阀可以控制气体单向流动,由于二氧化硫易溶于水,所以单向阀的作用是防止溶液倒吸,
A正确;B.先通入SO 和Zn反应制得ZnS O,反应完全时悬浊液变澄清,再打开滴液漏斗活塞,B正确;
2 2 4
C. 是强碱弱酸盐,水解呈碱性,碱性环境中会抑制其水解,因此NaOH溶液不宜加入过多的原
因不是防止 水解,其目的是防止Zn(OH) 溶解,不利于与 分离,C错误;D.加入NaCl
2
固体,增大Na+的浓度,有利于析出 晶体,提高产率,D正确;故选C。
11.(2023·山东淄博·统考三模)室温下,通过下列实验探究 溶液的性质。
实验 实验操作和现象
Ⅰ 用 计测定 溶液的 为6.2
Ⅱ 取少量新制饱和氯水于试管中,向其中加入 溶液至过量,产生大量无色气泡……
向 溶液中滴加少量 溶液,溶液迅速变黄,稍后产生气体;再加入几滴
Ⅲ
溶液,溶液变红,一段时间后,溶液颜色明显变浅
Ⅳ 向 溶液中滴加 溶液,很快有大量气体逸出, 后,蓝色溶液变为红色浑浊 ,继续加入 溶液,红色浑浊又变为蓝色溶液
下列有关说法错误的是
A.由实验Ⅰ可知,室温下
B.实验Ⅱ中还可观察到溶液的颜色逐渐变浅,最后消失
C.实验Ⅲ中一段时间后,溶液颜色明显变浅,原因是过量的 有氧化作用
D.实验Ⅲ、Ⅳ表明 溶液、 溶液对 溶液的分解均有一定的催化作用
【答案】D
【解析】A.忽略水的电离与过氧化氢的第二步电离, ,
,A正确;B.氯水中的Cl 与过氧化氢发生反应
2
,可观察到溶液的颜色逐渐变浅,最后消失,B正确;C.向 溶液
中滴加少量 溶液,溶液迅速变黄,发生反应: ,然后产生气体且
加入KSCN溶液变红,说明 催化过氧化氢分解,如果是 与过氧化氢发生氧化还原反应则不会变红,
一段时间后,溶液颜色明显变浅,有可能是过量的 将SCN-氧化,C正确;D.实验Ⅳ中Cu2+先被
还原,最后又得到Cu2+,说明Cu2+有催化作用,而实验Ⅲ经C选项分析可知 未作催化剂,D错
误;故选D。
12.(2023·浙江金华·浙江省丽水中学校联考一模)下列实验现象和结论正确的是
选项 实验目的 实验操作 实验现象、结论
取5mL0.1mol/LFeCl 溶液,滴加0.1mol/LKI溶
3
探究化学反 若溶液呈现血红色和蓝色,则
A 液5~6滴,充分反应后,取溶液分别加入到
应的限度 该反应是有限度
KSCN溶液和淀粉溶液中
醋酸钠溶液 取CHCOONa溶液于试管中并加入几滴酚酞试
3
若溶液颜色加深,则存在水解
B 中存在水解 剂,再加入醋酸铵固体
平衡
平衡 K(CHCOOH)=Kb(NH ·HO),观察溶液颜色变化
a 3 3
比较AgCl和
向等浓度的NaCl和NaI的混合溶液中滴加少量 若溶液中产生黄色沉淀,则
C AgI的Ksp
AgNO 溶液,观察现象 K (AgI)