文档内容
第3课时 学科素养——氯气的制备及综合实验
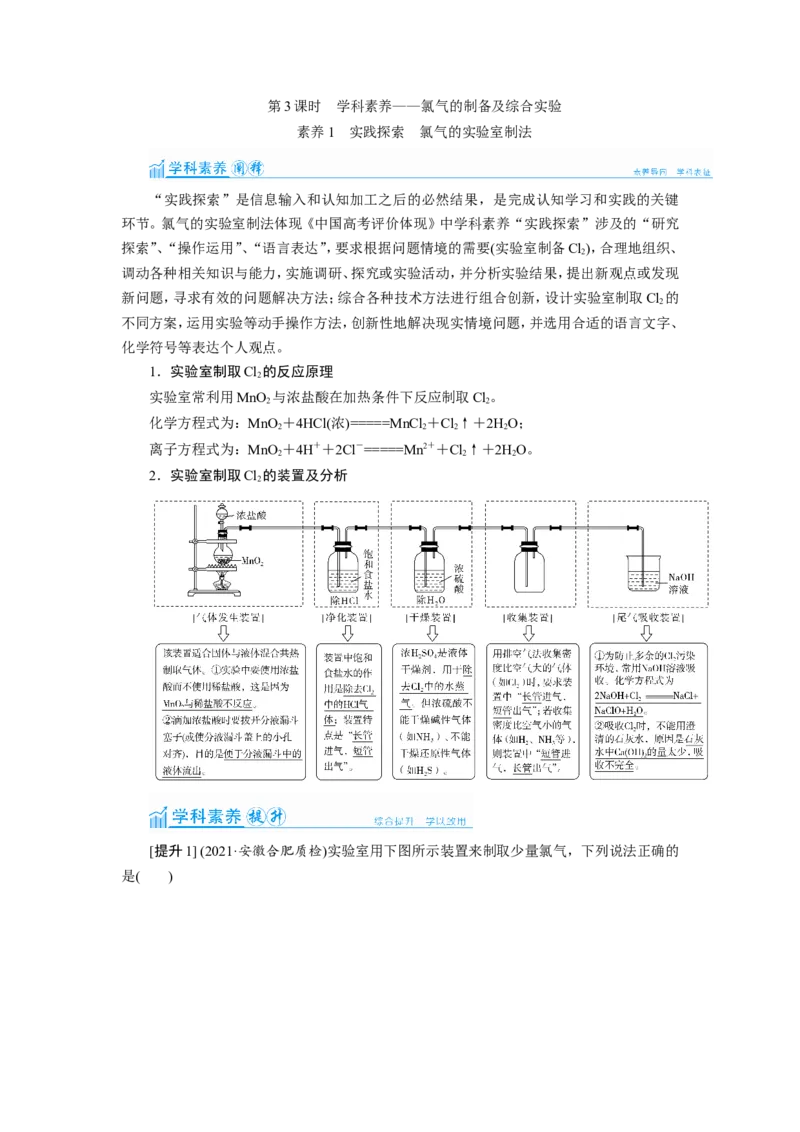
素养1 实践探索 氯气的实验室制法
“实践探索”是信息输入和认知加工之后的必然结果,是完成认知学习和实践的关键
环节。氯气的实验室制法体现《中国高考评价体现》中学科素养“实践探索”涉及的“研究
探索”、“操作运用”、“语言表达”,要求根据问题情境的需要(实验室制备Cl),合理地组织、
2
调动各种相关知识与能力,实施调研、探究或实验活动,并分析实验结果,提出新观点或发现
新问题,寻求有效的问题解决方法;综合各种技术方法进行组合创新,设计实验室制取Cl 的
2
不同方案,运用实验等动手操作方法,创新性地解决现实情境问题,并选用合适的语言文字、
化学符号等表达个人观点。
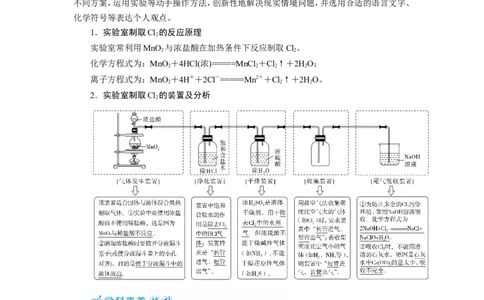
1.实验室制取Cl 的反应原理
2
实验室常利用MnO 与浓盐酸在加热条件下反应制取Cl。
2 2
化学方程式为:MnO +4HCl(浓)=====MnCl +Cl↑+2HO;
2 2 2 2
离子方程式为:MnO +4H++2Cl-=====Mn2++Cl↑+2HO。
2 2 2
2.实验室制取Cl 的装置及分析
2
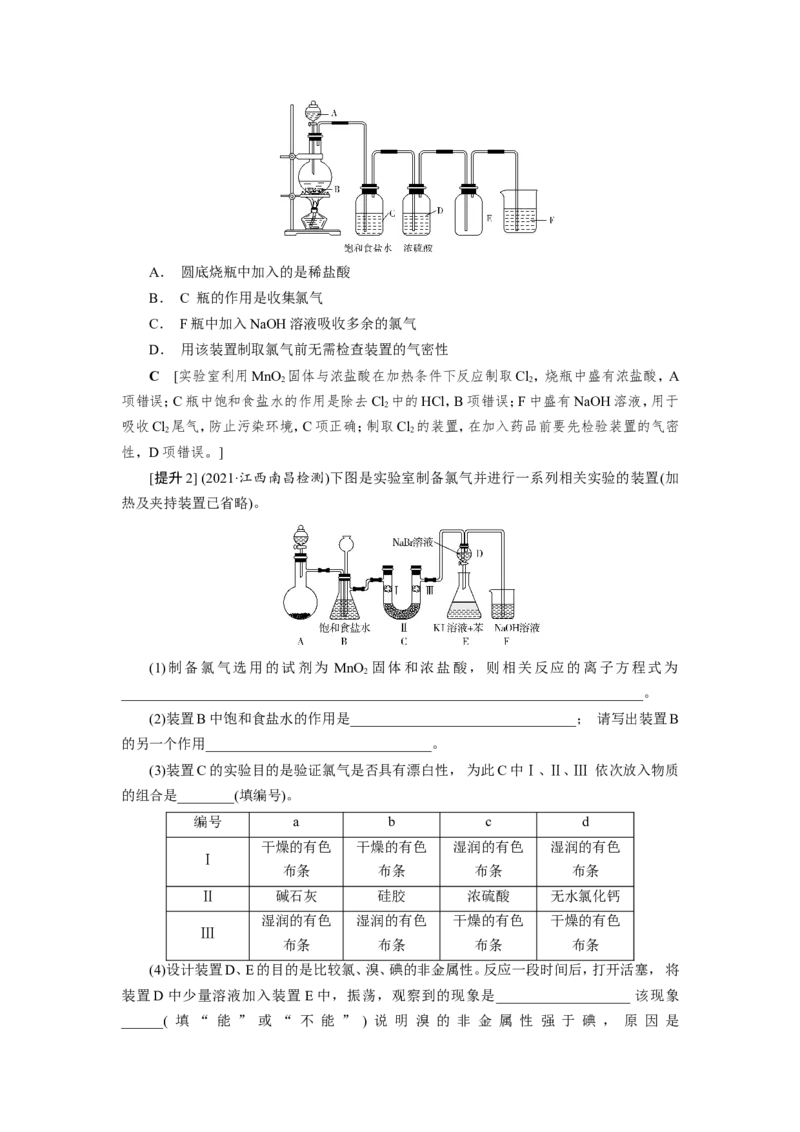
[提升1] (2021·安徽合肥质检)实验室用下图所示装置来制取少量氯气,下列说法正确的
是( )A. 圆底烧瓶中加入的是稀盐酸
B. C 瓶的作用是收集氯气
C. F瓶中加入NaOH溶液吸收多余的氯气
D. 用该装置制取氯气前无需检查装置的气密性
C [实验室利用MnO 固体与浓盐酸在加热条件下反应制取Cl,烧瓶中盛有浓盐酸,A
2 2
项错误;C瓶中饱和食盐水的作用是除去Cl 中的HCl,B项错误;F中盛有NaOH溶液,用于
2
吸收Cl 尾气,防止污染环境,C项正确;制取Cl 的装置,在加入药品前要先检验装置的气密
2 2
性,D项错误。]
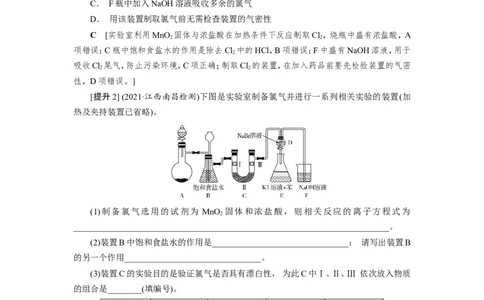
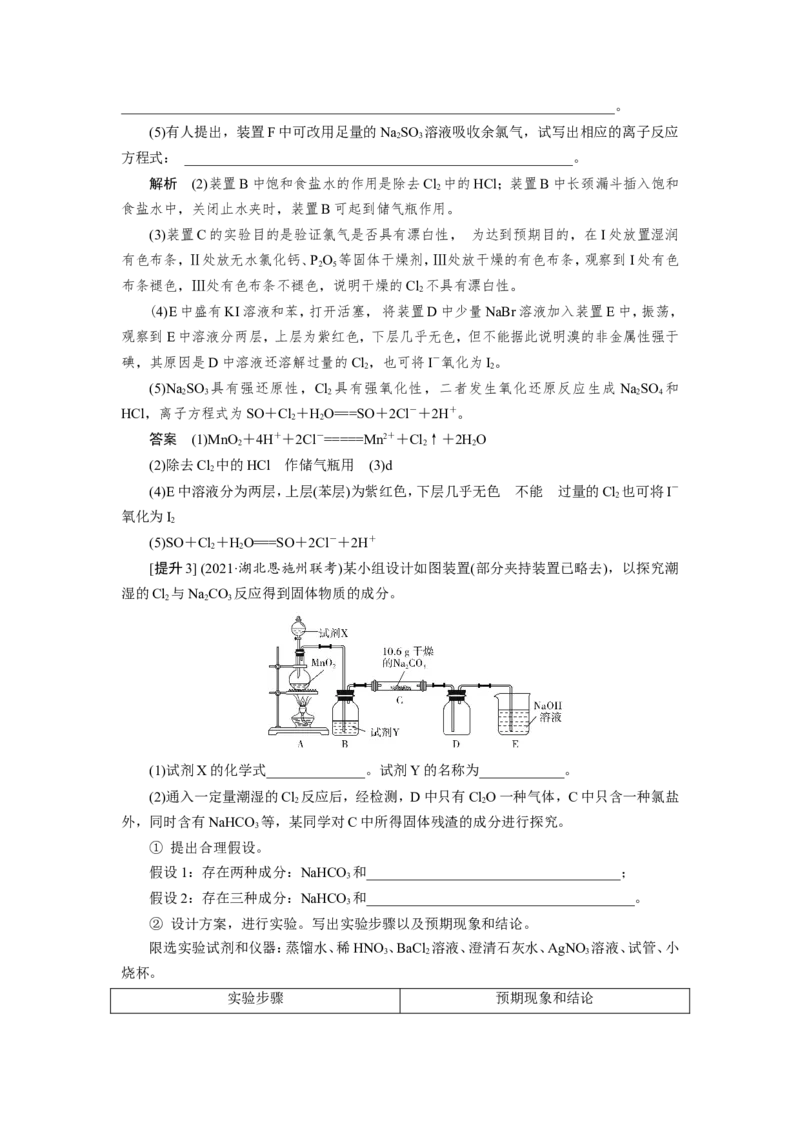
[提升2] (2021·江西南昌检测)下图是实验室制备氯气并进行一系列相关实验的装置(加
热及夹持装置已省略)。
(1)制备氯气选用的试剂为 MnO 固体和浓盐酸,则相关反应的离子方程式为
2
__________________________________________________________________________。
(2)装置B中饱和食盐水的作用是________________________________; 请写出装置B
的另一个作用________________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性, 为此C中Ⅰ、Ⅱ、Ⅲ 依次放入物质
的组合是________(填编号)。
编号 a b c d
干燥的有色 干燥的有色 湿润的有色 湿润的有色
Ⅰ
布条 布条 布条 布条
Ⅱ 碱石灰 硅胶 浓硫酸 无水氯化钙
湿润的有色 湿润的有色 干燥的有色 干燥的有色
Ⅲ
布条 布条 布条 布条
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。反应一段时间后,打开活塞, 将
装置D中少量溶液加入装置E中,振荡,观察到的现象是___________________ 该现象
______( 填 “ 能 ” 或 “ 不 能 ” ) 说 明 溴 的 非 金 属 性 强 于 碘 , 原 因 是______________________________________________________________________。
(5)有人提出,装置F中可改用足量的NaSO 溶液吸收余氯气,试写出相应的离子反应
2 3
方程式: _______________________________________________________。
解析 (2)装置B中饱和食盐水的作用是除去Cl 中的HCl;装置B中长颈漏斗插入饱和
2
食盐水中,关闭止水夹时,装置B可起到储气瓶作用。
(3)装置C的实验目的是验证氯气是否具有漂白性, 为达到预期目的,在I处放置湿润
有色布条,Ⅱ处放无水氯化钙、PO 等固体干燥剂,Ⅲ处放干燥的有色布条,观察到I处有色
2 5
布条褪色,Ⅲ处有色布条不褪色,说明干燥的Cl 不具有漂白性。
2
(4)E中盛有KI溶液和苯,打开活塞, 将装置D中少量NaBr溶液加入装置E中,振荡,
观察到E中溶液分两层,上层为紫红色,下层几乎无色,但不能据此说明溴的非金属性强于
碘,其原因是D中溶液还溶解过量的Cl,也可将I-氧化为I。
2 2
(5)Na SO 具有强还原性,Cl 具有强氧化性,二者发生氧化还原反应生成 NaSO 和
2 3 2 2 4
HCl,离子方程式为SO+Cl+HO===SO+2Cl-+2H+。
2 2
答案 (1)MnO +4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
(2)除去Cl 中的HCl 作储气瓶用 (3)d
2
(4)E中溶液分为两层,上层(苯层)为紫红色,下层几乎无色 不能 过量的Cl 也可将I-
2
氧化为I
2
(5)SO+Cl+HO===SO+2Cl-+2H+
2 2
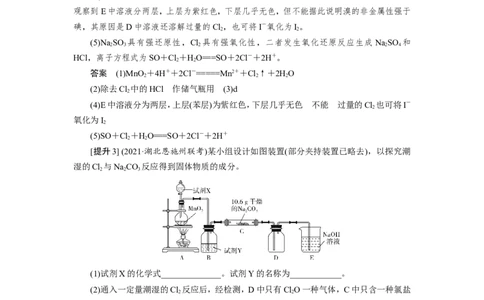
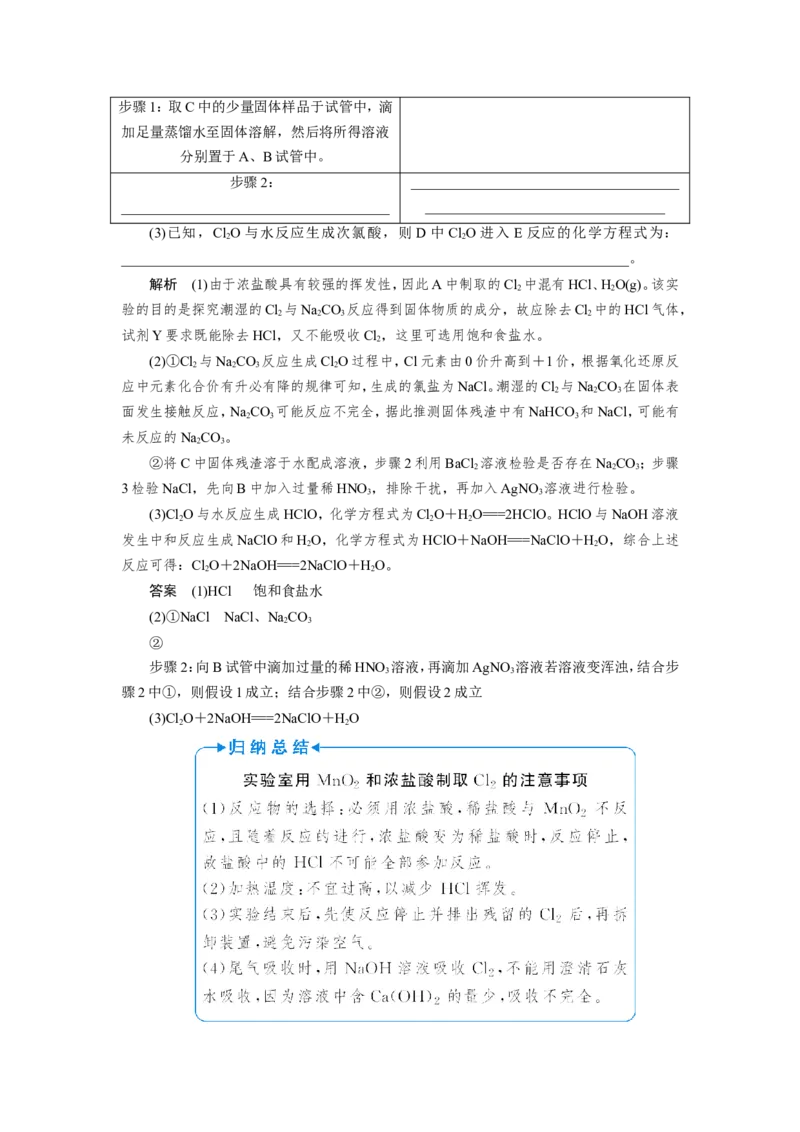
[提升3] (2021·湖北恩施州联考)某小组设计如图装置(部分夹持装置已略去),以探究潮
湿的Cl 与NaCO 反应得到固体物质的成分。
2 2 3
(1)试剂X的化学式______________。试剂Y的名称为____________。
(2)通入一定量潮湿的Cl 反应后,经检测,D中只有ClO一种气体,C中只含一种氯盐
2 2
外,同时含有NaHCO 等,某同学对C中所得固体残渣的成分进行探究。
3
① 提出合理假设。
假设1:存在两种成分:NaHCO 和____________________________________;
3
假设2:存在三种成分:NaHCO 和______________________________________。
3
② 设计方案,进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂和仪器:蒸馏水、稀HNO、BaCl 溶液、澄清石灰水、AgNO 溶液、试管、小
3 2 3
烧杯。
实验步骤 预期现象和结论步骤1:取C中的少量固体样品于试管中,滴
加足量蒸馏水至固体溶解,然后将所得溶液
分别置于A、B试管中。
步骤2: ______________________________________
______________________________________ __________________________________
(3)已知,ClO与水反应生成次氯酸,则D中ClO进入 E反应的化学方程式为:
2 2
________________________________________________________________________。
解析 (1)由于浓盐酸具有较强的挥发性,因此A中制取的Cl 中混有HCl、HO(g)。该实
2 2
验的目的是探究潮湿的Cl 与NaCO 反应得到固体物质的成分,故应除去Cl 中的HCl气体,
2 2 3 2
试剂Y要求既能除去HCl,又不能吸收Cl,这里可选用饱和食盐水。
2
(2)①Cl 与NaCO 反应生成ClO过程中,Cl元素由0价升高到+1价,根据氧化还原反
2 2 3 2
应中元素化合价有升必有降的规律可知,生成的氯盐为NaCl。潮湿的Cl 与NaCO 在固体表
2 2 3
面发生接触反应,NaCO 可能反应不完全,据此推测固体残渣中有NaHCO 和NaCl,可能有
2 3 3
未反应的NaCO。
2 3
②将C中固体残渣溶于水配成溶液,步骤2利用BaCl 溶液检验是否存在NaCO;步骤
2 2 3
3检验NaCl,先向B中加入过量稀HNO,排除干扰,再加入AgNO 溶液进行检验。
3 3
(3)Cl O与水反应生成HClO,化学方程式为ClO+HO===2HClO。HClO与NaOH溶液
2 2 2
发生中和反应生成NaClO和HO,化学方程式为HClO+NaOH===NaClO+HO,综合上述
2 2
反应可得:ClO+2NaOH===2NaClO+HO。
2 2
答案 (1)HCl 饱和食盐水
(2)①NaCl NaCl、NaCO
2 3
②
步骤2:向B试管中滴加过量的稀HNO 溶液,再滴加AgNO 溶液若溶液变浑浊,结合步
3 3
骤2中①,则假设1成立;结合步骤2中②,则假设2成立
(3)Cl O+2NaOH===2NaClO+HO
2 2素养2 思维方法 与氯气有关的综合实验
“思维方法”是思维的品质、方式和能力的综合,是个体高质量地解决生活实践或学习
探索情境中的各种问题的基础。与氯气有关的综合实验题大多以氯气的制备为载体,利用净
化后的Cl 与金属、非金属、碱或盐等反应,制备氯化物、氯的氧化物(ClO、ClO 等)、氯的含
2 2 2
氧酸盐等,此类问题要求考生运用开放性、创新性的思维方式应对问题情境,组织相关的知
识与能力,注重独立性、批判性、发散性的思考;综合运用直觉的、顿悟的、灵感的、形象的、
逻辑的方法,提出新视角、新观点、新方法、新设想,创新性地解决学习探索情境(与氯气有关
的探究实验)中的各种问题。
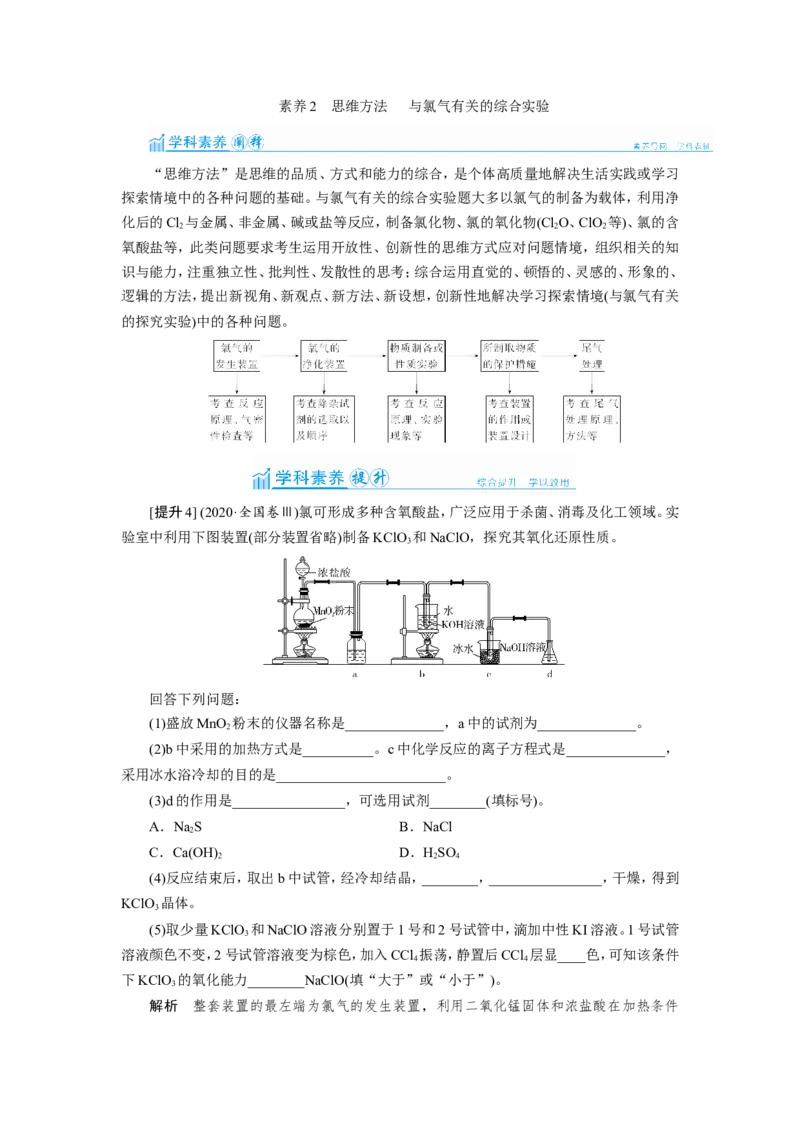
[提升4] (2020·全国卷Ⅲ)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实
验室中利用下图装置(部分装置省略)制备KClO 和NaClO,探究其氧化还原性质。
3
回答下列问题:
(1)盛放MnO 粉末的仪器名称是______________,a中的试剂为______________。
2
(2)b中采用的加热方式是__________。c中化学反应的离子方程式是______________,
采用冰水浴冷却的目的是________________________。
(3)d的作用是________________,可选用试剂________(填标号)。
A.NaS B.NaCl
2
C.Ca(OH) D.HSO
2 2 4
(4)反应结束后,取出b中试管,经冷却结晶,________,________________,干燥,得到
KClO 晶体。
3
(5)取少量KClO 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管
3
溶液颜色不变,2号试管溶液变为棕色,加入CCl 振荡,静置后CCl 层显____色,可知该条件
4 4
下KClO 的氧化能力________NaClO(填“大于”或“小于”)。
3
解析 整套装置的最左端为氯气的发生装置,利用二氧化锰固体和浓盐酸在加热条件下制取氯气,由于盐酸具有挥发性,导致氯气中含有杂质HCl和水蒸气。其中,氯气中的杂质
气体HCl会影响后面的KClO 和NaClO的制备,故而需要用饱和食盐水(a中盛放的试剂)除
3
去氯气中的HCl杂质。b为氯气与KOH溶液在加热(热水浴)条件下制取KClO 的装置,发生
3
的反应为3Cl +6KOH=====KClO +5KCl+3HO。c为氯气与NaOH溶液在较低温度下制
2 3 2
取NaClO的装置,发生的反应为Cl+2NaOH===NaCl+NaClO+HO。d为尾气的吸收装置,
2 2
可防止污染环境,吸收氯气可用还原性物质或碱性溶液。(1)盛放二氧化锰固体的仪器为圆底
烧瓶。除去氯气中的HCl杂质可用饱和食盐水。(2)b中采用的是水浴加热。c装置中的离子反
应方程式为Cl +2OH-===Cl-+ClO-+HO,c中采用冰水浴冷却的目的是防止氯气和
2 2
NaOH溶液在较高温度下生成NaClO。(3)d装置中应盛放还原性物质或碱性物质,故符合条
3
件的试剂为AC。(4)从溶液中获得晶体可采用的方法步骤为冷却结晶→过滤→洗涤→干燥等。
(5)1号试管中的KClO 溶液不能将I-氧化为单质I ,而2号试管中的NaClO溶液可将I-氧
3 2
化为I,故氧化性:KClO 小于NaClO。四氯化碳萃取出碘水中的I 后,静置一段时间可观察
2 3 2
到液体分为两层,由于四氯化碳的密度大于水的密度,则碘的四氯化碳溶液在下层,呈紫色。
答案 (1)圆底烧瓶 饱和食盐水
(2)水浴加热 Cl+2OH-===ClO-+Cl-+HO 避免生成NaClO
2 2 3
(3)吸收尾气(Cl ) AC
2
(4)过滤 少量(冷)水洗涤 (5)紫 小于
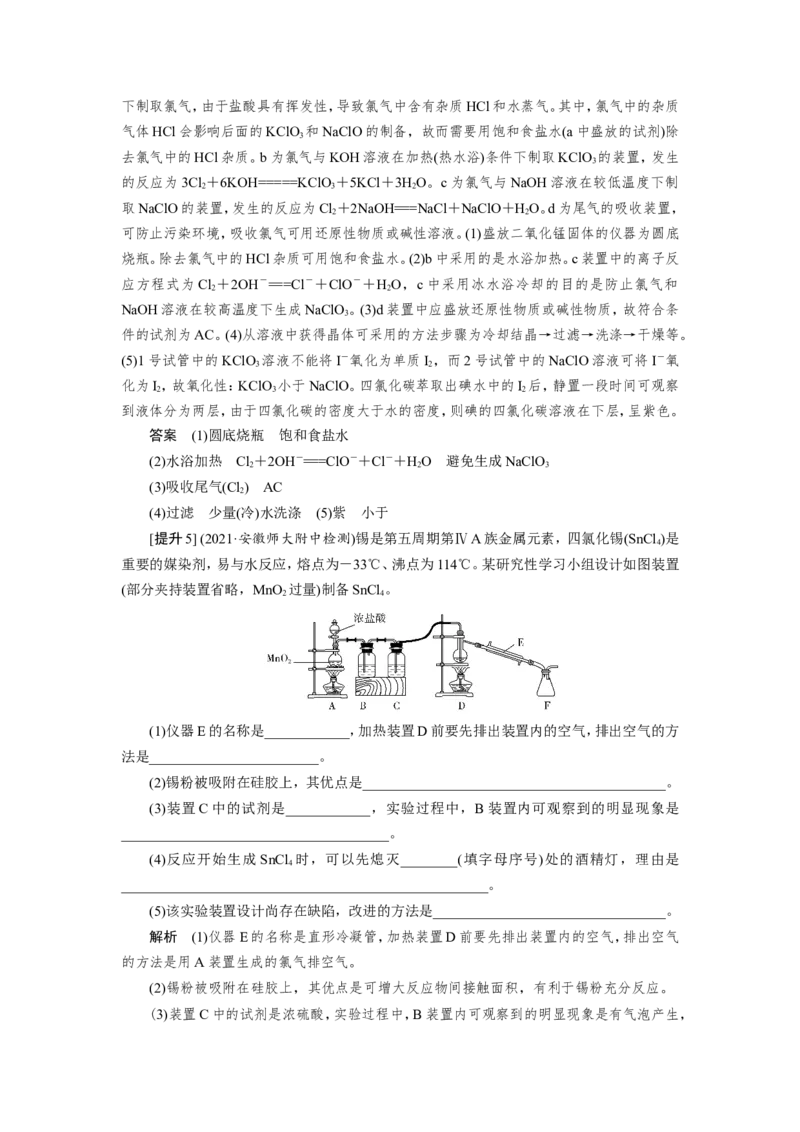
[提升5] (2021·安徽师大附中检测)锡是第五周期第ⅣA族金属元素,四氯化锡(SnCl )是
4
重要的媒染剂,易与水反应,熔点为-33℃、沸点为114℃。某研究性学习小组设计如图装置
(部分夹持装置省略,MnO 过量)制备SnCl 。
2 4
(1)仪器E的名称是____________,加热装置D前要先排出装置内的空气,排出空气的方
法是________________________。
(2)锡粉被吸附在硅胶上,其优点是___________________________________________。
(3)装置C中的试剂是____________,实验过程中,B装置内可观察到的明显现象是
______________________________________。
(4)反应开始生成SnCl 时,可以先熄灭________(填字母序号)处的酒精灯,理由是
4
____________________________________________________。
(5)该实验装置设计尚存在缺陷,改进的方法是_________________________________。
解析 (1)仪器E的名称是直形冷凝管,加热装置D前要先排出装置内的空气,排出空气
的方法是用A装置生成的氯气排空气。
(2)锡粉被吸附在硅胶上,其优点是可增大反应物间接触面积,有利于锡粉充分反应。
(3)装置C中的试剂是浓硫酸,实验过程中,B装置内可观察到的明显现象是有气泡产生,液面上方充满黄绿色气体。
(4)反应开始生成SnCl 时,可以先熄灭D处的酒精灯,理由是熔融的金属锡与氯气反应
4
过程中放出大量的热,能维持该反应继续进行。
(5)该实验装置设计尚存在缺陷,改进的方法是需要温度计或者在装置F后应连接一个
装有碱石灰(或氢氧化钠固体)的干燥管(或U形管)。
答案 (1)直形冷凝管 用A装置生成的氯气排空气
(2)可增大反应物间接触面积,有利于锡粉充分反应,有晶体析出
(3)浓硫酸 有气泡产生,液面上方充满黄绿色气体
(4)D 熔融的金属锡与氯气反应过程中放出大量的热,能维持该反应继续进行
(5)需要温度计或者在装置F后应连接一个装有碱石灰(或氢氧化钠固体)的干燥管(或U
形管)
训练(十九) 氯气的制备及综合实验1.(2021·重庆巴蜀中学月考)下列关于实验室制Cl 的认识正确的是( )
2
A.还原剂是MnO
2
B.发生氧化反应的是HCl
C.向含有4 mol HCl的浓盐酸中加入足量MnO 并加热,反应过程中转移电子数为2N
2 A
D.收集Cl 宜采用向上排空气法收集
2
答案 B
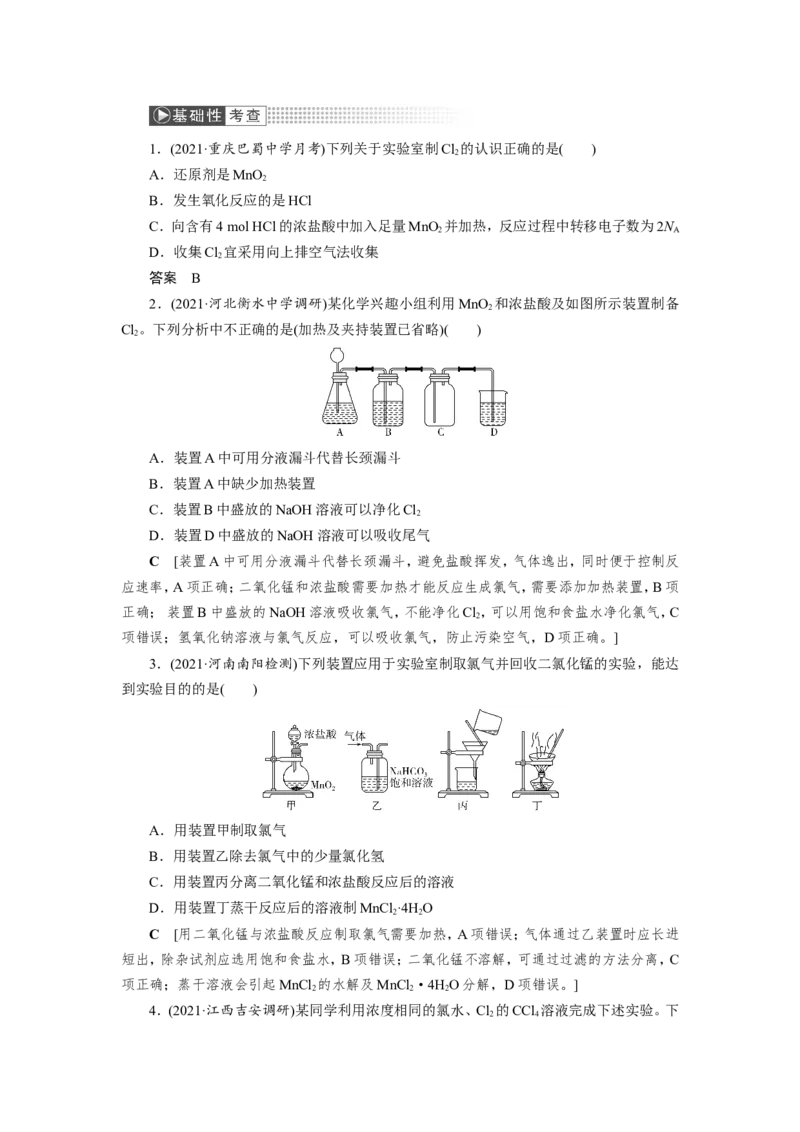
2.(2021·河北衡水中学调研)某化学兴趣小组利用MnO 和浓盐酸及如图所示装置制备
2
Cl。下列分析中不正确的是(加热及夹持装置已省略)( )
2
A.装置A中可用分液漏斗代替长颈漏斗
B.装置A中缺少加热装置
C.装置B中盛放的NaOH 溶液可以净化Cl
2
D.装置D中盛放的NaOH 溶液可以吸收尾气
C [装置A中可用分液漏斗代替长颈漏斗,避免盐酸挥发,气体逸出,同时便于控制反
应速率,A项正确;二氧化锰和浓盐酸需要加热才能反应生成氯气,需要添加加热装置,B项
正确; 装置B中盛放的NaOH溶液吸收氯气,不能净化Cl,可以用饱和食盐水净化氯气,C
2
项错误;氢氧化钠溶液与氯气反应,可以吸收氯气,防止污染空气,D项正确。]
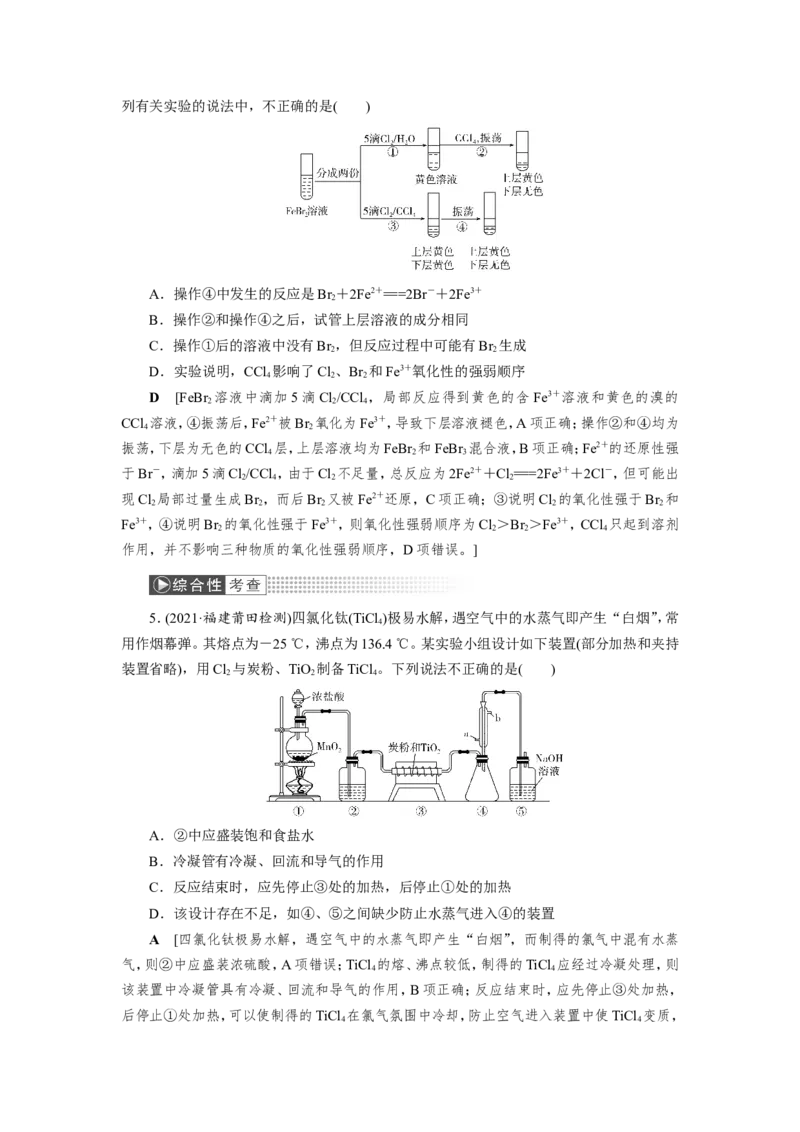
3.(2021·河南南阳检测)下列装置应用于实验室制取氯气并回收二氯化锰的实验,能达
到实验目的的是( )
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和浓盐酸反应后的溶液
D.用装置丁蒸干反应后的溶液制MnCl ·4H O
2 2
C [用二氧化锰与浓盐酸反应制取氯气需要加热,A项错误;气体通过乙装置时应长进
短出,除杂试剂应选用饱和食盐水,B项错误;二氧化锰不溶解,可通过过滤的方法分离,C
项正确;蒸干溶液会引起MnCl 的水解及MnCl ·4HO分解,D项错误。]
2 2 2
4.(2021·江西吉安调研)某同学利用浓度相同的氯水、Cl 的CCl 溶液完成下述实验。下
2 4列有关实验的说法中,不正确的是( )
A.操作④中发生的反应是Br +2Fe2+===2Br-+2Fe3+
2
B.操作②和操作④之后,试管上层溶液的成分相同
C.操作①后的溶液中没有Br ,但反应过程中可能有Br 生成
2 2
D.实验说明,CCl 影响了Cl、Br 和Fe3+氧化性的强弱顺序
4 2 2
D [FeBr 溶液中滴加5滴Cl/CCl ,局部反应得到黄色的含Fe3+溶液和黄色的溴的
2 2 4
CCl 溶液,④振荡后,Fe2+被Br 氧化为Fe3+,导致下层溶液褪色,A项正确;操作②和④均为
4 2
振荡,下层为无色的CCl 层,上层溶液均为FeBr 和FeBr 混合液,B项正确;Fe2+的还原性强
4 2 3
于Br-,滴加5滴Cl/CCl ,由于Cl 不足量,总反应为2Fe2++Cl===2Fe3++2Cl-,但可能出
2 4 2 2
现Cl 局部过量生成Br ,而后Br 又被Fe2+还原,C项正确;③说明Cl 的氧化性强于Br 和
2 2 2 2 2
Fe3+,④说明Br 的氧化性强于Fe3+,则氧化性强弱顺序为Cl>Br >Fe3+,CCl 只起到溶剂
2 2 2 4
作用,并不影响三种物质的氧化性强弱顺序,D项错误。]
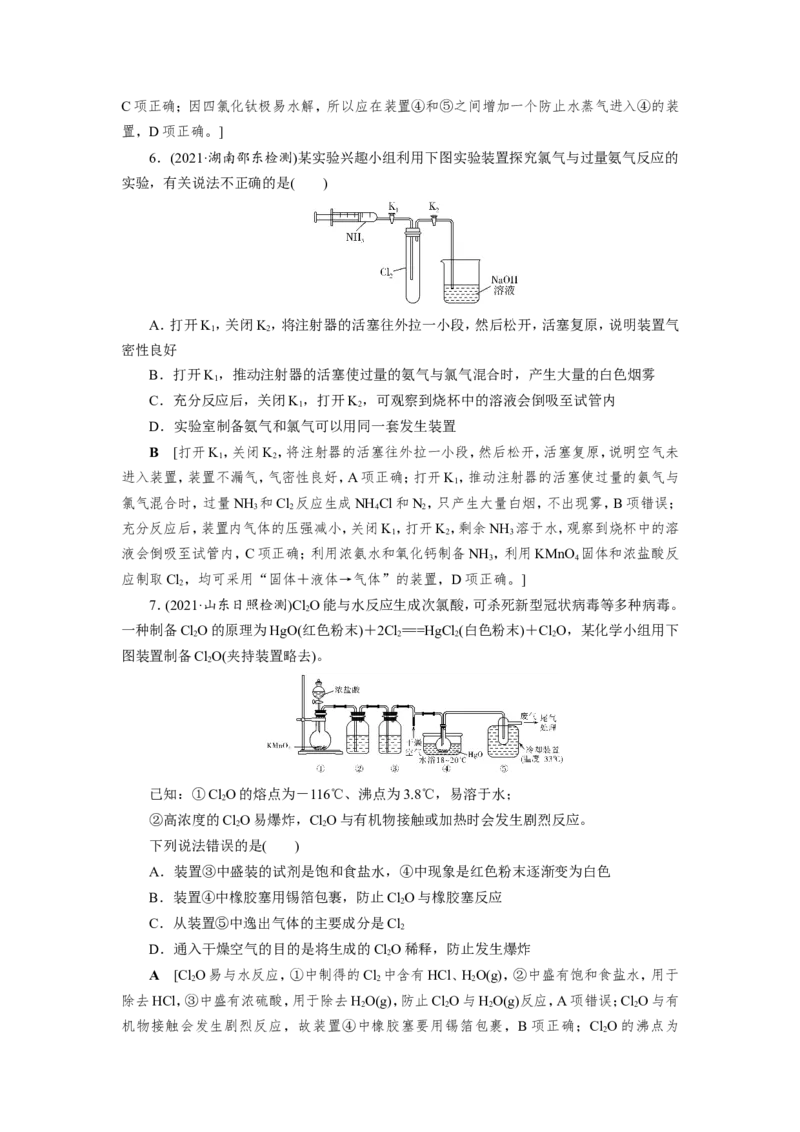
5.(2021·福建莆田检测)四氯化钛(TiCl )极易水解,遇空气中的水蒸气即产生“白烟”,常
4
用作烟幕弹。其熔点为-25 ℃,沸点为136.4 ℃。某实验小组设计如下装置(部分加热和夹持
装置省略),用Cl 与炭粉、TiO 制备TiCl 。下列说法不正确的是( )
2 2 4
A.②中应盛装饱和食盐水
B.冷凝管有冷凝、回流和导气的作用
C.反应结束时,应先停止③处的加热,后停止①处的加热
D.该设计存在不足,如④、⑤之间缺少防止水蒸气进入④的装置
A [四氯化钛极易水解,遇空气中的水蒸气即产生“白烟”,而制得的氯气中混有水蒸
气,则②中应盛装浓硫酸,A项错误;TiCl 的熔、沸点较低,制得的TiCl 应经过冷凝处理,则
4 4
该装置中冷凝管具有冷凝、回流和导气的作用,B项正确;反应结束时,应先停止③处加热,
后停止①处加热,可以使制得的TiCl 在氯气氛围中冷却,防止空气进入装置中使TiCl 变质,
4 4C项正确;因四氯化钛极易水解,所以应在装置④和⑤之间增加一个防止水蒸气进入④的装
置,D项正确。]
6.(2021·湖南邵东检测)某实验兴趣小组利用下图实验装置探究氯气与过量氨气反应的
实验,有关说法不正确的是( )
A.打开K,关闭K,将注射器的活塞往外拉一小段,然后松开,活塞复原,说明装置气
1 2
密性良好
B.打开K,推动注射器的活塞使过量的氨气与氯气混合时,产生大量的白色烟雾
1
C.充分反应后,关闭K,打开K,可观察到烧杯中的溶液会倒吸至试管内
1 2
D.实验室制备氨气和氯气可以用同一套发生装置
B [打开K,关闭K,将注射器的活塞往外拉一小段,然后松开,活塞复原,说明空气未
1 2
进入装置,装置不漏气,气密性良好,A项正确;打开K,推动注射器的活塞使过量的氨气与
1
氯气混合时,过量NH 和Cl 反应生成NH Cl和N,只产生大量白烟,不出现雾,B项错误;
3 2 4 2
充分反应后,装置内气体的压强减小,关闭K,打开K,剩余NH 溶于水,观察到烧杯中的溶
1 2 3
液会倒吸至试管内,C项正确;利用浓氨水和氧化钙制备NH ,利用KMnO 固体和浓盐酸反
3 4
应制取Cl,均可采用“固体+液体→气体”的装置,D项正确。]
2
7.(2021·山东日照检测)ClO能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。
2
一种制备ClO的原理为HgO(红色粉末)+2Cl===HgCl (白色粉末)+ClO,某化学小组用下
2 2 2 2
图装置制备ClO(夹持装置略去)。
2
已知:①ClO的熔点为-116℃、沸点为3.8℃,易溶于水;
2
②高浓度的ClO易爆炸,ClO与有机物接触或加热时会发生剧烈反应。
2 2
下列说法错误的是( )
A.装置③中盛装的试剂是饱和食盐水,④中现象是红色粉末逐渐变为白色
B.装置④中橡胶塞用锡箔包裹,防止ClO与橡胶塞反应
2
C.从装置⑤中逸出气体的主要成分是Cl
2
D.通入干燥空气的目的是将生成的ClO稀释,防止发生爆炸
2
A [Cl O易与水反应,①中制得的Cl 中含有HCl、HO(g),②中盛有饱和食盐水,用于
2 2 2
除去HCl,③中盛有浓硫酸,用于除去HO(g),防止ClO与HO(g)反应,A项错误;ClO与有
2 2 2 2
机物接触会发生剧烈反应,故装置④中橡胶塞要用锡箔包裹,B项正确;ClO的沸点为
23.8℃,装置⑤中冷却装置的温度为-33℃,因此⑤中逸出气体不是ClO,应是未反应的Cl,
2 2
C项正确;高浓度的ClO易爆炸,通入干燥空气,可稀释生成的ClO,防止发生爆炸,D项正
2 2
确。]
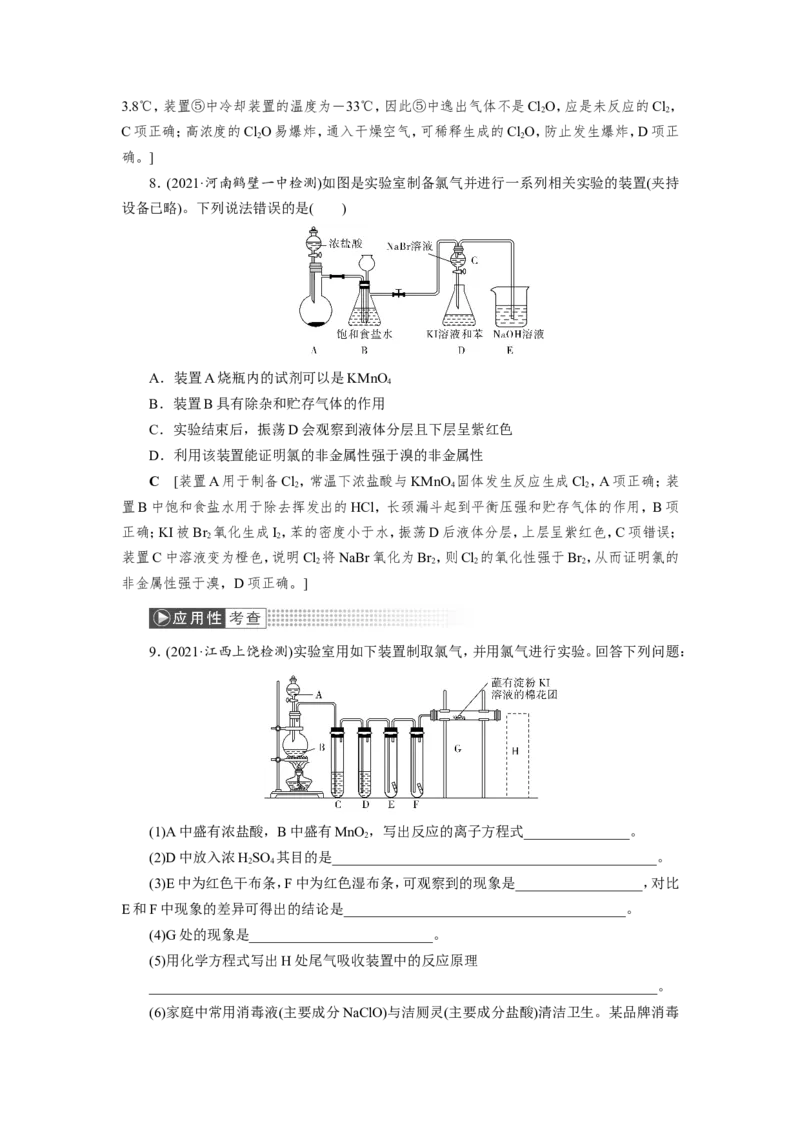
8.(2021·河南鹤壁一中检测)如图是实验室制备氯气并进行一系列相关实验的装置(夹持
设备已略)。下列说法错误的是( )
A.装置A烧瓶内的试剂可以是KMnO
4
B.装置B具有除杂和贮存气体的作用
C.实验结束后,振荡D会观察到液体分层且下层呈紫红色
D.利用该装置能证明氯的非金属性强于溴的非金属性
C [装置A用于制备Cl,常温下浓盐酸与KMnO 固体发生反应生成Cl,A项正确;装
2 4 2
置B中饱和食盐水用于除去挥发出的HCl,长颈漏斗起到平衡压强和贮存气体的作用,B项
正确;KI被Br 氧化生成I,苯的密度小于水,振荡D后液体分层,上层呈紫红色,C项错误;
2 2
装置C中溶液变为橙色,说明Cl 将NaBr氧化为Br ,则Cl 的氧化性强于Br ,从而证明氯的
2 2 2 2
非金属性强于溴,D项正确。]
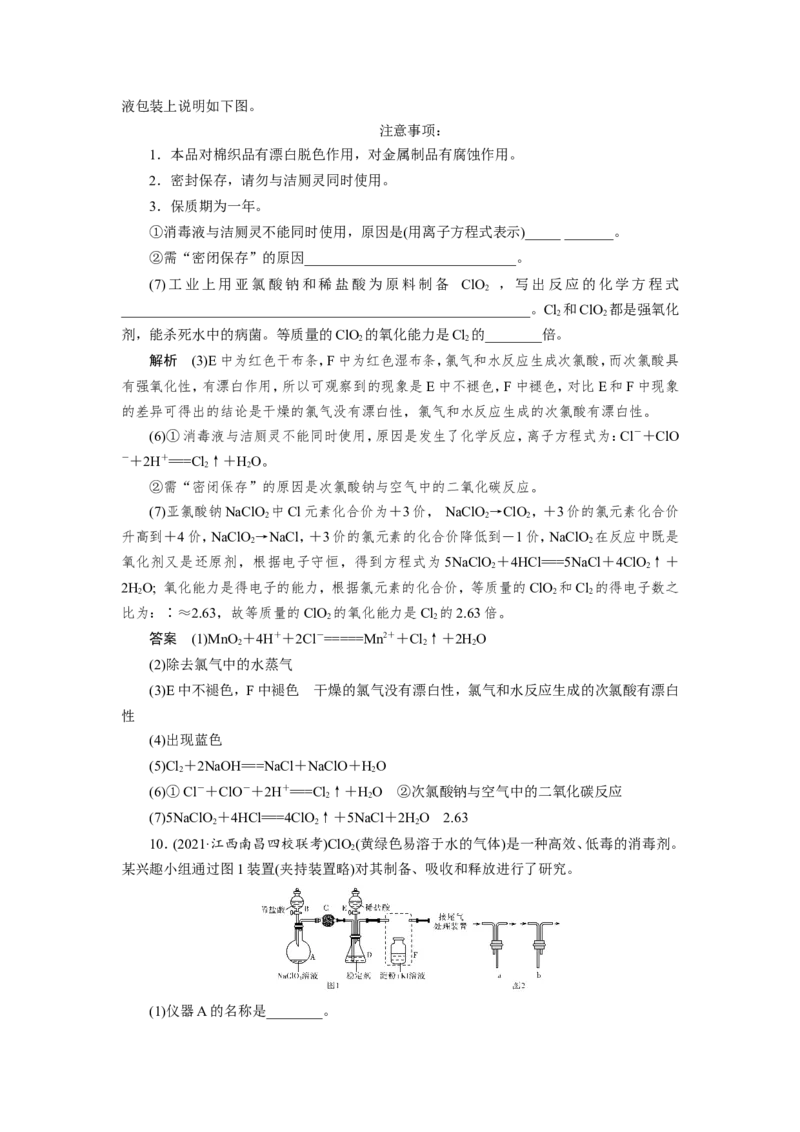
9.(2021·江西上饶检测)实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:
(1)A中盛有浓盐酸,B中盛有MnO ,写出反应的离子方程式_______________。
2
(2)D中放入浓HSO 其目的是______________________________________________。
2 4
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是__________________,对比
E和F中现象的差异可得出的结论是________________________________________。
(4)G处的现象是__________________________。
(5)用化学方程式写出H处尾气吸收装置中的反应原理
________________________________________________________________________。
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
注意事项:
1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。
2.密封保存,请勿与洁厕灵同时使用。
3.保质期为一年。
①消毒液与洁厕灵不能同时使用,原因是(用离子方程式表示)_____ _______。
②需“密闭保存”的原因______________________________。
(7)工业上用亚氯酸钠和稀盐酸为原料制备 ClO ,写出反应的化学方程式
2
__________________________________________________________。Cl 和ClO 都是强氧化
2 2
剂,能杀死水中的病菌。等质量的ClO 的氧化能力是Cl 的________倍。
2 2
解析 (3)E中为红色干布条,F中为红色湿布条,氯气和水反应生成次氯酸,而次氯酸具
有强氧化性,有漂白作用,所以可观察到的现象是E中不褪色,F中褪色,对比E和F中现象
的差异可得出的结论是干燥的氯气没有漂白性,氯气和水反应生成的次氯酸有漂白性。
(6)①消毒液与洁厕灵不能同时使用,原因是发生了化学反应,离子方程式为:Cl-+ClO
-+2H+===Cl↑+HO。
2 2
②需“密闭保存”的原因是次氯酸钠与空气中的二氧化碳反应。
(7)亚氯酸钠NaClO 中Cl元素化合价为+3价, NaClO →ClO ,+3价的氯元素化合价
2 2 2
升高到+4价,NaClO→NaCl,+3价的氯元素的化合价降低到-1价,NaClO 在反应中既是
2 2
氧化剂又是还原剂,根据电子守恒,得到方程式为5NaClO +4HCl===5NaCl+4ClO ↑+
2 2
2HO; 氧化能力是得电子的能力,根据氯元素的化合价,等质量的ClO 和Cl 的得电子数之
2 2 2
比为:∶≈2.63,故等质量的ClO 的氧化能力是Cl 的2.63倍。
2 2
答案 (1)MnO +4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
(2)除去氯气中的水蒸气
(3)E中不褪色,F中褪色 干燥的氯气没有漂白性,氯气和水反应生成的次氯酸有漂白
性
(4)出现蓝色
(5)Cl +2NaOH===NaCl+NaClO+HO
2 2
(6)① Cl-+ClO-+2H+===Cl↑+HO ②次氯酸钠与空气中的二氧化碳反应
2 2
(7)5NaClO+4HCl===4ClO ↑+5NaCl+2HO 2.63
2 2 2
10.(2021·江西南昌四校联考)ClO (黄绿色易溶于水的气体)是一种高效、低毒的消毒剂。
2
某兴趣小组通过图1装置(夹持装置略)对其制备、吸收和释放进行了研究。
(1)仪器A的名称是________。(2)安装F中导管时,应选用图2中的________。
(3)A中发生反应生成ClO 和Cl,其氧化产物和还原产物物质的量之比为________。
2 2
(4)关闭B的活塞,ClO 在D中被稳定剂完全吸收生成NaClO,此时F中溶液的颜色不
2 2
变,则装置C的作用是
__________________________。
(5)已知在酸性条件下NaClO 可发生反应生成NaCl并释放出ClO ,该反应的离子方程
2 2
式为________________________________________________________________________。
(6)ClO 很不稳定,需随用随制,产物用水吸收得到ClO 溶液。为测定所得溶液中ClO 的
2 2 2
浓度,进行了下列实验:
步骤1:准确量取ClO 溶液10.00 mL,稀释成100.00 mL试样,量取V mL试样加入到
2 0
锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L-1 NaSO 溶液滴定至终点,重复2次,测得消耗
2 2 3
NaSO 溶液平均值为V mL。(已知2ClO +10I-+8H+===2Cl-+5I +4HO、 2NaSO +
2 2 3 1 2 2 2 2 2 3
I===Na SO+2NaI),计算该ClO 的浓度为________g/L(用含字母的代数式表示,计算结果
2 2 4 6 2
化简)。
解析 (2)F装置应是Cl 和KI反应,还需要连接尾气处理装置,所以应长管进气,短管
2
出气。
(3)氯酸钠和稀盐酸混合产生Cl 和ClO ,NaClO 中氯为+5价被还原成ClO 中+4价,
2 2 3 2
盐酸中氯为-1价,被氧化成0价氯,转移电子数为2,则NaClO、ClO 前系数为2,Cl 前系
3 2 2
数为1,反应化学方程式:2NaClO+4HCl===2ClO ↑+Cl↑+2NaCl+2HO,其氧化产物
3 2 2 2
Cl 和还原产物ClO 物质的量之比为1∶2。
2 2
(4)F装置中发生Cl+2KI===2KCl+I 时,碘遇淀粉变蓝,而F中溶液的颜色不变,则装
2 2
置C的作用是吸收Cl。
2
(5)在酸性条件下NaClO 可发生反应生成NaCl并释放出ClO ,根据元素守恒可知应还
2 2
有水生成,该反应的离子方程式为4H++5ClO===Cl-+4ClO ↑+2HO。
2 2
(6)设原ClO 溶液的浓度为x,
2
2ClO ~5I~ 10NaSO
2 2 2 2 3
2 10
1×10-3cV mol
1
则有x= mol/L= g/L。
答案 (1)圆底烧瓶 (2)b (3)1∶2 (4)吸收Cl
2
(5)4H++5ClO===Cl-+4ClO ↑+2HO (6)
2 2
11.(2021·山东济南检测)“84消毒液”是生活中常用的消毒剂,可与硫酸溶液反应制取
氯气,反应原理为: NaClO+NaCl+HSO =====NaSO +Cl↑+HO; 为探究氯气的性质,
2 4 2 4 2 2
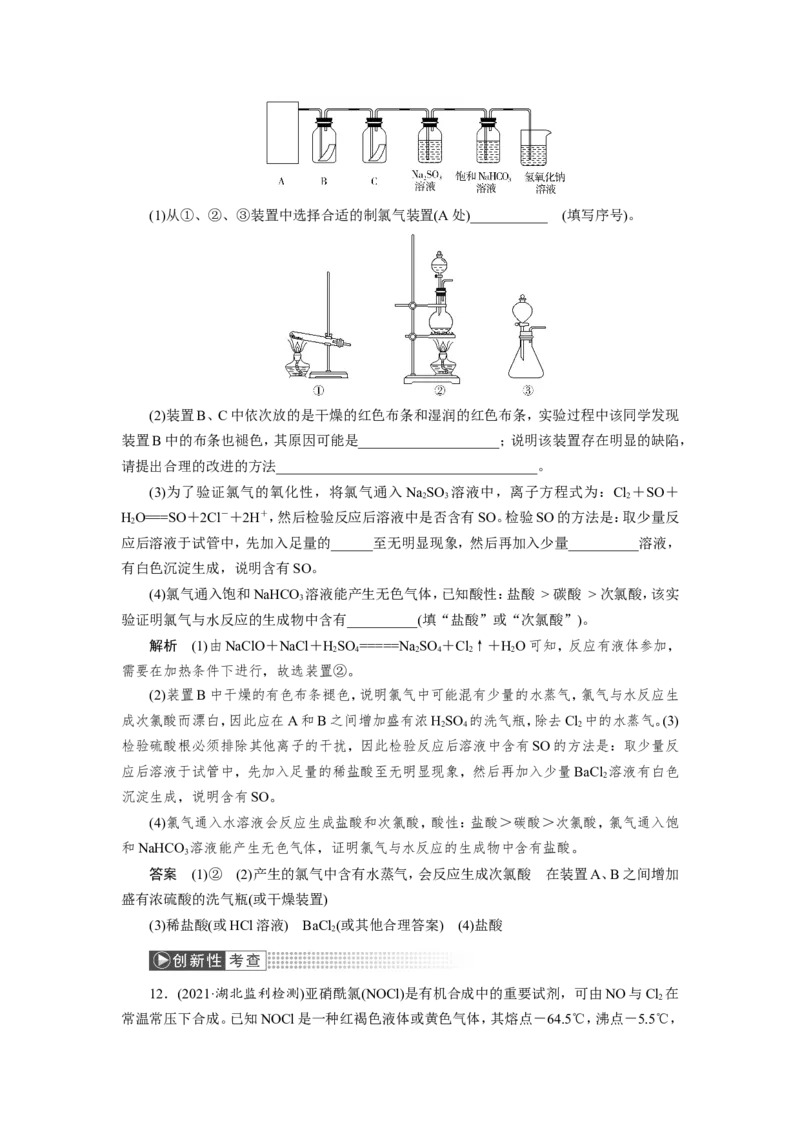
某同学利用此原理制氯气并设计了如下所示的实验装置:(1)从①、②、③装置中选择合适的制氯气装置(A处)___________ (填写序号)。
(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现
装置B中的布条也褪色,其原因可能是____________________;说明该装置存在明显的缺陷,
请提出合理的改进的方法_____________________________________。
(3)为了验证氯气的氧化性,将氯气通入NaSO 溶液中,离子方程式为:Cl +SO+
2 3 2
HO===SO+2Cl-+2H+,然后检验反应后溶液中是否含有SO。检验SO的方法是:取少量反
2
应后溶液于试管中,先加入足量的______至无明显现象,然后再加入少量__________溶液,
有白色沉淀生成,说明含有SO。
(4)氯气通入饱和NaHCO 溶液能产生无色气体,已知酸性:盐酸 > 碳酸 > 次氯酸,该实
3
验证明氯气与水反应的生成物中含有__________(填“盐酸”或“次氯酸”)。
解析 (1)由NaClO+NaCl+HSO =====NaSO +Cl↑+HO可知,反应有液体参加,
2 4 2 4 2 2
需要在加热条件下进行,故选装置②。
(2)装置B中干燥的有色布条褪色,说明氯气中可能混有少量的水蒸气,氯气与水反应生
成次氯酸而漂白,因此应在A和B之间增加盛有浓HSO 的洗气瓶,除去Cl 中的水蒸气。(3)
2 4 2
检验硫酸根必须排除其他离子的干扰,因此检验反应后溶液中含有SO的方法是:取少量反
应后溶液于试管中,先加入足量的稀盐酸至无明显现象,然后再加入少量BaCl 溶液有白色
2
沉淀生成,说明含有SO。
(4)氯气通入水溶液会反应生成盐酸和次氯酸,酸性:盐酸>碳酸>次氯酸,氯气通入饱
和NaHCO 溶液能产生无色气体,证明氯气与水反应的生成物中含有盐酸。
3
答案 (1)② (2)产生的氯气中含有水蒸气,会反应生成次氯酸 在装置A、B之间增加
盛有浓硫酸的洗气瓶(或干燥装置)
(3)稀盐酸(或HCl溶液) BaCl (或其他合理答案) (4)盐酸
2
12.(2021·湖北监利检测)亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl 在
2
常温常压下合成。已知NOCl是一种红褐色液体或黄色气体,其熔点-64.5℃,沸点-5.5℃,遇水易水解。
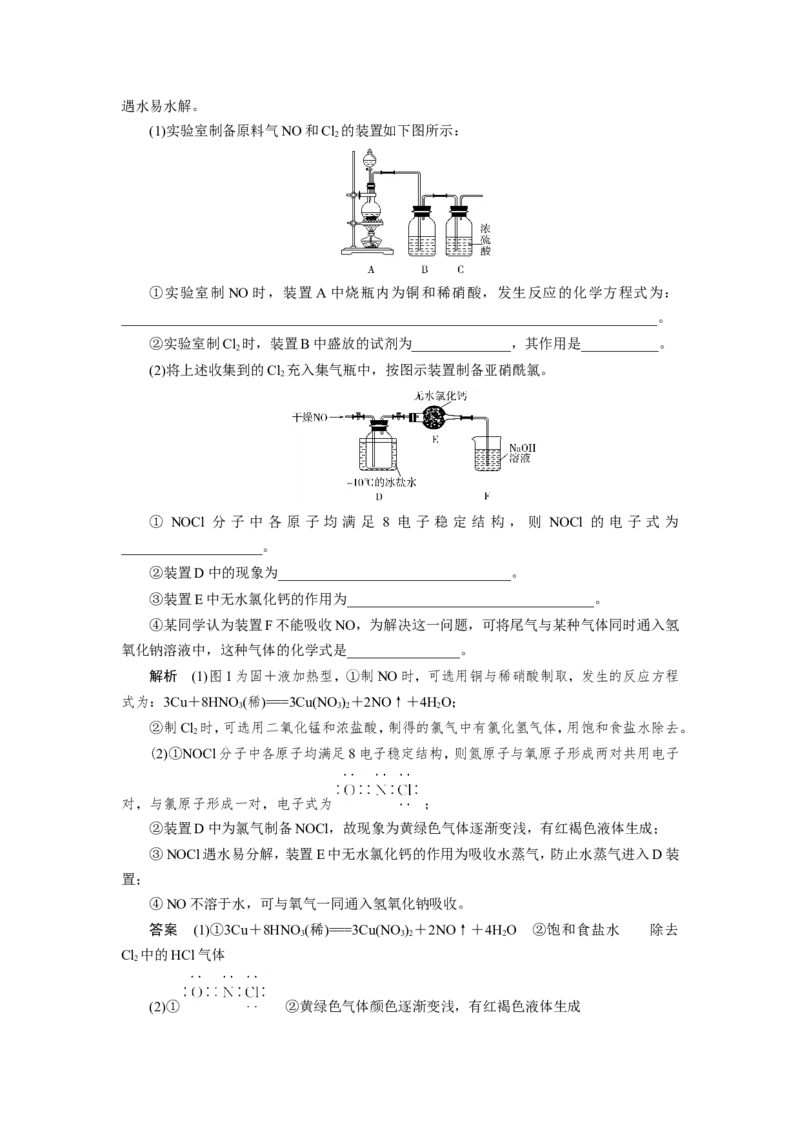
(1)实验室制备原料气NO和Cl 的装置如下图所示:
2
①实验室制 NO时,装置A中烧瓶内为铜和稀硝酸,发生反应的化学方程式为:
____________________________________________________________________________。
②实验室制Cl 时,装置B中盛放的试剂为______________,其作用是___________。
2
(2)将上述收集到的Cl 充入集气瓶中,按图示装置制备亚硝酰氯。
2
① NOCl 分 子 中 各 原 子 均 满 足 8 电 子 稳 定 结 构 , 则 NOCl 的 电 子 式 为
____________________。
②装置D中的现象为_________________________________。
③装置E中无水氯化钙的作用为___________________________________。
④某同学认为装置F不能吸收NO,为解决这一问题,可将尾气与某种气体同时通入氢
氧化钠溶液中,这种气体的化学式是________________。
解析 (1)图1为固+液加热型,①制NO时,可选用铜与稀硝酸制取,发生的反应方程
式为:3Cu+8HNO(稀)===3Cu(NO)+2NO↑+4HO;
3 3 2 2
②制Cl 时,可选用二氧化锰和浓盐酸,制得的氯气中有氯化氢气体,用饱和食盐水除去。
2
(2)①NOCl分子中各原子均满足8电子稳定结构,则氮原子与氧原子形成两对共用电子
对,与氯原子形成一对,电子式为 ;
②装置D中为氯气制备NOCl,故现象为黄绿色气体逐渐变浅,有红褐色液体生成;
③NOCl遇水易分解,装置E中无水氯化钙的作用为吸收水蒸气,防止水蒸气进入D装
置;
④NO不溶于水,可与氧气一同通入氢氧化钠吸收。
答案 (1)①3Cu+8HNO(稀)===3Cu(NO) +2NO↑+4HO ②饱和食盐水 除去
3 3 2 2
Cl 中的HCl气体
2
(2)① ②黄绿色气体颜色逐渐变浅,有红褐色液体生成③吸收水蒸气,防止水蒸气进入D装置 ④O
2
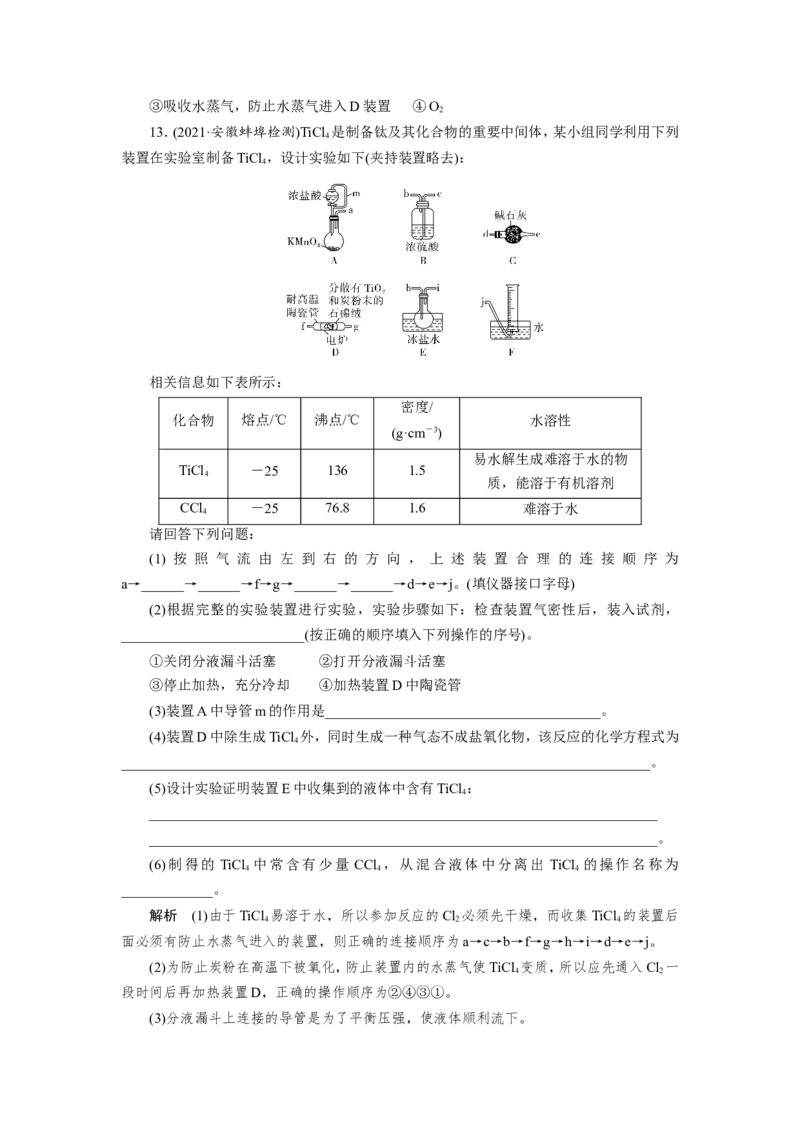
13.(2021·安徽蚌埠检测)TiCl 是制备钛及其化合物的重要中间体,某小组同学利用下列
4
装置在实验室制备TiCl ,设计实验如下(夹持装置略去):
4
相关信息如下表所示:
密度/
化合物 熔点/℃ 沸点/℃ 水溶性
(g·cm-3)
易水解生成难溶于水的物
TiCl -25 136 1.5
4
质,能溶于有机溶剂
CCl -25 76.8 1.6 难溶于水
4
请回答下列问题:
(1) 按 照 气 流 由 左 到 右 的 方 向 , 上 述 装 置 合 理 的 连 接 顺 序 为
a→______→______→f→g→______→______→d→e→j。(填仪器接口字母)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入试剂,
__________________________(按正确的顺序填入下列操作的序号)。
①关闭分液漏斗活塞 ②打开分液漏斗活塞
③停止加热,充分冷却 ④加热装置D中陶瓷管
(3)装置A中导管m的作用是_______________________________________。
(4)装置D中除生成TiCl 外,同时生成一种气态不成盐氧化物,该反应的化学方程式为
4
___________________________________________________________________________。
(5)设计实验证明装置E中收集到的液体中含有TiCl :
4
________________________________________________________________________
________________________________________________________________________。
(6)制得的 TiCl 中常含有少量 CCl ,从混合液体中分离出 TiCl 的操作名称为
4 4 4
_____________。
解析 (1)由于TiCl 易溶于水,所以参加反应的Cl 必须先干燥,而收集TiCl 的装置后
4 2 4
面必须有防止水蒸气进入的装置,则正确的连接顺序为a→c→b→f→g→h→i→d→e→j。
(2)为防止炭粉在高温下被氧化,防止装置内的水蒸气使TiCl 变质,所以应先通入Cl 一
4 2
段时间后再加热装置D,正确的操作顺序为②④③①。
(3)分液漏斗上连接的导管是为了平衡压强,使液体顺利流下。(4)装置D中的反应物为TiO、C和Cl,而生成物为TiCl 和CO,所以反应的化学方程式
2 2 4
为TiO+2C+2Cl=====TiCl +2CO。
2 2 4
(5)根据表中信息,TiCl 遇水生成难溶物,所以可取少量收集到的液体于洁净试管中,滴
4
加适量水,液体变浑浊,即证明收集到的液体中含有TiCl 。
4
(6)由于二者的沸点相差较大,所以可用蒸馏的方法分离TiCl 中含有的CCl 。
4 4
答案 (1)c b h i (2)②④③①
(3)平衡压强,使浓盐酸更易滴落
(4)TiO+2C+2Cl=====TiCl +2CO
2 2 4
(5)取少量收集到的液体于洁净试管中,滴加适量水,液体变浑浊,则收集到的液体中含
有TiCl (或其他合理答案也可)
4
(6)蒸馏