文档内容
第 26 讲 氨和铵盐
[复习目标] 1.掌握NH 及铵盐的性质与用途。2.掌握喷泉实验、NH 的实验室制法的原理
3 3
及操作。
考点一 氨
1.氨的分子结构和物理性质
电子式 密度 气味 水溶性
比空气的____ ______性气味 极易溶于水(1∶700)
思考 试从结构和性质上解释NH 极易溶于水的原因。
3
________________________________________________________________________
2.氨的化学性质
提醒 ①NH 是中学化学中唯一的碱性气体,能使湿润的红色石蕊试纸变蓝,可在推断题
3
中作为解题突破口。
②氨水呈碱性,NH ·H O属于一元弱碱,计算氨水的浓度时,溶质按NH 进行计算。
3 2 3
3.喷泉实验
如图为氨喷泉实验的装置(夹持装置均已略去)。
(1)用图1装置进行喷泉实验。①引发“喷泉”的方法是__________________________________________________
________________________________________________________________________。
②简述产生喷泉的原理: _________________________________________________
________________________________________________________________________。
(2)只使用图2所示装置进行喷泉实验。
①打开止水夹,水不能倒吸入烧瓶的原因是
________________________________________________________________________。
②如何引发图2装置的“喷泉”?
________________________________________________________________________。
(3)指出下面几种常见的能形成喷泉的气体的吸收剂。
CO、Cl、 NO、O NO 、O
2 2 2 2 2
气体 HCl NH NO
3 2
SO 、HS (4∶3) (4∶1)
2 2
水、
吸收剂
_______
4.喷泉实验产物的浓度计算
关键是确定所得溶液中溶质的物质的量和溶液的体积,标准状况下的气体进行喷泉实验后所
得溶液的物质的量浓度:
(1)HCl、NH 、NO 气体或它们与其他不溶于水的气体混合时,所得溶液的物质的量浓度为
3 2
mol·L-1。
(2)当是NO 和O 的混合气体且体积比为4∶1时,c(HNO)= mol·L-1。
2 2 3
1.液氨制冷、碘的升华、加热法分离NH Cl和NaCl都不涉及化学变化( )
4
2.现有1 mol·L-1的氨水,则该溶液中NH ·H O的浓度是1 mol·L-1( )
3 2
3.氨水具有弱碱性,说明氨水是弱电解质( )
4.浓氨水可检验氯气管道是否漏气( )
一、从“类别”和“价态”的视角理解NH 的性质
3
1.下列根据实验现象得出的结论不正确的是( )
A.将集有氨的试管倒扣于盛有水的水槽中,液体迅速充满试管,说明氨极易溶于水
B.将湿润的红色石蕊试纸放入集有氨的集气瓶中,试纸由红色变为蓝色,说明氨水呈碱性
C.将蘸有浓氨水和浓硝酸的玻璃棒靠近,观察到白烟,说明氨具有碱性且易与酸化合生成
铵盐
D.将红热的Pt丝伸入盛有浓氨水的锥形瓶中,瓶口出现少量红棕色气体,说明氨的直接氧
化产物为NO
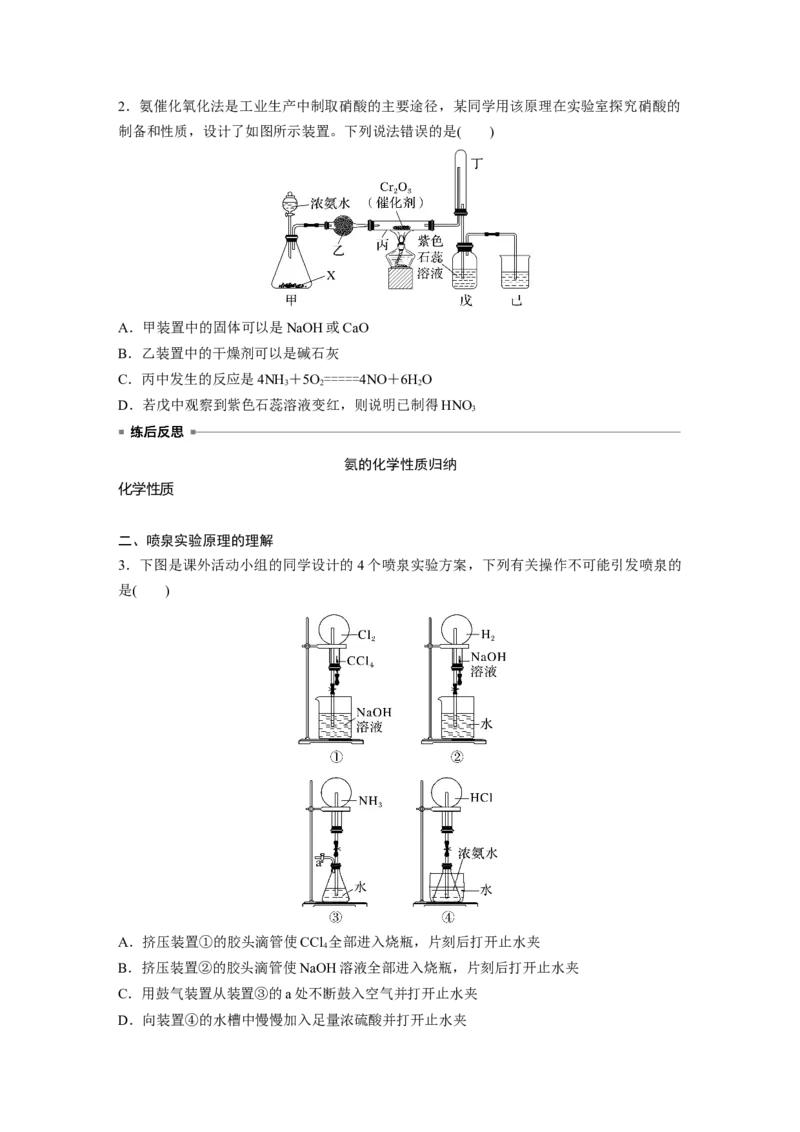
22.氨催化氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的
制备和性质,设计了如图所示装置。下列说法错误的是( )
A.甲装置中的固体可以是NaOH或CaO
B.乙装置中的干燥剂可以是碱石灰
C.丙中发生的反应是4NH +5O=====4NO+6HO
3 2 2
D.若戊中观察到紫色石蕊溶液变红,则说明已制得HNO
3
氨的化学性质归纳
化学性质
二、喷泉实验原理的理解
3.下图是课外活动小组的同学设计的4个喷泉实验方案,下列有关操作不可能引发喷泉的
是( )
A.挤压装置①的胶头滴管使CCl 全部进入烧瓶,片刻后打开止水夹
4
B.挤压装置②的胶头滴管使NaOH溶液全部进入烧瓶,片刻后打开止水夹
C.用鼓气装置从装置③的a处不断鼓入空气并打开止水夹
D.向装置④的水槽中慢慢加入足量浓硫酸并打开止水夹4.如图为化学教学中所用的喷泉实验装置。
某同学在烧瓶中盛不同成分的气体进行喷泉实验,请帮助分析实验后烧瓶中所得溶液的浓度。
(假设是在标准状况下完成实验,且溶质不扩散)
(1)若用HCl气体,则c(HCl)=_____________________________________________。
(2)若用NO 气体,则c(HNO)=___________________________________________。
2 3
(3)若用n(NO )∶n(O )=2∶1的混合气体,则c(HNO)=____________________。
2 2 3
考点二 铵盐、NH 的检验
1.铵盐及NH的检验
(1)铵盐的物理性质
铵盐大多数是____色固体,绝大多数易溶于水。
(2)铵盐的化学性质
(3)NH的检验步骤
未知液――――→产生使湿润的红色石蕊试纸变______的气体,则证明含NH
2.氨的实验室制法
(1)加热固态铵盐和碱的混合物
简易装置干燥 用________
①将湿润的红色石蕊试纸置于试管口,试纸变____;
验满
②将蘸有浓盐酸的玻璃棒置于试管口,有白烟产生
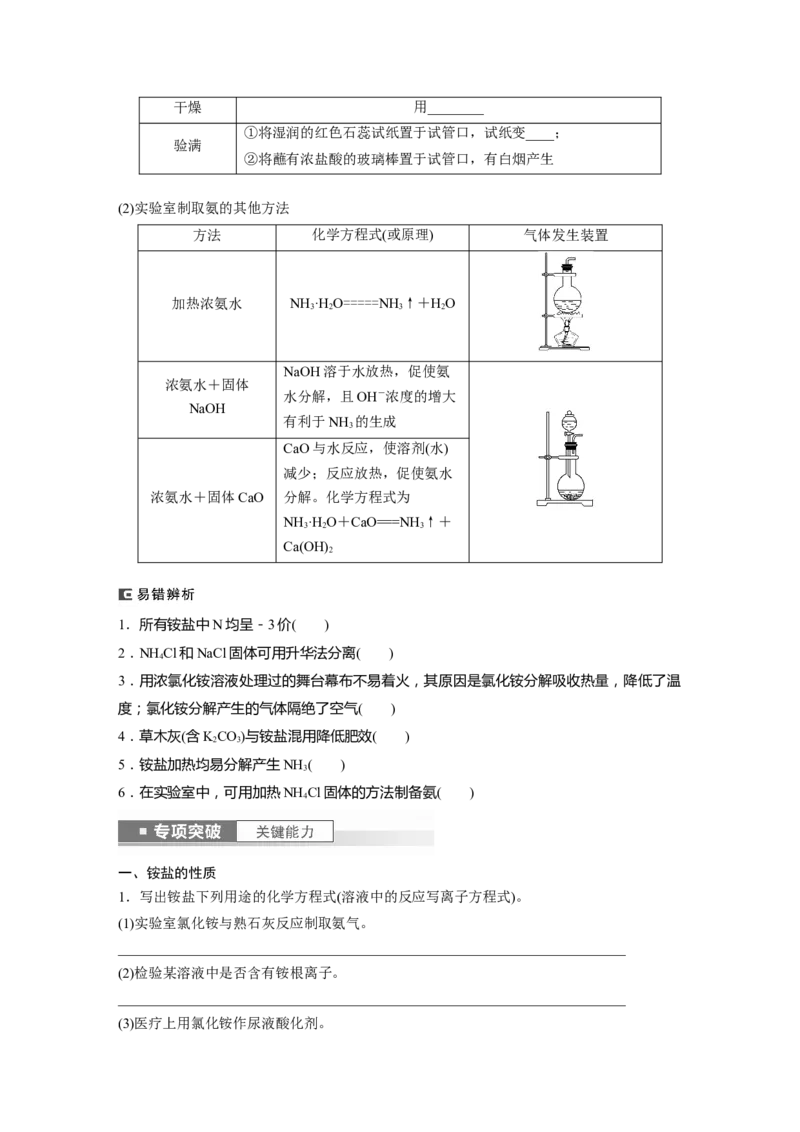
(2)实验室制取氨的其他方法
方法 化学方程式(或原理) 气体发生装置
加热浓氨水 NH ·H O=====NH ↑+HO
3 2 3 2
NaOH溶于水放热,促使氨
浓氨水+固体
水分解,且OH-浓度的增大
NaOH
有利于NH 的生成
3
CaO与水反应,使溶剂(水)
减少;反应放热,促使氨水
浓氨水+固体CaO 分解。化学方程式为
NH ·H O+CaO===NH ↑+
3 2 3
Ca(OH)
2
1.所有铵盐中N均呈-3价( )
2.NH Cl和NaCl固体可用升华法分离( )
4
3.用浓氯化铵溶液处理过的舞台幕布不易着火,其原因是氯化铵分解吸收热量,降低了温
度;氯化铵分解产生的气体隔绝了空气( )
4.草木灰(含KCO)与铵盐混用降低肥效( )
2 3
5.铵盐加热均易分解产生NH ( )
3
6.在实验室中,可用加热NH Cl固体的方法制备氨( )
4
一、铵盐的性质
1.写出铵盐下列用途的化学方程式(溶液中的反应写离子方程式)。
(1)实验室氯化铵与熟石灰反应制取氨气。
________________________________________________________________________
(2)检验某溶液中是否含有铵根离子。
________________________________________________________________________
(3)医疗上用氯化铵作尿液酸化剂。________________________________________________________________________
(4)硝酸铵用作炸药,分解产物均为空气的成分。
________________________________________________________________________
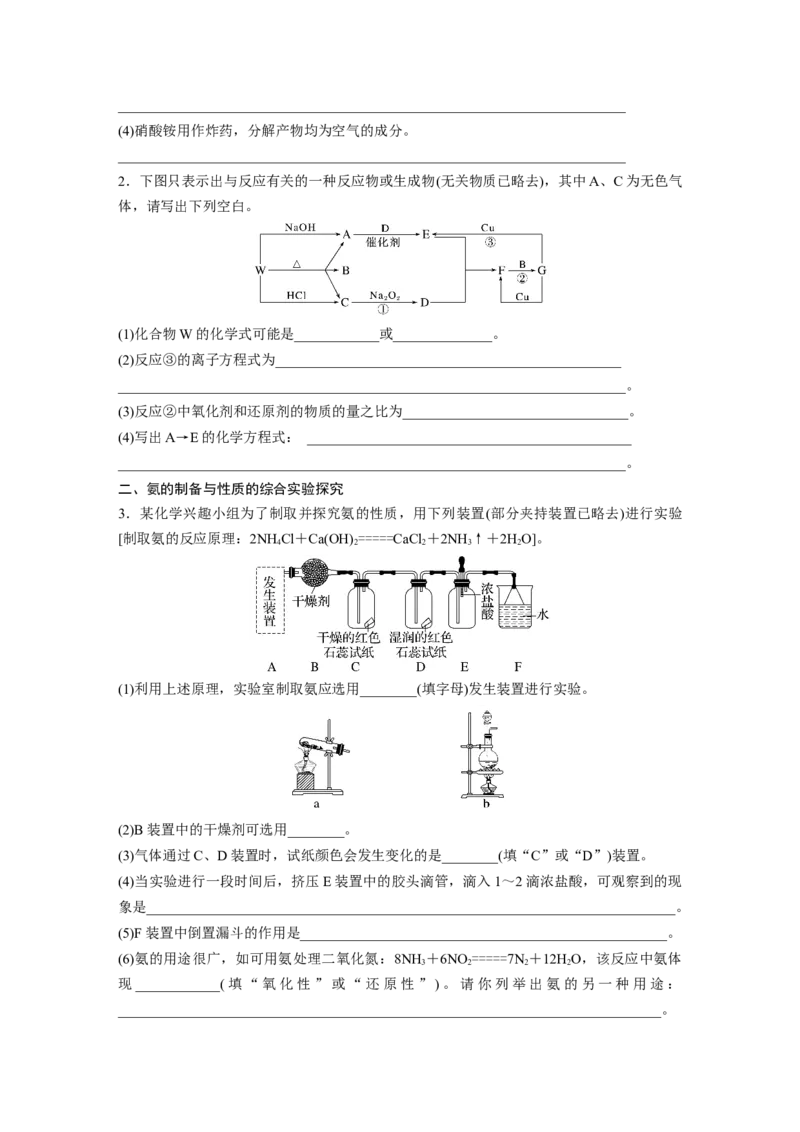
2.下图只表示出与反应有关的一种反应物或生成物(无关物质已略去),其中A、C为无色气
体,请写出下列空白。
(1)化合物W的化学式可能是____________或______________。
(2)反应③的离子方程式为_________________________________________________
________________________________________________________________________。
(3)反应②中氧化剂和还原剂的物质的量之比为________________________________。
(4)写出A→E的化学方程式: ______________________________________________
________________________________________________________________________。
二、氨的制备与性质的综合实验探究
3.某化学兴趣小组为了制取并探究氨的性质,用下列装置(部分夹持装置已略去)进行实验
[制取氨的反应原理:2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO]。
4 2 2 3 2
(1)利用上述原理,实验室制取氨应选用________(填字母)发生装置进行实验。
(2)B装置中的干燥剂可选用________。
(3)气体通过C、D装置时,试纸颜色会发生变化的是________(填“C”或“D”)装置。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现
象是___________________________________________________________________________。
(5)F装置中倒置漏斗的作用是____________________________________________________。
(6)氨的用途很广,如可用氨处理二氧化氮:8NH +6NO =====7N +12HO,该反应中氨体
3 2 2 2
现____________(填“氧化性”或“还原性”)。请你列举出氨的另一种用途:
_____________________________________________________________________________。1.正误判断,正确的打“√”,错误的打“×”。
(1)加热盛有少量NH HCO 固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变
4 3
蓝,说明NH HCO 显碱性(2017·全国卷Ⅱ,13B)( )
4 3
(2)用烧碱处理含高浓度NH的废水并回收利用氨(2017·天津,1D)( )
(3)NH HCO 受热易分解,因而可用作化肥(2019·江苏,3A)( )
4 3
(4)氨气使AlCl 溶液产生白色沉淀,反应中氨气被还原(2017·北京,8D)( )
3
2.(2021·江苏,7)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化生
2 3
产HNO;HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条
3 3
件下,N 与O 反应生成NO,NO进一步氧化生成NO 。2NO(g)+O(g)===2NO (g) ΔH=
2 2 2 2 2
-116.4 kJ·mol-1。大气中过量的NO 和水体中过量的NH、NO均是污染物。通过催化还原
x
的方法,可将烟气和机动车尾气中的NO转化为N ,也可将水体中的NO转化为N 。在指
2 2
定条件下,下列选项所示的物质间转化能实现的是( )
A.NO(g)HO,HNO (aq)
2 3
B.稀HNO(aq)Cu,NO(g)
3 2
C.NO(g)――→N(g)
2
D.NO(aq)O,N (g)
3 2
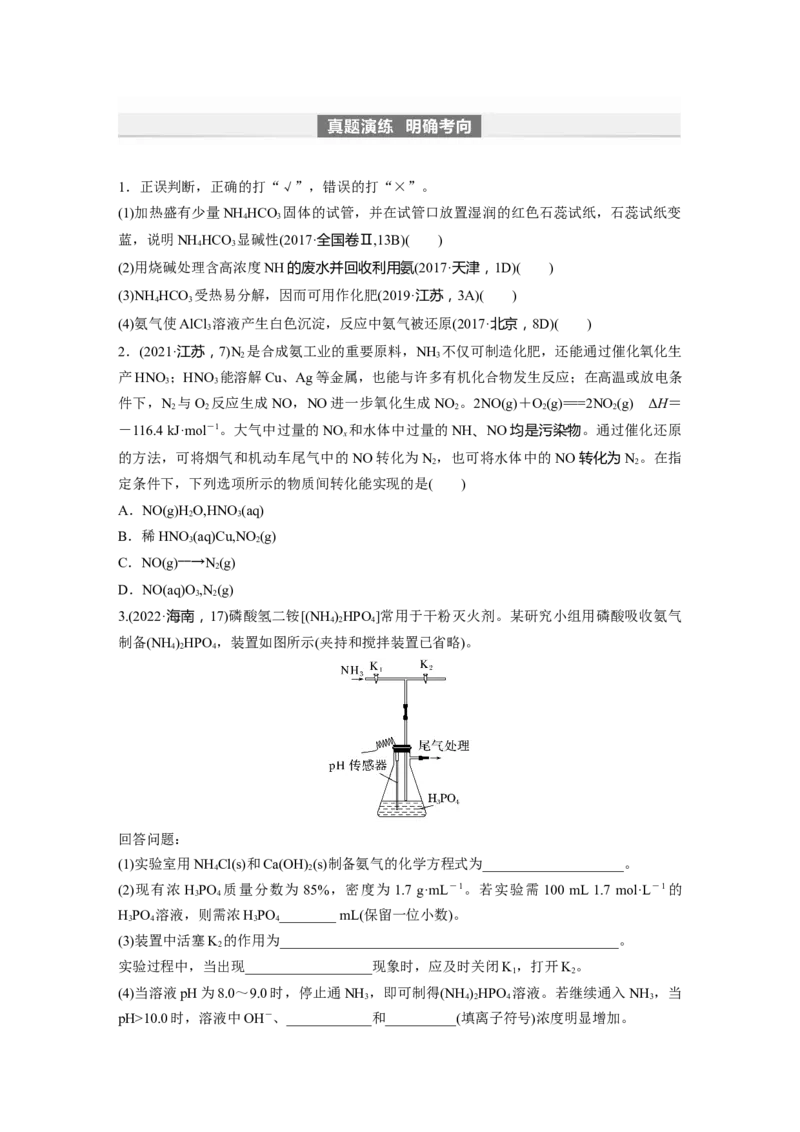
3.(2022·海南,17)磷酸氢二铵[(NH )HPO ]常用于干粉灭火剂。某研究小组用磷酸吸收氨气
4 2 4
制备(NH )HPO ,装置如图所示(夹持和搅拌装置已省略)。
4 2 4
回答问题:
(1)实验室用NH Cl(s)和Ca(OH) (s)制备氨气的化学方程式为____________________。
4 2
(2)现有浓 HPO 质量分数为 85%,密度为 1.7 g·mL-1。若实验需 100 mL 1.7 mol·L-1的
3 4
HPO 溶液,则需浓HPO ________ mL(保留一位小数)。
3 4 3 4
(3)装置中活塞K 的作用为________________________________________________。
2
实验过程中,当出现__________________现象时,应及时关闭K,打开K。
1 2
(4)当溶液pH为8.0~9.0时,停止通NH ,即可制得(NH )HPO 溶液。若继续通入NH ,当
3 4 2 4 3
pH>10.0时,溶液中OH-、____________和__________(填离子符号)浓度明显增加。(5)若本实验不选用 pH 传感器,还可选用______________作指示剂,当溶液颜色由
____________变为__________时,停止通NH 。
3