文档内容
训练(二十一) 氮及其重要化合物
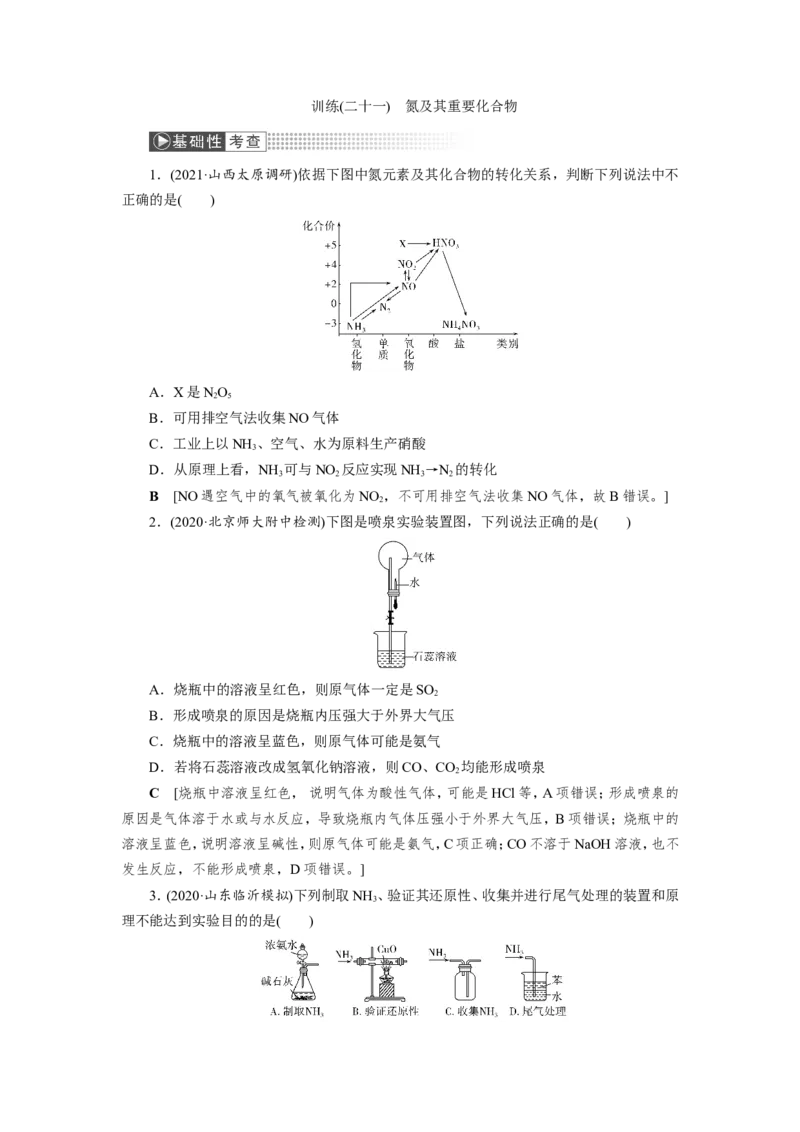
1.(2021·山西太原调研)依据下图中氮元素及其化合物的转化关系,判断下列说法中不
正确的是( )
A.X是NO
2 5
B.可用排空气法收集NO气体
C.工业上以NH 、空气、水为原料生产硝酸
3
D.从原理上看,NH 可与NO 反应实现NH →N 的转化
3 2 3 2
B [NO遇空气中的氧气被氧化为NO ,不可用排空气法收集NO气体,故B错误。]
2
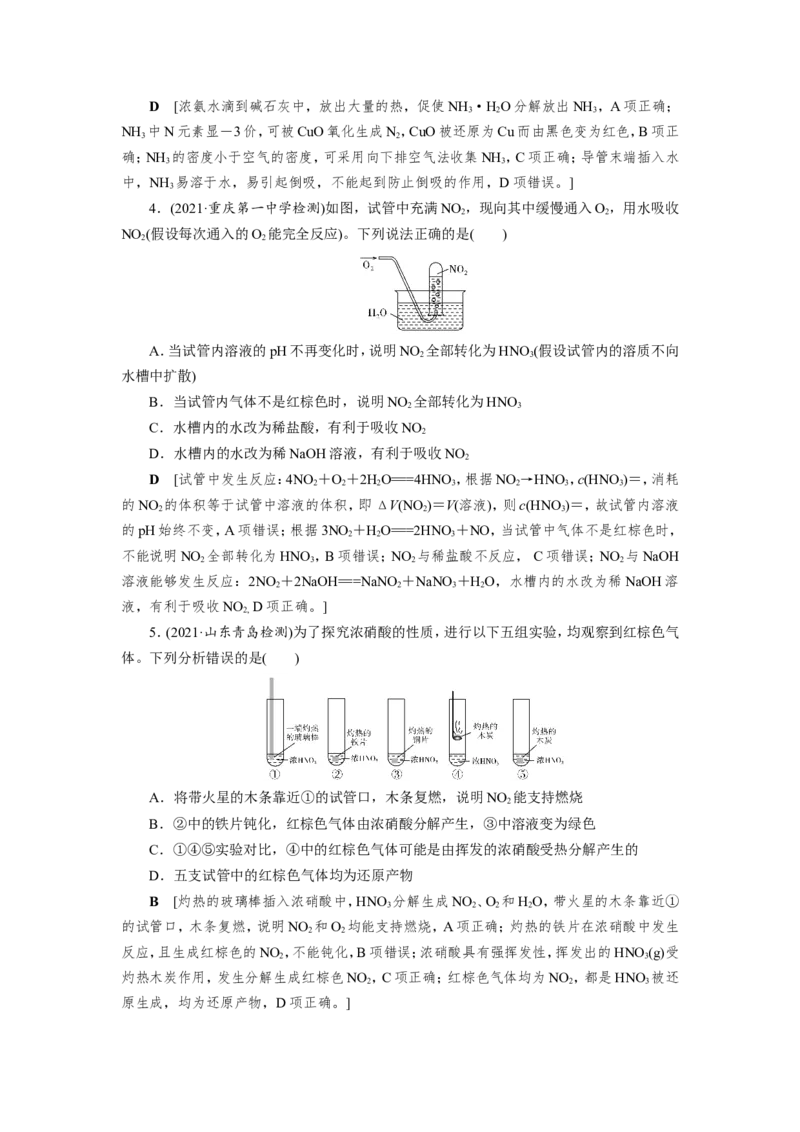
2.(2020·北京师大附中检测)下图是喷泉实验装置图,下列说法正确的是( )
A.烧瓶中的溶液呈红色,则原气体一定是SO
2
B.形成喷泉的原因是烧瓶内压强大于外界大气压
C.烧瓶中的溶液呈蓝色,则原气体可能是氨气
D.若将石蕊溶液改成氢氧化钠溶液,则CO、CO 均能形成喷泉
2
C [烧瓶中溶液呈红色, 说明气体为酸性气体,可能是HCl等,A项错误;形成喷泉的
原因是气体溶于水或与水反应,导致烧瓶内气体压强小于外界大气压,B项错误;烧瓶中的
溶液呈蓝色,说明溶液呈碱性,则原气体可能是氨气,C项正确;CO不溶于NaOH溶液,也不
发生反应,不能形成喷泉,D项错误。]
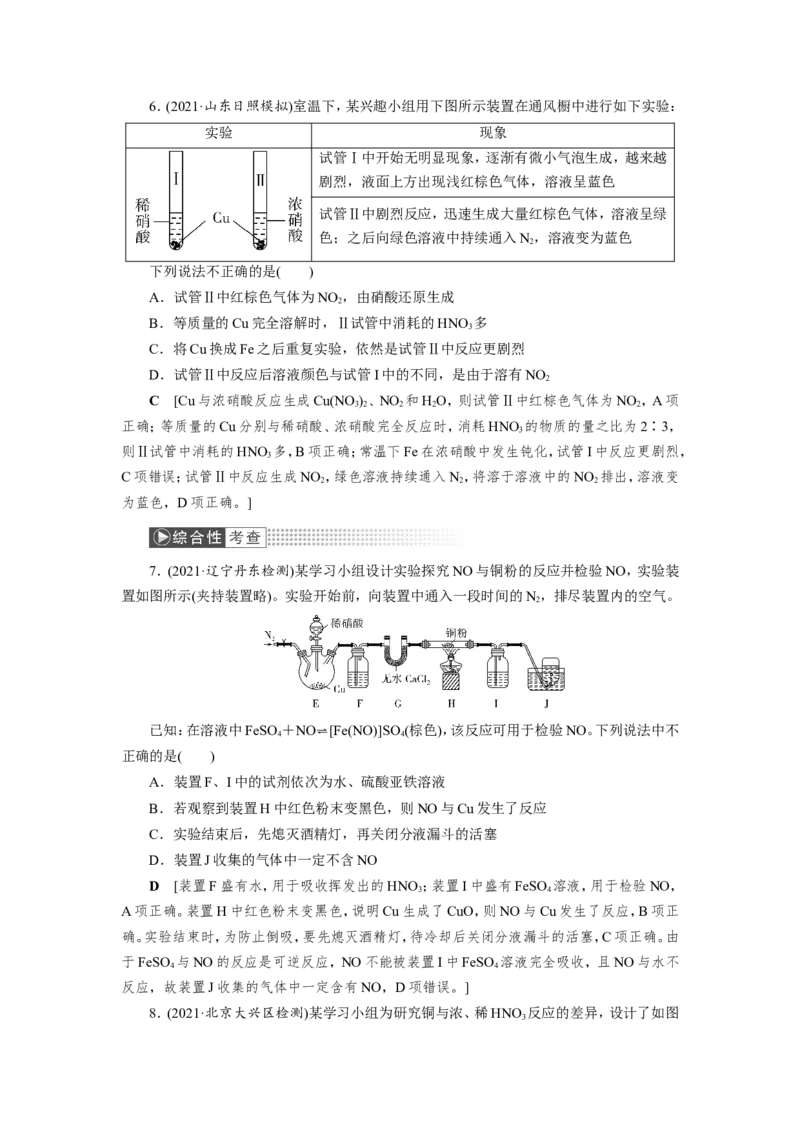
3.(2020·山东临沂模拟)下列制取NH 、验证其还原性、收集并进行尾气处理的装置和原
3
理不能达到实验目的的是( )D [浓氨水滴到碱石灰中,放出大量的热,促使NH ·HO分解放出NH ,A项正确;
3 2 3
NH 中N元素显-3价,可被CuO氧化生成N,CuO被还原为Cu而由黑色变为红色,B项正
3 2
确;NH 的密度小于空气的密度,可采用向下排空气法收集NH ,C项正确;导管末端插入水
3 3
中,NH 易溶于水,易引起倒吸,不能起到防止倒吸的作用,D项错误。]
3
4.(2021·重庆第一中学检测)如图,试管中充满NO ,现向其中缓慢通入O,用水吸收
2 2
NO (假设每次通入的O 能完全反应)。下列说法正确的是( )
2 2
A.当试管内溶液的pH不再变化时,说明NO 全部转化为HNO(假设试管内的溶质不向
2 3
水槽中扩散)
B.当试管内气体不是红棕色时,说明NO 全部转化为HNO
2 3
C.水槽内的水改为稀盐酸,有利于吸收NO
2
D.水槽内的水改为稀NaOH溶液,有利于吸收NO
2
D [试管中发生反应:4NO +O+2HO===4HNO ,根据NO →HNO,c(HNO)=,消耗
2 2 2 3 2 3 3
的NO 的体积等于试管中溶液的体积,即ΔV(NO )=V(溶液),则c(HNO)=,故试管内溶液
2 2 3
的pH始终不变,A项错误;根据3NO +HO===2HNO +NO,当试管中气体不是红棕色时,
2 2 3
不能说明NO 全部转化为HNO,B项错误;NO 与稀盐酸不反应, C项错误;NO 与NaOH
2 3 2 2
溶液能够发生反应:2NO +2NaOH===NaNO +NaNO +HO,水槽内的水改为稀NaOH溶
2 2 3 2
液,有利于吸收NO D项正确。]
2,
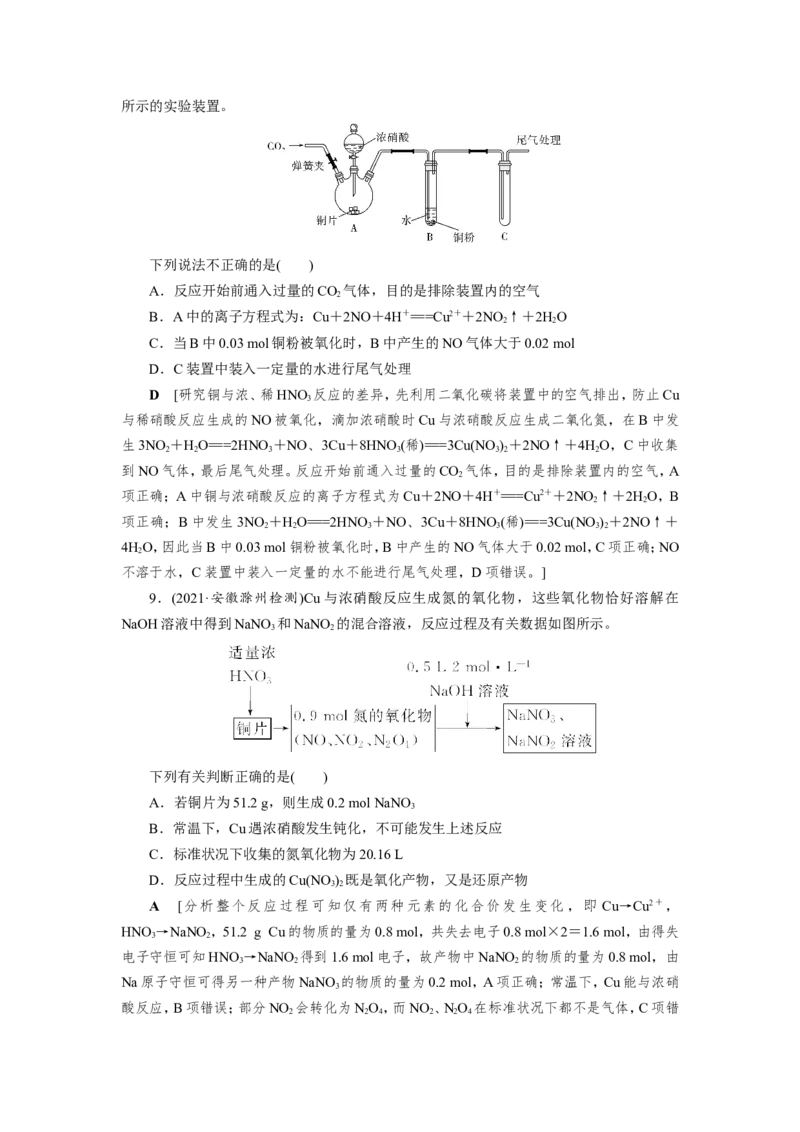
5.(2021·山东青岛检测)为了探究浓硝酸的性质,进行以下五组实验,均观察到红棕色气
体。下列分析错误的是( )
A.将带火星的木条靠近①的试管口,木条复燃,说明NO 能支持燃烧
2
B.②中的铁片钝化,红棕色气体由浓硝酸分解产生,③中溶液变为绿色
C.①④⑤实验对比,④中的红棕色气体可能是由挥发的浓硝酸受热分解产生的
D.五支试管中的红棕色气体均为还原产物
B [灼热的玻璃棒插入浓硝酸中,HNO 分解生成NO 、O 和HO,带火星的木条靠近①
3 2 2 2
的试管口,木条复燃,说明NO 和O 均能支持燃烧,A项正确;灼热的铁片在浓硝酸中发生
2 2
反应,且生成红棕色的NO ,不能钝化,B项错误;浓硝酸具有强挥发性,挥发出的HNO(g)受
2 3
灼热木炭作用,发生分解生成红棕色NO ,C项正确;红棕色气体均为NO ,都是HNO 被还
2 2 3
原生成,均为还原产物,D项正确。]6.(2021·山东日照模拟)室温下,某兴趣小组用下图所示装置在通风橱中进行如下实验:
实验 现象
试管Ⅰ中开始无明显现象,逐渐有微小气泡生成,越来越
剧烈,液面上方出现浅红棕色气体,溶液呈蓝色
试管Ⅱ中剧烈反应,迅速生成大量红棕色气体,溶液呈绿
色;之后向绿色溶液中持续通入N,溶液变为蓝色
2
下列说法不正确的是( )
A.试管Ⅱ中红棕色气体为NO ,由硝酸还原生成
2
B.等质量的Cu完全溶解时,Ⅱ试管中消耗的HNO 多
3
C.将Cu换成Fe之后重复实验,依然是试管Ⅱ中反应更剧烈
D.试管Ⅱ中反应后溶液颜色与试管I中的不同,是由于溶有NO
2
C [Cu与浓硝酸反应生成Cu(NO )、NO 和HO,则试管Ⅱ中红棕色气体为NO ,A项
3 2 2 2 2
正确;等质量的Cu分别与稀硝酸、浓硝酸完全反应时,消耗HNO 的物质的量之比为2∶3,
3
则Ⅱ试管中消耗的HNO 多,B项正确;常温下Fe在浓硝酸中发生钝化,试管I中反应更剧烈,
3
C项错误;试管Ⅱ中反应生成NO ,绿色溶液持续通入N,将溶于溶液中的NO 排出,溶液变
2 2 2
为蓝色,D项正确。]
7.(2021·辽宁丹东检测)某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装
置如图所示(夹持装置略)。实验开始前,向装置中通入一段时间的N,排尽装置内的空气。
2
已知:在溶液中FeSO
4
+NO⇌[Fe(NO)]SO
4
(棕色),该反应可用于检验NO。下列说法中不
正确的是( )
A.装置F、I中的试剂依次为水、硫酸亚铁溶液
B.若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应
C.实验结束后,先熄灭酒精灯,再关闭分液漏斗的活塞
D.装置J收集的气体中一定不含NO
D [装置F盛有水,用于吸收挥发出的HNO;装置I中盛有FeSO 溶液,用于检验NO,
3 4
A项正确。装置H中红色粉末变黑色,说明Cu生成了CuO,则NO与Cu发生了反应,B项正
确。实验结束时,为防止倒吸,要先熄灭酒精灯,待冷却后关闭分液漏斗的活塞,C项正确。由
于FeSO 与NO的反应是可逆反应,NO不能被装置I中FeSO 溶液完全吸收,且NO与水不
4 4
反应,故装置J收集的气体中一定含有NO,D项错误。]
8.(2021·北京大兴区检测)某学习小组为研究铜与浓、稀HNO 反应的差异,设计了如图
3所示的实验装置。
下列说法不正确的是( )
A.反应开始前通入过量的CO 气体,目的是排除装置内的空气
2
B.A中的离子方程式为:Cu+2NO+4H+===Cu2++2NO ↑+2HO
2 2
C.当B中0.03 mol铜粉被氧化时,B中产生的NO气体大于0.02 mol
D.C装置中装入一定量的水进行尾气处理
D [研究铜与浓、稀HNO 反应的差异,先利用二氧化碳将装置中的空气排出,防止Cu
3
与稀硝酸反应生成的NO被氧化,滴加浓硝酸时Cu与浓硝酸反应生成二氧化氮,在B中发
生3NO +HO===2HNO +NO、3Cu+8HNO(稀)===3Cu(NO) +2NO↑+4HO,C中收集
2 2 3 3 3 2 2
到NO气体,最后尾气处理。反应开始前通入过量的CO 气体,目的是排除装置内的空气,A
2
项正确;A中铜与浓硝酸反应的离子方程式为Cu+2NO+4H+===Cu2++2NO ↑+2HO,B
2 2
项正确;B中发生3NO +HO===2HNO +NO、3Cu+8HNO(稀)===3Cu(NO) +2NO↑+
2 2 3 3 3 2
4HO,因此当B中0.03 mol铜粉被氧化时,B中产生的NO气体大于0.02 mol,C项正确;NO
2
不溶于水,C装置中装入一定量的水不能进行尾气处理,D项错误。]
9.(2021·安徽滁州检测)Cu与浓硝酸反应生成氮的氧化物,这些氧化物恰好溶解在
NaOH溶液中得到NaNO 和NaNO 的混合溶液,反应过程及有关数据如图所示。
3 2
下列有关判断正确的是( )
A.若铜片为51.2 g,则生成0.2 mol NaNO
3
B.常温下,Cu遇浓硝酸发生钝化,不可能发生上述反应
C.标准状况下收集的氮氧化物为20.16 L
D.反应过程中生成的Cu(NO ) 既是氧化产物,又是还原产物
3 2
A [分析整个反应过程可知仅有两种元素的化合价发生变化,即 Cu→Cu2+,
HNO→NaNO ,51.2 g Cu的物质的量为0.8 mol,共失去电子0.8 mol×2=1.6 mol,由得失
3 2
电子守恒可知HNO→NaNO 得到1.6 mol电子,故产物中NaNO 的物质的量为0.8 mol,由
3 2 2
Na原子守恒可得另一种产物NaNO 的物质的量为0.2 mol,A项正确;常温下,Cu能与浓硝
3
酸反应,B项错误;部分NO 会转化为NO,而NO 、NO 在标准状况下都不是气体,C项错
2 2 4 2 2 4误;反应过程中生成的Cu(NO ) 是氧化产物,不是还原产物,D项错误。]
3 2
10.(2021·黑龙江大庆检测)Zn与硝酸反应时,硝酸溶液的浓度不同,产物也不同。与不
同浓度硝酸反应时,反应的Zn与被还原硝酸的物质的量关系如图。还原产物为NH NO 的曲
4 3
线是( )
A [生成1 mol NH NO 时,HNO 得到8 mol电子,据得失电子守恒可知,反应要消耗4
4 3 3
mol Zn,必然生成4 mol Zn(NO ),故生成NH NO 时,消耗Zn和被还原的HNO 的物质的量
3 2 4 3 3
之比为4 mol∶1 mol=4∶1。]
11.(2019·江苏卷,节选)NO、NO和NO 等氮氧化物是空气污染物,含有氮氧化物的尾
2 2
气需处理后才能排放。
(1)NO和NO 的处理。已除去NO的硝酸尾气可用NaOH溶液吸收,主要反应为:
2 2
NO+NO +2OH-===2NO+HO
2 2
2NO +2OH-===NO+NO+HO
2 2
①下列措施能提高尾气中NO和NO 去除率的有________(填字母)。
2
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO 晶体,该晶体中的主要杂质是
2
________(填化学式);吸收后排放的尾气中含量较高的氮氧化物是________(填化学式)。
(2)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条
件相同,NO转化为NO的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性 NaClO 溶液中,HClO 氧化 NO 生成 Cl-和 NO,其离子方程式为
________________________________________________________________________。
② NaClO 溶 液 的 初 始 pH 越 小 , NO 转 化 率 越 高 。 其 原 因 是
________________________________________________________________________。解析 (1)①根据化学平衡的影响因素,为提高尾气中NO和NO 的去除率,采用气、液
2
逆流的方式吸收尾气可保证尾气更充分地吸收,吸收尾气过程中定期补加适量NaOH溶液,
可提高尾气的转化率。
②由尾气吸收的主要反应NO+NO +2OH-===2NO+HO、2NO +2OH-===NO+NO
2 2 2
+HO可知,吸收后的溶液经浓缩、结晶、过滤,得到NaNO 晶体,该晶体中含有的杂质为
2 2
NaNO ;NO不溶于水也不与水反应,吸收后排放的尾气中含量较高的氮氧化物是NO。
3
(2)①根据题目信息在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO,利用电子守恒
法可配平反应的离子方程式:3HClO+2NO+HO===3Cl-+2NO+5H+。
2
②在酸性条件下,ClO-转化成HClO,溶液的pH越小,生成的HClO浓度越大,HClO的
氧化性越强,则NO转化率越高。
答案 (1)①BC ②NaNO NO
3
(2)①3HClO+2NO+HO===3Cl-+2NO+5H+
2
②溶液pH越小,溶液中HClO的浓度越大,氧化NO的能力越强
12.(2021·云南昆明调研)某校化学研究性学习小组设计实验验证NH 能还原CuO,并对
3
还原产物进行探究。
请回答下列问题:
Ⅰ.验证NH 能还原CuO
3
(1)试剂X为________________。
(2)请将提供的装置按合理顺序连接:g→_________________________________。
(3)装置B的作用是__________________________________________。
(4)证明NH 能还原CuO的实验现象是_______________________________。
3
Ⅱ.探究还原产物的成分
[查阅资料] Cu O粉末呈红色,在酸性溶液中不稳定:Cu O+HSO (稀)===Cu+CuSO
2 2 2 4 4
+HO。
2
[实验探究]
实验操作 实验现象 实验结论
(5)证明红色固体为______(填
若无现象
取10.4 g红色固体于烧杯中, 名称,下同)
加入足量稀硫酸,充分搅拌, (6)证明红色固体肯定含有
若溶液
静置 __________,可能含有
变蓝
____________(7)经计算,红色固体的成分
取上述反应后的混合物过滤、
及其物质的量为
洗涤、干燥、称重,得固体6.4
_________________________
g
_________________________
解析 (1)氯化铵和氢氧化钙反应生成氯化钙、氨气和水,试剂X用于干燥氨气且不与氨
气反应,则为碱石灰。
(2)装置C生成氨气后,首先经过E干燥,再通入A中反应,生成的气体通过D进行检测,
最后用B装置吸收尾气。所以连接顺序为g→f→h→a→b→d→e→c。
(3)氨气极易溶于水,吸收氨气时一定要考虑防止倒吸,B装置中,氨气通入后先与CCl
4
接触,并不溶于CCl ,会溶于上层的水,可以防止倒吸;B装置前连接D装置,其用于检验A
4
装置中是否产生水,则不能让空气中的水蒸气进入D装置,所以B装置还可以隔绝空气,防
止空气中的水蒸气进入D装置中。
(4)A中黑色粉末变为红色能证明CuO与NH 反应生成了Cu或Cu O,D中白色固体变
3 2
为蓝色能证明CuO与NH 反应生成了HO。
3 2
(5)向红色固体中加入稀硫酸无现象,说明红色固体为Cu,其不与稀HSO 反应。
2 4
(6)有CuSO 生成,溶液变蓝,则红色固体中肯定含有Cu O,不能确定是否含有Cu。
4 2
(7)所得固体为Cu,物质的量为0.1 mol;由反应前红色固体质量为10.4 g,反应后得固体
质量为6.4 g,可知红色固体中一定有Cu O,Cu O的物质的量可根据发生反应的化学方程式
2 2
列式进行计算:
Cu O+2H+===Cu2++Cu+HO Δm
2 2
1 mol 1 mol 80 g
0.05 mol 0.05 mol 4 g
则原固体中还含有0.05 mol Cu。红色固体的成分及其物质的量:铜和氧化亚铜各 0.05
mol。
答案 (1)碱石灰 (2)f→h→a→b→d→e→c
(3)吸收尾气,防止倒吸,隔绝空气,防止空气中的水蒸气进入D中
(4)A中黑色粉末变为红色,D中白色固体变为蓝色
(5)铜 (6)氧化亚铜 铜 (7)铜和氧化亚铜各0.05 mol