文档内容
第5课时 关键能力——水溶液中微粒浓度的关系
水溶液中微粒浓度的关系是高考命题的热点和重点,主要在选择题中结合酸碱中和滴
定曲线呈现,考查溶液中微粒浓度的大小关系和等量关系,考查考生运用知识、能力和素养
解决实际问题的能力,突出考查考生对“平衡观念”和“守恒思想”的理解及运用,体现
《中国高考评价体系》中对于阅读理解能力、信息搜索能力、信息整理能力、抽象思维能力、演
绎推理能力、辩证思维能力等关键能力的要求,要求考生能够从多个视角观察、思考同一个
问题;能够灵活地运用不同方法,发散地、逆向地解决问题;能够通过敏锐的洞察能力,发现
复杂、新颖情境中的关键事实特征,将所学知识迁移到新情境,解决新问题。
一、熟悉两大理论,构建思维基点
1.电离理论
(1)弱电解质的电离是微弱的,电离产生的微粒都非常少,同时还要考虑水的电离,如氨
水溶液中:NH ·H O、NH、OH-浓度的大小关系是c(NH ·H O)>c(OH-)>c(NH)。
3 2 3 2
(2)多元弱酸的电离是分步进行的,其主要是第一步电离(第一步电离程度远大于第二步
电离)。如在HS溶液中:HS、HS-、S2-、H+的浓度大小关系是c(H S)>c(H+)>c(HS-)>c(S2-)。
2 2 2
2.水解理论
(1)弱电解质离子的水解损失是微量的(双水解除外),但由于水的电离,故水解后酸性溶
液中c(H+)或碱性溶液中c(OH-)总是大于水解产生的弱电解质的浓度。如NH Cl溶液中:
4
NH、Cl-、NH ·H O、H+的浓度大小关系是c(Cl-)>c(NH)>c(H+)>c(NH ·H O)。
3 2 3 2
(2)多元弱酸酸根离子的水解是分步进行的,其主要是第一步水解,如在NaCO 溶液中:
2 3
CO、HCO、HCO 的浓度大小关系应是c(CO)>c(HCO)>c(H CO)。
2 3 2 3
二、把握三种守恒,明确等量关系
1.电荷守恒
电解质溶液中,无论存在多少种离子,溶液都是呈电中性,即阴离子所带负电荷总数一
定等于阳离子所带正电荷总数。如NaHCO 溶液中存在着Na+、H+、HCO、CO、OH-,存在如
3
下关系:c(Na+)+c(H+)=c(HCO)+c(OH-)+2c(CO)。
2.物料守恒(原子守恒)
电解质溶液中,由于某些离子能够水解,离子种类增多,但元素总是守恒的。如KS溶液
2
中S2-、HS-都能水解,故S元素以S2-、HS-、HS三种形式存在,它们之间有如下守恒关系:
2
c(K+)=2c(S2-)+2c(HS-)+2c(H S)。
23.质子守恒
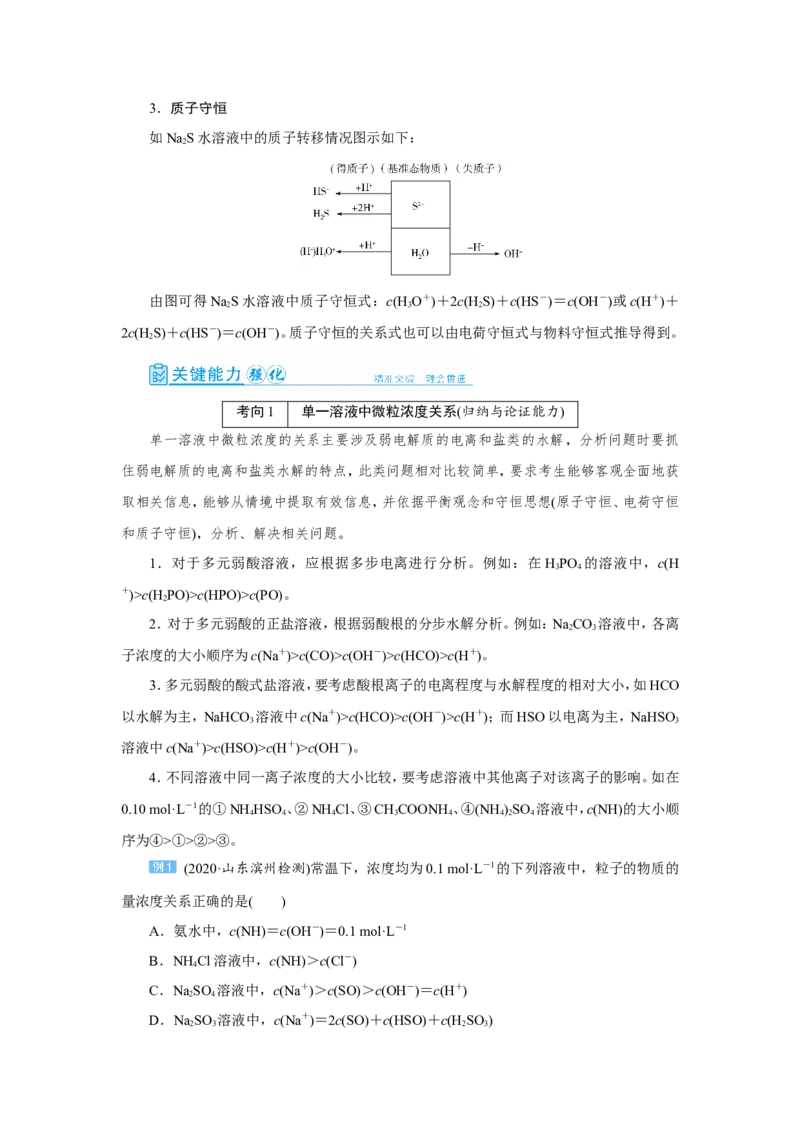
如NaS水溶液中的质子转移情况图示如下:
2
由图可得NaS水溶液中质子守恒式:c(H O+)+2c(H S)+c(HS-)=c(OH-)或c(H+)+
2 3 2
2c(H S)+c(HS-)=c(OH-)。质子守恒的关系式也可以由电荷守恒式与物料守恒式推导得到。
2
考向1 单一溶液中微粒浓度关系(归纳与论证能力)
单一溶液中微粒浓度的关系主要涉及弱电解质的电离和盐类的水解,分析问题时要抓
住弱电解质的电离和盐类水解的特点,此类问题相对比较简单,要求考生能够客观全面地获
取相关信息,能够从情境中提取有效信息,并依据平衡观念和守恒思想(原子守恒、电荷守恒
和质子守恒),分析、解决相关问题。
1.对于多元弱酸溶液,应根据多步电离进行分析。例如:在 HPO 的溶液中,c(H
3 4
+)>c(HPO)>c(HPO)>c(PO)。
2
2.对于多元弱酸的正盐溶液,根据弱酸根的分步水解分析。例如:NaCO 溶液中,各离
2 3
子浓度的大小顺序为c(Na+)>c(CO)>c(OH-)>c(HCO)>c(H+)。
3.多元弱酸的酸式盐溶液,要考虑酸根离子的电离程度与水解程度的相对大小,如HCO
以水解为主,NaHCO 溶液中c(Na+)>c(HCO)>c(OH-)>c(H+);而HSO以电离为主,NaHSO
3 3
溶液中c(Na+)>c(HSO)>c(H+)>c(OH-)。
4.不同溶液中同一离子浓度的大小比较,要考虑溶液中其他离子对该离子的影响。如在
0.10 mol·L-1的①NH HSO 、②NH Cl、③CHCOONH、④(NH )SO 溶液中,c(NH)的大小顺
4 4 4 3 4 4 2 4
序为④>①>②>③。
(2020·山东滨州检测)常温下,浓度均为0.1 mol·L-1的下列溶液中,粒子的物质的
量浓度关系正确的是( )
A.氨水中,c(NH)=c(OH-)=0.1 mol·L-1
B.NH Cl溶液中,c(NH)>c(Cl-)
4
C.NaSO 溶液中,c(Na+)>c(SO)>c(OH-)=c(H+)
2 4
D.NaSO 溶液中,c(Na+)=2c(SO)+c(HSO)+c(H SO )
2 3 2 3C [氨水为弱碱溶液,NH ·HO只能部分电离出OH-,结合电荷守恒c(NH)+c(H+)=
3 2
c(OH-)可得:c(NH)<c(OH-)<0.1 mol·L-1,A项错误;NH Cl溶液中,NH部分水解,Cl-浓度
4
不变,则溶液中c(NH)<c(Cl-),B项错误;NaSO 溶液显中性,c(OH-)=c(H+),结合电荷守
2 4
恒可得:c(Na+)=2c(SO),溶液中离子浓度大小为c(Na+)>c(SO)>c(OH-)=c(H+),C项正确;
根据NaSO 溶液中的物料守恒可得:c(Na+)=2c(SO)+2c(HSO)+2c(H SO ),D项错误。]
2 3 2 3
[强化1] (2021·河北廊坊联考)常温下,下列溶液中有关微粒的物质的量浓度关系正确的
是( )
A.pH=8的CHCOONa溶液:c(CHCOOH)=9.9×10-7 mol·L-1
3 3
B.0.1 mol·L-1NaSO 溶液:c(Na+)+c(H+)=c(SO)+c(HSO)+c(OH-)
2 3
C.0.1 mol·L-1NaHCO 溶液:c(Na+)+c(OH-)=c(HCO)+c(H CO)+c(H+)
3 2 3
D.0.1 mol·L-1CHCOONa溶液中通入HCl至溶液pH=7:c(Na+)>c(CHCOOH)>c(Cl
3 3
-)
A [CHCOONa溶液中存在水解平衡:CHCOO-+HOCHCOOH+OH-,据物料守
3 3 2 3
恒可得:c(Na+)=c(CHCOOH)+c(CHCOO-);据电荷守恒可得:c(Na+)+c(H+)=c(CHCOO
3 3 3
-)+c(OH-),则有c(CHCOOH)=c(Na+)-c(CHCOO-)=c(OH-)-c(H+)=10-6 mol·L-1-
3 3
10-8 mol·L-1=9.9×10-7 mol·L-1,A正确;NaSO 溶液中,据电荷守恒可得:c(Na+)+c(H
2 3
+)=c(HSO)+2c(SO)+c(OH-),B错误;NaHCO 溶液中,据物料守恒可得:c(Na+)=c(HCO)
3
+c(CO)+c(H CO);据电荷守恒可得:c(Na+)+c(H+)=c(HCO)+2c(CO)+c(OH-),联立两
2 3
式可得:c(Na+)+c(OH-)=c(HCO)+2c(H CO)+c(H+),C错误;CHCOONa溶液中通入HCl
2 3 3至溶液pH=7,溶液呈中性,结合电荷守恒推知:c(Na+)=c(CHCOO-)+c(Cl-);据物料守恒
3
推知:c(Na+)=c(CHCOOH)+c(CHCOO-),综合可得:c(Cl-)=c(CHCOOH),D错误。]
3 3 3
[强化2] (2021·湖南衡阳八中检测)室温下,下列溶液中粒子浓度关系正确的是( )
A.NaS溶液:c(Na+)>c(HS-)>c(OH-)>c(H S)
2 2
B.NaC O 溶液:c(OH-)=c(H+)+c(HC O)+2c(H C O)
2 2 4 2 2 2 4
C.NaCO 溶液:c(Na+)+c(H+)=2c(CO)+c(OH-)
2 3
D.CHCOONa和CaCl 混合溶液:c(Na+)+c(Ca2+)=c(CHCOO-)+c(CHCOOH)+
3 2 3 3
2c(Cl-)
B [由质子守恒可知,NaS溶液中c(OH-)=c(H+)+c(HS-)+2c(HS),c(OH-)>c(HS
2 2
-),A项错误;同理,NaCO 溶液中c(OH-)=c(H+)+c(HCO)+2c(HCO),B项正确;NaCO 溶
2 2 4 2 2 2 4 2 3
液中的电荷守恒关系式为c(Na+)+c(H+)=c(OH-)+c(HCO)+2c(CO),C项错误;CHCOONa
3
和CaCl 混合溶液,根据物料守恒关系:c(CHCOO-)+c(CHCOOH)=c(Na+),c(Cl-)=2c(Ca2
2 3 3
+),即正确的关系式为c(Na+)+2c(Ca2+)=c(CHCOO-)+c(CHCOOH)+c(Cl-),D项错误。]
3 3
考向2 混合溶液中微粒浓度关系(归纳与论证能力)
分析混合溶液中微粒浓度的关系,首先考虑两溶液是否反应,若不反应,分析盐的水解
程度和酸(碱)的电离程度的大小;若能反应,则按反应后混合组成综合考虑水解和电离两种
因素。此类问题较为复杂,要求考生依据平衡观念和守恒思想(原子守恒、电荷守恒和质子守
恒),分析、解决相关问题。分析混合溶液中微粒浓度关系的思路如下:
1.弱电解质的电离程度大于相应离子的水解程度
例如,等物质的量浓度的NH Cl与NH ·H O混合溶液,c(NH)>c(Cl-)>c(OH-)>c(H+);等
4 3 2
物质的量浓度的CHCOONa与CHCOOH混合溶液,c(CHCOO-)>c(Na+)>c(H+)>c(OH-)。
3 3 3
2.弱电解质的电离程度小于相应离子的水解程度
例如,在0.1 mol·L-1的NaCN和0.1 mol·L-1的HCN溶液的混合液中,各离子浓度的大
小顺序为c(Na+)>c(CN-)>c(OH-)>c(H+)。
(2020.7·浙江选考)常温下,用0.1 mol·L-1氨水滴定10 mL浓度均为0.1 mol·L-1的
HCl和CHCOOH的混合液,下列说法不正确的是( )
3
A.在氨水滴定前,HCl和CHCOOH的混合液中c(Cl-)>c(CHCOO-)
3 3B.当滴入氨水10 mL时,c(NH)+c(NH ·H O)=c(CHCOO-)+c(CHCOOH)
3 2 3 3
C.当滴入氨水20 mL时,c(CHCOOH)+c(H+)=c(NH ·H O)+c(OH-)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20 mL,c(NH)<c(Cl-)
D [HCl是强酸,CHCOOH是弱酸,浓度均为0.1 mol·L-1时,c(Cl-)>c(CHCOO-),A
3 3
正确;滴入10 mL氨水时,加入的NH ·HO和CHCOOH的物质的量相等,据物料守恒可得
3 2 3
c(NH)+c(NH ·HO)=c(CHCOO-)+c(CHCOOH),B正确;滴入20 mL氨水时,恰好完全
3 2 3 3
反应,所得溶液为等浓度的NH Cl和CHCOONH 的混合溶液,据离子电荷守恒可得c(NH)
4 3 4
+c(H+)=c(Cl-)+c(CHCOO-)+c(OH-),据物料守恒可得 c(NH)+c(NH ·HO)=
3 3 2
c(CHCOOH)+c(CHCOO-)+c(Cl-),联立两式可得c(CHCOOH)+c(H+)=c(NH ·HO)+
3 3 3 3 2
c(OH-),C正确;滴入20 mL氨水时,所得混合液呈酸性,若溶液呈中性,氨水滴入量要大于
20 mL,结合电荷守恒关系c(NH)+c(H+)=c(Cl-)+c(CHCOO-)+c(OH-),溶液呈中性时,
3
c(H+)=c(OH-),得c(NH)=c(Cl-)+c(CHCOO-),则有c(NH)>c(Cl-),D错误。]
3
[强化 3] (2021·湖北武汉联考)25 ℃时,在 10 mL 浓度均为 0.1 mol·L-1 NaOH 和
NH ·H O混合溶液中,滴加0.1 mol·L-1的盐酸。下列有关溶液中粒子浓度关系正确的是(
3 2
)
A.未加盐酸时:c(OH-)>c(Na+)=c(NH ·H O)
3 2
B.加入10 mL盐酸时:c(NH)+c(H+)=c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
D.加入20 mL盐酸时:c(Cl-)=c(NH)+c(Na+)B [未加盐酸时,NaOH和NH ·H O混合溶液中,NaOH完全电离,NH ·H O部分电离,
3 2 3 2
则粒子浓度关系为c(OH-)>c(Na+)>c(NH ·H O),A项错误;加入10 mL盐酸时,根据电荷
3 2
守恒可得c(NH)+c(H+)+c(Na+)=c(OH-)+c(Cl-),由于NaCl不发生水解,则有c(Cl-)=
c(Na+),从而可得c(NH)+c(H+)=c(OH-),B项正确;加入盐酸至溶液pH=7时,溶液呈中性,
则有c(H+)=c(OH-);根据电荷守恒可得c(NH)+c(Na+)=c(Cl-),C项错误;加入20 mL盐
酸时,恰好完全反应生成NaCl和NH Cl,由于NH发生水解而使溶液呈酸性,则有c(H+)>
4
c(OH-);根据电荷守恒可得c(NH)+c(H+)+c(Na+)=c(OH-)+c(Cl-),从而可得c(Cl-)>
c(NH)+c(Na+),D项错误。]
考向3 以酸碱滴定图像为载体的微粒浓度关系
以酸碱滴定图像为载体的微粒浓度关系是高考命题的热点,涉及图像主要有pH~V(酸)
或V(碱)图像、分布系数图像等,要求考生从图像中准确获得有效信息,运用抽象与联想、归
纳与概括、推演与计算模型与建模等思维方法来组织、调动相关的知识与能力,解决酸碱中
和滴定中微粒浓度大小比较和等量关系确定的各种问题。
1.酸碱中和滴定图像
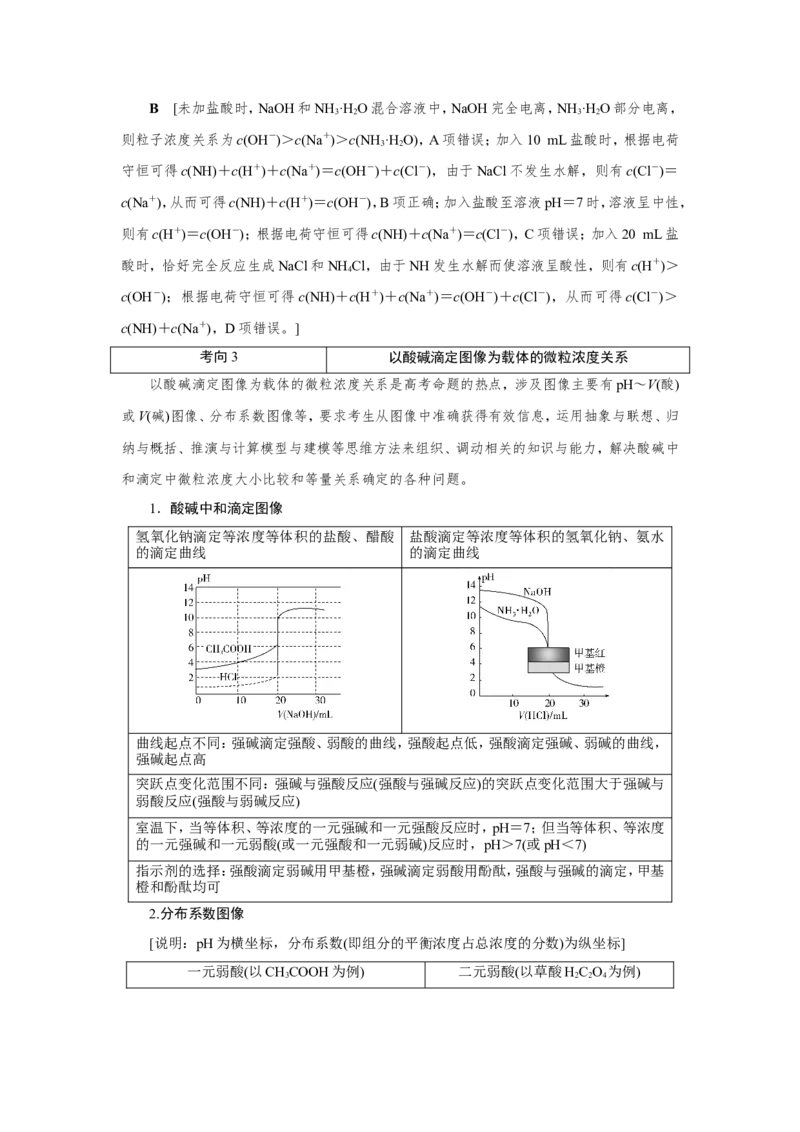
氢氧化钠滴定等浓度等体积的盐酸、醋酸 盐酸滴定等浓度等体积的氢氧化钠、氨水
的滴定曲线 的滴定曲线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低,强酸滴定强碱、弱碱的曲线,
强碱起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围大于强碱与
弱酸反应(强酸与弱碱反应)
室温下,当等体积、等浓度的一元强碱和一元强酸反应时,pH=7;但当等体积、等浓度
的一元强碱和一元弱酸(或一元强酸和一元弱碱)反应时,pH>7(或pH<7)
指示剂的选择:强酸滴定弱碱用甲基橙,强碱滴定弱酸用酚酞,强酸与强碱的滴定,甲基
橙和酚酞均可
2.分布系数图像
[说明:pH为横坐标,分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标]
一元弱酸(以CHCOOH为例) 二元弱酸(以草酸HC O 为例)
3 2 2 4注:pK
a
为电离常数的负对数 注:pK
a1
、pK
a2
为电离常数的负对数
δ 为HC O 分布系数
0 2 2 4
δ 为CHCOOH分布系数
0 3
δ 为HC O分布系数
1 2
δ 为CHCOO-分布系数
1 3
δ 为C O分布系数
2 2
随着pH增大,溶质分子浓度不断减小,离子浓度逐渐增大,酸根离子增多,根据分布系
数可以书写一定pH时所发生反应的离子方程式
同一pH条件下可以存在多种溶质微粒。根据在一定pH的微粒分布系数和酸的分析浓
度,就可以计算各成分在pH时的平衡浓度
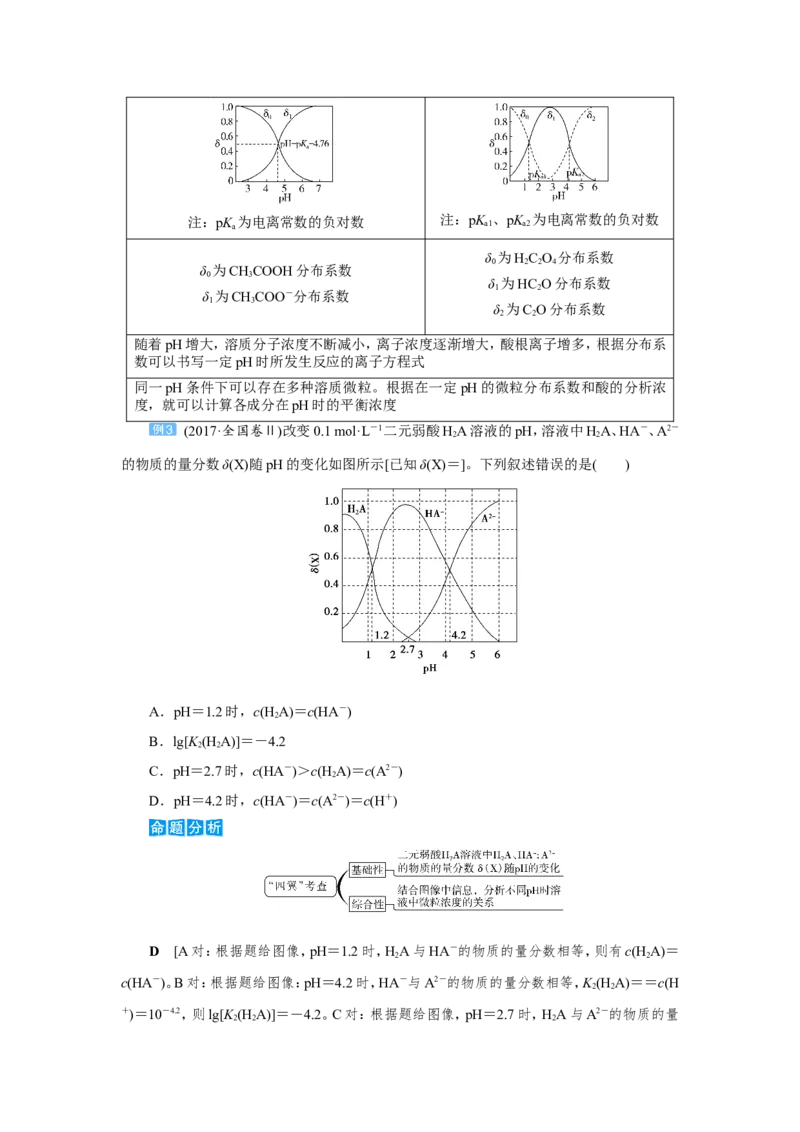
(2017·全国卷Ⅱ)改变0.1 mol·L-1二元弱酸HA溶液的pH,溶液中HA、HA-、A2-
2 2
的物质的量分数δ(X)随pH的变化如图所示[已知δ(X)=]。下列叙述错误的是( )
A.pH=1.2时,c(H A)=c(HA-)
2
B.lg[K (H A)]=-4.2
2 2
C.pH=2.7时,c(HA-)>c(H A)=c(A2-)
2
D.pH=4.2时,c(HA-)=c(A2-)=c(H+)
D [A对:根据题给图像,pH=1.2时,HA与HA-的物质的量分数相等,则有c(H A)=
2 2
c(HA-)。B对:根据题给图像:pH=4.2时,HA-与A2-的物质的量分数相等,K (H A)==c(H
2 2
+)=10-4.2,则lg[K (H A)]=-4.2。C对:根据题给图像,pH=2.7时,HA与A2-的物质的量
2 2 2分数相等,且远小于HA-的物质的量分数,则有c(HA-)>c(H A)=c(A2-)。D错:根据题给图
2
像,pH=4.2时,HA-与A2-的物质的量分数相等,c(HA-)=c(A2-),且c(HA-)+c(A2-)约为
0.1 mol·L-1,c(H+)=10-4.2 mol·L-1,则c(HA-)=c(A2-)>c(H+)。]
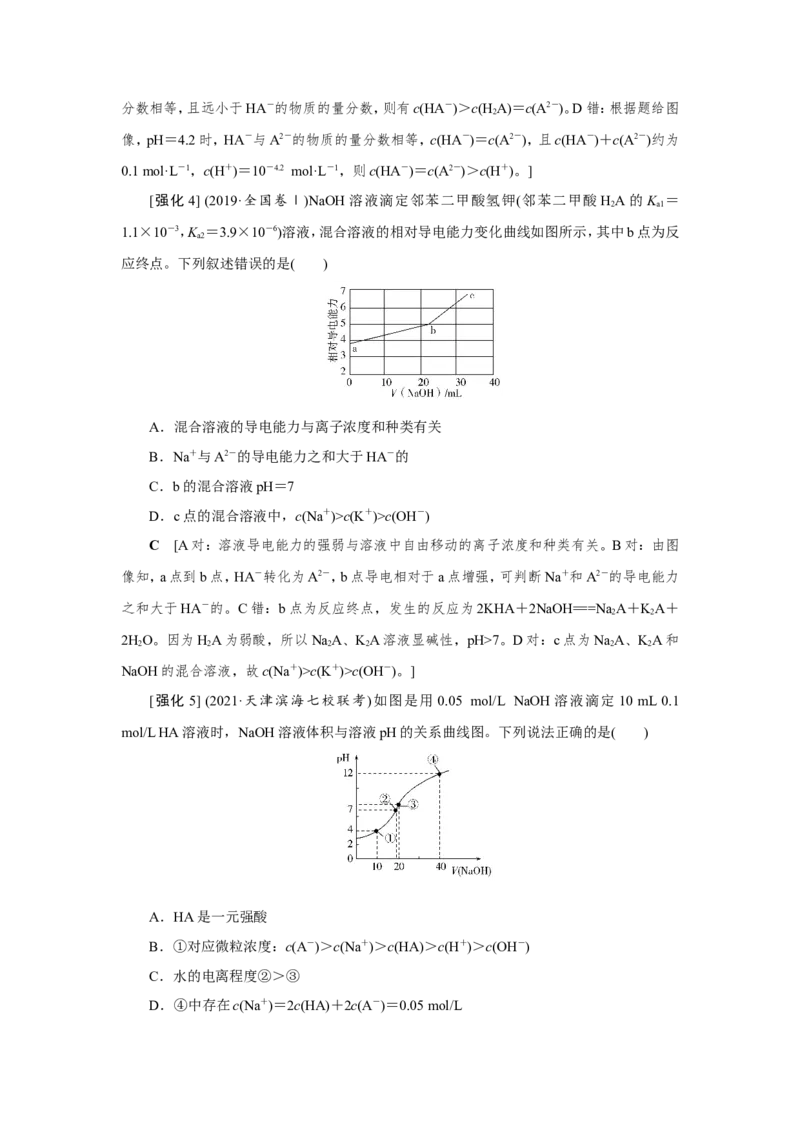
[强化4] (2019·全国卷Ⅰ)NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸HA的K =
2 a1
1.1×10-3,K =3.9×10-6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反
a2
应终点。下列叙述错误的是( )
A.混合溶液的导电能力与离子浓度和种类有关
B.Na+与A2-的导电能力之和大于HA-的
C.b的混合溶液pH=7
D.c点的混合溶液中,c(Na+)>c(K+)>c(OH-)
C [A对:溶液导电能力的强弱与溶液中自由移动的离子浓度和种类有关。B对:由图
像知,a点到b点,HA-转化为A2-,b点导电相对于a点增强,可判断Na+和A2-的导电能力
之和大于HA-的。C错:b点为反应终点,发生的反应为2KHA+2NaOH===Na A+KA+
2 2
2HO。因为HA为弱酸,所以NaA、KA溶液显碱性,pH>7。D对:c点为NaA、KA和
2 2 2 2 2 2
NaOH的混合溶液,故c(Na+)>c(K+)>c(OH-)。]
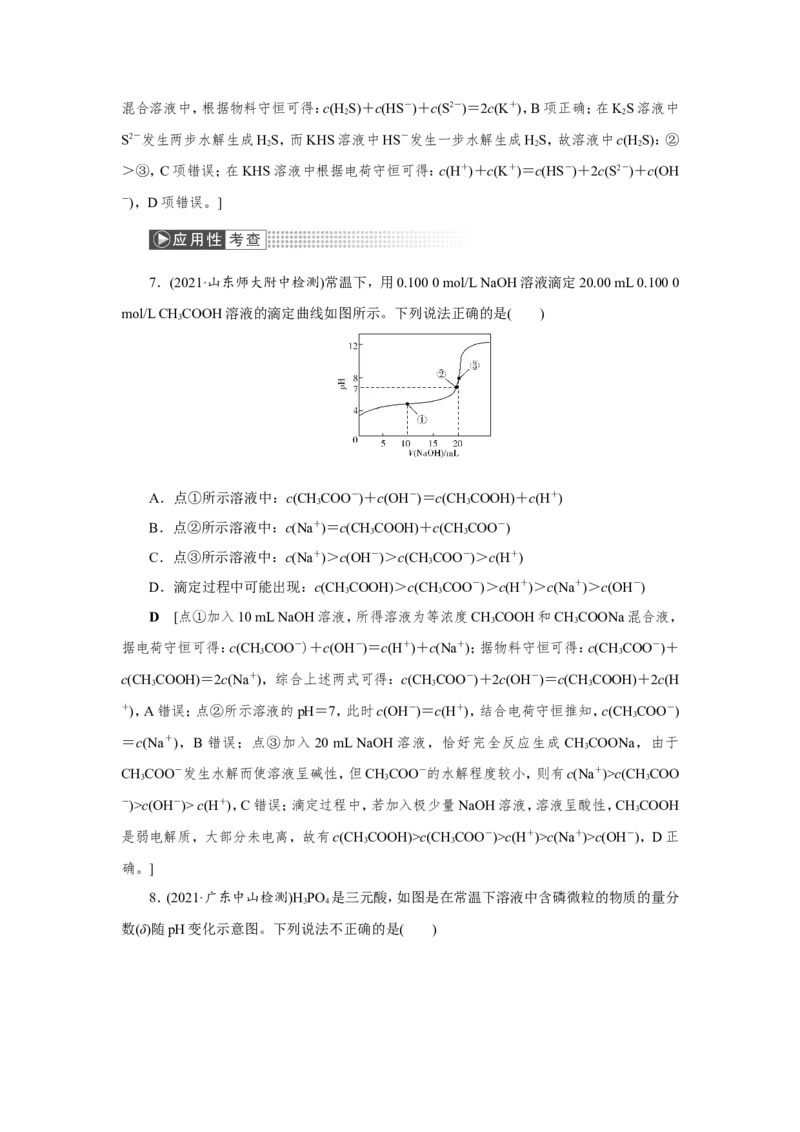
[强化 5] (2021·天津滨海七校联考)如图是用 0.05 mol/L NaOH 溶液滴定 10 mL 0.1
mol/L HA溶液时,NaOH溶液体积与溶液pH的关系曲线图。下列说法正确的是( )
A.HA是一元强酸
B.①对应微粒浓度:c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-)
C.水的电离程度②>③
D.④中存在c(Na+)=2c(HA)+2c(A-)=0.05 mol/LB [V(NaOH)=0时,0.1 mol/L HA 溶液的pH>2,说明HA未完全电离,则HA是一元
弱酸,A错误;①点加入10 mL NaOH溶液,所得溶液为等浓度HA和NaA混合液,溶液的
pH=4,溶液呈酸性,说明HA的电离程度大于NaA的水解程度,由于HA的电离程度较小,
则溶液中离子浓度:c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-),B正确;②点溶液pH=7,为HA和
NaA的混合液,HA抑制A-的水解;③点加入20 mL NaOH溶液,恰好完全反应,所得溶液为
NaA溶液,A-水解程度大于②点溶液,水解促进了水的电离,故水的电离程度:②<③,C错
误;④点加入40 mL NaOH溶液,所得溶液为等浓度NaA和NaOH混合液,据物料守恒可得:
c(Na+)=2c(A-)+2c(HA)==0.04 mol/L,D错误。]
训练(四十二) 水溶液中微粒浓度的关系
1.(2021·天津第一中学检测)有4种混合溶液,分别由等体积0.1 mol·L-1 的两种溶液混
合而成:① NH Cl 和 CHCOONa;② NH Cl 和 HCl;③ NH Cl 和 NaCl;④ NH Cl 和
4 3 4 4 4
NH ·H O(混合溶液呈碱性)。下列各项排序正确的是( )
3 2
A.pH:②<①<③<④
B.溶液中c(H+):①<③<②<④
C.c(NH):①<③<②<④
D.c(NH ·H O):①<③<④<②
3 2
C [酸性越强,pH越小,四种混合物中,②NH Cl与HCl的pH最小,④NH Cl与
4 4
NH ·HO的pH最大,①NH Cl与CHCOONa 的溶液显示中性,③NH Cl与NaCl 显示酸
3 2 4 3 4
性,故正确pH关系应该为②<③<①<④,A错误;c(H+)=10-pH溶液中c(H+)越大,pH越
小,借助A选项可知,c(H+)正确顺序为④<①<③<②,B错误;四种溶液中,④NH Cl与
4
NH •HO的c(NH)最大,大于0.1 mol·L-1;其次是②NH Cl与HCl,接近0.1 mol·L-1;
3 2 4
①NH Cl与CHCOONa,发生了双水解,c(NH)最小,所以正确排序为①<③<②<④,C正
4 3
确;由于④NH Cl与NH ·HO中,氨水是弱电解质,部分电离,c(NH ·HO)最大,其次是①
4 3 2 3 2
NH Cl与CHCOONa,发生了双水解,NH的水解程度稍大;氨水浓度最小的是②NH Cl与
4 3 4
HCl,几乎没有氨水存在,所以氨水浓度大小顺序为②<③<①<④,D错误。]
2.(2021·安徽宣城检测)一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的HS溶液中,c(H+)=c(HS-)=1×10-5 mol·L-1
2
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的HC O 溶液与pH=12的NaOH溶液以任意比例混合:c(Na+)+c(H+)=
2 2 4c(OH-)+c(HC O)
2
D.pH相同的①CHCOONa,②NaHCO ,③NaClO三种溶液的c(Na+):①>②>③
3 3
D [pH=5的HS溶液中,H+的浓度为1×10-5 mol·L-1,但是HS-的浓度会小于H+的
2
浓度,H+来自于HS的第一步电离、HS-的电离和水的电离,故H+的浓度大于HS-的浓度,
2
A项错误;弱碱不完全电离,弱碱稀释10倍时,pH减小不到一个单位,a<b+1,B项错误;
草酸是弱酸,氢氧化钠是强碱,无论怎样混合得到的溶液都符合电荷守恒,而该等式中缺少
草酸根离子,不符合电荷守恒,C项错误;因为酸性:醋酸>碳酸>次氯酸,根据越弱越水解的
原则,pH相同的三种钠盐,浓度的大小关系为醋酸钠>碳酸氢钠>次氯酸钠,则钠离子的浓度
为①>②>③,D项正确。]
3.(2021·安徽淮北检测)将0.1 mol·L-1 (CHCOO)Ba溶液与0.1 mol·L-1 NaOH溶液等
3 2
体积混合,下列关系不正确的是( )
A.3c(Na+)+c(H+)=c(OH-)+c(CHCOO-)
3
B.2c(Ba2+)=c(CHCOOH)+c(CHCOO-)
3 3
C.c(CHCOO-)>c(Na+)=c(Ba2+)>c(OH-)>c(H+)
3
D.c(OH-)=c(H+)+c(CHCOOH)+0.05 mol·L-1
3
C [由电荷守恒式2c(Ba2+)+c(Na+)+c(H+)=c(OH-)+c(CHCOO-),两溶液均为0.1
3
mol·L-1,则c(Ba2+)=c(Na+), A项正确;因CHCOO-在溶液中部分水解,由物料守恒:2c(Ba2
3
+)=c(CHCOOH)+c(CHCOO-),B项正确;该溶液中的OH-来自NaOH的电离和CHCOO
3 3 3
-的水解,故c(CHCOO-)>c(OH-)>c(Na+)=c(Ba2+)>c(H+),C项错误;电荷守恒式为c(Na
3
+)+2c(Ba2+)+c(H+)=c(OH-)+c(CHCOO-),把c(Na+)=0.05 mol·L-1和物料守恒式
3
2c(Ba2+)=c(CHCOOH)+c(CHCOO-)代入电荷守恒式,即得 c(OH-)=c(H+)+
3 3
c(CHCOOH)+0.05 mol·L-1,D项正确。]
3
4.(2019·上海卷)常温下,0.1 mol/L :①CHCOOH、②NaOH、③CHCOONa,下列叙述
3 3
正确的是( )
A.①中c(CHCOOH)>c(CHCOO-)>c(H+)>c(OH-)
3 3
B.①②等体积混合后,醋酸根离子浓度小于③的二分之一
C.①③等体积混合以后,溶液呈酸性,则c(Na+)>c(CHCOO-)>c(H+)
3
D.①②等体积混合以后,水的电离程度比①③等体积混合的电离程度小
B [CHCOOH是弱电解质,电离是极其微弱的,溶剂水电离产生氢离子,所以①中
3
c(CHCOOH)>c(H+)>c(CHCOO-)>c(OH-),A项错误;①②等体积混合后,两者恰好完全
3 3反应,所以浓度是原来的一半,但溶液的体积变大促进醋酸根离子的水解,所以①②等体积
混合后,醋酸根离子浓度小于③的二分之一, B项正确;①③等体积混合以后,以醋酸的电
离为主,所以溶液呈酸性,则c(CHCOO-)>c(Na+)>c(H+),C项错误;①②等体积混合恰好
3
完全反应生成醋酸钠,醋酸钠是强碱弱酸盐,水解对水的电离起促进作用,而①③等体积混
合以醋酸电离为主,溶液呈酸性,对水的电离起抑制作用,所以①②等体积混合以后,水的电
离程度比①③等体积混合的电离程度大, D项错误。]
5.(2020·北京延庆区一模)常温下,2 mL 1 mol·L-1 NaHCO 溶液,pH约为8。向其中滴
3
加等体积等浓度的饱和CaCl 溶液,有白色沉淀和无色气体生成。下列说法中,正确的是(
2
)
A.NaHCO 溶液中, c(H+)+c(Na+)=c(HCO)+c(CO)+c(OH-)
3
B.NaHCO 溶液中,c(Na+) >c(OH-)> c(HCO) > c(H+)
3
C.加热NaHCO 溶液,pH增大,一定是HCO水解程度增大的结果
3
D.滴加饱和CaCl 溶液发生了反应:Ca2++2HCO===CaCO ↓+HO+CO↑
2 3 2 2
D [NaHCO 溶液中,据电荷守恒可得c(H+)+c(Na+)=c(HCO)+2c(CO)+c(OH-),A
3
项错误;常温下,1 mol·L-1 NaHCO 溶液的pH约为8,说明HCO的水解程度大于其电离程
3
度,但其水解程度较小,故溶液中:c(Na+)>c(HCO)> c(OH-) > c(H+),B项错误;加热
NaHCO 溶液,可能是HCO水解程度增大的结果,也可能是NaHCO 受热分解生成NaCO,
3 3 2 3
CO的水解程度大于HCO,溶液的碱性增强,C项错误;滴加饱和CaCl 溶液,有白色沉淀和
2
无色气体生成,Ca2+与CO结合生成CaCO 沉淀,促使HCO的电离平衡正向移动,H+与
3
HCO结合生成CO 和HO,D项正确。]
2 2
6.(2021·甘肃甘谷检测)下列各组溶液中的各种溶质的物质的量浓度均为0.1 mol·L-1:
①HS溶液、②KHS溶液、③KS溶液、④HS和KHS混合溶液(已知常温下KHS溶液的
2 2 2
pH>7)。下列说法正确的是( )
A.溶液的pH从大到小的顺序为③>②>①>④
B.在HS和KHS混合溶液中:c(H S)+c(HS-)+c(S2-)=2c(K+)
2 2
C.c(H S)从大到小的顺序为①>④>③>②
2
D.在KHS溶液中:c(H+)+c(K+)=c(HS-)+c(S2-)+c(OH-)
B [H S溶液、HS和KHS混合溶液均显酸性,但HS-的存在抑制了HS的电离,故
2 2 2
pH:④>①;KS溶液中S2-的水解程度大于KHS溶液中HS-的水解程度,则pH:③>②,故
2
溶液pH从大到小的顺序为③>②>④>①,A项错误;在浓度均为0.1 mol·L-1 HS和KHS
2混合溶液中,根据物料守恒可得:c(H S)+c(HS-)+c(S2-)=2c(K+),B项正确;在KS溶液中
2 2
S2-发生两步水解生成HS,而KHS溶液中HS-发生一步水解生成HS,故溶液中c(H S):②
2 2 2
>③,C项错误;在KHS溶液中根据电荷守恒可得:c(H+)+c(K+)=c(HS-)+2c(S2-)+c(OH
-),D项错误。]
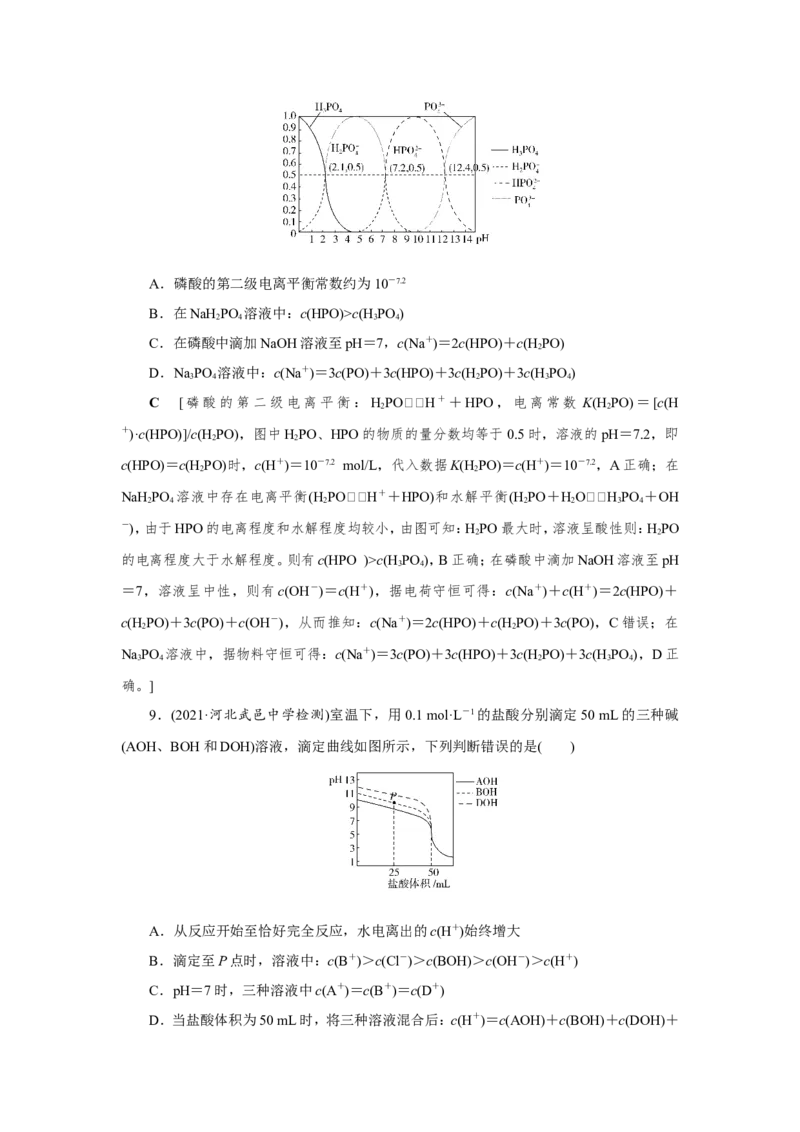
7.(2021·山东师大附中检测)常温下,用0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0
mol/L CH COOH溶液的滴定曲线如图所示。下列说法正确的是( )
3
A.点①所示溶液中:c(CHCOO-)+c(OH-)=c(CHCOOH)+c(H+)
3 3
B.点②所示溶液中:c(Na+)=c(CHCOOH)+c(CHCOO-)
3 3
C.点③所示溶液中:c(Na+)>c(OH-)>c(CHCOO-)>c(H+)
3
D.滴定过程中可能出现:c(CHCOOH)>c(CHCOO-)>c(H+)>c(Na+)>c(OH-)
3 3
D [点①加入10 mL NaOH溶液,所得溶液为等浓度CHCOOH和CHCOONa混合液,
3 3
据电荷守恒可得:c(CHCOO-)+c(OH-)=c(H+)+c(Na+);据物料守恒可得:c(CHCOO-)+
3 3
c(CHCOOH)=2c(Na+),综合上述两式可得:c(CHCOO-)+2c(OH-)=c(CHCOOH)+2c(H
3 3 3
+),A错误;点②所示溶液的pH=7,此时c(OH-)=c(H+),结合电荷守恒推知,c(CHCOO-)
3
=c(Na+),B错误;点③加入20 mL NaOH溶液,恰好完全反应生成CHCOONa,由于
3
CHCOO-发生水解而使溶液呈碱性,但CHCOO-的水解程度较小,则有c(Na+)>c(CHCOO
3 3 3
-)>c(OH-)> c(H+),C错误;滴定过程中,若加入极少量NaOH溶液,溶液呈酸性,CHCOOH
3
是弱电解质,大部分未电离,故有c(CHCOOH)>c(CHCOO-)>c(H+)>c(Na+)>c(OH-),D正
3 3
确。]
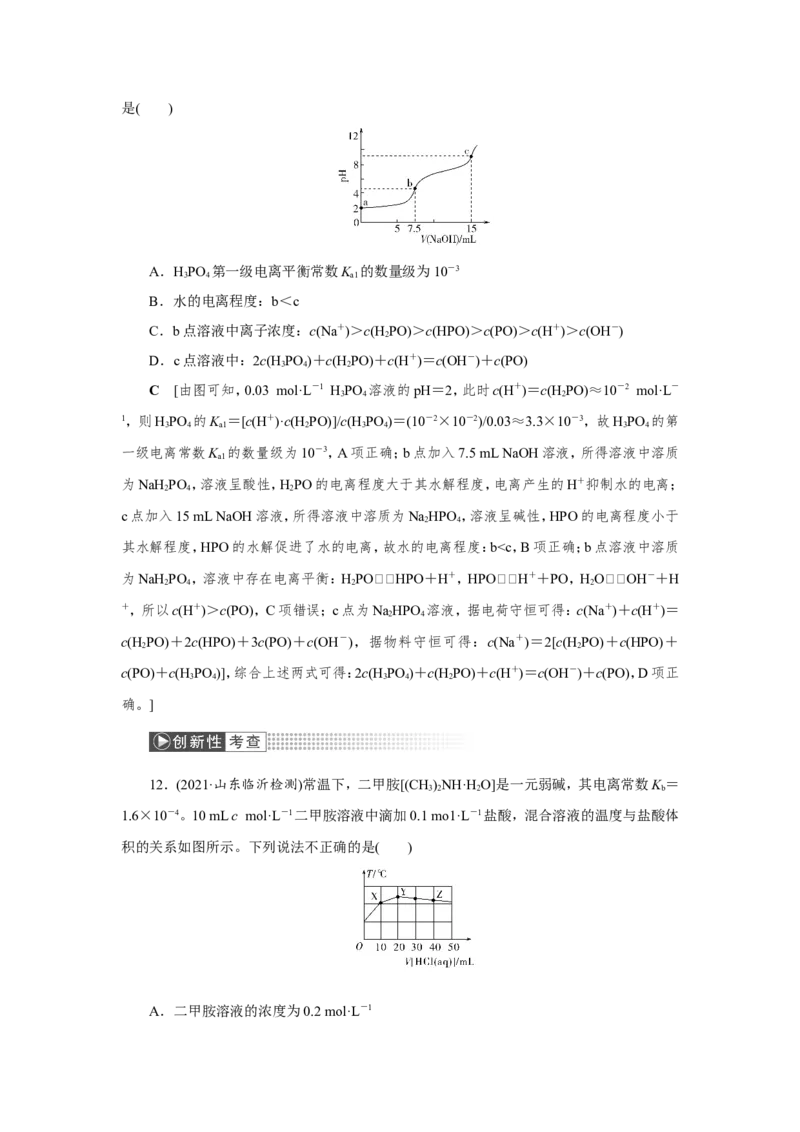
8.(2021·广东中山检测)HPO 是三元酸,如图是在常温下溶液中含磷微粒的物质的量分
3 4
数(δ)随pH变化示意图。下列说法不正确的是( )A.磷酸的第二级电离平衡常数约为10-7.2
B.在NaH PO 溶液中:c(HPO)>c(H PO )
2 4 3 4
C.在磷酸中滴加NaOH溶液至pH=7,c(Na+)=2c(HPO)+c(H PO)
2
D.NaPO 溶液中:c(Na+)=3c(PO)+3c(HPO)+3c(H PO)+3c(H PO )
3 4 2 3 4
C [磷酸的第二级电离平衡:HPOH++HPO,电离常数 K(H PO)=[c(H
2 2
+)·c(HPO)]/c(H PO),图中HPO、HPO的物质的量分数均等于0.5时,溶液的pH=7.2,即
2 2
c(HPO)=c(H PO)时,c(H+)=10-7.2 mol/L,代入数据K(H PO)=c(H+)=10-7.2,A正确;在
2 2
NaH PO 溶液中存在电离平衡(H POH++HPO)和水解平衡(H PO+HOHPO +OH
2 4 2 2 2 3 4
-),由于HPO的电离程度和水解程度均较小,由图可知:HPO最大时,溶液呈酸性则:HPO
2 2
的电离程度大于水解程度。则有c(HPO )>c(H PO ),B正确;在磷酸中滴加NaOH溶液至pH
3 4
=7,溶液呈中性,则有c(OH-)=c(H+),据电荷守恒可得:c(Na+)+c(H+)=2c(HPO)+
c(H PO)+3c(PO)+c(OH-),从而推知:c(Na+)=2c(HPO)+c(H PO)+3c(PO),C错误;在
2 2
NaPO 溶液中,据物料守恒可得:c(Na+)=3c(PO)+3c(HPO)+3c(H PO)+3c(H PO ),D正
3 4 2 3 4
确。]
9.(2021·河北武邑中学检测)室温下,用0.1 mol·L-1的盐酸分别滴定50 mL的三种碱
(AOH、BOH和DOH)溶液,滴定曲线如图所示,下列判断错误的是( )
A.从反应开始至恰好完全反应,水电离出的c(H+)始终增大
B.滴定至P点时,溶液中:c(B+)>c(Cl-)>c(BOH)>c(OH-)>c(H+)
C.pH=7时,三种溶液中c(A+)=c(B+)=c(D+)
D.当盐酸体积为50 mL时,将三种溶液混合后:c(H+)=c(AOH)+c(BOH)+c(DOH)+c(OH-)
C [三种碱溶液中分别滴加盐酸至恰好完全反应,溶液的碱性减弱,对水的电离抑制程
度减小,故水电离出的c(H+)始终增大,A项正确;由图可知,消耗盐酸的体积都为50 mL,则
三种碱的浓度均为0.1 mol·L-1;P点时,V(盐酸)=25 mL,此时溶液为等浓度BOH和BCl混
合液,由于溶液pH>9,溶液呈碱性,则BOH的电离程度大于BCl的水解程度,故溶液中c(B
+)>c(Cl-)>c(BOH)>c(OH-)>c(H+),B项正确;pH=7时,三种溶液中均存在c(OH-)=c(H
+),且存在电荷守恒关系:c(X+)+c(H+)=c(OH-)+c(Cl-)(X+=A+、B+或D+),则有c(X+)=
c(Cl-),由于三种碱的碱性不同,则pH=7时加入盐酸的体积不同,c(Cl-)不同,故pH=7时,
三种溶液中c(A+)≠c(B+)≠c(D+),C项错误;当盐酸体积为50 mL时,三种碱溶液均恰好与
盐酸反应生成相应的盐,将三种溶液混合,据质子守恒可得c(H+)=c(AOH)+c(BOH)+
c(DOH)+c(OH-),D项正确。]
10.(2019.4·浙江选考)室温下,取20 mL 0.1 mol·L-1某二元酸HA,滴加0.2 mol·L-1
2
NaOH溶液。已知:HA===H++HA-,HA-H++A2-。下列说法不正确的是( )
2
A.0.1 mol·L-1 HA溶液中有c(H+)-c(OH-)-c(A2-)=0.1 mol·L-1
2
B.当滴加至中性时,溶液中c(Na+)=c(HA-)+2c(A2-),用去NaOH溶液的体积小于10
mL
C.当用去NaOH溶液体积10 mL时,溶液的pH<7,此时溶液中有c(A2-)=c(H+)-
c(OH-)
D.当用去NaOH溶液体积20 mL时,此时溶液中有c(Na+)=2c(HA-)+2c(A2-)
B [根据HA===H++HA-、HA-H++A2-可知,HA的第一步完全电离,第二步部
2 2
分电离。根据电荷守恒可得:c(H+)=c(OH-)+c(HA-)+2c(A2-),根据物料守恒:c(HA-)+
c(A2-)=0.1 mol·L-1,二者结合可得:c(H+)-c(OH-)-c(A2-)=0.1 mol·L-1, A项正确;当滴加
至中性时c(H+)=c(OH-),结合电荷守恒可知c(Na+)=c(HA-)+2c(A2-),由于HA-只发生
电离,则NaHA溶液呈酸性,若为中性,加入的氢氧化钠溶液应该大于10 mL, B项错误;当用
去NaOH溶液体积10 mL时,反应后溶质为NaHA,HA-只发生电离,则NaHA溶液呈酸性,
溶液的pH<7,根据质子守恒可得:c(A2-)=c(H+)-c(OH-),C项正确;当用去NaOH溶液体
积20 mL时,反应后溶质为NaA,结合物料守恒可得:c(Na+)=2c(HA-)+2c(A2-),D项正
2
确。]
11.(2020·山东潍坊二模)向7.5 mL 0.03 mol·L-1的HPO 溶液中,逐滴加入相同浓度的
3 4
NaOH溶液,溶液pH与NaOH溶液体积关系如图所示,已知K ≫K ≫K ,下列说法错误的
a1 a2 a3是( )
A.HPO 第一级电离平衡常数K 的数量级为10-3
3 4 a1
B.水的电离程度:b<c
C.b点溶液中离子浓度:c(Na+)>c(H PO)>c(HPO)>c(PO)>c(H+)>c(OH-)
2
D.c点溶液中:2c(H PO )+c(H PO)+c(H+)=c(OH-)+c(PO)
3 4 2
C [由图可知,0.03 mol·L-1 HPO 溶液的pH=2,此时c(H+)=c(H PO)≈10-2 mol·L-
3 4 2
1,则HPO 的K =[c(H+)·c(H PO)]/c(H PO )=(10-2×10-2)/0.03≈3.3×10-3,故HPO 的第
3 4 a1 2 3 4 3 4
一级电离常数K 的数量级为10-3,A项正确;b点加入7.5 mL NaOH溶液,所得溶液中溶质
a1
为NaH PO ,溶液呈酸性,HPO的电离程度大于其水解程度,电离产生的H+抑制水的电离;
2 4 2
c点加入15 mL NaOH溶液,所得溶液中溶质为NaHPO ,溶液呈碱性,HPO的电离程度小于
2 4
其水解程度,HPO的水解促进了水的电离,故水的电离程度:bc[(CH )NH]>c(H+)>c(OH-)
3 2
D.常温下,(CH)NH Cl水解常数K =6.25×10-11
3 2 2 h
B [二甲胺与盐酸恰好完全中和时放出热量最多,溶液温度最高,即Y点表示酸碱恰好
完全反应。根据(CH)NH·HO+HCl===(CH )NH Cl+HO,c=0.2 mol·L-1,A项正确;二甲
3 2 2 3 2 2 2
胺是弱碱,Y点对应溶质是强酸弱碱盐,其溶液呈酸性,X点对应的溶液中(CH)NH·HO、
3 2 2
(CH)NH Cl的浓度相等,其混合溶液呈碱性,故中性点应在X点与Y点之间,B项错误;二
3 2 2
甲胺是弱碱,Y 点对应溶质是强酸弱碱盐,其溶液呈酸性,Y 点存在:c(Cl
-)>c[(CH )NH]>c(H+)>c(OH-),C项正确;K =K /K =1×10-14/1.6×10-4=6.25×10-11,D
3 2 h w b
项正确。]
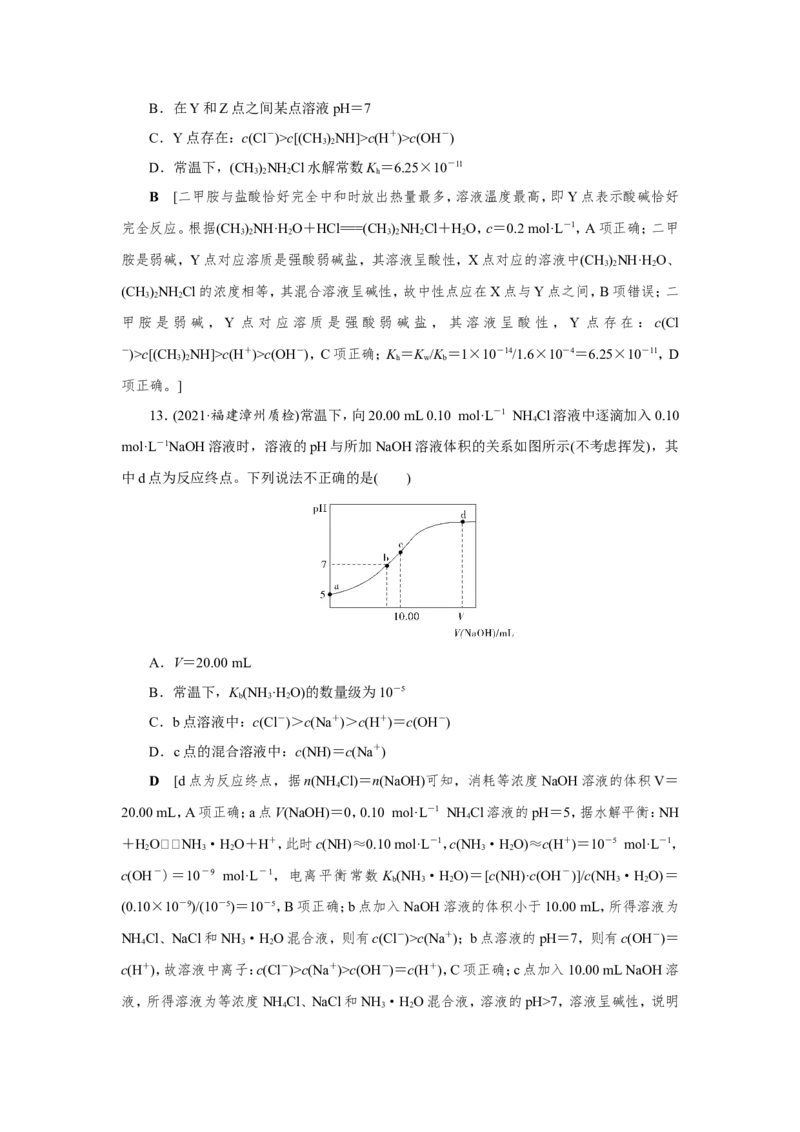
13.(2021·福建漳州质检)常温下,向20.00 mL 0.10 mol·L-1 NH Cl溶液中逐滴加入0.10
4
mol·L-1NaOH溶液时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发),其
中d点为反应终点。下列说法不正确的是( )
A.V=20.00 mL
B.常温下,K (NH ·H O)的数量级为10-5
b 3 2
C.b点溶液中:c(Cl-)>c(Na+)>c(H+)=c(OH-)
D.c点的混合溶液中:c(NH)=c(Na+)
D [d点为反应终点,据n(NH Cl)=n(NaOH)可知,消耗等浓度NaOH溶液的体积V=
4
20.00 mL,A项正确;a点V(NaOH)=0,0.10 mol·L-1 NH Cl溶液的pH=5,据水解平衡:NH
4
+HONH ·HO+H+,此时c(NH)≈0.10 mol·L-1,c(NH ·HO)≈c(H+)=10-5 mol·L-1,
2 3 2 3 2
c(OH-)=10-9 mol·L-1,电离平衡常数 K (NH ·HO)=[c(NH)·c(OH-)]/c(NH ·HO)=
b 3 2 3 2
(0.10×10-9)/(10-5)=10-5,B项正确;b点加入NaOH溶液的体积小于10.00 mL,所得溶液为
NH Cl、NaCl和NH ·HO混合液,则有c(Cl-)>c(Na+);b点溶液的pH=7,则有c(OH-)=
4 3 2
c(H+),故溶液中离子:c(Cl-)>c(Na+)>c(OH-)=c(H+),C项正确;c点加入10.00 mL NaOH溶
液,所得溶液为等浓度NH Cl、NaCl和NH ·HO混合液,溶液的pH>7,溶液呈碱性,说明
4 3 2NH ·HO的电离程度大于NH的水解程度,则有c(NH)>c(Na+),D项错误。]
3 2
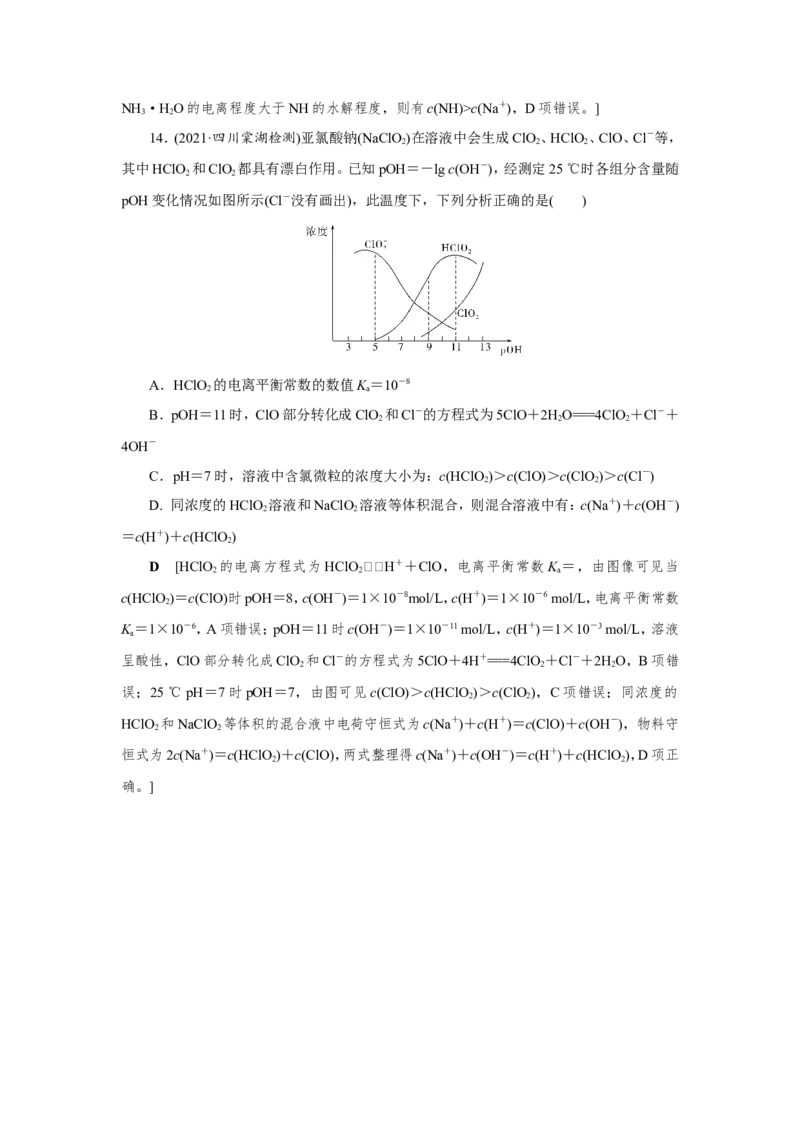
14.(2021·四川棠湖检测)亚氯酸钠(NaClO)在溶液中会生成ClO 、HClO、ClO、Cl-等,
2 2 2
其中HClO 和ClO 都具有漂白作用。已知pOH=-lg c(OH-),经测定25 ℃时各组分含量随
2 2
pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析正确的是( )
A.HClO 的电离平衡常数的数值K=10-8
2 a
B.pOH=11时,ClO部分转化成ClO 和Cl-的方程式为5ClO+2HO===4ClO +Cl-+
2 2 2
4OH-
C.pH=7时,溶液中含氯微粒的浓度大小为:c(HClO)>c(ClO)>c(ClO )>c(Cl-)
2 2
D. 同浓度的HClO 溶液和NaClO 溶液等体积混合,则混合溶液中有:c(Na+)+c(OH-)
2 2
=c(H+)+c(HClO)
2
D [HClO 的电离方程式为HClOH++ClO,电离平衡常数K =,由图像可见当
2 2 a
c(HClO)=c(ClO)时pOH=8,c(OH-)=1×10-8mol/L,c(H+)=1×10-6 mol/L,电离平衡常数
2
K=1×10-6,A项错误;pOH=11时c(OH-)=1×10-11 mol/L,c(H+)=1×10-3 mol/L,溶液
a
呈酸性,ClO部分转化成ClO 和Cl-的方程式为5ClO+4H+===4ClO +Cl-+2HO,B项错
2 2 2
误;25 ℃ pH=7时pOH=7,由图可见c(ClO)>c(HClO)>c(ClO ),C项错误;同浓度的
2 2
HClO 和NaClO 等体积的混合液中电荷守恒式为c(Na+)+c(H+)=c(ClO)+c(OH-),物料守
2 2
恒式为2c(Na+)=c(HClO)+c(ClO),两式整理得c(Na+)+c(OH-)=c(H+)+c(HClO),D项正
2 2
确。]