文档内容
第六、七讲 氧化还原反应的基本概念、规律、及其配平
【基础巩固】
1.(2020·北京卷)水与下列物质反应时,水表现出氧化性的是( )
A.Na B.Cl C.NO D.Na O
2 2 2
2.下列装置工作原理与氧化还原反应无关的是( )
A.臭氧消毒柜 B.甲烷燃料电池 C.太阳能集热器 D.燃气灶
3.(2022·山东卷)古医典富载化学知识,下述之物见其氧化性者为( )
A.金(Au):“虽被火亦未熟”
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳(CaCO):“色黄,以苦酒(醋)洗刷则白”
3
4.(2021·天津卷)关于反应HSO +NaSO ===Na SO +SO ↑+HO所涉及的物质,下列说法错误的是( )
2 4 2 3 2 4 2 2
A.HSO 在该反应中为氧化剂 B.Na SO 容易被空气中的O 氧化变质
2 4 2 3 2
C.Na SO 是含有共价键的离子化合物 D.SO 是导致酸雨的主要有害污染物
2 4 2
5.(2022·浙江1月选考)关于反应4CO+SiH=====4CO+2HO+SiO,下列说法正确的是( )
2 4 2 2
A.CO是氧化产物 B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4 D.生成1 mol SiO 时,转移8 mol电子
2
6.含元素碲(Te)的几种物质存在如图所示转化关系。下列说法错误的是( )
A.反应①利用了HTe的还原性 B.反应②中HO作氧化剂
2 2
C.反应③利用了HO 的氧化性 D.HTeO 转化为HTeO 发生了氧化还原反应
2 2 2 2 5 2 4 9
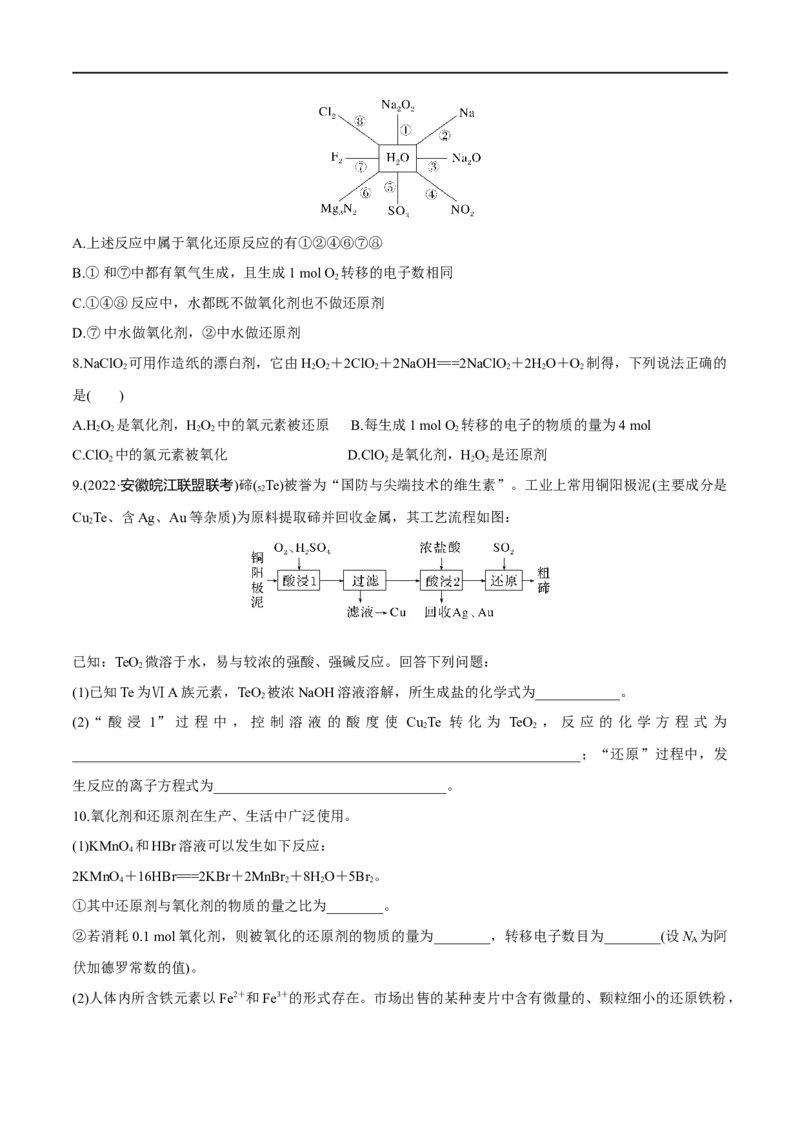
7、水是一种重要的资源,它同时在化学反应中担任着重要的角色,既可作为反应物又可作为生成物,如
图中和水相连的物质都能和水发生反应,则有关说法正确的是( )A.上述反应中属于氧化还原反应的有①②④⑥⑦⑧
B.①和⑦中都有氧气生成,且生成1 mol O 转移的电子数相同
2
C.①④⑧反应中,水都既不做氧化剂也不做还原剂
D.⑦中水做氧化剂,②中水做还原剂
8.NaClO 可用作造纸的漂白剂,它由HO+2ClO +2NaOH===2NaClO +2HO+O 制得,下列说法正确的
2 2 2 2 2 2 2
是( )
A.HO 是氧化剂,HO 中的氧元素被还原 B.每生成1 mol O 转移的电子的物质的量为4 mol
2 2 2 2 2
C.ClO 中的氯元素被氧化 D.ClO 是氧化剂,HO 是还原剂
2 2 2 2
9.(2022·安徽皖江联盟联考)碲( Te)被誉为“国防与尖端技术的维生素”。工业上常用铜阳极泥(主要成分是
52
Cu Te、含Ag、Au等杂质)为原料提取碲并回收金属,其工艺流程如图:
2
已知:TeO 微溶于水,易与较浓的强酸、强碱反应。回答下列问题:
2
(1)已知Te为ⅥA族元素,TeO 被浓NaOH溶液溶解,所生成盐的化学式为____________。
2
(2)“ 酸 浸 1” 过 程 中 , 控 制 溶 液 的 酸 度 使 Cu Te 转 化 为 TeO , 反 应 的 化 学 方 程 式 为
2 2
________________________________________________________________________;“还原”过程中,发
生反应的离子方程式为_________________________________。
10.氧化剂和还原剂在生产、生活中广泛使用。
(1)KMnO 和HBr溶液可以发生如下反应:
4
2KMnO +16HBr===2KBr+2MnBr +8HO+5Br 。
4 2 2 2
①其中还原剂与氧化剂的物质的量之比为________。
②若消耗0.1 mol氧化剂,则被氧化的还原剂的物质的量为________,转移电子数目为________(设N 为阿
A
伏加德罗常数的值)。
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的、颗粒细小的还原铁粉,这 些 铁 粉 在 人 体 胃 酸 的 作 用 下 转 化 成 亚 铁 盐 , 此 反 应 的 离 子 方 程 式 为
_____________________________________________________,但Fe2+在酸性条件下很容易被空气中的O
2
氧化,写出该反应的离子方程式:_____________________________________。
(3)次磷酸(H PO )是一种精细化工产品,具有较强还原性,可与足量的NaOH溶液完全中和生成NaH PO ,
3 2 2 2
NaH PO 溶液可使酚酞试液变红,回答下列问题:
2 2
①HPO 中,磷元素的化合价为________。
3 2
②写出HPO 电离方程式:_____________________________________________________。
3 2
③HPO 及NaH PO 均可将溶液中的Ag+还原为金属银,从而用于化学镀银。利用(H PO )进行的化学镀银
3 2 2 2 3 2
反 应 中 , 氧 化 剂 与 还 原 剂 的 物 质 的 量 之 比 为 4∶1 , 写 出 该 反 应 的 离 子 方 程 式 :
____________________________________________________________。
【拔高练习】
1.(2022·山东卷)实验室制备 KMnO 过程为:①高温下在熔融强碱性介质中用 KClO 氧化 MnO 制备
4 3 2
KMnO ;②水溶后冷却,调溶液pH至弱碱性,KMnO 歧化生成KMnO 和MnO ;③减压过滤,将滤液
2 4 2 4 4 2
蒸发浓缩、冷却结晶,再减压过滤得KMnO 。下列说法正确的是( )
4
A.①中用瓷坩埚作反应器 B.①中用NaOH作强碱性介质
C.②中KMnO 只体现氧化性 D.MnO 转化为KMnO 的理论转化率约为66.7%
2 4 2 4
2.(2021·浙江1月选考)关于反应8NH +6NO ===7N +12HO,下列说法正确的是( )
3 2 2 2
A.NH 中H元素被氧化 B.NO 在反应过程中失去电子
3 2
C.还原剂与氧化剂的物质的量之比为3∶4 D.氧化产物与还原产物的质量之比为4∶3
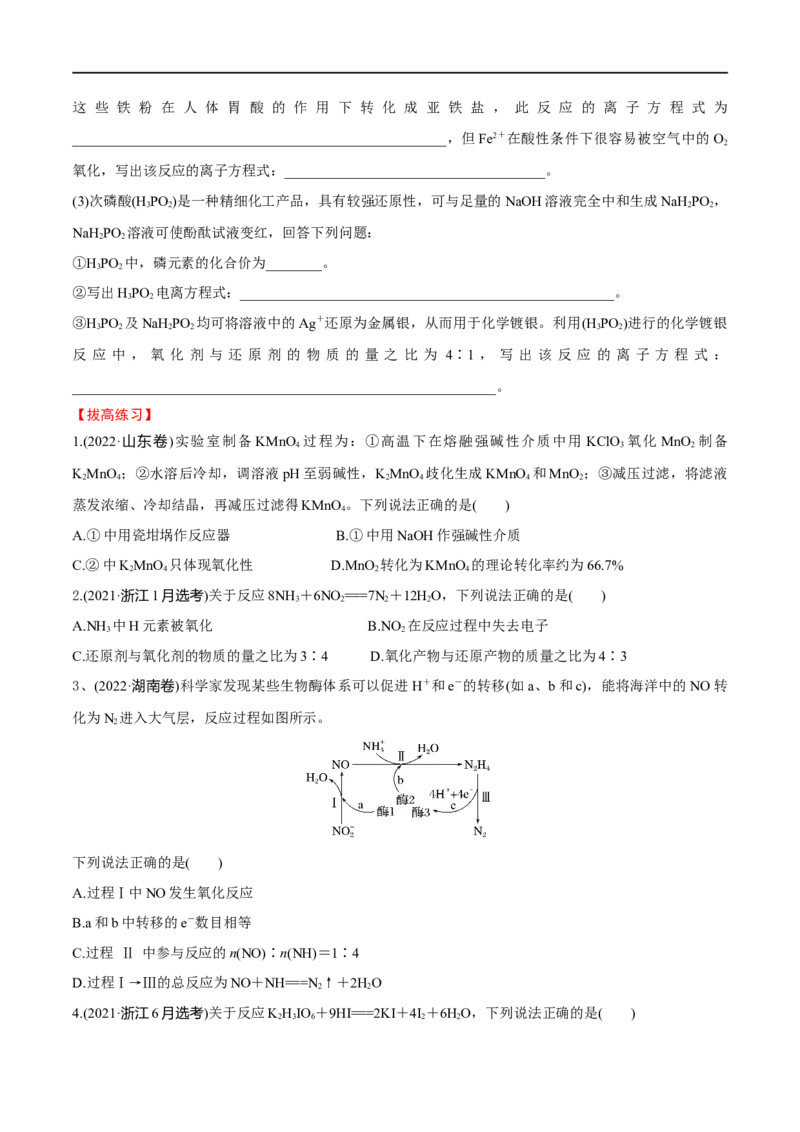
3、(2022·湖南卷)科学家发现某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将海洋中的NO转
化为N 进入大气层,反应过程如图所示。
2
下列说法正确的是( )
A.过程Ⅰ中NO发生氧化反应
B.a和b中转移的e-数目相等
C.过程 Ⅱ 中参与反应的n(NO)∶n(NH)=1∶4
D.过程Ⅰ→Ⅲ的总反应为NO+NH===N ↑+2HO
2 2
4.(2021·浙江6月选考)关于反应KHIO +9HI===2KI+4I+6HO,下列说法正确的是( )
2 3 6 2 2A.KHIO 发生氧化反应 B.KI是还原产物
2 3 6
C.生成12.7 g I 时,转移0.1 mol电子 D.还原剂与氧化剂的物质的量之比为7∶1
2
5.(2021·山东卷改编)实验室中利用固体KMnO 进行如图实验,下列说法错误的是( )
4
A.G与H均为氧化产物 B.实验中KMnO 既作氧化剂又作还原剂
4
C.Mn元素至少参与了3个氧化还原反应 D.G与H的物质的量之和可能为0.25 mol
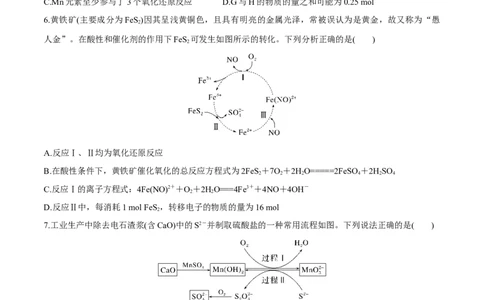
6.黄铁矿(主要成分为FeS)因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚
2
人金”。在酸性和催化剂的作用下FeS 可发生如图所示的转化。下列分析正确的是( )
2
A.反应Ⅰ、Ⅱ均为氧化还原反应
B.在酸性条件下,黄铁矿催化氧化的总反应方程式为2FeS+7O+2HO=====2FeSO +2HSO
2 2 2 4 2 4
C.反应Ⅰ的离子方程式:4Fe(NO)2++O+2HO===4Fe3++4NO+4OH-
2 2
D.反应Ⅱ中,每消耗1 mol FeS ,转移电子的物质的量为16 mol
2
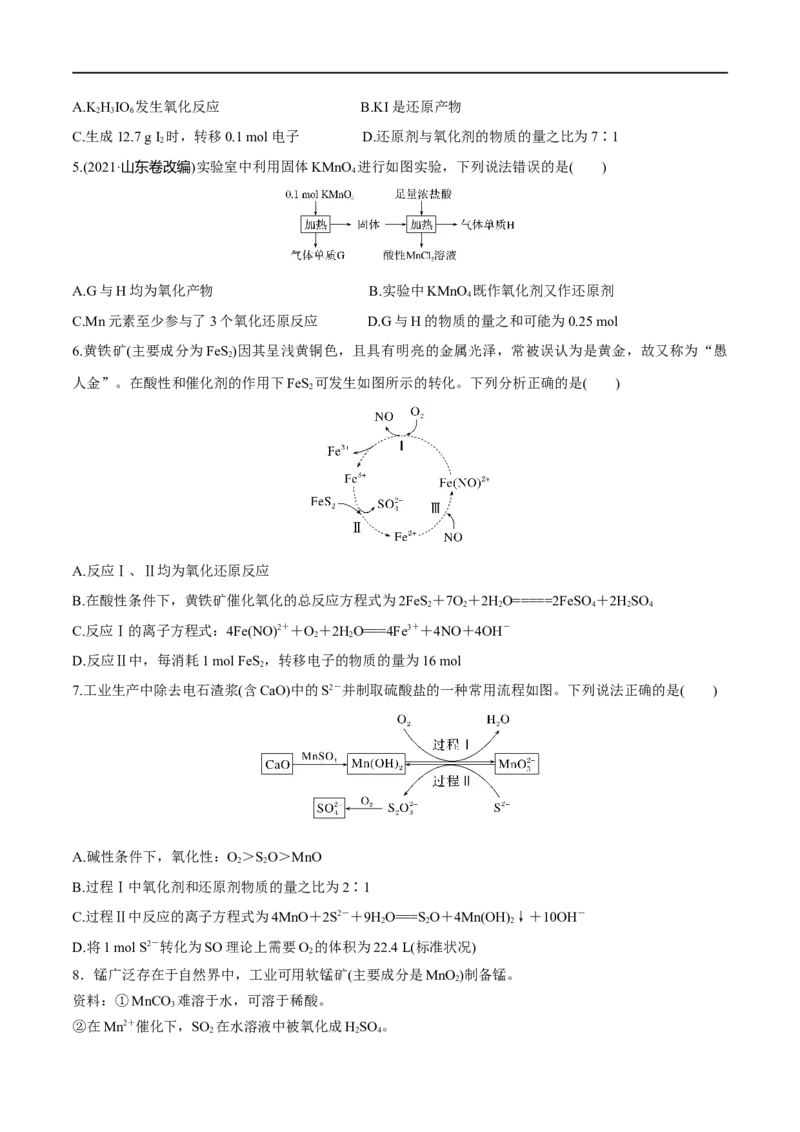
7.工业生产中除去电石渣浆(含CaO)中的S2-并制取硫酸盐的一种常用流程如图。下列说法正确的是( )
A.碱性条件下,氧化性:O>SO>MnO
2 2
B.过程Ⅰ中氧化剂和还原剂物质的量之比为2∶1
C.过程Ⅱ中反应的离子方程式为4MnO+2S2-+9HO===S O+4Mn(OH) ↓+10OH-
2 2 2
D.将1 mol S2-转化为SO理论上需要O 的体积为22.4 L(标准状况)
2
8.锰广泛存在于自然界中,工业可用软锰矿(主要成分是MnO )制备锰。
2
资料:①MnCO 难溶于水,可溶于稀酸。
3
②在Mn2+催化下,SO 在水溶液中被氧化成HSO 。
2 2 4Ⅰ.制备
(1)写出铝热法还原MnO 制备锰的化学方程式:_____________________________________。
2
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度SO 的烟气,可用以下方法处理。
2
方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用 MnO 进行脱硫的化
2
学方程式:__________________________________________________。
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如图所示:
过程 Ⅰ:……
过程 Ⅱ:2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
过程 Ⅰ 的离子方程式是__________________________________________________。
方法二:
③用MnCO 进行脱硫,可提高脱硫率。结合化学用语解释原因:_______________
3
________________________________________________________________________。
Ⅱ.废水中锰含量的测定
(3)取1 mL废水置于20 mL磷酸介质中,加入 HClO ,将溶液中的 Mn2+氧化为Mn3+,用c mol·L-1
4
(NH )Fe(SO ) 溶液进行滴定,达到滴定终点时,滴定管刻度由 V mL变为V mL,废水中锰的含量为
4 2 4 2 0 1
________g·mL-1。
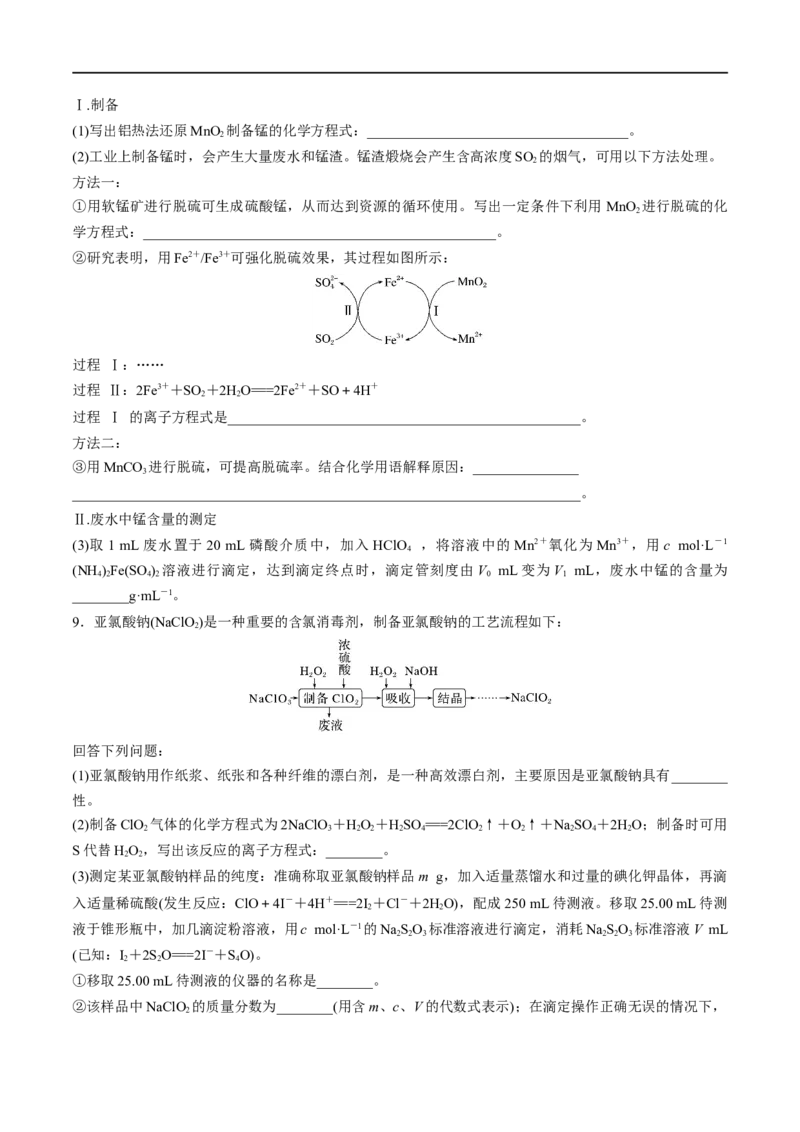
9.亚氯酸钠(NaClO)是一种重要的含氯消毒剂,制备亚氯酸钠的工艺流程如下:
2
回答下列问题:
(1)亚氯酸钠用作纸浆、纸张和各种纤维的漂白剂,是一种高效漂白剂,主要原因是亚氯酸钠具有________
性。
(2)制备ClO 气体的化学方程式为2NaClO +HO +HSO ===2ClO ↑+O↑+NaSO +2HO;制备时可用
2 3 2 2 2 4 2 2 2 4 2
S代替HO,写出该反应的离子方程式:________。
2 2
(3)测定某亚氯酸钠样品的纯度:准确称取亚氯酸钠样品m g,加入适量蒸馏水和过量的碘化钾晶体,再滴
入适量稀硫酸(发生反应:ClO+4I-+4H+===2I +Cl-+2HO),配成250 mL待测液。移取25.00 mL待测
2 2
液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1的NaSO 标准溶液进行滴定,消耗NaSO 标准溶液V mL
2 2 3 2 2 3
(已知:I+2SO===2I-+SO)。
2 2 4
①移取25.00 mL待测液的仪器的名称是________。
②该样品中NaClO 的质量分数为________(用含m、c、V的代数式表示);在滴定操作正确无误的情况下,
2此实验测得结果偏高,其可能的原因是________。