文档内容
第 6 讲 钠及其化合物
【学科核心素养】
1.宏观辨识与微观探析:认识钠及其化合物的性质和应用。能从钠的原子结构及其重要化合物的微观
结构理解其性质,领悟结构决定性质。
2.科学探究与创新意识:了解钠及其化合物的性质探究方案,并积极参与实验探究过程,得出相关结
论。
【核心素养发展目标】
1.能从钠原子的结构(微观)分析认识钠是一种非常活泼的金属,具有很强的还原性(宏观)。
2.设计实验探究钠与氯气、水的反应,会分析钠与酸、碱溶液的反应,促进“证据推理与模型认知”
化学核心素养的发展。
1.从物质类别、元素化合价的角度认识氧化钠与过氧化钠的性质,熟知过氧化钠与水和二氧化碳反应
的应用。
2.会设计实验探究过氧化钠与水的反应,探究并比较碳酸钠与碳酸氢钠的性质,学会焰色试验操作,
增强科学探究与创新意识。
【知识点解读】
知识点一 钠与碱金属
一、钠的性质及应用
1.钠的物理性质
(金属的)通性 个性
颜色 导电性、导热性 熔点 硬度 密度
银白色 良好 低 小 比水的小,比煤油的大
2.从钠原子的原子结构认识钠的化学性质——还原性
Na ―――――――――→Na+
(1)与非金属单质(如O、Cl)的反应
2 2
O
2
Cl:2Na+Cl=====2NaCl
2 2
(2)与水反应
①离子方程式:2Na+2HO===2Na++2OH-+H↑。
2 2
②钠与水(含酚酞)反应的实验现象及解释(3)与盐酸反应
离子方程式:2Na+2H+===2Na++H↑。
2
【特别提醒】Na先与酸反应,再与水反应——先酸后水。
(4)与盐的反应
①Na与盐反应的原理
与熔融盐发生置换反应:
4Na+TiCl =====4NaCl+Ti,Na+KCl=====NaCl+K↑
与熔融盐 4
(Na能够制取K并不能说明Na的还原性比K强,因为K的沸点比Na
低,使K成为蒸气逸出)
与盐溶液反应时先与水反应,生成的碱与盐可能发生复分解反应:
如与CuSO 溶液反应:
4
与盐溶液 先发生2Na+2HO===2NaOH+H↑
2 2
再发生2NaOH+CuSO ===Cu(OH) ↓+NaSO
4 2 2 4
总反应为2Na+2HO+CuSO ===Cu(OH) ↓+NaSO +H↑
2 4 2 2 4 2
②钠与盐溶液反应的分析方法
第一步:钠与水反应生成NaOH和H;
2
第二步:生成的NaOH如果能与溶质反应,则发生的是NaOH与溶质的复分解反应。
生成气体型 钠与NH Cl溶液反应生成H 和NH
4 2 3
生成沉淀型 钠与铜盐、铁盐等溶液反应生成Cu(OH) 或Fe(OH)
2 3
钠与AlCl 稀溶液反应,如果钠量较多,则先生成Al(OH) 沉淀,后沉淀溶
复杂型 3 3
解
(5)与羟基化合物的反应
2Na+2C HOH―→2C HONa+H↑
2 5 2 5 2
(6)钠在空气中的变化过程
过程 现象 反应原理
① 变暗 4Na+O===2Na O
2 2
② 成液 NaO+HO===2NaOH
2 2
③ 结块 2NaOH+CO+9HO===Na CO·10H O
2 2 2 3 2
④ 变成粉末 NaCO·10H O===Na CO+10HO
2 3 2 2 3 2因此,钠久置在空气中,最终变成NaCO 粉末。
2 3
3.钠的制取及保存
(1)制取:化学方程式为2NaCl(熔融)=====2Na+Cl↑。
2
(2)保存:密封保存,通常保存在石蜡油或煤油中。
4.钠的用途
(1)钠钾合金(液态)可用于原子反应堆的导热剂。
(2)用作电光源,制作高压钠灯。
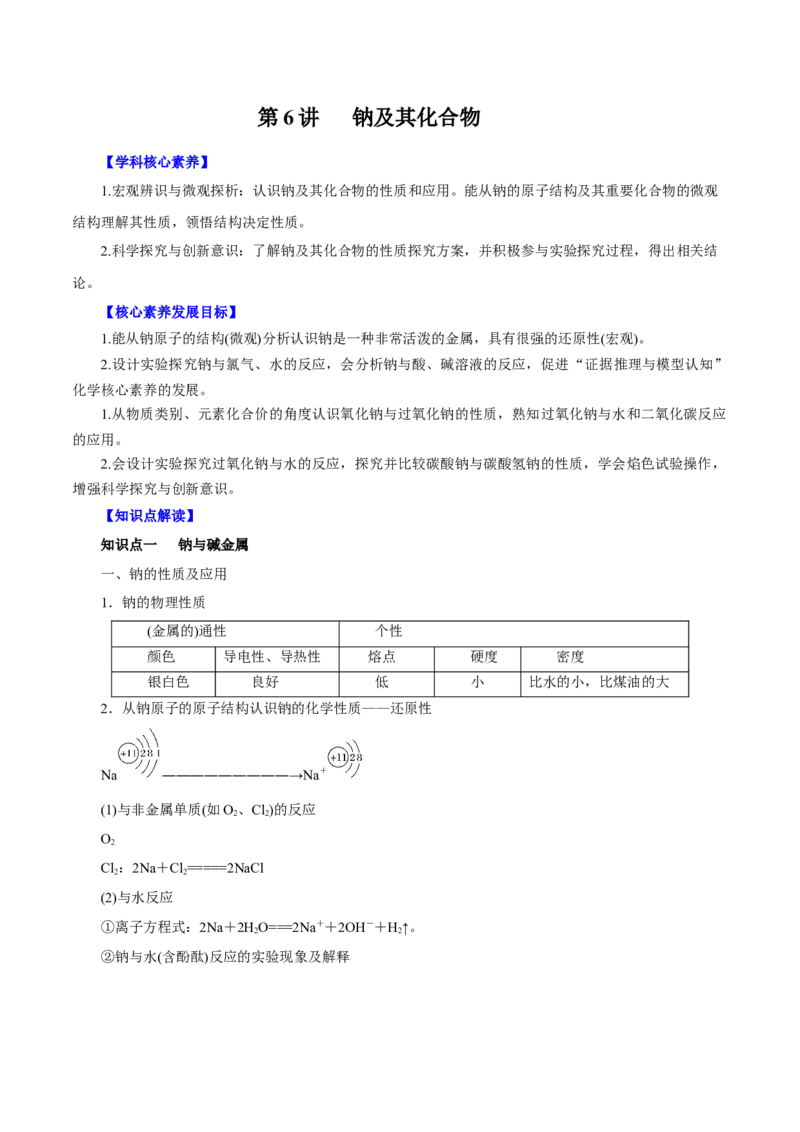
(3)冶炼某些金属
金属钠具有强还原性,熔融状态下可以用于制取金属,如4Na+TiCl =====4NaCl+Ti。
4
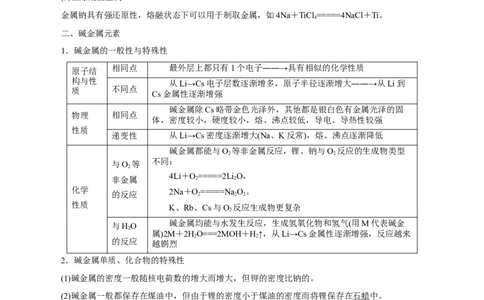
二、碱金属元素
1.碱金属的一般性与特殊性
相同点 最外层上都只有1个电子――→具有相似的化学性质
原子结
构与性 从Li→Cs电子层数逐渐增多,原子半径逐渐增大――→从Li到
质 不同点
Cs金属性逐渐增强
碱金属除Cs略带金色光泽外,其他都是银白色有金属光泽的固
物理 相同点
体,密度较小,硬度较小,熔、沸点较低,导电、导热性较强
性质
递变性 从Li→Cs密度逐渐增大(Na、K反常),熔、沸点逐渐降低
碱金属都能与O 等非金属反应,锂、钠与O 反应的生成物类型
2 2
不同:
与O 等
2
4Li+O=====2LiO,
非金属 2 2
化学 的反应 2Na+O 2 =====Na 2 O 2 。
性质
K、Rb、Cs与O 反应生成物更复杂
2
与HO
碱金属均能与水发生反应,生成氢氧化物和氢气(用M代表碱金
2
属)2M+2HO===2MOH+H↑,从Li→Cs金属性逐渐增强,反应越来
2 2
的反应
越剧烈
2.碱金属单质、化合物的特殊性
(1)碱金属的密度一般随核电荷数的增大而增大,但钾的密度比钠的。
(2)碱金属一般都保存在煤油中,但由于锂的密度小于煤油的密度而将锂保存在石蜡中。
(3)碱金属跟氢气反应生成的碱金属氢化物(如NaH)都是离子化合物,其中氢以H-形式存在,显-1价,
碱金属氢化物是强还原剂。
(4)一般情况下,碱金属所形成的盐均溶于水,并且在一定温度下,酸式盐比正盐的溶解度大(但
NaHCO 的溶解度比NaCO 的小)。
3 2 3
(5)试剂瓶中的试剂取出后,一般不能放回原瓶,但金属Na、K等需立即放回原瓶。
(6)锂与O 反应与钠不同,只生成LiO,而不生成LiO。
2 2 2 2
3.焰色反应(1)焰色反应的概念
某些金属或它们的化合物在灼烧时都会使火焰呈现出特殊的颜色,属于物理变化,是元素的性质。
(2)焰色反应的操作
铂丝――→无色――→待测物――→观察火焰颜色――→铂丝――→无色
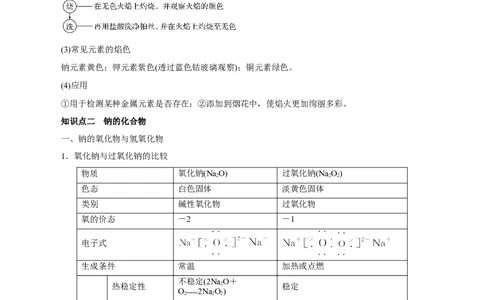
(3)常见元素的焰色
钠元素黄色;钾元素紫色(透过蓝色钴玻璃观察);铜元素绿色。
(4)应用
①用于检测某种金属元素是否存在;②添加到烟花中,使焰火更加绚丽多彩。
知识点二 钠的化合物
一、钠的氧化物与氢氧化物
1.氧化钠与过氧化钠的比较
物质 氧化钠(Na O) 过氧化钠(Na O)
2 2 2
色态 白色固体 淡黄色固体
类别 碱性氧化物 过氧化物
氧的价态 -2 -1
电子式
生成条件 常温 加热或点燃
不稳定(2Na O+
热稳定性 2 稳定
O 2NaO)
2===== 2 2
与水反应 NaO+HO===2NaOH 2NaO+2HO===4NaOH+O↑
化学 2 2 2 2 2 2
性质 与CO 反应 NaO+CO===Na CO 2NaO+2CO===2Na CO+O
2 2 2 2 3 2 2 2 2 3 2
NaO+2HCl===2NaCl+ 2NaO+4HCl===4NaCl+2HO
与酸反应(盐酸) 2 2 2 2
HO +O↑
2 2
强氧化剂、漂白剂、供氧剂、消
主要性质与用途 具有碱性氧化物通性
毒剂,具有强氧化性
2.氢氧化钠
(1)物理性质:NaOH的俗名为烧碱、火碱或苛性钠;它是一种白色固体,易溶于水并放出大量的热,
有吸水性;吸收空气中的水分而潮解;有很强的腐蚀性。(2)化学性质
①具有碱的通性
②其他反应
与金属铝反应:2Al+2OH-+6HO===2Na[Al(OH) ]+3H↑
2 4 2
与非金属单质反应:Cl+2OH-===Cl-+ClO-+HO
2 2
(3)NaOH的制取
①土法制碱:NaCO+Ca(OH) ===CaCO ↓+2NaOH
2 3 2 3
②现代工业制碱:2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
二 、碳酸钠与碳酸氢钠
1.NaCO 和NaHCO 的比较
2 3 3
名称 碳酸钠(Na CO) 碳酸氢钠(NaHCO )
2 3 3
俗名 纯碱或苏打 小苏打
易溶于水,溶液呈碱 易溶于水(但比NaCO 溶解度小),
水溶性 2 3
性 溶液呈碱性
稳定,但结晶碳酸钠 受热易分解,其分解反应的方程式
稳定性
(Na CO·10H O)易风化 为2NaHCO NaCO+CO↑+HO
2 3 2 3===== 2 3 2 2
CO+2H+===HO+
2 HCO+H+===HO+CO↑
与H+反应 CO 2 ↑ 2 2
主
产生CO 气体的速率NaCO