文档内容
训练(十一) 氧化还原反应的配平及计算
1.(2021·河南信阳调研)将Cl 通入400 mL 0.5 mol·L-1 KOH溶液中,二者恰好完全反应
2
得到KCl、KClO、KClO 的混合溶液,经测定ClO-与ClO的物质的量之比是1∶2,则所得混
3
合液中n(KClO)等于( )
3
A.0.014 3 mol B.0.028 6 mol
C.0.143 mol D.0.286 mol
B [Cl 通入KOH溶液中,恰好完全反应生成KCl、KClO、KClO,根据元素守恒,反应
2 3
后的混合液中n(KCl)+n(KClO)+n(KClO)=n(KOH)=0.4 L×0.5 mol/L=0.2 mol;又知ClO
3
-与ClO的物质的量之比是1∶2,设n(KClO)=x mol,推知n(KClO)=2x mol,n(KCl)=(0.2
3
-3x) mol,据得失电子守恒可得:n(KCl)×e-=n(KClO)×e-+n(KClO)×5e-,即(0.2-
3
3x)mol=x mol+2x mol×5,解得x≈0.014 3 mol,从而推知n(KClO)=2×0.014 3 mol=
3
0.028 6 mol。
2.(2021·河南洛阳一中检测)某强氧化剂XO(OH)被NaSO 还原。如果还原2.4×10-3
2 3
mol XO(OH),需用30 mL 0.2 mol·L-1的NaSO 溶液,那么X元素被还原后的价态是( )
2 3
A.-1 B.0
C.+1 D.+2
B [Na SO 还原 2.4×10-3 mol XO(OH)到 X 元素的低价态,则 NaSO 被氧化为
2 3 2 3
NaSO ,反应中S的化合价由+4价升高为+6价,令X元素在还原产物中的化合价为x,由
2 4
得失电子守恒可知,2.4×10-3 mol×(5-x)=0.03 L×0.2 mol·L-1×(6-4),解得x=0。]
3.(2021·陕西西安检测)工业上常利用反应Cr O+CHOH+H+―→Cr3++CO↑+
2 3 2
HO(未配平)来测定工业甲醇中甲醇的含量。下列说法中正确的是( )
2
A.该反应中,氧化产物是CO 和HO
2 2
B.Cr O发生氧化反应
2
C.若配平后Cr3+和CO 的化学计量数比为2∶1,则Cr O中的n=2
2 2
D.若有3.2 g CH OH参加反应,则转移的电子数为6.02×1022
3
C [该反应中,C由-2价升高到+4价,H、O的化合价均未变化,则氧化产物是CO,A
2
项错误;Cr O是氧化剂,发生还原反应,B项错误;若配平后Cr3+和CO 的化学计量数比为
2 2
2∶1,据得失电子守恒可知,参与反应的Cr O和CHOH的物质的量之比为1∶1,则Cr显+
2 3
6价,从而推知Cr O中的n=2,C项正确;3.2 g CH OH为0.1 mol,参加反应时,转移电子为
2 3
0.6 mol,则转移的电子数为3.612×1023,D项错误。]
4.(2021·陕西四校联考)已知NaClO溶液与Ag反应的产物为AgCl、NaOH和O,下列说
2
法正确的是( )
A.氧气是还原产物
B.还原剂与氧化剂的物质的量之比为1∶1
C.反应物中有水,且反应方程式中水的化学计量数为2D.若生成4.48 L(标准状况下)O ,则反应转移0.8 mol电子
2
C [NaClO溶液与Ag反应生成AgCl、NaOH和O,O由-2价升高到0价,则O 是氧
2 2
化产物,A项错误;还原剂是Ag和HO,氧化剂是NaClO,据得失电子守恒可知,还原剂和氧
2
化剂的物质的量之比为3∶2,B项错误;据得失电子守恒、原子守恒配平:4Ag+4NaClO+
2HO===4AgCl+4NaOH+O↑,则水的化学计量数为2,C项正确;生成标准状况下4.48 L
2 2
O(即0.2 mol)时,转移电子为1.6 mol,D项错误。]
2
5.(2021·辽宁省实验中学检测)R O离子在一定条件下可以将Mn2+氧化为MnO,若反应
2
后R O离子变为RO离子,又知反应中氧化剂与还原剂的离子数之比为5∶2,则n的值是(
2
)
A.1 B.2
C.3 D.4
B [R O离子中R元素的化合价为+(16-n)/2,分析题意可知,Mn由+2价升高到+7
2
价,R 元素由+(16-n)/2 价降低到+6 价,则 R O 是氧化剂,Mn2+是还原剂。又知
2
N(R O)∶N(Mn2+)=5∶2,则有n(R O)∶n(Mn2+)=5∶2,根据氧化还原反应中电子得失守恒
2 2
的规律列式:n(R O)×2×[(16-n)/2-6]=n(Mn2+)×(7-2),综合上述两式解得n=2。]
2
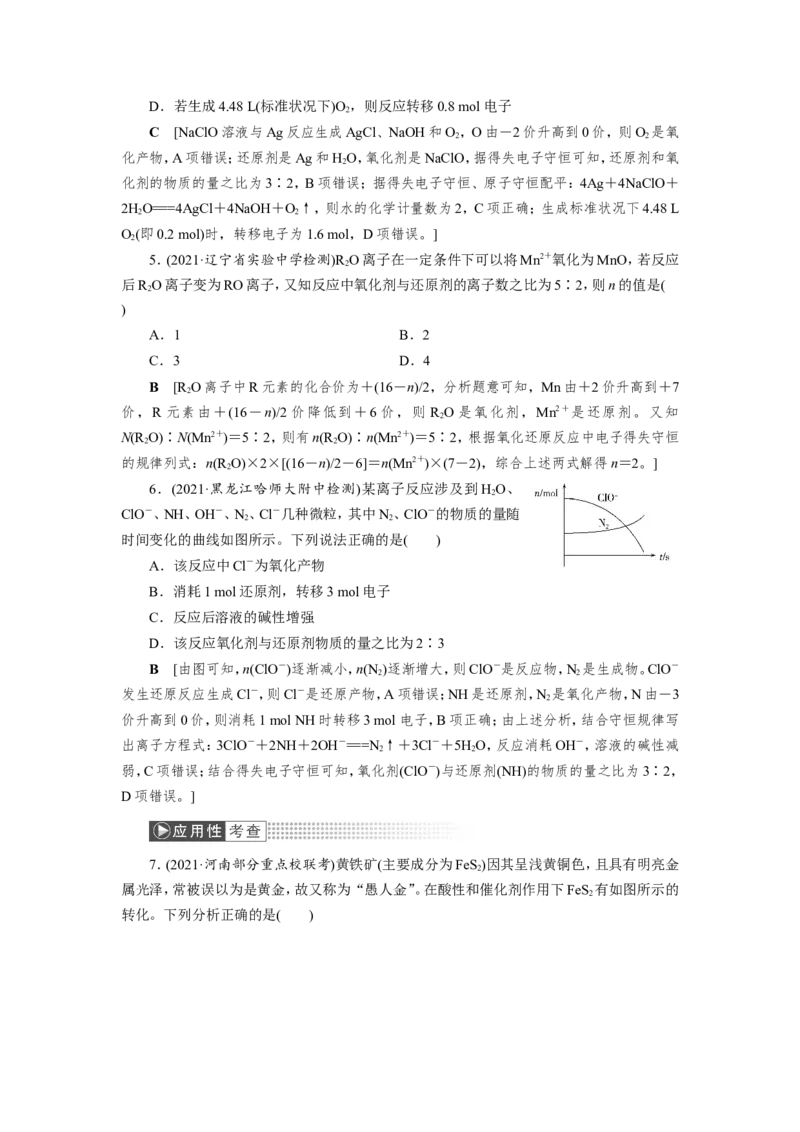
6.(2021·黑龙江哈师大附中检测)某离子反应涉及到HO、
2
ClO-、NH、OH-、N、Cl-几种微粒,其中N、ClO-的物质的量随
2 2
时间变化的曲线如图所示。下列说法正确的是( )
A.该反应中Cl-为氧化产物
B.消耗1 mol还原剂,转移3 mol电子
C.反应后溶液的碱性增强
D.该反应氧化剂与还原剂物质的量之比为2∶3
B [由图可知,n(ClO-)逐渐减小,n(N )逐渐增大,则ClO-是反应物,N 是生成物。ClO-
2 2
发生还原反应生成Cl-,则Cl-是还原产物,A项错误;NH是还原剂,N 是氧化产物,N由-3
2
价升高到0价,则消耗1 mol NH时转移3 mol 电子,B项正确;由上述分析,结合守恒规律写
出离子方程式:3ClO-+2NH+2OH-===N ↑+3Cl-+5HO,反应消耗OH-,溶液的碱性减
2 2
弱,C项错误;结合得失电子守恒可知,氧化剂(ClO-)与还原剂(NH)的物质的量之比为3∶2,
D项错误。]
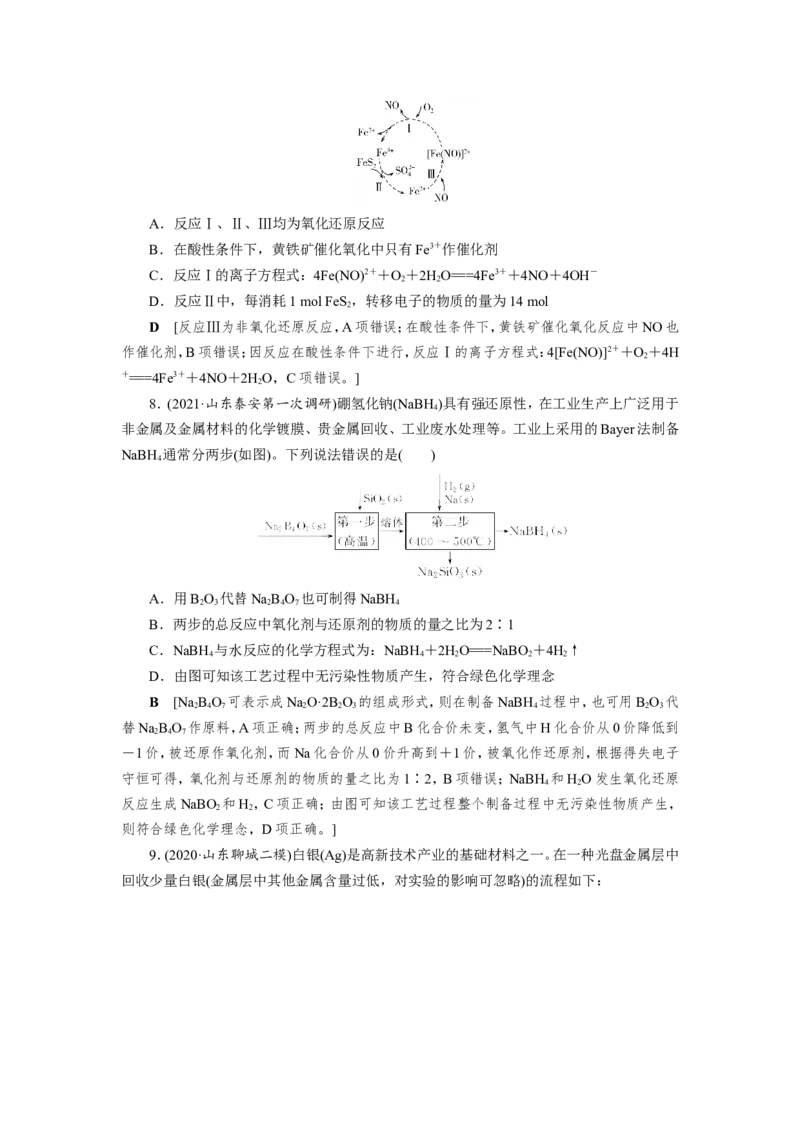
7.(2021·河南部分重点校联考)黄铁矿(主要成分为FeS)因其呈浅黄铜色,且具有明亮金
2
属光泽,常被误以为是黄金,故又称为“愚人金”。在酸性和催化剂作用下FeS 有如图所示的
2
转化。下列分析正确的是( )A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B.在酸性条件下,黄铁矿催化氧化中只有Fe3+作催化剂
C.反应Ⅰ的离子方程式:4Fe(NO)2++O+2HO===4Fe3++4NO+4OH-
2 2
D.反应Ⅱ中,每消耗1 mol FeS ,转移电子的物质的量为14 mol
2
D [反应Ⅲ为非氧化还原反应,A项错误;在酸性条件下,黄铁矿催化氧化反应中NO也
作催化剂,B项错误;因反应在酸性条件下进行,反应Ⅰ的离子方程式:4[Fe(NO)]2++O+4H
2
+===4Fe3++4NO+2HO,C项错误。]
2
8.(2021·山东泰安第一次调研)硼氢化钠(NaBH )具有强还原性,在工业生产上广泛用于
4
非金属及金属材料的化学镀膜、贵金属回收、工业废水处理等。工业上采用的Bayer法制备
NaBH 通常分两步(如图)。下列说法错误的是( )
4
A.用B O 代替NaB O 也可制得NaBH
2 3 2 4 7 4
B.两步的总反应中氧化剂与还原剂的物质的量之比为2∶1
C.NaBH 与水反应的化学方程式为:NaBH +2HO===NaBO +4H↑
4 4 2 2 2
D.由图可知该工艺过程中无污染性物质产生,符合绿色化学理念
B [Na B O 可表示成NaO·2B O 的组成形式,则在制备NaBH 过程中,也可用B O 代
2 4 7 2 2 3 4 2 3
替NaB O 作原料,A项正确;两步的总反应中B化合价未变,氢气中H化合价从0价降低到
2 4 7
-1价,被还原作氧化剂,而Na化合价从0价升高到+1价,被氧化作还原剂,根据得失电子
守恒可得,氧化剂与还原剂的物质的量之比为1∶2,B项错误;NaBH 和HO发生氧化还原
4 2
反应生成NaBO 和H,C项正确;由图可知该工艺过程整个制备过程中无污染性物质产生,
2 2
则符合绿色化学理念,D项正确。]
9.(2020·山东聊城二模)白银(Ag)是高新技术产业的基础材料之一。在一种光盘金属层中
回收少量白银(金属层中其他金属含量过低,对实验的影响可忽略)的流程如下:已知:NaClO溶液在受热或酸性条件下易分解。
下列叙述正确的是( )
A.“氧化”过程若在加强热和强酸性条件下进行时可提高氧化速率
B.“操作1”所用到的玻璃仪器是玻璃棒、烧杯、分液漏斗
C.若“还原”过程通过原电池来实现,则N 为正极产物
2
D.“还原”过程中参加反应的n[Ag(NH)]∶n[N H·H O]=4∶1
3 2 4 2
D [氧化过程加入NaClO,若反应在强酸性或加强热条件下进行,ClO-结合H+生成
HClO,HClO受热则分解为HCl和O,氧化速率反而会降低,A项错误;“操作1”是过滤,
2
用到的玻璃仪器有漏斗、烧杯和玻璃棒,B项错误;还原过程加入NH·HO,生成的N 是氧
2 4 2 2
化产物,若通过原电池来实现,则N 是负极产物,C项错误;还原过程中,Ag由+1价变为0
2
价,NH·HO 中 N 由-2 价升高到 0 价,据得失电子守恒可得,参加反应的
2 4 2
n[Ag(NH)]∶n(N H·HO)=4∶1,D项正确。]
3 2 4 2