文档内容
2023-2024 学年高三第一次月考试卷
化 学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干
净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cl 35.5 Mg24 Fe56
第Ⅰ卷(选择题 共42分)
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学与生产、生活、科技和环境等密切相关。下列有关说法正确的是
A.“光化学烟雾”的形成与氮氧化物有关
B.储氢合金是一类通过物理方法吸附 的新型合金材料
C.为了实现“碳达峰、碳中和”,可对燃煤进行脱硫处理
D.三星堆出土的青铜面具呈红棕色斑迹,是由于铜发生了吸氧腐蚀
2.设N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.N 个 胶粒的质量为107g
A
B. (碳正离子)中含电子数目为10N
A
C.0.1mol乙酸与足量乙醇充分反应生成的乙酸乙酯分子数目为
D.标况下, 和 混合气体完全燃烧,消耗 分子数目可能为
3.下列化学用语正确的是
A.乙烯的结构简式:B.甲基的电子式:
C.基态C原子的轨道表示式:
D.Cr元素的原子结构示意图:
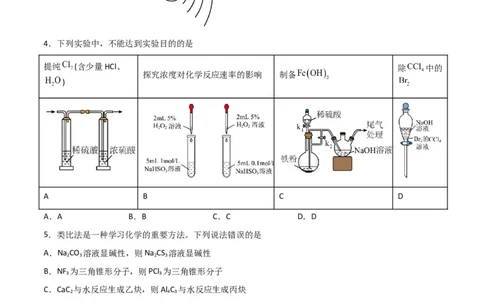
4.下列实验中,不能达到实验目的的是
提纯 (含少量HCl、 除 中的
探究浓度对化学反应速率的影响 制备
)
A B C D
A.A B.B C.C D.D
5.类比法是一种学习化学的重要方法。下列说法错误的是
A.Na CO 溶液显碱性,则Na CS 溶液显碱性
2 3 2 3
B.NF 为三角锥形分子,则PCl 为三角锥形分子
3 3
C.CaC 与水反应生成乙炔,则Al C 与水反应生成丙炔
2 4 3
D.CCl COOH酸性强于CH COOH,则CF COOH酸性强于CCl COOH
3 3 3 3
6.一种化工原料的结构如图所示,其中短周期元素X、Y、Z、R、Q的原子序数依次增大,R、Q处于不同
周期,基态R原子最高能层电子数是基态Y原子最高能层电子数的2倍。下列说法正确的是A.电负性:
B.原子半径:
C.Z与Q形成的化合物均属于非极性分子
D.R与Q形成的一种化合物可用于饮用水消毒
7.下列用于解释事实的方程式书写不正确的是
A.新切开的钠的光亮表面在空气中很快变暗:
B.将 通入苯酚钠溶液中出现浑浊:2 +CO +H O→2 +Na CO
2 2 2 3
C.向 溶液中滴加氨水产生白色沉淀:
D.向 悬浊液中滴加 溶液产生黄色沉淀:
8.下列叙述Ⅰ和Ⅱ均正确且有因果关系的是
选项 叙述Ⅰ 叙述Ⅱ
石墨能导电且化学性质不活
A 外加电流法保护金属可用石墨作辅助阳极
泼
B 氢氟酸是挥发性弱酸 氢氟酸可用于刻蚀玻璃器皿
C 铁的金属性比铜强 溶液可用于铜质印刷电路板的制作
D 难溶于水 可用于治疗胃酸过多
A.A B.B C.C D.D
9.氯气是一种重要的工业原料,工业上利用下列反应来检查氯气管道是否漏气:
。下列说法不正确的是
A.生成物 是离子晶体
B. 的结构式为 , 分子中含有 键和 键
C.可通过原电池将 与 反应的化学能转化为电能
D.该反应氧化剂和还原剂的物质的量之比为3:8
10.化合物Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,可由下列反应制得。下列有关X、Y、Z的说法正确的是
A.1molX最多与 发生加成反应
B.Y与足量HBr反应生成的有机化合物中不含手性碳原子
C.Z在水中的溶解度比Y在水中的溶解度大
D.X、Y、Z分别与足量酸性 溶液反应所得芳香族化合物相同
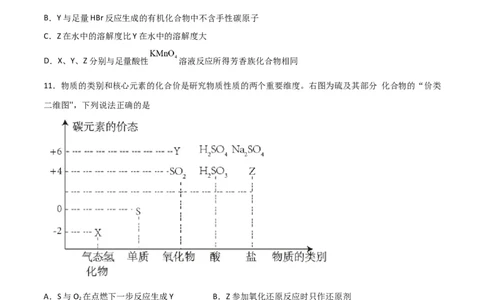
11.物质的类别和核心元素的化合价是研究物质性质的两个重要维度。右图为硫及其部分 化合物的“价类
二维图'',下列说法正确的是
A.S与O 在点燃下一步反应生成Y B.Z参加氧化还原反应时只作还原剂
2
C.X、Y属于非电解质 D.X的水溶液在空气中放置,易被氧化
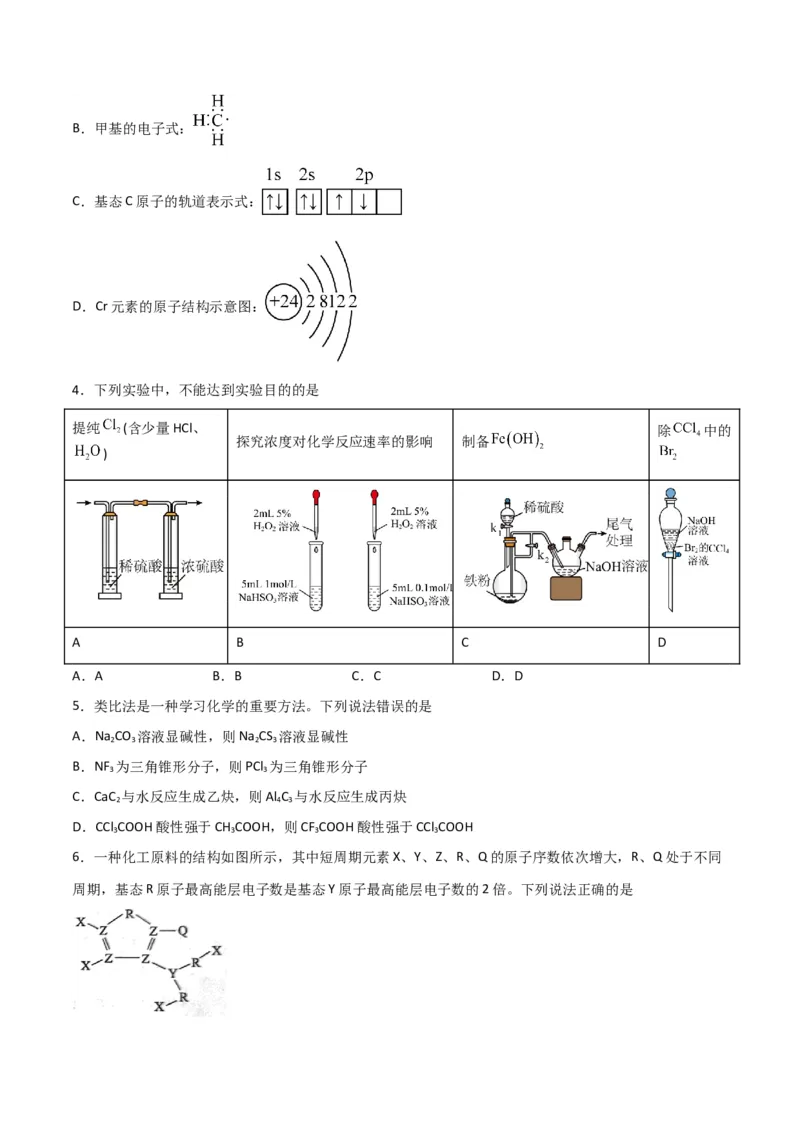
12.温度为T℃,向体积不等的恒容密闭容器中均充入1mol气体X,发生反应:X(g) Y(g)+Z(g)ΔH,反应均
进行10min,测得各容器中X的转化率与容器体积的关系如图所示。下列说法正确的⇌是A.a点再充入一定量的X,X的转化率减小
B.d点有ν =ν
正 逆
C.正反应速率v(b)=v(d)
D.若c点为平衡点,则浓度平衡常数K=0.9
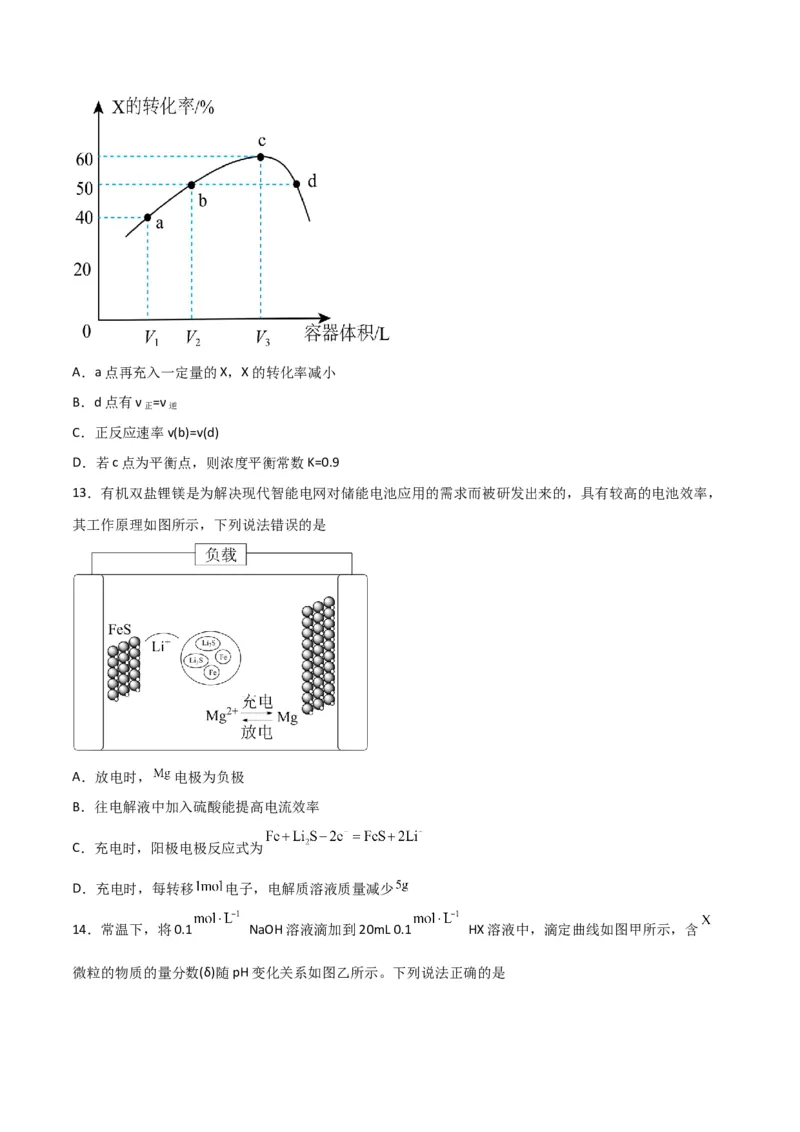
13.有机双盐锂镁是为解决现代智能电网对储能电池应用的需求而被研发出来的,具有较高的电池效率,
其工作原理如图所示,下列说法错误的是
A.放电时, 电极为负极
B.往电解液中加入硫酸能提高电流效率
C.充电时,阳极电极反应式为
D.充电时,每转移 电子,电解质溶液质量减少
14.常温下,将0.1 NaOH溶液滴加到20mL 0.1 HX溶液中,滴定曲线如图甲所示,含
微粒的物质的量分数(δ)随pH变化关系如图乙所示。下列说法正确的是A.b点时
B.图乙中A点对应的
C.c点对应溶液中离子浓度大小关系:
D.d点时,溶液中
第 II 卷(非选择题 共 58 分)
二、非选择题:本题共4个小题,共58分。
15.(14分)三氯化氮是一种黄色油状液体,可用于漂白和杀菌。已知: 熔点为-40℃,沸点为
70℃,95℃以上易爆炸。在弱酸性溶液中稳定,在热水中易水解,遇碱则迅速反应。在实验室可用 和
溶液反应制取 ,所用仪器如图(忽略部分夹持装置):
回答下列问题:(1)根据气流方向,各仪器的连接顺序为a接 , 接 ,g接d;装置A中使用恒压滴液
漏斗的优点是
(2)若用装置A制取氯气,则试剂X可选用 (填字母);D中仪器的名称为
A. B. C. D.
(3)实验过程中,在B中蒸馏烧瓶中观察到的现象是 ,反应生成的 遇热水易水解,反应液有漂
白性.写出 水解的化学方程式:
(4) 纯度测定: 的制取是可逆反应,根据反应 ,利用间接碘量法测定
氯气的量即可测定 的纯度
实验步骤:ⅰ.准确称量C中的产物0.4g置于三颈烧瓶中,加入10mL足量浓盐酸,使用磁力搅拌器搅拌,
并鼓入氮气
ⅱ.将混合气通入200mL KI溶液中,待试管中无色液体变成黄色,关闭氮气(溶液体积变化忽略不
计)
ⅲ.量取20.00mL吸收液,加入淀粉指示剂,用 标准液进行滴定,滴定至终点时消耗
溶液18.00mL。
(已知:反应原理为 )
①确定滴定终点的现象为
② 的纯度为 (保留三位有效数字)
16.(15分)氧化铬(Cr O )可用作着色剂、分析试剂、催化剂等。以含铬废料(含FeCr O 、MgO、SiO 、
2 3 2 4 2
Al O 等)为原料制备氧化铬的一种流程如图所示。
2 3
已知:烧渣的成分为Na CrO 、NaAlO 、Na SiO 、Fe O 、MgO;25℃时,K [Fe(OH) ]=4×10-38、
2 4 2 2 3 2 3 sp 3K [Al(OH) ]=1×l0-33、K [Mg(OH) ]=2×10-11,溶液中离子浓度≤10-5mol·L-1时,认为该离子沉淀完全。回答下列
sp 3 sp 2
问题:
(1)“研磨”的目的是 ;“焙烧”过程发生的氧化还原反应中,氧化剂与还原剂的物质的量之比是
。
(2)25℃时,若滤液l中金属离子的浓度均为0.2mol·L-1,则“调pH”的最小值为 。(保留两位有效数
字)。
(3)“除镁”工序不能在陶瓷容器中进行的原因是 。
(4)“转化”时加入适量H SO 的作用是 。
2 4
(5)“煅烧”反应生成的气体中含有一种单质,该反应的化学方程式 。
(6)已知MgO具有NaCl型晶体结构,其结构如图所示。
则每个Mg2+周围距离最近的Mg2+个数为 。已知MgO晶胞边长为0.4nm,则MgO的密度为
g/cm3(设N 为阿伏加德罗常数的值,只需列出算式)。
A
17.(14分) 转化为高附加值的产品是应对气候变化和能源高速消耗的有效措施,我国科学家研究
加氢制备甲醇方面取得一定进展。在一定温度和压强下, 加氢制备甲醇的过程中主要发生如下三
个反应,反应I、II、III对应的平衡常数分别为 、 和 。
I.
II.
III.
回答下列问题:
(1) ; 、 和 三者之间的关系为 。(2)为提高甲醇的平衡产率,可通过 (填“升高”或“降低”)温度, (填“增大”或
“减小”)压强来实现。
(3)在两种不同的条件下, 的平衡转化率和 的选择性如下表所示。条件 (填“1”或
“2”)中甲醇的产率更高。
条件 的平衡转化率/% 的选择性/%
1 27 68
2 21.3 97.7
(4)T℃时,将 的混合气体充入压强为 的恒压密闭容器中,在催化剂的作用下发生
如下两个反应:
①
②
反应达到平衡状态时, 和 的分压相等,甲醇的选择性是CO的2倍,则 的平衡转化率为
,反应②的 (列出计算式即可,分压=总压×物质的量分数)。
(5)某甲醇燃料电池,电极材料为铂,电解质溶液为KOH溶液。写出负极电极反应式: ;铂电
极除了起导电作用外,还起着 作用。
18.(15分)丹皮酚(G)具有抗心律失常、增强免疫力等多种药理作用,一种合成丹皮酚及其衍生物H的合
成路线如下:
回答下列问题:
(1)A的化学名称为 ,C中的官能团名称为 。(2)每个D分子中含有 个手性碳(连有4个不同的原子或基团的碳原子称为手性碳)。
(3)反应②的反应类型为 ,反应④的化学方程式为 。
(4)芳香化合物X是G的同分异构体,满足下列条件的X共有 种 。
①与NaHCO 溶液反应放出CO
3 2
②与FcCl 溶液显色
3
③苯环上有两个取代基
其中,符合上述条件的X中,核磁共振氢谱峰面积比为3∶2∶2∶1∶1∶1的结构简式为 。
(5)根据上述路线中的有关知识,由甲醇、环己醇和丙氨酸( )为主要原料,设计制备
的合成路线: 。