文档内容
第十一章 有机化学基础
能力提升检测卷
时间:90分钟 分值:100分
可能用到的相对原子质量:H 1 C 12 O16 Na 23 Al 27 P 31 S 32 Cl 35.5 K 39 Ca 40
Fe 56 Cu 64 Zn 65 As 75 Cd 112
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2022·山东·模拟预测)某同学进行乙酸与乙醇的酯化反应实验,操作如下:向试管I中依次加入5mL
无水乙醇和5ml冰醋酸,滴入3滴浓硫酸,塞紧橡胶塞,大火加热试管I5分钟,将试管I产生的气体通过
导气管通到盛有饱和碳酸钠溶液的试管II底部。实验中存在的错误有几处?
A.1 B.2 C.3 D.4
【答案】C
【解析】第1处错误:混合液加热需要加入沸石,防止暴沸;第2处错误:一开始加热进行酯化反应时,
由于反应物乙醇、乙酸易挥发,故开始反应时需要小火均匀加热,后大火蒸出产物;第3处错误:试管I
产生的气体不能通过导气管通到盛有饱和碳酸钠溶液的试管II底部,试管Ⅰ产生的气体通入到饱和碳酸钠
溶液液面上方,防止倒吸,即导气管的管口接近饱和NaCO 溶液的液面、但不能伸入饱和NaCO 溶液中;
2 3 2 3
共3处错误;答案选C。
2.(2022·浙江·模拟预测)下列说法正确的是
A.聚氯乙烯薄膜可以用来包装食品
B.天然气是高热值的清洁能源
C.可降解餐具用聚乳酸制造,聚乳酸是一种天然高分子材料
D.高纤维食物是富含膳食纤维的食物,在人体内都可通过水解反应提供能量
【答案】B
【解析】A.聚乙烯属于无毒高分子,而聚氯乙烯有毒,所以不能用聚氯乙烯替代聚乙烯生产食品保鲜膜、
塑料水杯等生活用品,故A错误;
B. 天然气的主要成分是甲烷,甲烷含氢量高、是高热值的清洁能源,故B正确;C. 可降解餐具用聚乳
酸制造,聚乳酸是一种人工合成的高分子材料、不是天然高分子材料,故C错误;D.人体内没有纤维素
酶,纤维素在人体内不能被水解,故D错误;答案选B。
3.(2021·河北·石家庄二中模拟预测)某羧酸酯的分子式为C H O,1mol该酯完全水解可得到1mol羧
18 26 5
酸和2mol乙醇,该羧酸的分子式为A.C H O B.C H O C.C H O D.C H O
16 22 5 16 20 5 14 18 5 14 16 4
【答案】C
【解析】某羧酸酯的分子式为C H O,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,说明酯中含有
18 26 5
2个酯基,设羧酸为M,则反应的方程式为C H O+2H O= M+2C HO,由质量守恒可知M的分子式为
18 26 5 2 2 6
C H O,答案选C。
14 18 5
4.(2022·山东·泰安一中模拟预测)甲烷经过一系列反应后能够合成 ,合成路线如图所示。
下列说法错误的是
A.步骤2的反应类型为取代反应
B.可用红外光谱鉴别甲醇和甲醛
C.0.1mol HCHO与足量银氨溶液反应最多生成21.6gAg
D.步骤3的反应条件和所需试剂为加热、氧化铜
【答案】C
【解析】A.CHCl+NaOH CHOH+NaCl,该反应属于卤代烃的水解,又属于取代反应,A错误;
3 3
B.甲醇中含有羟基,甲醛中为醛基,可以用红外光谱鉴别,B正确;C.根据HCHO+4Ag(NH )OH
3 2
(NH )CO+4Ag↓+6NH+2H O,可知HCHO~4Ag↓,0.1mol HCHO与足量银氨溶液反应最多生
4 2 3 3 2
成0.1mol×4×108g/mol=43.2g,C错误;D.甲醇变甲醛属于醇氧化为醛,氧化剂为氧化铜,条件加热,D
正确;故选C。
5.(2022·江苏淮安·模拟预测)有机物Z为是合成某药物的重要中间体,可由下列反应制得。
下列有关化合物X、Y和Z的说法正确的是
A.1molX中含有6mol碳氧σ键
B.Y分子含有三种官能团C.X、Y可用酸性KMnO 溶液鉴别
4
D.Z分子与足量H 加成后的产物中含有3个手性碳原子
2
【答案】B
【解析】A.X中每1个O可形成2个碳氧键,但该有机物中有一个醛基,为1个碳氧双键,故1molX中
含有5mol碳氧σ键,A项错误;B.Y分子中有醚键、羰基、碳碳双键三种官能团,B项正确;C.X中含
有的醛基可使高锰酸钾溶液褪色,Y中碳碳双键可使高锰酸钾溶液褪色,故X、Y不能用高锰酸钾溶液鉴
别,C项错误;D.Z分子与足量H 加成后的产物的结构简式为 ,含有4个手性碳原子,D
2
项错误;答案选B。
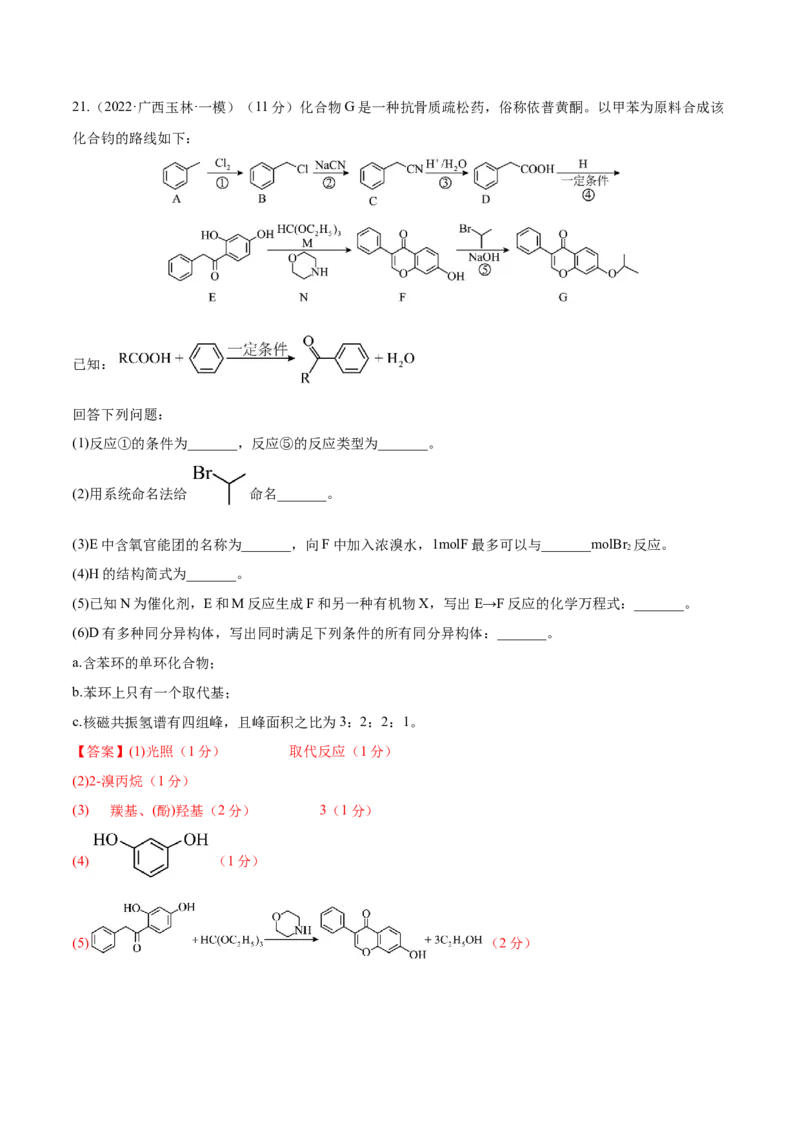
6.(2022·湖北·华中师大一附中模拟预测)脲醛树脂(UF)可用于生产木材黏合剂、生活器具和电器开关。
尿素( )和甲醛在一定条件下发生类似苯酚和甲醛的反应得到线型脲醛树脂,再通过交联形
成网状结构,其结构片段如图所示(图中 表示链延长),下列说法错误的是
A.脲醛树脂难溶于水
B.形成线型结构的过程发生了缩聚反应
C.脲醛树脂合成过程中可能存在中间体
D.脲醛树脂在一定条件下可以发生水解反应,重新生成尿素和甲醛【答案】D
【解析】A.脲醛树脂为高分子材料,难溶于水, A选项正确;B.尿素和甲醛先发生加成反应,后再发
生聚合反应,生成物有小分子水,属于缩聚反应,B选项正确;C.尿素和甲醛发生加成反应,生成
,C选项正确;D.交联脲醛树脂存在可水解基团酰胺键(肽键),故可发生水解,
但水解产物不是尿素和甲醛,故D错误。
答案选D。
7.(2022·青海西宁·二模)人们将有机物中连有四个不同原子(或基团)的碳原子称为手性碳原子。某有机
物的结构简式如图所示,下列关于该有机物的叙述正确的是
A.该分子中含有1个手性碳原子
B.在一定条件下可与HCHO发生缩聚反应
C.该物质遇FeCl 溶液不发生显色反应
3
D.1mol该物质与足量NaOH溶液反应,消耗NaOH的物质的量为3mol
【答案】B
【解析】A.该有机物中没有连有四个不同原子(或基团)的碳原子,即没有手性碳原子,故A项错误;B.
该物质有酚羟基,会影响苯环上邻位上的氢,使邻位上H变的更活泼,更容易反应,所以反应时相当于苯
环是还有两个半键,而甲醛中的碳氧双键同时断开,与苯环是的俩个半键结合,发生缩聚反应,故B项正
确;C.该物质有酚羟基,遇FeCl 溶液发生显色反应(显紫色),故C项错误;D.酚羟基和酯基均可以与
3
氢氧化钠反应,故1mol该物质与足量NaOH溶液反应,消耗NaOH的物质的量为2mol,故D项错误;故
答案选B。
8.(2022·上海上海·模拟预测)四氯乙烯是一种衣物干洗剂,以下不是它的性质
A.易挥发 B.所有原子共平面 C.易溶于水 D.不能发生加成反应
【答案】C
【解析】A.四氯乙烯易溶于有机溶剂,较易挥发,可作为干洗剂,A不符合题意;B.四氯乙烯可看作是
乙烯中的四个氢原子被四个氯原子取代,乙烯分子中的所有原子共平面,则四氯乙烯的所有原子也共平面,
B不符合题意;C.四氯乙烯为卤代烃,难溶于水,C符合题意;D.四氯乙烯含有碳碳双键,能发生加成
反应,D不符合题意;故选C。9.(2022·广西柳州·模拟预测)国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚( )、
75%乙醇、含氯消毒剂过氧乙酸( )、氯仿( )等均可有效灭活病毒。对于上述化学药品,
下列说法错误的是
A.氯仿与水互不相溶
B.乙醇与乙醚互为同分异构体
C.NaClO比HClO稳定
D.过氧乙酸主要通过氧化灭活病毒
【答案】B
【解析】A.氯仿属于氯代烃,不溶于水,与水互不相溶,故A正确;B.乙醇与乙醚的分子式不同,不
可能互为同分异构体,故B错误;C.次氯酸钠遇光不易发生分解反应,次氯酸遇光易发生分解反应,所
以次氯酸钠比次氯酸稳定,故C正确;D.过氧乙酸中含有过氧链,主要通过氧化灭活病毒,故D正确;
故选B。
10.(2022·北京·杨镇第一中学模拟预测)下列方法不能区分苯与乙醇的是
A.燃烧 B.与金属钠反应
C.观察颜色 D.观察在水中的溶解性
【答案】C
【解析】A.燃烧时苯有浓烟而乙醇无烟,二者现象各不相同,可鉴别,A不合题意;B.乙醇与金属钠反
应产生大量的气泡,而苯不能,可鉴别,B不合题意;C.从颜色看,苯和乙醇都是无色液体,无法从颜
色区别,C符合题意;D.从溶解性看,溴和乙醇与水混溶,苯不溶于水,但可萃取溴,使溶液分层,故
可区分,D不合题意;故答案为:C。
11.(2022·江苏泰州·模拟预测)乙醚、75%乙醇、过氧乙酸(CHCOOOH)、氯仿等化学药品均可有效灭活
3
新冠病毒。下列说法正确的是
A.乙醚可由2分子乙醇脱水制得 B.乙醇通过氧化灭活病毒
C.过氧乙酸中O原子均为-2价 D.氯仿的化学名称是二氯甲烷
【答案】A
【解析】A.乙醚可由2分子乙醇在浓硫酸存在条件下加热140℃发生分子间脱水制得,A正确;B.乙醇
通过使病毒脱水而灭活病毒,不具有强氧化性,B错误;C.过氧乙酸分子中羰基O原子为-2价,另外过
氧链中的两个O原子均为-1价,C错误;D.氯仿的化学名称是三氯甲烷,D错误;故合理选项是A。
12.(2022·辽宁·渤海大学附属高级中学模拟预测)实验室制备1-溴丁烷的原理为CHCHCHCHOH+
3 2 2 2NaBr+ H SO CHCHCHCHBr+NaHSO + H O,其中副产物有1-丁烯、丁醚和溴化氢,某同学设计
2 4 3 2 2 2 4 2
的实验装置(夹持装置已略去)如图所示,其中B、C装置为部分副产物的检验装置。下列说法不正确的是
A.使用玻璃棒搅拌的目的是使反应物充分反应,提高反应速率
B.装置B的作用是检验副产物中的溴化氢
C.装置C用于检验副产物1-丁烯,其中盛放的试剂可以是溴水
D.装置D冷凝时,冷水从c处流入
【答案】D
【解析】本实验欲使用丁醇制备1-溴丁烷,实验中利用A装置进行反应,装置A中的搅拌棒用于搅拌混合
反应物使反应物充分的反应,随着反应的进行1-溴丁烷蒸出在D的冷凝下液化流入到E的锥形瓶中。装置
B可用于检验副产物中的溴化氢,装置B中的硝酸银溶液可以与溴化氢反应生成淡黄色的溴化银沉淀;装
置C用于检验1-丁烯,装置C可盛装溴水、酸性高锰酸钾溶液等。A.使用玻璃棒搅拌的目的是使反应物
充分混合反应,从而达到提高反应速率的目的,A正确;B.硝酸银与溴化氢反应生成溴化银淡黄色沉淀,
装置B的作用是检验副产物中的溴化氢,B正确;C.装置C用于检验副产物1-丁烯,其中盛放的试剂可
以是溴水,烯烃与溴发生加成反应,溶液褪色,C正确;D.装置D冷凝时,冷水从d处流入,冷凝水需
要下进上出,D错误;答案选D。
13.(2022·天津河西·三模)下列关于2-溴丁烷结构与性质的实验叙述不正确的是
A.2-溴丁烷中C-Br键较C-C键的键长短但极性大,故易断裂
B.用NaOH水溶液、AgNO 溶液、硝酸可鉴定其含有溴元素
3
C.用水、酸性KMnO 溶液可鉴定其发生消去反应的有机产物
4
D.与NaOH的乙醇溶液在加热条件下反应,有机产物可能有三种不同的结构
【答案】A
【解析】A.溴原子的原子半径大于碳原子,则2-溴丁烷中C-Br键的键长比C-C键的键长要长,故A
错误;B.2-溴丁烷在氢氧化钠溶液中共热会发生水解反应生成溴化钠,加入稀硝酸中和氢氧化钠溶液排
出氢氧根离子对溴离子检验的干扰,加入硝酸银溶液会有淡黄色沉淀生成,则用氢氧化钠水溶液、硝酸银溶液、硝酸可鉴定2-溴丁烷中含有溴元素,故B正确;C.一定条件下密度比水大的2-溴丁烷发生消去
反应生成密度比水小的1—丁烯或2—丁烯,用水分离2-溴丁烷和1—丁烯或2—丁烯后,向上层1—丁烯
或2—丁烯中加入酸性高锰酸钾溶液,溶液会褪色,则用水、酸性高锰酸钾溶液可鉴定2-溴丁烷发生消去
反应生成的1—丁烯或2—丁烯,故C正确;D.2-溴丁烷与氢氧化钠的乙醇溶液在加热条件下反应时,2
-溴丁烷可能发生消去反应生成1—丁烯或2—丁烯,也可能因反应生成的水得到氢氧化钠溶液,与氢氧化
钠溶液发生水解反应生成2—丁醇,所得产物可能为1—丁烯、2—丁烯、2—丁醇,可能有3种,故D正确;
故选A。
14.(2022·上海上海·二模)化学法镀银的过程如下:
Ⅰ.向容器中加入一定量2%AgNO 溶液,边振荡边滴加2%氨水至沉淀恰好完全溶解;Ⅱ.加入10%葡萄糖
3
溶液至充满容器,在60~70℃水浴中加热,片刻后容器内壁便镀上一层银。
下列说法正确的是
A.该实验证明葡萄糖与甲醛、乙醛等互为同系物
B.步骤Ⅰ后的溶液中大量存在Ag+、 和
C.步骤Ⅱ可使用酒精灯直接加热以加快银的析出
D.可用硝酸洗涤除去容器壁上的银
【答案】D
【解析】A.该实验只能证明葡萄糖分子中含有醛基,但不能证明其与甲醛、乙醛等互为同系物,A不正
确;B.步骤Ⅰ中,AgNO 与氨水反应生成AgOH和NH NO ,AgOH再溶于氨水生成Ag(NH)OH,所以
3 4 3 3 2
溶液中不存在大量的Ag+,B不正确;C.步骤Ⅱ中,若使用酒精灯直接加热,则反应速率过快,生成的银
在试管内壁附着不均匀,且易脱落,C不正确;D.银能与硝酸反应从而发生溶解,所以可用硝酸洗涤容
器壁上的银,D正确;故选D。
15.(2022·北京育才学校三模)探究乙醛的银镜反应,实验如下(水浴加热装置已略去,水浴温度均相同)。
已知:i.银氨溶液用2%AgNO 溶液和稀氨水配制
3
ii.[Ag(NH )]++2H O Ag++2NH·H O
3 2 2 3 2
序 ⇌
① ② ③ ④
号装
置
现 d中较长时间无银镜产生,e中有银
一直无明显现象 8min有银镜产生 3min有银镜产生
象 镜产生
下列说法不正确的是A.a与b中现象不同的原因是[Ag(NH)]+能氧化乙醛而Ag+不能
3 2
B.c中发生的氧化反应为CHCHO+3OH--2e-=CH COO-+2H O
3 3 2
C.其他条件不变时,增大pH能增强乙醛的还原性
D.由③和④可知,c与d现象不同的原因是c(Ag+)不同
【答案】A
【解析】A.对比a、b,除了银离子与银氨离子的差别外,两者的pH不同。且b中碱性更强,a未发生银
镜反应也可能由于碱性不够,因此无法得出银离子不能氧化乙醛。A选项错误;B.B选项正确;C.对比
b、c,c中增大pH银镜产生得更快,说明增大pH增强乙醛的还原性。C选项正确;D.对比c、d,其他
条件相同而d中NH 更多,导致平衡 正向移动,Ag+减少d无银镜。当e中补加
3
AgNO 时出现了银镜,正好验证了这一说法。D选项正确。答案选A。
3
16.(2022·山东聊城·一模)有机物M( 甲基 氯丁烷)常用作有机合成中间体,存在如图转化关系,
下列说法正确的是
A.N可能具有顺反异构
B.L中含有手性碳原子
C.L一定能被氧化为醛或酮
D.M的同分异构体中,含两种化学环境氢的只有1种
【答案】D【解析】由图给转化关系可知,2—甲基—2—氯丁烷在氢氧化钠醇溶液中共热发生消去反应生成2—甲基
—1—丁烯或2—甲基—2—丁烯,则N为2—甲基—1—丁烯或2—甲基—2—丁烯;2—甲基—1—丁烯或2
—甲基—2—丁烯在催化剂作用下与水发生加成反应生成2—甲基—2—丁醇,则L为2—甲基—2—丁醇;2
—甲基—2—丁醇与浓盐酸共热发生取代反应生成2—甲基—2—氯丁烷。A.2—甲基—1—丁烯或2—甲基
—2—丁烯中碳碳双键中两个碳原子都连接两个相同的原子或原子团,该分子没有顺反异构,故A错误;
B.2—甲基—2—丁醇中不含有连接4个不同原子或原子团的手性碳原子,故B错误;C.2—甲基—2—丁
醇中与羟基相连的碳原子上没有连接氢原子,不能发生氧化反应生成醛或酮,故C错误;D.2—甲基—2
—氯丁烷的同分异构体中,只有2,2—二甲基—1—氯丙烷分子中含有两种化学环境氢,故D正确;答案
选D。
二、主观题(共5小题,共52分)
17.(2021·安徽合肥·一模)(10分)乙烯产量是衡量一个国家石油化工水平的重要标志。回答下列问题:
(1)实验室可用乙醇与浓硫酸共热制取乙烯,乙醇所含官能团的名称为_______。
(2)一种由乙烯制备聚丙烯酸甲酯的合成路线如图:
① 的反应类型是_______。
②D的结构简式为_______,与E具有相同官能团的同分异构体还有_______种。
③出由E合成聚丙烯酸甲酯的化学方程式_______。
【答案】(每空2分)(1)羟基
(2)①氧化反应 ② 4 ③nCH=CHCOOCH
2 3
【解析】(1)乙醇的结构简式为CHCHOH,所含官能团的名称为羟基;
3 2
(2)① 是丙烯发生氧化反应生成丙烯醛,反应类型是氧化反应;
②D与甲醇在浓硫酸催化下发生酯化反应生成丙烯酸甲酯和水,则D为丙烯酸,其结构简式为
,E为 ,与E具有相同官能团的同分异构体的还有HCOOCH=CHCH 、
3HCOOCH CH=CH、HCOOC(CH )=CH 、CHCOOCH=CH 共4种;
2 2 3 2 3 2
③由E合成聚丙烯酸甲酯的化学方程式为nCH=CHCOOCH 。
2 3
18.(2021·全国·高三专题练习)(8分)某有机物的结构简式如图所示
(1)该有机物含有的官能团有___。
(2)1mol该有机物与足量H 反应,消耗H 的物质的量为___。
2 2
(3)1mol该有机物与足量Na反应,消耗Na的物质的量为___。
(4)1mol该有机物与足量NaOH反应,消耗NaOH的物质的量为__。
【答案】(每小题2分)(1)—C≡C—、—OH、—COO—、—COOH(每个0.5分)
(2)5mol
(3)2mol
(4)3mol
【解析】(1)该有机物含有的官能团有—C≡C—、—OH、—COO—、—COOH。
(2)1mol碳碳三键和2mol氢气加成,1mol苯环和3mol氢气加成,故1mol该有机物共需要5mol氢气。
(3)1mol-OH和1molNa反应,1mol-COOH和1molNa反应,故1mol该有机物共需要2molNa。
(4)1mol酚酯基和2molNaOH反应,1mol-COOH和1molNaOH反应,故1mol该有机物共需要3molNaOH。
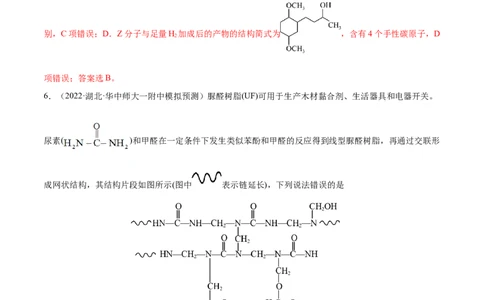
19.(2021·全国·高三专题练习)(12分)苯基环丁烯酮( PCBO)是一种十分活泼的
反应物,可利用它的开环反应合成一系列多官能团化合物。近期我国科学家报道用PCBO与醛或酮发生
[4+2]环加成反应,合成了具有生物活性的多官能团化合物(E),部分合成路线如图:已知如下信息:
回答下列问题:
(1)A的化学名称是_______。
(2)B的结构简式为_______。
(3)由C生成D所用的试剂和反应条件为_______;该步反应中,若反应温度过高,C易发生脱羧反应,生
成分子式为C HO 的副产物,该副产物的结构简式为_______。
8 8 2
(4)M为C的一种同分异构体。已知:1 mol M与饱和碳酸氢钠溶液充分反应能放出2 mol二氧化碳;M与
酸性高锰酸钾溶液反应生成对苯二甲酸。M的结构简式为_______。
(5)对于 ,选用不同的取代基R',在催化剂作用下与PCBO发生的[4+2]反应进行深入研究,
R'对产率的影响见表:
R' -CH -C H -CHCHC H
3 2 5 2 2 6 5
产率/% 91 80 63
请找出规律,并解释原因_______。
【答案】(每空2分)(1)2-羟基苯甲醛(或水杨醛)
(2)(3) 乙醇、浓硫酸/加热
(4)
(5)随着R'体积增大,产率降低
【解析】(1)根据 的结构特点可知该物质的名称为2-羟基苯甲醛;
(2)由题给的苯甲醛与乙醒反应的信息及酚羟基能与NaOH反应可知,B的结构简式为B为
;
(3)由C D 的结构变化可知该反应为酯化反应,所以反
应所用的试剂为浓硫酸与乙醇,反应条件为加热;根据副反应的特点为“脱羧”,而副产物分子式为
C HO,可知该副产物的结构简式为 ;
8 8 2
(4)C的分子式为C HO,根据“1 mol M与饱和碳酸氢钠溶液充分反应能放出2 mol二氧化碳”可知含有2
9 8 4
个—COOH,“与酸性高锰酸钾溶液反应生成对苯二甲酸”可知其结构为 ;
(5)由题给表格中的信息可知,R'的相对分子质量越大(体积越大),产物的产率越低,原因是R'体积越大,
位阻越大,越不容易与PCBO发生[4+2]反应;
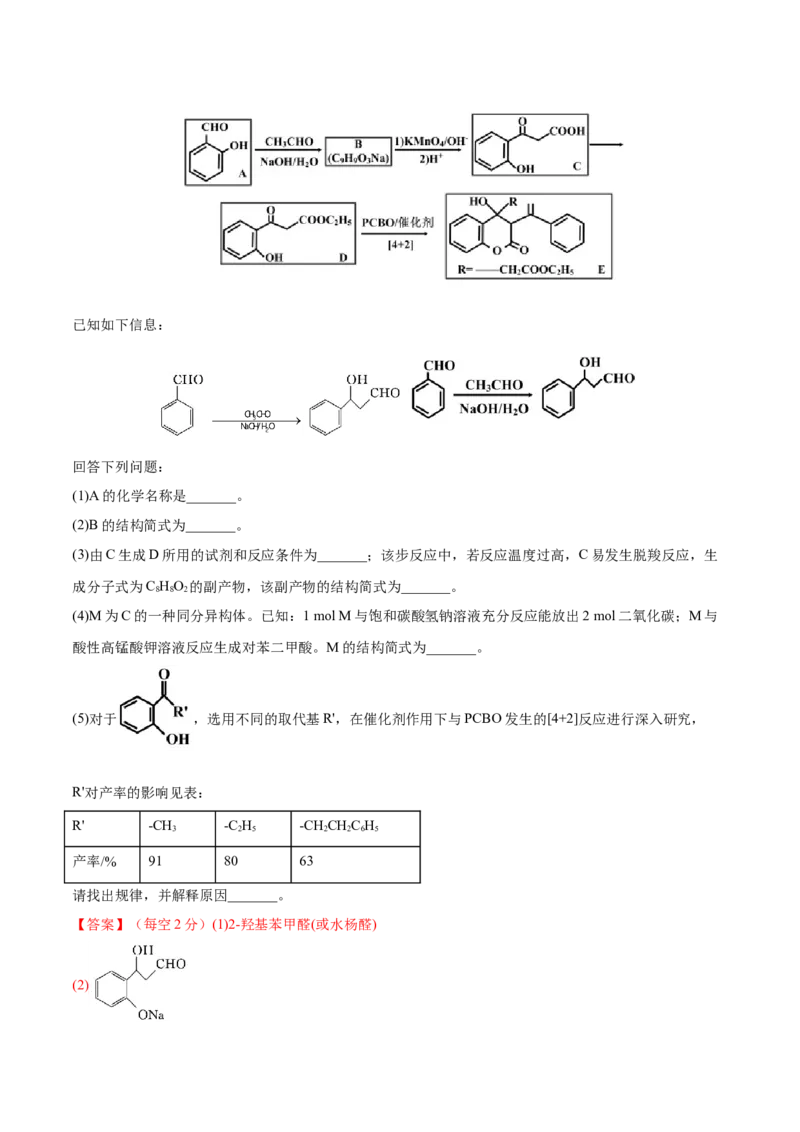
20.(2022·宁夏·石嘴山市第三中学三模)(11分)肉桂酸( )主要用于香精香料、食品添加剂、
医药工业、美容、农药有机合成等方面。实验室可通过如下反应合成,实验装置如图所示:主反应: +(CH CO) O(乙酸酐) +CH COOH
3 2 3
副反应: (树脂状物)
实验所用药品信息如表所示:
名称 相对分子质量 熔点/℃ 沸点/℃ 密度/g mL-1 溶解性
乙酸 60 16.6 117.9 1.05 能与冷水任意比互溶
苯甲醛 106 -26 179 1.06 微溶于水,与苯,乙醇、乙醚混溶
乙酸酐 102 -73.1 138.6 1.082 能溶于冷水
不溶于冷水,易溶于苯、乙醚,在热
肉桂酸 148 133 300 1.248
水中溶于乙醇
实验步骤:
Ⅰ.将7.00g无水KCO、14.5mL乙酸酐和5.0mL苯甲醛依次加入150mL仪器a中,加热至微沸后保持温度
2 3
150-170℃加热回流30-45min。
Ⅱ.将反应后的混合物冷却,边搅拌边分次加入40mL水浸泡。
Ⅲ.连接水蒸气蒸馏装置将未完全反应的苯甲醛用水蒸气蒸馏除去。
Ⅳ.将仪器a冷却,加入40mL10%NaOH溶液,使所有的肉桂酸形成钠盐而溶解。加入90mL蒸馏水,将混
合物加热,活性炭脱色,趁热过滤除去树脂状物,将滤液冷却至室温以下。
Ⅴ.边搅拌边将20mL浓盐酸和20mL水的混合物加到肉桂酸盐溶液中至呈酸性。用冷水冷却,待结晶完全
后抽滤得到粗产品,粗产品经进一步提纯后,得到3.56g产品。
回答下列问题:
(1)仪器a的名称为 _______,仪器b的作用为 _______。
(2)冷却水的入口为 _______(填“m”或“n”)。(3)水蒸气蒸馏将苯甲醛完全除去的标志是_______。
(4)步骤Ⅳ趁热过滤的目的是 _______。
(5)加入浓盐酸与水的混合物后发生反应的化学方程式为 _______。
(6)将粗产品提纯的操作名称为_______ ;本实验中肉桂酸的产率为_______%(保留三位有效数字)。
【答案】(1)三颈烧瓶(1分) 冷凝回流(1分)
(2)n(1分)
(3)冷凝器中无油状馏出液(1分)
(4)分离出活性炭,防止温度降低使肉桂酸盐析出而损耗(2分)
(5)HCl+ →NaCl+ (2分)
(6)重结晶(1分) 48.1%(2分)
【解析】利用苯甲醛和乙酸酐在碳酸钾作用下加热到150-170℃条件下反应制肉桂酸( ),加
热回流30-45min,将反应后的混合物冷却,边搅拌边分次加入40mL水浸泡,连接水蒸气蒸馏装置将未完
全反应的苯甲醛用水蒸气蒸馏除去,用NaOH溶液处理提纯后进行产品纯度测定,计算产率。
(1)仪器a为三颈烧瓶,仪器b为冷凝管,作用是冷凝回流,使反应物充分反应,故答案为:三颈烧瓶;冷凝
回流,使反应物充分反应;
(2)冷凝水应该是下口进,故答案为: n;
(3)水蒸气蒸馏时,当冷凝器中无油状馏出液.时,证明蒸馏分离完全,故答案为:冷凝器中无油状馏出液;
(4)结合肉桂酸盐的溶解度分析可知,趁热过滤,分离出活性炭,防止温度降低使肉桂酸盐析出而损耗,故
答案为:分离出活性炭,防止温度降低使肉桂酸盐析出而损耗;
(5)加入浓盐酸与水的混合物后发生反应,将肉桂酸盐转化为肉桂酸,对应的方程式为HCl+
→NaCl+ ;
(6)将粗产品提纯可以经过多次溶解重新结晶,对应操作为重结晶,根据方程式可知,14.5mL乙酸酐即
14.5mL 1.082g/mL = 15.689g和5.0mL苯甲醛即5mL 1.06g/L = 5.3g依次加入150mL仪器a中,可知醋酸
酐过量,5.3g苯甲醛完全反应生成肉桂酸5.3 g= 7.4g,若提纯后得到肉桂酸3.56g,则产率为
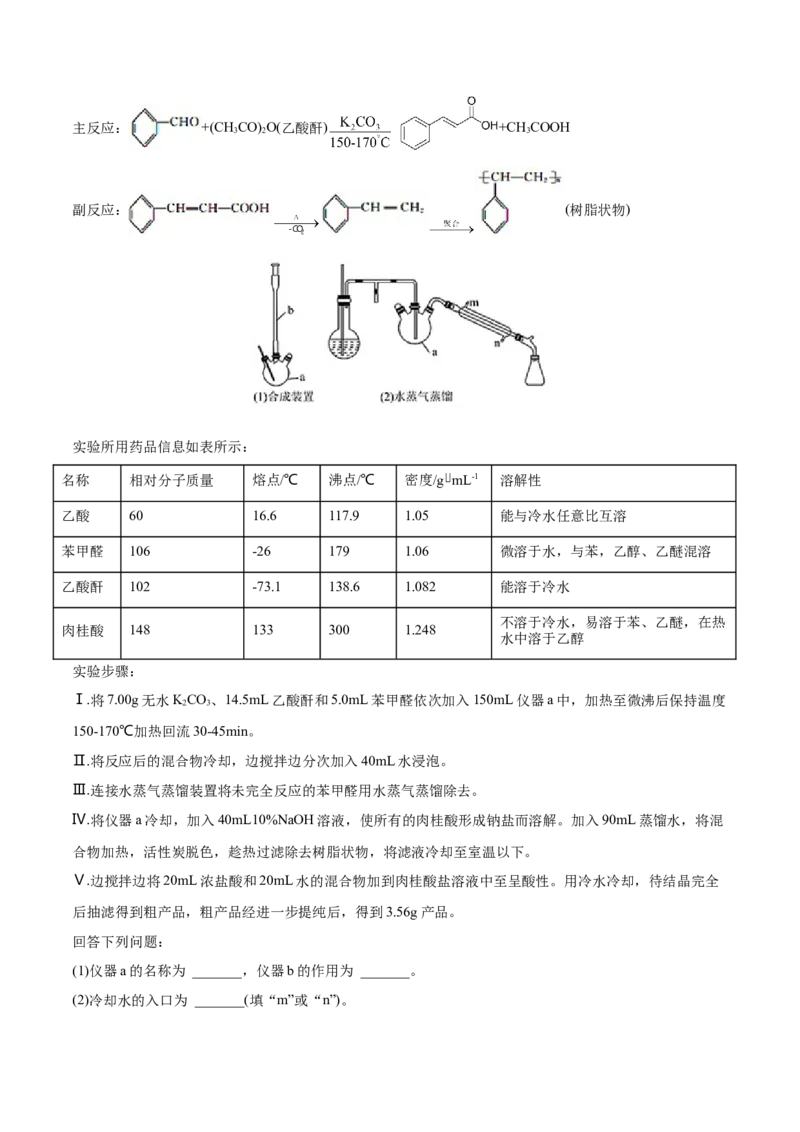
100% = 48.1%,故答案为:重结晶;48.1%。21.(2022·广西玉林·一模)(11分)化合物G是一种抗骨质疏松药,俗称依普黄酮。以甲苯为原料合成该
化合钧的路线如下:
已知:
回答下列问题:
(1)反应①的条件为_______,反应⑤的反应类型为_______。
(2)用系统命名法给 命名_______。
(3)E中含氧官能团的名称为_______,向F中加入浓溴水,1molF最多可以与_______molBr 反应。
2
(4)H的结构简式为_______。
(5)已知N为催化剂,E和M反应生成F和另一种有机物X,写出E→F反应的化学万程式:_______。
(6)D有多种同分异构体,写出同时满足下列条件的所有同分异构体:_______。
a.含苯环的单环化合物;
b.苯环上只有一个取代基;
c.核磁共振氢谱有四组峰,且峰面积之比为3:2:2:1。
【答案】(1)光照(1分) 取代反应(1分)
(2)2-溴丙烷(1分)
(3) 羰基、(酚)羟基(2分) 3(1分)
(4) (1分)
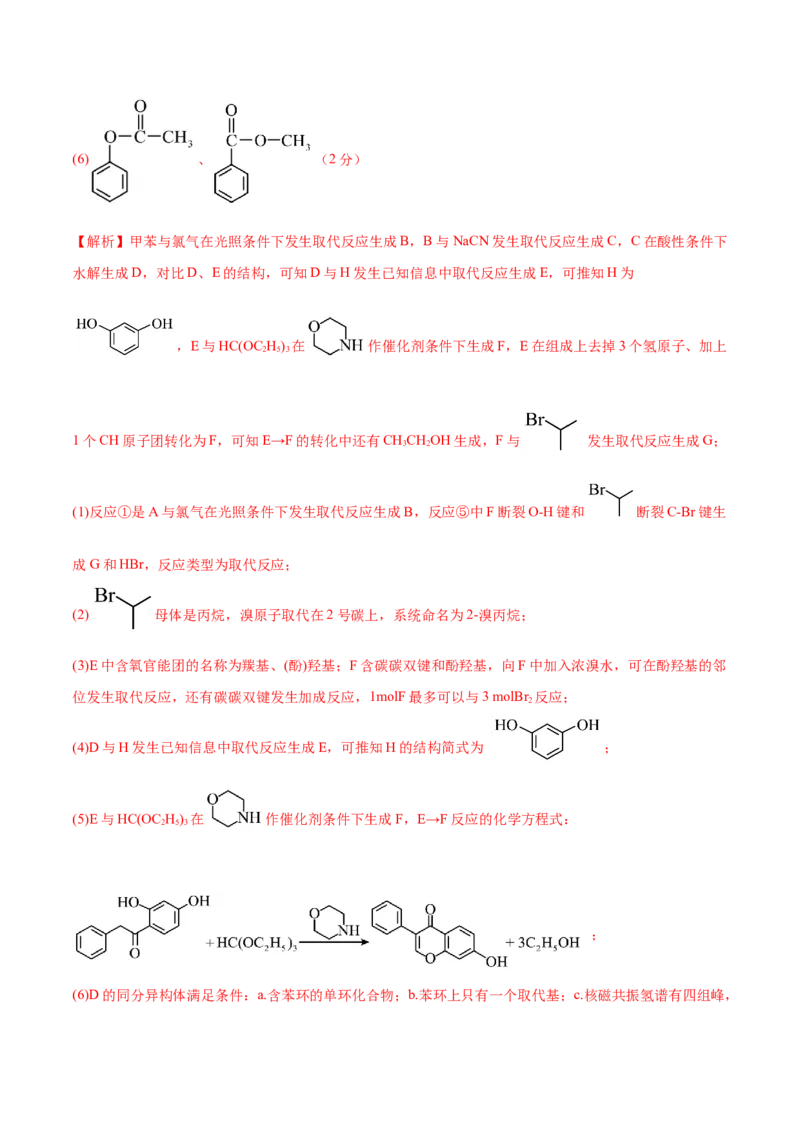
(5) (2分)(6) 、 (2分)
【解析】甲苯与氯气在光照条件下发生取代反应生成B,B与NaCN发生取代反应生成C,C在酸性条件下
水解生成D,对比D、E的结构,可知D与H发生已知信息中取代反应生成E,可推知H为
,E与HC(OC H) 在 作催化剂条件下生成F,E在组成上去掉3个氢原子、加上
2 5 3
1个CH原子团转化为F,可知E→F的转化中还有CHCHOH生成,F与 发生取代反应生成G;
3 2
(1)反应①是A与氯气在光照条件下发生取代反应生成B,反应⑤中F断裂O-H键和 断裂C-Br键生
成G和HBr,反应类型为取代反应;
(2) 母体是丙烷,溴原子取代在2号碳上,系统命名为2-溴丙烷;
(3)E中含氧官能团的名称为羰基、(酚)羟基;F含碳碳双键和酚羟基,向F中加入浓溴水,可在酚羟基的邻
位发生取代反应,还有碳碳双键发生加成反应,1molF最多可以与3 molBr 反应;
2
(4)D与H发生已知信息中取代反应生成E,可推知H的结构简式为 ;
(5)E与HC(OC H) 在 作催化剂条件下生成F,E→F反应的化学方程式:
2 5 3
;
(6)D的同分异构体满足条件:a.含苯环的单环化合物;b.苯环上只有一个取代基;c.核磁共振氢谱有四组峰,且峰面积之比为3:2:2:1,结构为 、 。