文档内容
盐城市伍佑中学
2022-2023 学年秋学期高三期初考试
化学试题
考试时间:75分钟 总分:100分
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Fe:56 C1:35.5 Mg:24
一、选择题。每题只有一个选项符合题目要求。(每题3分,共42分)
1. 2021年“神舟十二号”载人飞船成功发射,“天问一号”开启火星探测之旅,对其所涉及材料说法正确的是
A. 飞船船体覆盖的耐高温陶瓷材料属于传统无机非金属材料
B. “天问一号”所用的太阳能电池板使用的主要原料是SiO
2
C. 航天员所使用的操纵杄采用碳纤维材料制作,碳纤维属于有机高分子材料
D. 探测器使用了大量的镁铝合金材料,是因为镁铝合金的密度小、强度高
2. 下列有关化学用语使用正确的是( )
A. CO 的电子式: B. 次氯酸的结构式:H-O-Cl
2
C. 乙烯的球棍模型: D. 钾原子结构示意图:
3. N 为阿伏加德罗常数的值.下列说法正确的是
A
A. 18g重水(D O)中含有的质子数为9N
2 A
为
B. 标准状况下,2.24LBr 中含原子数目 0.2N
2 A
C. 1molH O 中含有极性键数目为3N
2 2 A
D. 室温下,pH=5的CHCOOH溶液中,由水电离的H+数目为10-9N
3 A
4. 化学与生活密切相关,下列说法错误的是( )
A. 二氧化硫可用于食品增白
B. 过氧化钠可用于呼吸面具
C. 高纯度的单质硅可用于制光电池
D. 用含有橙色酸性重铬酸钾的仪器检验酒驾
5. 能正确表示下列变化的离子方程式是
A. 大理石与醋酸反应:
下载最新免费模拟卷,到公众号:一枚试卷君B. 用氢氧化钠溶液吸收少量二氧化硫气体:
C. 硫酸铝溶液与过量氨水反应:
D. 向 溶液中加过量的 溶液:
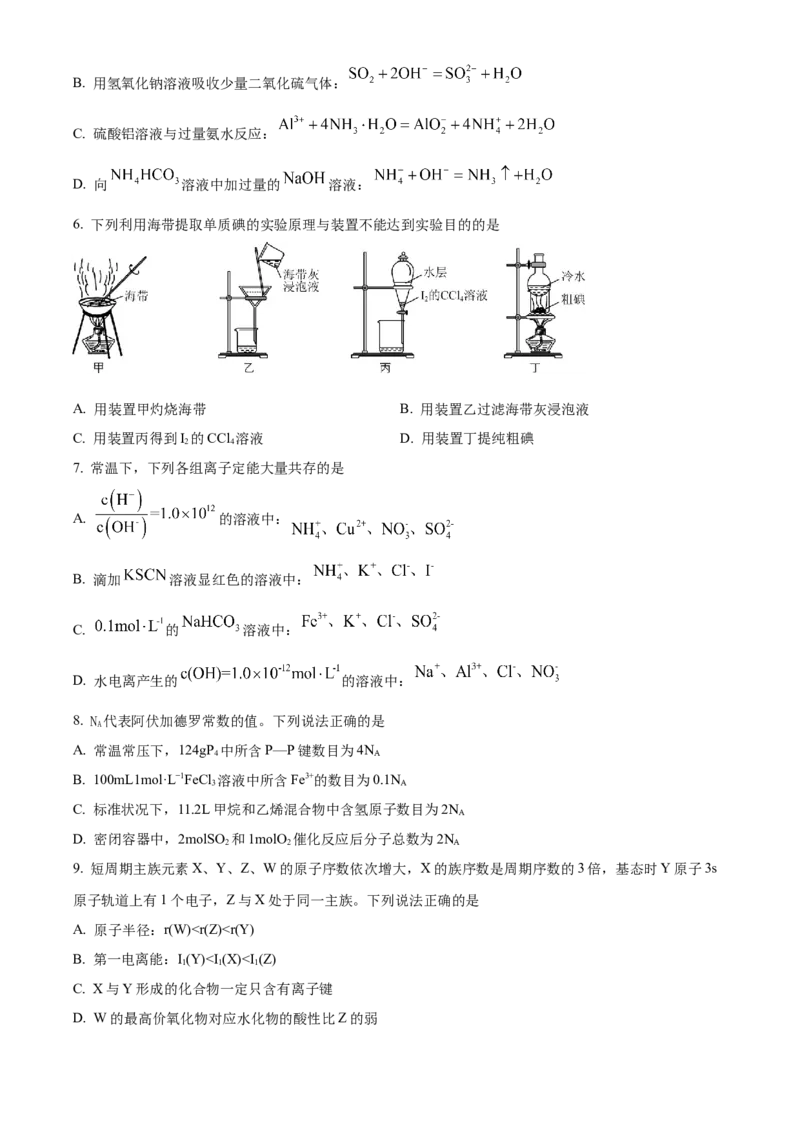
6. 下列利用海带提取单质碘的实验原理与装置不能达到实验目的的是
A. 用装置甲灼烧海带 B. 用装置乙过滤海带灰浸泡液
C. 用装置丙得到I 的CCl 溶液 D. 用装置丁提纯粗碘
2 4
7. 常温下,下列各组离子定能大量共存的是
A. 的溶液中:
B. 滴加 溶液显红色的溶液中:
C. 的 溶液中:
D. 水电离产生的 的溶液中:
8. N 代表阿伏加德罗常数的值。下列说法正确的是
A
A. 常温常压下,124gP 中所含P—P键数目为4N
4 A
B. 100mL1mol·L−1FeCl 溶液中所含Fe3+的数目为0.1N
3 A
C. 标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为2N
A
D. 密闭容器中,2molSO 和1molO 催化反应后分子总数为2N
2 2 A
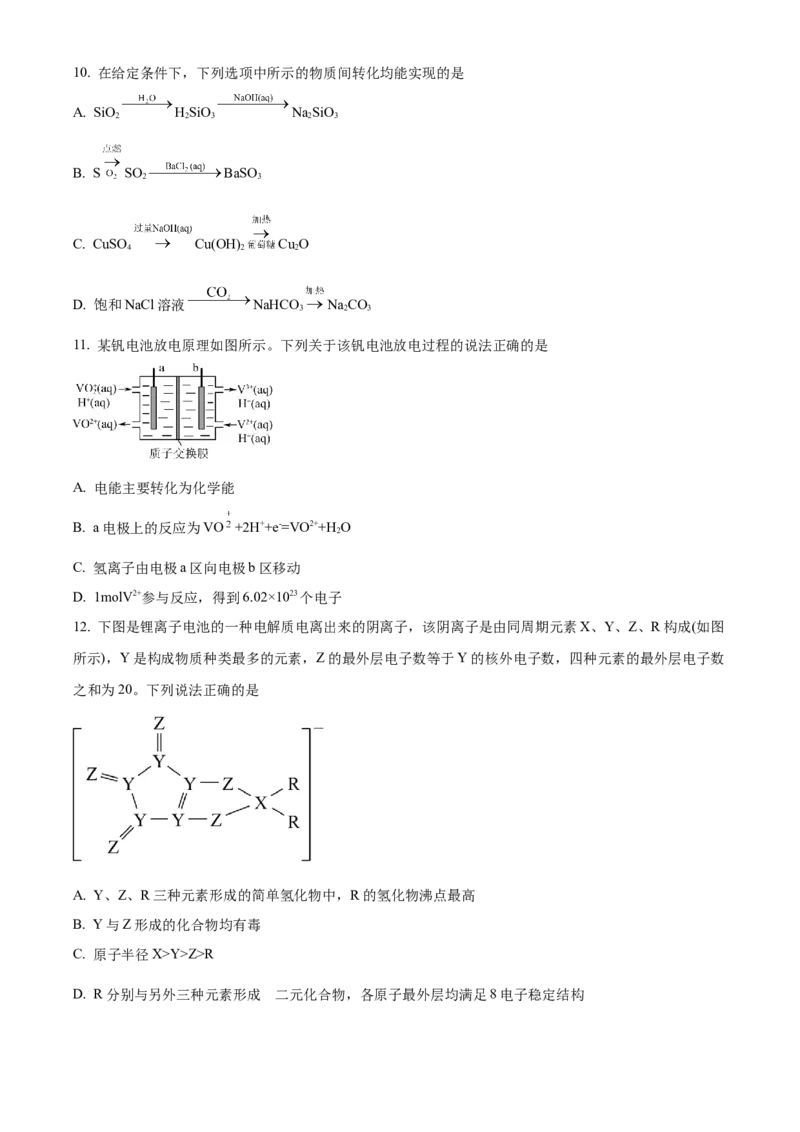
9. 短周期主族元素X、Y、Z、W的原子序数依次增大,X的族序数是周期序数的3倍,基态时Y原子3s
原子轨道上有1个电子,Z与X处于同一主族。下列说法正确的是
A. 原子半径:r(W)Y>Z>R
的
D. R分别与另外三种元素形成 二元化合物,各原子最外层均满足8电子稳定结构13. 二氧化氯具有杀菌消毒作用,是一种广谱型消毒剂。工业上常用Cl 氧化NaClO 制得,方程式为:
2 2
Cl+2NaClO =2ClO +2NaCl,下列相关说法正确的是
2 2 2
A. 反应中Cl 被氧化 B. 消耗0.1 mol NaClO 时,转移0.1 mol电子
2 2
C. ClO 是还原产物 D. 还原剂与氧化剂的物质的量之比为1:2
2
14. 室温下,通过下列实验探究NaHCO 溶液的性质。
3
实验 实验操作和现象
1 用pH试纸测得0.1mol·L-1NaHCO 溶液的pH约为8
3
2 向0.1mol·L-1NaHCO 溶液中加入过量0.1mol·L-1Ba(OH) 溶液,产生白色沉淀
3 2
3 向0.1mol·L-1NaHCO 溶液中加入等体积0.1mol·L-1NaOH溶液
3
4 向浓NaHCO 溶液中加入浓Al (SO ) 溶液,有气体和沉淀生成
3 2 4 3
下列说法不正确的是
A. 实验1的溶液中存在c(H CO)>c(CO )
2 3
B. 实验2所得上层清液中存在c(Ba2+)·c(CO )=K (BaCO)
sp 3
C. 实验3反应后的溶液中存在c(OH—)=c(H+)+c(HCO )+c(H CO)
2 3
D. 实验4中生成的气体是CO
2
二、非选择题(共计58分)
15. 实验室模拟工业利用某铁矿石(含 、 、 、CaO等)制备磁性 胶体的流程如图:
(1)过程Ⅱ的操作名称是_______,过程Ⅰ中采用加热、适当增加 的浓度等措施,是为了_______。
(2)过程Ⅰ得到的滤渣的主要成分的化学式为_______。
的
(3)过程Ⅰ进行了酸溶和过滤,在实验操作中两次用到玻璃棒,玻璃棒在两次操作中 作用分别是
_______、_______。
(4)过程Ⅳ中 作还原剂,被氧化为 ,写出在碱性条件下过程Ⅳ中反应的离子方程式:_______。
的
(5)过程Ⅴ中通入 ,使 部分被氧化为 ,为了得到1mol纯净 ,反应中参加反应的的物质的量为_______。
(6) 可用 表示, 是_______(填“纯净物”或“混合物”),磁性 能与HI溶液
反应,反应的离子方程式为_______。
16. 是化工合成中最重要的镍源,在实验室中模拟工业上以金属镍废料(含Fe、Al等杂质)为原料生
产 的工艺流程如下:
下表列出了相关金属离子生成氢氧化物沉淀的pH
氢氧化物
开始沉淀的pH 2.1 6.5 3.7 7.1
沉淀完全的pH 3.3 9.7 4.7 9.2
(1)为了提高镍元素的漫出率,在“酸浸”时可采取的措施有_______(写一条即可)。
(2)铁和盐酸反应的离子方程式_______。
(3)加入 时发生主要反应的离子方程式为_______。
(4)“调pH”时,控制溶液pH的范围为_______。
(5)流程中由溶液得到 的实验操作步骤依次为_______、_______、过滤、洗涤、干燥。
17. 草酸亚铁晶体(FeC O·2H O)可作为制备电池正极材料磷酸铁锂的原料。以FeSO 溶液制备电池级草酸
2 4 2 4
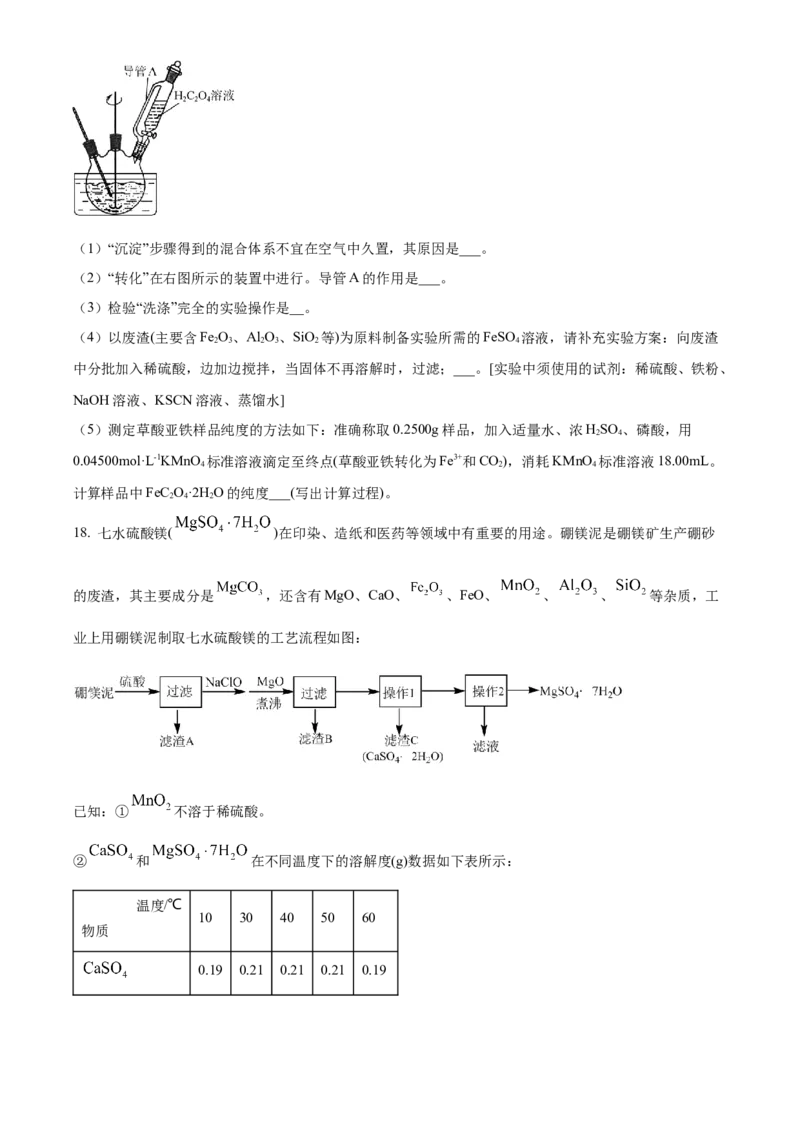
亚铁晶体的实验流程如图:(1)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是___。
(2)“转化”在右图所示的装置中进行。导管A的作用是___。
(3)检验“洗涤”完全的实验操作是__。
(4)以废渣(主要含Fe O、Al O、SiO 等)为原料制备实验所需的FeSO 溶液,请补充实验方案:向废渣
2 3 2 3 2 4
中分批加入稀硫酸,边加边搅拌,当固体不再溶解时,过滤;___。[实验中须使用的试剂:稀硫酸、铁粉、
NaOH溶液、KSCN溶液、蒸馏水]
(5)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓HSO 、磷酸,用
2 4
0.04500mol·L-1KMnO 标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO),消耗KMnO 标准溶液18.00mL。
4 2 4
计算样品中FeC O·2H O的纯度___(写出计算过程)。
2 4 2
18. 七水硫酸镁( )在印染、造纸和医药等领域中有重要的用途。硼镁泥是硼镁矿生产硼砂
的废渣,其主要成分是 ,还含有MgO、CaO、 、FeO、 、 、 等杂质,工
业上用硼镁泥制取七水硫酸镁的工艺流程如图:
已知:① 不溶于稀硫酸。
② 和 在不同温度下的溶解度(g)数据如下表所示:
温度/℃
10 30 40 50 60
物质
0.19 0.21 0.21 0.21 0.19.
309 35.5 40.8 45.6 ——
(1)硼镁泥用硫酸溶解之前,先将硼镁泥粉碎,其目的是_______。
(2)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为_______。
(3)“煮沸”的目的是_______。
(4)若滤渣B的主要成分为 和 ,则加入NaClO发生氧化还原反应的离子方程式为
_______。
(5)流程中操作1为蒸发浓缩、趁热过滤,这样既可得到 ,又防止_______。
(6)获取 的操作2中,不需要的操作是_______(填标号)。
(7)取24.6g 加热至不同温度,剩余固体的质量如下表:
温度/℃ 150 200 780 1124
质量/g 13.80 12.00 9.33 4.00
则780℃时所得固体的化学式为_______(填标号)。
A. MgO B. C. D.下载最新免费模拟卷,到公众号:一枚试卷君