文档内容
综合大题标准练(一)
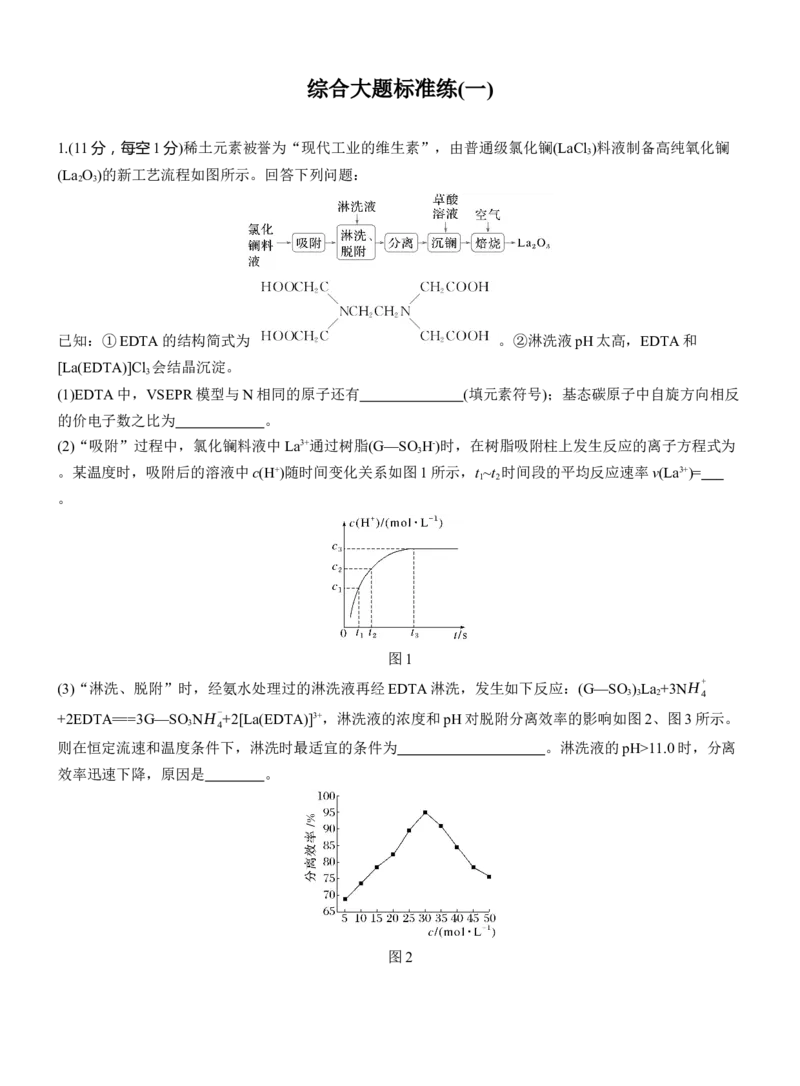
1.(11分,每空1分)稀土元素被誉为“现代工业的维生素”,由普通级氯化镧(LaCl )料液制备高纯氧化镧
3
(La O )的新工艺流程如图所示。回答下列问题:
2 3
已知:①EDTA的结构简式为 。②淋洗液pH太高,EDTA和
[La(EDTA)]Cl 会结晶沉淀。
3
(1)EDTA中,VSEPR模型与N相同的原子还有 (填元素符号);基态碳原子中自旋方向相反
的价电子数之比为 。
(2)“吸附”过程中,氯化镧料液中La3+通过树脂(G—SO H-)时,在树脂吸附柱上发生反应的离子方程式为
3
。某温度时,吸附后的溶液中c(H+)随时间变化关系如图1所示,t ~t 时间段的平均反应速率v(La3+)=
1 2
。
图1
(3)“淋洗、脱附”时,经氨水处理过的淋洗液再经EDTA淋洗,发生如下反应:(G—SO ) La
+3NH+
3 3 2 4
+2EDTA===3G—SO NH- +2[La(EDTA)]3+,淋洗液的浓度和pH对脱附分离效率的影响如图2、图3所示。
3 4
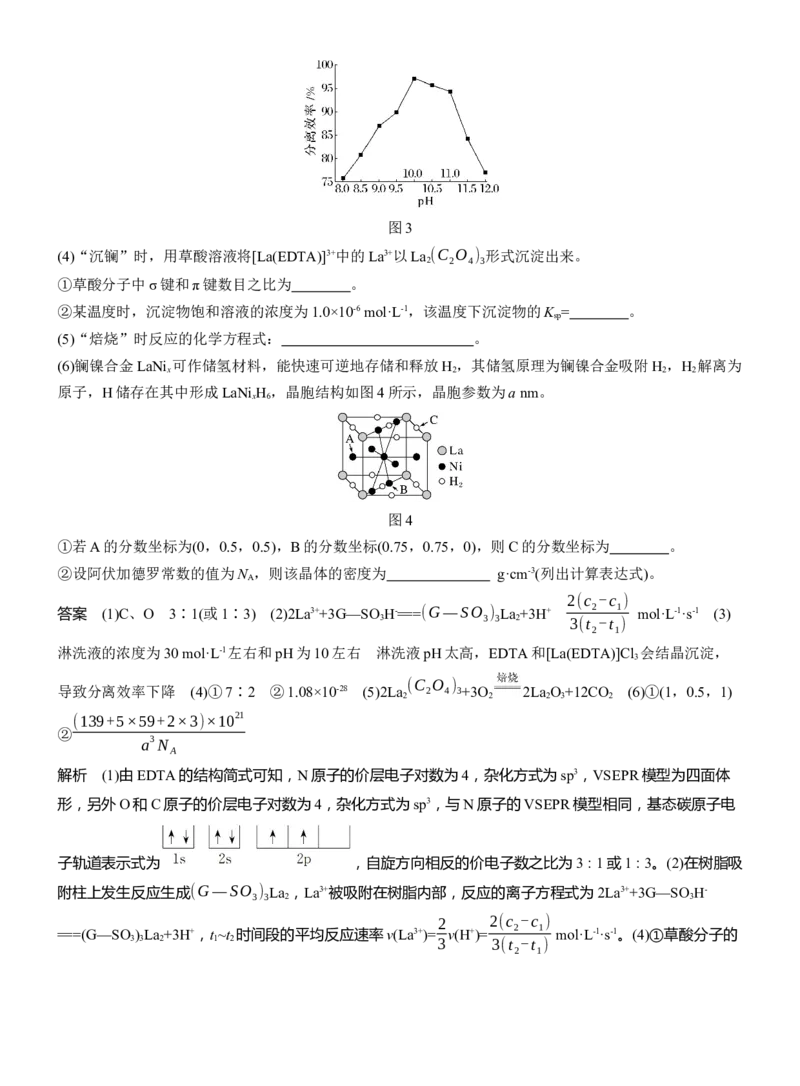
则在恒定流速和温度条件下,淋洗时最适宜的条件为 。淋洗液的pH>11.0时,分离
效率迅速下降,原因是 。
图2图3
(4)“沉镧”时,用草酸溶液将[La(EDTA)]3+中的La3+以La (C O ) 形式沉淀出来。
2 2 4 3
①草酸分子中σ键和π键数目之比为 。
②某温度时,沉淀物饱和溶液的浓度为1.0×10-6 mol·L-1,该温度下沉淀物的K = 。
sp
(5)“焙烧”时反应的化学方程式: 。
(6)镧镍合金LaNi 可作储氢材料,能快速可逆地存储和释放H ,其储氢原理为镧镍合金吸附H ,H 解离为
x 2 2 2
原子,H储存在其中形成LaNiH ,晶胞结构如图4所示,晶胞参数为a nm。
x 6
图4
①若A的分数坐标为(0,0.5,0.5),B的分数坐标(0.75,0.75,0),则C的分数坐标为 。
②设阿伏加德罗常数的值为N ,则该晶体的密度为 g·cm-3(列出计算表达式)。
A
2(c -c )
答案 (1)C、O 3∶1(或1∶3) (2)2La3++3G—SO H-===(G—SO ) La +3H+ 2 1 mol·L-1·s-1 (3)
3 3 3 2 3(t -t )
2 1
淋洗液的浓度为30 mol·L-1左右和pH为10左右 淋洗液pH太高,EDTA和[La(EDTA)]Cl 会结晶沉淀,
3
(C O )
导致分离效率下降 (4)①7∶2 ②1.08×10-28 (5)2La 2 4 3+3O 2La O +12CO (6)①(1,0.5,1)
2 2 2 3 2
(139+5×59+2×3)×1021
②
a3N
A
解析 (1)由EDTA的结构简式可知,N原子的价层电子对数为4,杂化方式为sp3,VSEPR模型为四面体
形,另外O和C原子的价层电子对数为4,杂化方式为sp3,与N原子的VSEPR模型相同,基态碳原子电
子轨道表示式为 ,自旋方向相反的价电子数之比为3∶1或1∶3。(2)在树脂吸
附柱上发生反应生成(G—SO ) La ,La3+被吸附在树脂内部,反应的离子方程式为2La3++3G—SO H-
3 3 2 3
2 2(c -c )
2 1
===(G—SO ) La +3H+,t ~t 时间段的平均反应速率v(La3+)= v(H+)= mol·L-1·s-1。(4)①草酸分子的
3 3 2 1 2 3 3(t -t )
2 1结构简式为 ,碳氧双键中含有1个σ键和1个π键,则草酸分子中σ键和π键数目之比为
7∶2;②某温度时,沉淀物La (C O ) 饱和溶液的浓度为1.0×10-6 mol·L-1,则溶液中c(La3+)=2.0×10-6
2 2 4 3
mol·L-1,c(C
O2-
)=3.0×10-6 mol·L-1,则K =c2(La3+)·c3(C
O2-
)=(2.0×10-6)2×(3.0×10-6)3=1.08×10-28。(6)①若A
2 4 sp 2 4
的分数坐标为(0,0.5,0.5),B的分数坐标(0.75,0.75,0),由晶胞结构可知,C的分数坐标为(1,0.5,
1 1 1 1
1);②该晶胞中含有H 的个数为8× +2× =3,La原子的个数为8× =1,Ni原子的个数为1+8× =5,设
2 4 2 8 2
(139+5×59+2×3) (139+5×59+2×3)×1021
阿伏加德罗常数的值为N ,则该晶体的密度为 g·cm-3=
A N (a×10-7 ) 3 a3N
A A
g·cm-3。
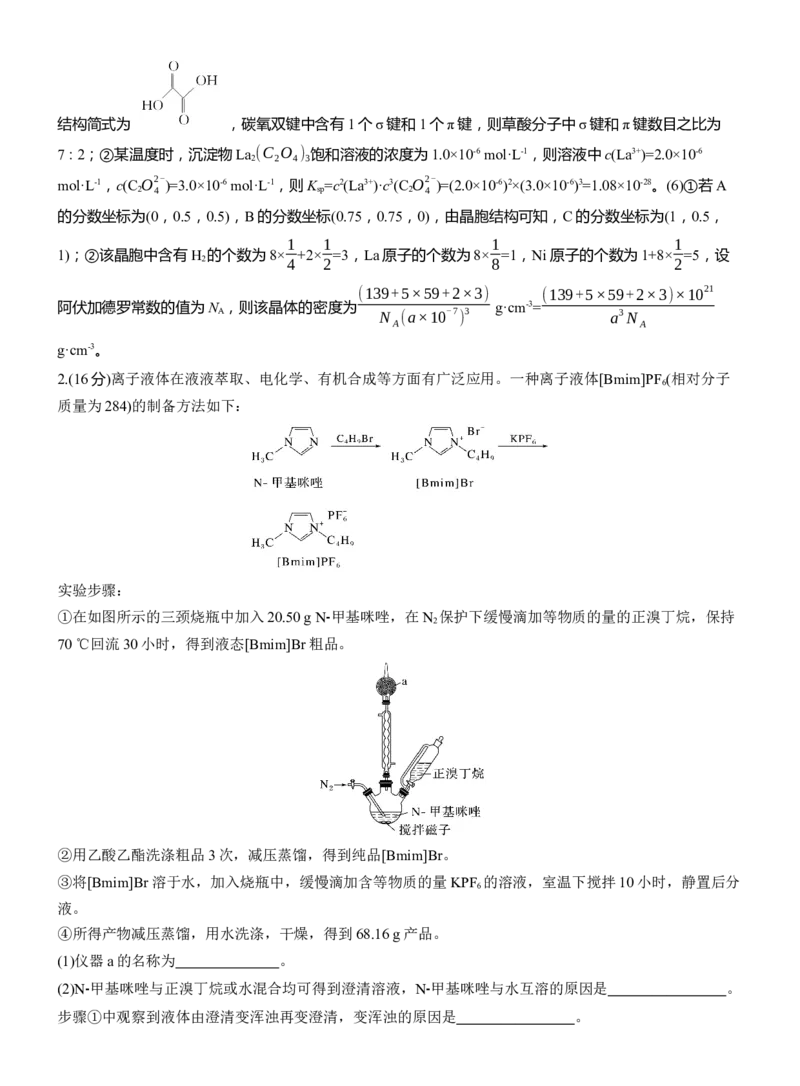
2.(16分)离子液体在液液萃取、电化学、有机合成等方面有广泛应用。一种离子液体[Bmim]PF (相对分子
6
质量为284)的制备方法如下:
实验步骤:
①在如图所示的三颈烧瓶中加入20.50 g N⁃ 甲基咪唑,在N
2
保护下缓慢滴加等物质的量的正溴丁烷,保持
70 ℃回流30小时,得到液态[Bmim]Br粗品。
②用乙酸乙酯洗涤粗品3次,减压蒸馏,得到纯品[Bmim]Br。
③将[Bmim]Br溶于水,加入烧瓶中,缓慢滴加含等物质的量KPF 的溶液,室温下搅拌10小时,静置后分
6
液。
④所得产物减压蒸馏,用水洗涤,干燥,得到68.16 g产品。
(1)仪器a的名称为 。
(2)N⁃ 甲基咪唑与正溴丁烷或水混合均可得到澄清溶液,N⁃ 甲基咪唑与水互溶的原因是 。
步骤①中观察到液体由澄清变浑浊再变澄清,变浑浊的原因是 。(3)步骤②减压蒸馏除去的物质主要为 。
(4)步骤④检验产物已洗涤干净的方法是 。
(5)[Bmim]PF 的产率为 。
6
(6)[Bmim]PF 可代替CCl 作萃取剂,其优点之一是比CCl 难挥发。[Bmim]PF 比CCl 沸点高的原因是
6 4 4 6 4
。
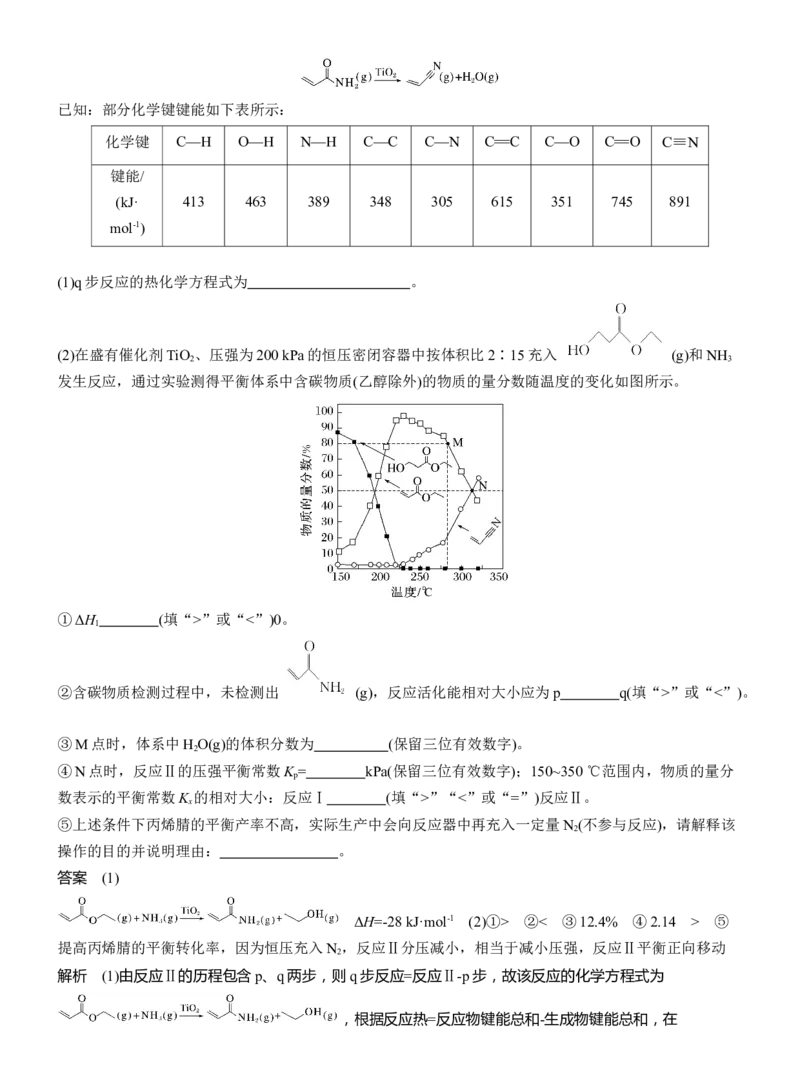
(7)以[Bmim]I与I 的混合液作为离子导体的一种染料(Dye)敏化太阳能电池,工作原理如图所示,光照射时
2
发生电极反应:Dye-e-===Dye+。已知I-+I
===I-
,该太阳能电池中染料再生的离子方程式为
2 3
。
答案 (1)球形干燥管 (2)N⁃ 甲基咪唑与水分子间能形成氢键 生成的[Bmim]Br和反应物不互溶,搅拌下
形成乳浊液 (3)乙酸乙酯 (4)取少量最后一次洗涤液于试管中,滴加AgNO 溶液不出现浅黄色沉淀
3
(5)96.00% (6)[Bmim]PF 为离子晶体,CCl 为分子晶体
(7)3I-+2Dye+===2Dye+I-
6 4 3
解析 (4)步骤③中[Bmim]Br和 KPF 反应生成[Bmim]PF ,有HBr生成,用水洗涤的目的是除去过量的
6 6
KPF 和HBr,检验产物已洗涤干净只需要检验洗涤液中的Br-即可,方法为取少量最后一次洗涤液于试管
6
20.50 g
中,滴加AgNO
3
溶液不出现浅黄色沉淀。(5)20.50 g N⁃甲基咪唑的物质的量为
82 g·mol-1
=0.25 mol,理
68.16 g
论上生成0.25 mol[Bmim]PF ,则[Bmim]PF 的产率为 ×100%=96.00%。(7)光照射
6 6 0.25mol×284 g·mol-1
时发生电极反应:Dye-e-===Dye+,导电玻璃上发生电极反应:I-
+2e-===3I-,结合两个电极方程式可知,
3
电池工作时总方程式为2Dye+I-
===3I-+2Dye+,则该太阳能电池中染料再生的离子方程式为3I-
3
+2Dye+===2Dye+I-
。
3
3.(10分)丙烯腈( )是合成橡胶及合成树脂等工业中的重要原料,以 为原料合成丙烯腈
的反应过程如下:
反应Ⅰ:
反应Ⅱ:
科学家通过DFT计算得出反应Ⅱ的历程包含p、q两步,其中p步反应的化学方程式为已知:部分化学键键能如下表所示:
化学键 C—H O—H N—H C—C C—N C==C C—O C==O C≡N
键能/
(kJ· 413 463 389 348 305 615 351 745 891
mol-1)
(1)q步反应的热化学方程式为 。
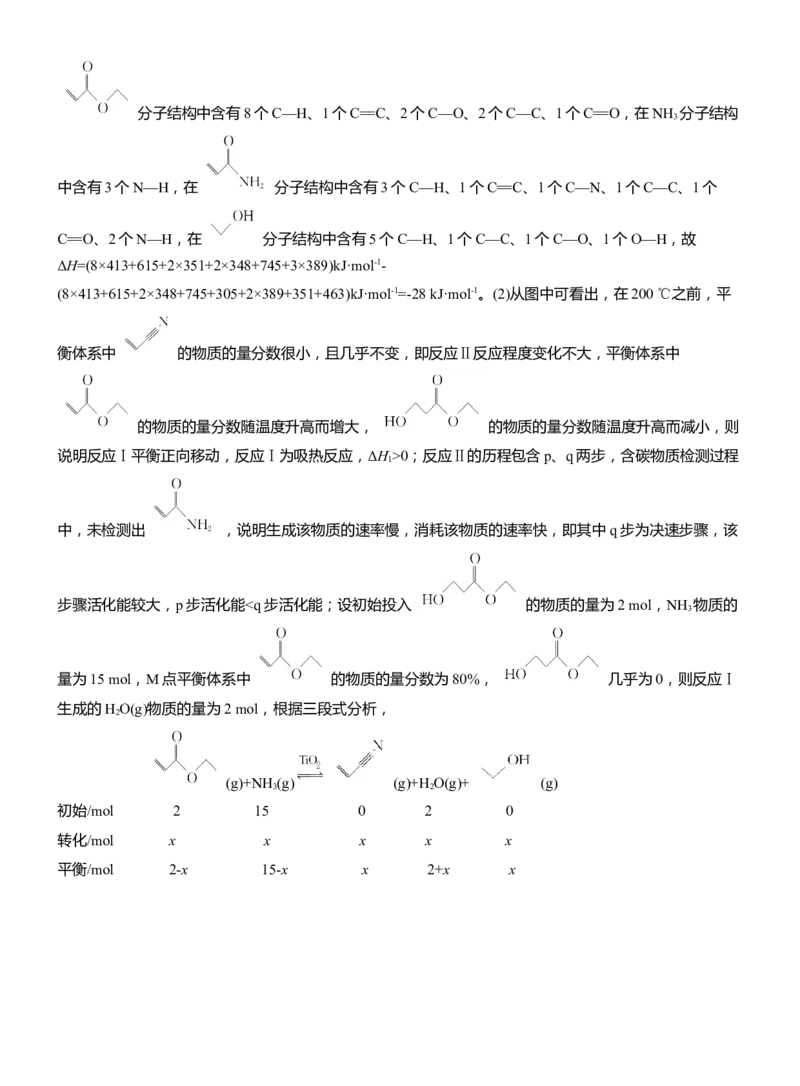
(2)在盛有催化剂TiO 、压强为200 kPa的恒压密闭容器中按体积比2∶15充入 (g)和NH
2 3
发生反应,通过实验测得平衡体系中含碳物质(乙醇除外)的物质的量分数随温度的变化如图所示。
①ΔH (填“>”或“<”)0。
1
②含碳物质检测过程中,未检测出 (g),反应活化能相对大小应为p q(填“>”或“<”)。
③M点时,体系中H O(g)的体积分数为 (保留三位有效数字)。
2
④N点时,反应Ⅱ的压强平衡常数K = kPa(保留三位有效数字);150~350 ℃范围内,物质的量分
p
数表示的平衡常数K 的相对大小:反应Ⅰ (填“>”“<”或“=”)反应Ⅱ。
x
⑤上述条件下丙烯腈的平衡产率不高,实际生产中会向反应器中再充入一定量N (不参与反应),请解释该
2
操作的目的并说明理由: 。
答案 (1)
ΔH=-28 kJ·mol-1 (2)①> ②< ③12.4% ④2.14 > ⑤
提高丙烯腈的平衡转化率,因为恒压充入N ,反应Ⅱ分压减小,相当于减小压强,反应Ⅱ平衡正向移动
2
解析 (1)由反应Ⅱ的历程包含p、q两步,则q步反应=反应Ⅱ-p步,故该反应的化学方程式为
,根据反应热=反应物键能总和-生成物键能总和,在分子结构中含有8个C—H、1个C==C、2个C—O、2个C—C、1个C==O,在NH 分子结构
3
中含有3个N—H,在 分子结构中含有3个C—H、1个C==C、1个C—N、1个C—C、1个
C==O、2个N—H,在 分子结构中含有5个C—H、1个C—C、1个C—O、1个O—H,故
ΔH=(8×413+615+2×351+2×348+745+3×389)kJ·mol-1-
(8×413+615+2×348+745+305+2×389+351+463)kJ·mol-1=-28 kJ·mol-1。(2)从图中可看出,在200 ℃之前,平
衡体系中 的物质的量分数很小,且几乎不变,即反应Ⅱ反应程度变化不大,平衡体系中
的物质的量分数随温度升高而增大, 的物质的量分数随温度升高而减小,则
说明反应Ⅰ平衡正向移动,反应Ⅰ为吸热反应,ΔH >0;反应Ⅱ的历程包含p、q两步,含碳物质检测过程
1
中,未检测出 ,说明生成该物质的速率慢,消耗该物质的速率快,即其中q步为决速步骤,该
步骤活化能较大,p步活化能105,反应Ⅱ随温度升高,平衡常数K 增大,
x x
但仍小于反应Ⅰ平衡常数K,故反应Ⅰ平衡常数K>反应Ⅱ平衡常数K。
x x x
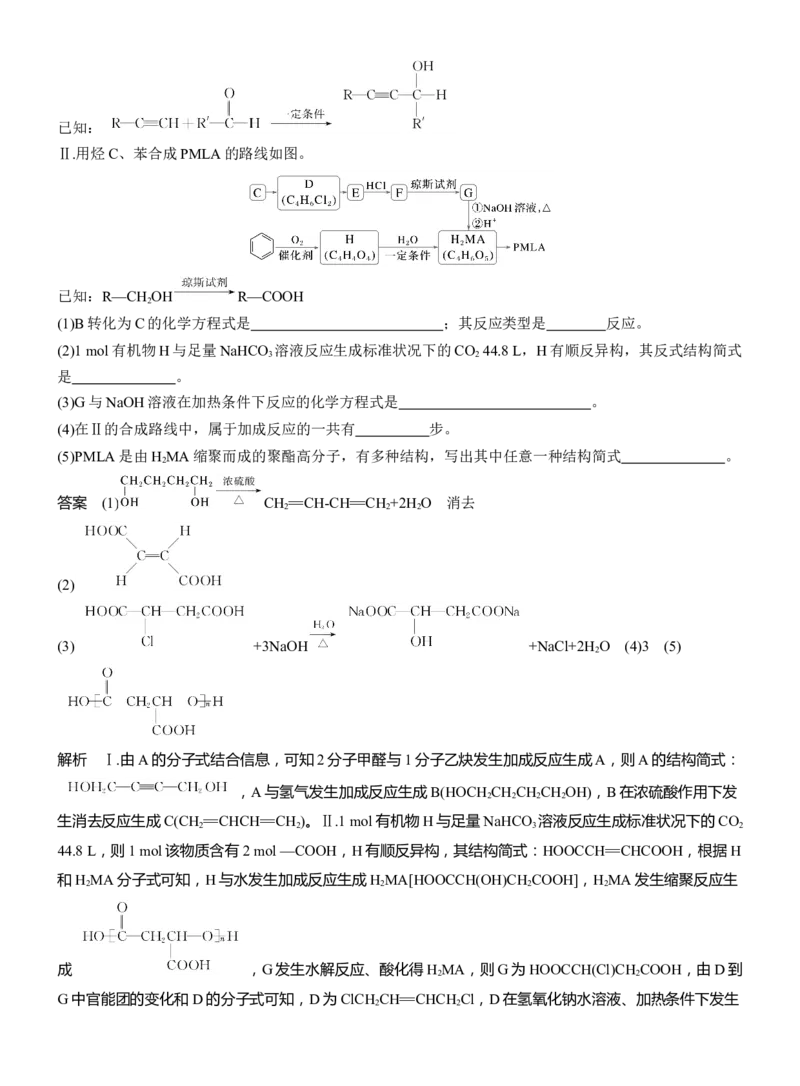
4.以乙炔或苯为原料可合成有机酸H MA,并进一步合成高分子化合物PMLA。
2
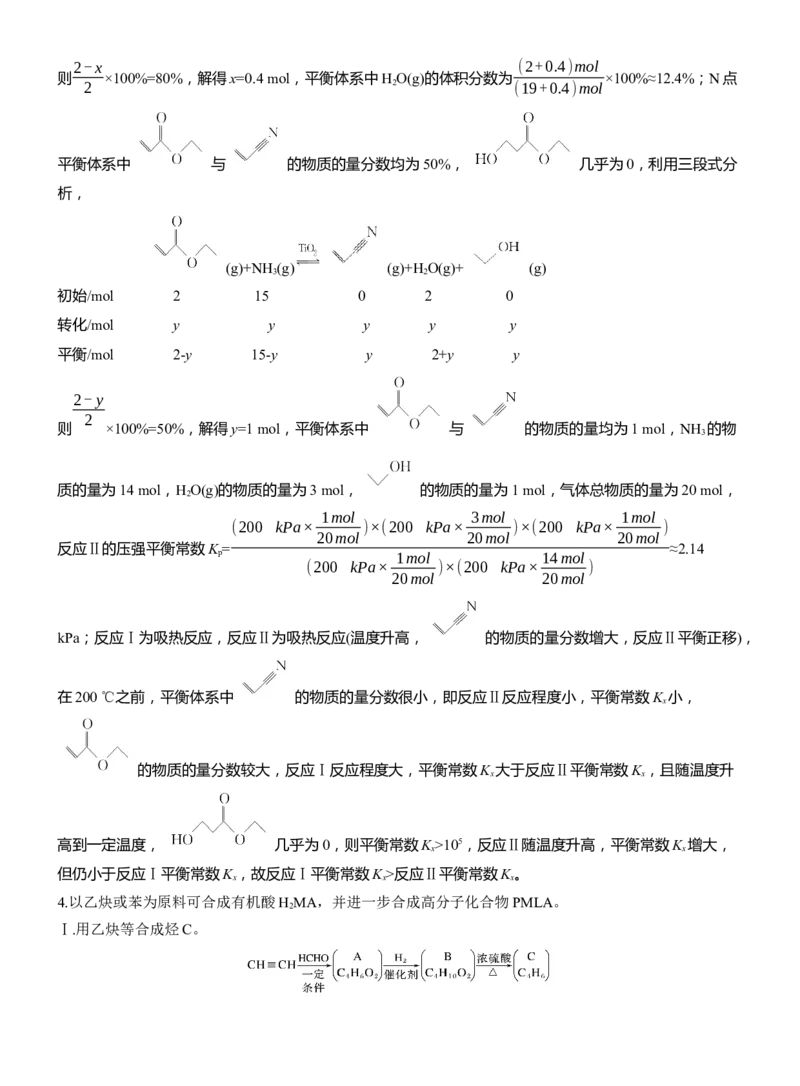
Ⅰ.用乙炔等合成烃C。已知:
Ⅱ.用烃C、苯合成PMLA的路线如图。
已知:R—CH OH R—COOH
2
(1)B转化为C的化学方程式是 ;其反应类型是 反应。
(2)1 mol有机物H与足量NaHCO 溶液反应生成标准状况下的CO 44.8 L,H有顺反异构,其反式结构简式
3 2
是 。
(3)G与NaOH溶液在加热条件下反应的化学方程式是 。
(4)在Ⅱ的合成路线中,属于加成反应的一共有 步。
(5)PMLA是由H MA缩聚而成的聚酯高分子,有多种结构,写出其中任意一种结构简式 。
2
答案 (1) CH ==CH-CH==CH +2H O 消去
2 2 2
(2)
(3) +3NaOH +NaCl+2H O (4)3 (5)
2
解析 Ⅰ.由A的分子式结合信息,可知2分子甲醛与1分子乙炔发生加成反应生成A,则A的结构简式:
,A与氢气发生加成反应生成B(HOCH CH CH CH OH),B在浓硫酸作用下发
2 2 2 2
生消去反应生成C(CH ==CHCH==CH )。Ⅱ.1 mol有机物H与足量NaHCO 溶液反应生成标准状况下的CO
2 2 3 2
44.8 L,则1 mol该物质含有2 mol —COOH,H有顺反异构,其结构简式:HOOCCH==CHCOOH,根据H
和H MA分子式可知,H与水发生加成反应生成H MA[HOOCCH(OH)CH COOH],H MA发生缩聚反应生
2 2 2 2
成 ,G发生水解反应、酸化得H MA,则G为HOOCCH(Cl)CH COOH,由D到
2 2
G中官能团的变化和D的分子式可知,D为ClCH CH==CHCH Cl,D在氢氧化钠水溶液、加热条件下发生
2 2水解反应生成E(HOCH CH==CHCH OH),E与HCl发生加成反应生成F[HOCH CH(Cl)CH CH OH]。(4)在
2 2 2 2 2
Ⅱ的合成路线中,属于加成反应的有:H→H MA、E→F、C→D。
2