文档内容
特色练 12 电解质溶液中的曲线分析
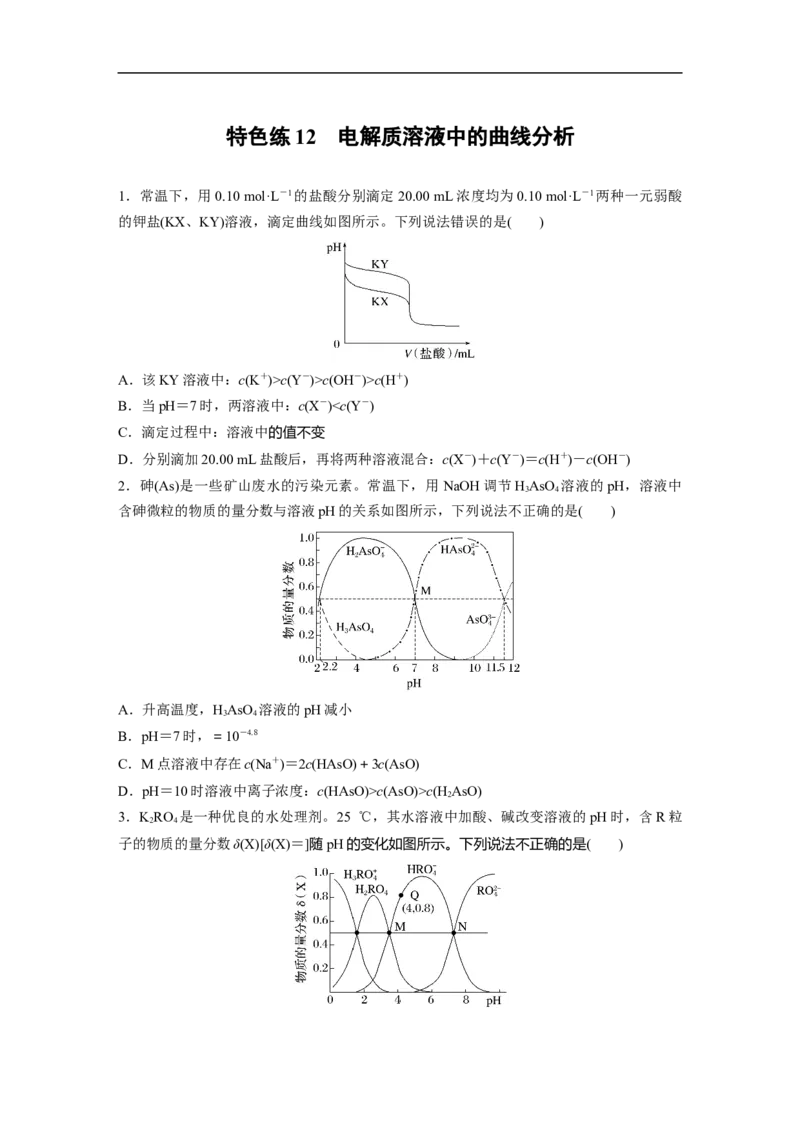
1.常温下,用0.10 mol·L-1的盐酸分别滴定20.00 mL浓度均为0.10 mol·L-1两种一元弱酸
的钾盐(KX、KY)溶液,滴定曲线如图所示。下列说法错误的是( )
A.该KY溶液中:c(K+)>c(Y-)>c(OH-)>c(H+)
B.当pH=7时,两溶液中:c(X-)c(AsO)>c(H AsO)
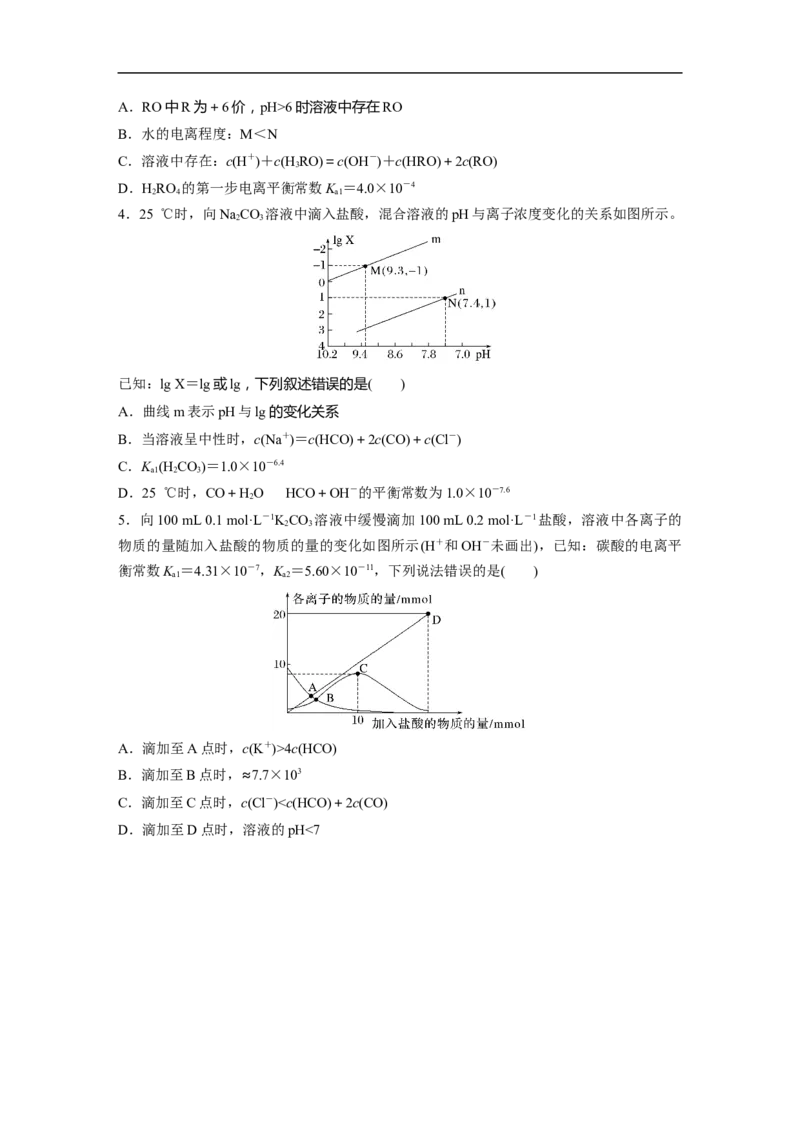
2
3.KRO 是一种优良的水处理剂。25 ℃,其水溶液中加酸、碱改变溶液的pH时,含R粒
2 4
子的物质的量分数δ(X)[δ(X)=]随pH的变化如图所示。下列说法不正确的是( )A.RO中R为+6价,pH>6时溶液中存在RO
B.水的电离程度:M<N
C.溶液中存在:c(H+)+c(H RO)=c(OH-)+c(HRO)+2c(RO)
3
D.HRO 的第一步电离平衡常数K =4.0×10-4
2 4 a1
4.25 ℃时,向NaCO 溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。
2 3
已知:lg X=lg或lg,下列叙述错误的是( )
A.曲线m表示pH与lg的变化关系
B.当溶液呈中性时,c(Na+)=c(HCO)+2c(CO)+c(Cl-)
C.K (H CO)=1.0×10-6.4
a1 2 3
D.25 ℃时,CO+HOHCO+OH-的平衡常数为1.0×10-7.6
2
5.向100 mL 0.1 mol·L-1KCO 溶液中缓慢滴加100 mL 0.2 mol·L-1盐酸,溶液中各离子的
2 3
物质的量随加入盐酸的物质的量的变化如图所示(H+和OH-未画出),已知:碳酸的电离平
衡常数K =4.31×10-7,K =5.60×10-11,下列说法错误的是( )
a1 a2
A.滴加至A点时,c(K+)>4c(HCO)
B.滴加至B点时,≈7.7×103
C.滴加至C点时,c(Cl-)