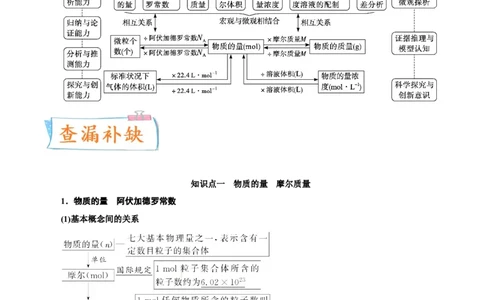
文档内容
考向 01 物质的量 气体摩尔体积
【2022广东卷】我国科学家进行了如图所示的碳循环研究。下列说法正确的是
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖与果糖互为同分异构体,都属于烃类
C. 中含有 个电子
D. 被还原生成
【答案】A
【解析】A.淀粉是由葡萄糖分子聚合而成的多糖,在一定条件下水解可得到葡萄糖,故A正确;
B.葡萄糖与果糖的分子式均为C H O,结构不同,二者互为同分异构体,但含有O元素,不是烃类,属
6 12 6
于烃的衍生物,故B错误;
C.一个CO分子含有14个电子,则1molCO中含有14×6.02×1023=8.428×1024个电子,故C错误;
D.未指明气体处于标况下,不能用标况下的气体摩尔体积计算其物质的量,故D错误;
答案选A。知识点一 物质的量 摩尔质量
1.物质的量 阿伏加德罗常数
(1)基本概念间的关系
(2)物质的量的规范表示方法
如:1 mol Fe、1 mol O 、1 mol Na+或钠离子。
2(3)物质的量与微粒数、阿伏加德罗常数之间的关系n=或N=n·N 。
A
[名师点拨] (1)物质的量作为研究微观粒子与宏观物质的桥梁,其单位摩尔后面应为确切的微粒名称
或微粒符号,如1 mol氢(不确切)和1 mol大米(宏观物质)皆为错误说法。
(2)物质的量描述的对象只能是微观粒子,如电子、质子、中子、原子、分子、离子、原子团等,不能
用于描述宏观物质。
2.摩尔质量
(1)概念:单位物质的量的物质所具有的质量,单位: g·mol - 1 。
(2)数值:当微粒的摩尔质量以 g·mol - 1 为单位时,在数值上等于该微粒的相对分子(原子)质量。
(3)物质的量、物质的质量与摩尔质量的关系为n=。
[名师点拨] 摩尔质量、相对分子质量、1 mol物质的质量在数值上是相同的,但三者的含义不同,单
位不同。摩尔质量的单位是g·mol-1,相对原子(分子)质量的单位是1,1 mol物质的质量单位是g。
3.求解气体摩尔质量“五方法”
(1)根据物质的质量(m)和物质的量(n):M=。
(2)根据一定质量(m)的物质中微粒数目(N)和阿伏加德罗常数(N ):M=N ·。
A A
(3)根据标准状况下气体的密度(ρ):
M=ρ×22.4(g·mol-1)。
(4)根据同温同压下气体的相对密度:=D。
(5)对于混合气体,求其平均摩尔质量,上述计算式仍然成立;还可以用下式计算:M=M×a%+
1
M×b%+M×c%……a%、b%、c%指混合物中各成分的物质的量分数(或体积分数)。
2 3
知识点二 气体的摩尔体积 阿伏加德罗定律
1.影响物质体积大小的因素
2.气体摩尔体积(V )
m
(1)概念:单位物质的量的气体所占的体积,单位为 L·mol - 1 (或L/mol)和m3/mol(或m3·mol-1)。
(2)特例:标准状况(0_ ℃ , 101 _kPa)下,V 为22.4_ L·mol - 1 。
m
(3)气体摩尔体积与物质的量、气体体积之间的关系为 n =。
[名师点拨] 抓“两看”,突破气体与状况陷阱
一看:气体是否处于标准状况(0 ℃、101 kPa)。二看:标准状况下,物质是否是气态。常见干扰物质:
①无机物Br 、SO 、HO、HF等;②有机物中碳原子数大于4的烃,如苯、己烷等;③有机物中烃
2 3 2
的衍生物CCl 、氯仿、乙醇等。
4
若题中给出非标准状况下的气体,切勿直接判断为错误说法,气体的物质的量或质量与温度、压强无
关,可直接计算。
3.阿伏加德罗定律及其推论
(1)阿伏加德罗定律:在同温同压下,相同体积的任何气体都含有相同数目的分子。
(2)推论
结论
相同条件
公式 语言叙述
T、p相同 = 同温、同压下,气体的物质的量与其体积成正比
T、p相同 = 同温、同压下,气体的密度与其摩尔质量成正比
T、V相同 = 同温、同体积下,气体的压强与其物质的量成正比
1.设阿伏加德罗常数的值为N ,下列说法正确的是( )
A
A.标准状况下,2.24 L CHOH分子中共价键的数目为0.5N
3 A
B.1 mol Na O 与足量CO 充分反应,转移的电子数为2N
2 2 2 A
C.用浓盐酸分别和KMnO 、KClO 反应制备1 mol氯气,转移的电子数均为2N
4 3 A
D.5.6 g Fe粉与足量S粉加热充分反应转移的电子数为0.2N
A
2.下列说法中正确的是(N 为阿伏加德罗常数的值)( )
A
A.O2-的电子式为 ,则O2-核外有8个电子
B.1 mol NH Cl中含有的H—Cl键的数目为N
4 A
C.CrO 中Cr元素的化合价为+6价,每个CrO 分子中存在两个过氧键
5 5
D.20 g Na O和NaO 的混合物中,所含阴、阳离子数目之比无法确定
2 2 2
3.据央视新闻报道,在政府工作报告中指出,建设一批光网城市,推进5万个行政村通光纤,让更多城乡居民享受数字化生活。光缆的主要成分为SiO。下列叙述正确的是( )
2
A.SiO 的摩尔质量为60
2
B.标准状况下,15 g SiO 的体积为5.6 L
2
C.SiO 中Si与O的质量比为7∶8
2
D.相同质量的SiO 和CO 中含有的氧原子数相同
2 2
4.用N 表示阿伏加德罗常数的值,下列叙述中正确的是( )
A
A.1 mol甲基(—CH)所含的电子数为10N
3 A
B.常温常压下,1 mol分子式为C HO的有机物中,含有C—O键的数目为N
2 6 A
C.14 g由乙烯和环丙烷( )组成的混合气体中,含有的原子总数为3N
A
D.标准状况下,22.4 L四氯化碳中含有共用电子对的数目为4N
A
5.空气中二氧化碳含量的持续增加,会产生温室效应,一种处理二氧化碳的重要方法是将二氧化碳还原:
CO(g)+4H(g)CH(g)+2HO(g)。下列说法(N 代表阿伏加德罗常数的值)正确的是( )
2 2 4 2 A
A.2.24 L CO 含有双键的数目为0.2N
2 A
B.1 mol CO 和2 mol H 充分反应生成CH 的分子数为0.5N
2 2 4 A
C.通常状况下,0.1 mol CH 中含有的电子数为N
4 A
D.生成18 g HO转移电子数为8N
2 A
1.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.2.0 g D 中含有的中子数目为0.8N
2 A
B.4.6 g C HO中含有C-H键的数目一定为0.6N
2 6 A
C.常温下,将2.8 g Fe置于足量的浓硝酸中,转移的电子数目一定为0.15N
A
D.11.2 L(标准状况)由甲烷和乙烯组成的混合气体中含有氢原子数目为2N
A
2.(广东省汕头市2022届高三下学期第一次模拟考试)2021年,我国科学家首次在实验室实现 到淀
粉的全合成,其合成路线如下:设 为阿伏伽德罗常数,下列有关说法不正确的是A.标况下,11.2L 中含有共用电子对数目为2
B.反应②、③无法在高温下进行
C.反应②中,3.2g 生成HCHO时转移电子数目为0.2
D.1mol DHA与乙酸发生取代反应,可消耗乙酸分子数目为
3.(广东省汕头市潮阳黄图盛中学2021-2022学年高三下学期一模检验)设阿伏加德罗常数的数值为
N ,下列说法正确的是
A
A.1L 1 mol·L-1 的NaHCO 溶液中含有的离子数为3N
3 A
B.22.4 L的CO 与过量NaO 充分反应转移的电子数为N
2 2 2 A
C.常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3N
A
D.常温常压下,14g由N 与CO组成的混合气体含有的原子数目为N
2 A
4.设N 为阿伏加德罗常数的值,下列说法不正确的是
A
A.1L0.1mol·L-1Fe (SO ) 溶液中含有的阳离子数目小于0.2N
2 4 3 A
B.0.24g Mg在O 和CO 的混合气体中完全燃烧,转移电子数为0.02N
2 2 A
C.3g由CO 和SO 组成的混合气体中含有的质子数为1.5N
2 2 A
D.1molNa O 与SO 完全反应,转移电子数为2N
2 2 2 A
5.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.14.0gFe发生吸氧腐蚀生成Fe O·xH O,电极反应转移的电子数为0.5N
2 3 2 A
B.标准状况下,11.2LH S溶于水,溶液中含硫粒子的数目大于0.5N
2 A
C.常温下,0.5LpH=14的Ba(OH) 溶液中Ba2+的数目为0.5N
2 A
D.向100mL0.5mol·L-1Fe(NO ) 溶液中通入足量SO 气体,转移电子数为0.05N
3 3 2 A
1.(2022·全国甲卷) 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
2.(2022·浙江卷6月) 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为
C. 含有中子数为
D. 和 于密闭容器中充分反应后, 分子总数为
3.(2022·浙江卷1月)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
4.(2021广东)设 为阿伏加德罗常数的值。下列说法正确的是
A. 含有 键的数目为
B. 的盐酸含有阴离子总数为
C. 与 混合后的分子数目为
D. 与足量 反应生成的 分子数目为
5.(2021全国甲卷) 为阿伏加德罗常数的值。下列叙述正确的是
A. 重水( )中含有的质子数为B. 的 与 完全反应时转移的电子数为
C. 环状 ( )分子中含有的 键数为
D. 的 溶液中 离子数为
1.【答案】D
【解析】标准状况下,CHOH是液体,2.24 L CHOH的物质的量不是0.1 mol,故A错误;NaO 与CO 的
3 3 2 2 2
反应中,NaO 既是氧化剂又是还原剂,1 mol Na O 与足量CO 充分反应,转移的电子数为N ,故B错误;
2 2 2 2 2 A
浓盐酸和KMnO 反应制备氯气,氯气是氧化产物,生成1 mol氯气转移2 mol电子;浓盐酸和KClO 反应
4 3
制备氯气,氯气既是氧化产物又是还原产物,生成1 mol氯气转移 mol电子,故C错误;Fe粉与足量S粉
反应生成硫化亚铁,5.6 g Fe粉与足量S粉加热充分反应转移的电子数为0.2N ,故D正确。
A
2.【答案】C
【解析】O2-的电子式为 ,表示O2-的最外层有8个电子,但其核外有10个电子,A错误;
NH Cl是离子化合物,NH与Cl-间形成离子键,无H—Cl共价键存在,B错误;根据化合物中所有元素化
4
合价的代数和为0原则,CrO 中5个O共为-6价,说明以-1价氧存在的共有两个过氧根,一个氧化合价
5
为-2价,C正确;NaO和NaO 都是离子化合物,其中含有的阴、阳离子数目之比都是 1∶2,与物质质
2 2 2
量的多少无关,D错误。
3.【答案】C
【解析】摩尔质量的单位为g·mol-1,A项错误;标准状况下SiO 为固体,B项错误;SiO 中Si与O的质
2 2
量比为28∶32=7∶8,C项正确;SiO 和CO 的摩尔质量不同,D项错误。
2 2
4.【答案】C
【解析】1个甲基中含有9个电子,则1 mol甲基(—CH)所含的电子数为9N ,A错误;分子式为C HO的
3 A 2 6
有机物可能是乙醇(CHCHOH),1个乙醇分子中含1个C—O键,也可能是二甲醚(CH—O—CH ),1个二
3 2 3 3甲醚分子中含2个C—O键,故不能确定其中含有的C—O键的数目,B错误;乙烯和环丙烷( )的最简式
都是CH,1个最简式中含有3个原子,14 g由乙烯和环丙烷( )组成的混合气体中含有最简式的物质的量
2
是1 mol,因此含有的原子总数为3N ,C正确;在标准状况下四氯化碳呈液态,不能用气体摩尔体积计算
A
四氯化碳的物质的量,D错误。
5.【答案】C
【解析】A项,没有指明是在标准状况下,错误;B项,该反应为可逆反应,不能进行到底,1 mol CO 和
2
2 mol H 充分反应不能生成0.5 mol CH ,即CH 分子数小于0.5N ,错误;C项,由于1个CH 中含有10
2 4 4 A 4
个电子,则 0.1 mol CH 中含有的电子数为 N ,与条件无关,正确;D 项,分析化学方程式
4 A
知,每生成2 mol 水转移8 mol电子,若生成18 g H O(即1
2
mol)则转移电子数为4N ,错误。
A
1.【答案】D
【详解】
A.D 的相对分子质量是4,其中含有2个中子,2.0 g D 的物质的量是0.5 mol,则其中含有的中子数目为
2 2
N ,A错误;
A
B.4.6 g C HO的物质的量是0.1 mol,由于C HO表示的物质可能是乙醇,也可能是而甲醚,因此不能根
2 6 2 6
据其质量计算其中含有的C-H键的数目,B错误;
C.浓硝酸具有强氧化性,在常温下浓硝酸遇铁、铝会在金属表面氧化产生一薄层致密的氧化物保护膜,
阻止金属的进一步反应,即发生钝化现象,因此不能计算反应过程中转移的电子数目,C错误;
D.标准状况下11.2 L由甲烷和乙烯组成的混合气体的物质的量是0.5 mol,由于CH、C H 分子中都含有
4 2 4
4个H原子,因此0.5 mol混合气体中含有的H原子数目为2N ,D正确;
A
故合理选项是D。
2.【答案】D
【详解】
A. 的结构式为O=C=O,标况下11.2L 中含有共用电子对数目为 ,故A正
确;B.反应②、③需要用酶作2催化剂,反应②、③无法在高温下进行,故B正确;
C.反应②中,3.2g 生成HCHO时转移电子数目为 ,故C正确;
D.DHA含有2个羟基,1mol DHA与乙酸发生取代反应,可消耗2mol乙酸,故D错误;
选D。
3.【答案】D
【详解】
A.HCO -不能完全电离,部分发生水解,因此1L、1 mol·L-1的NaHCO 溶液中含有的离子数小于3N ,
3 3 A
故A错误;
B.未注明气体的状况,无法确定气体的物质的量,故B错误;
C.铝片遇到冷的浓硫酸会钝化,铝失去的电子数小于0.3N ,故C错误;
A
D.氮气和一氧化碳的摩尔质量都是28g/mol,都是双原子分子,14g由N 与CO组成的混合气体的物质的
2
量为: =0.5mol,含有1mol原子,含有的原子数目为N ,故D正确;
A
故答案为D。
4.【答案】A
【解析】
A. 铁离子在溶液中水解导致阳离子个数增多,故溶液中阳离子个数多于0.2N 个,故A错误;
A
B. 0.24g Mg为0.01mol,Mg在O 和CO 的混合气体中完全燃烧生成MgO,失去0.02mol电子,则转移电
2 2
子数为0.02N ,故B正确;
A
C. CO 的摩尔质量为44g/mol,含22个质子;SO 的摩尔质量为64g/mol,含32个质子,即两者均是2g中
2 2
含1mol质子,故3g混合物中含1.5mol质子即1.5N 个质子,故C正确;
A
D.过氧化钠与二氧化硫反应生成硫酸钠,1mol过氧化钠中的−1价的氧原子变为−2价,故1mol过氧化钠转
移2mol电子即2N 个,故D正确;
A
答案选A。
5.【答案】A
【解析】
A.铁发生吸氧腐蚀电极反应式:Fe−2e−=Fe2+,14.0gFe物质的量为 =0.25mol,转移电子数为:0.25mol×2×N =0.5N ,故A正确;
A A
B.硫化氢为弱电解质,水溶液中不能完全电离,依据原子个数守恒可知:标准状况下,11.2LH S物质的
2
量为0.5mol,溶液中含硫粒子的数目等于0.5N ,故B错误;
A
C.pH=14的Ba(OH) 溶液中氢氧根离子浓度为1mol/L,0.5LpH=14的Ba(OH) 溶液含氢氧根离子物质的
2 2
量为0.5mol,所以钡离子物质的量为0.25N ,故C错误;
A
D.100mL0.5mol·L-1Fe(NO ) 溶液中n(Fe3+)=0.05mol,n(NO -)=0.15mol,通入足量SO 气体,Fe3+会被还原
3 3 3 2
为Fe2+,NO -会被还原为NO,转移电子数大于0.05N ,故D错误;
3 A
故答案选A。
1.【答案】C
【解析】A.25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质的量,故A错误;
B.Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小于2.0N ,故B错
3 3 A
误;
C.苯甲酸燃烧的化学方程式为 ,1mol苯甲酸燃烧生成7molCO ,则
2
0.2mol苯甲酸完全燃烧生成1.4molCO,数目为1.4N ,故C正确;
2 A
D.电解熔融CuCl 时,阳极反应为 ,阴极反应为 ,阴极增加的重量为Cu的质
2
量,6.4gCu的物质的量为0.1mol,根据阴极反应可知,外电路中通过电子的物质的量为0.2mol,数目为
0.2N ,故D错误;
A
答案选C。
2.【答案】C
【解析】A. 由钠离子和硫酸氢根离子构成,其中的阳离子只有钠离子, 的物质的量
为0.1mol,因此,其中只含有 个阳离子,A说法不正确;
B.没有指明气体的温度和压强,无法确定 乙烷和丙烯的混合气体的物质的量是多少,因此,无法确
定其中所含碳氢键的数目,B说法不正确;C. 分子中有6个中子, 的物质的量为0.5mol,因此, 含有的中子数为 ,C说法正
确;
D. 和 发生反应生成 ,该反应是可逆反应,反应物不能完全转化为生成物,因此, 和
于密闭容器中充分反应后, 分子总数小于 ,D说法不正确。
综上所述,本题选C。
3.【答案】A
【详解】
A.1LpH为12的Ba(OH) 溶液中含有OH-的浓度为0.01mol/L,物质的量0.01mol/L 1L=0.01mol,OH-的
2
数目为0.01N ,A正确;
A
B.1.8g重水(D O)的物质的量为:0.09mol,所含质子数为0.9N ,B错误;
2 A
C.足量的浓盐酸与8.7gMnO(0.1mol)反应,+4价Mn转化生成Mn2+,转移电子的数目为0.2N ,C错误;
2 A
D.甲醇的结构简式为:CHOH,32g (1mol)的分子中含有C—H键的数目为3N ,D错误;
3 A
答案选A。
4.【答案】A
【详解】
A.1个 分子中含有3个 键,微粒个数与物质的量成正比,故 含有3mol 键,
键的数目为 ,A正确;
B.盐酸为氯化氢的水溶液,氯化氢会全部电离出阴离子Cl-,水会部分电离出阴离子OH-,水的质量及电
离程度未知,故无法计算 的盐酸含有阴离子总数,B错误;
C.未提到具体的温度、压强(如标况下),故无法计算 与 混合后的分子数目,C错误;
D. 为1mol,钠与足量的水反应生成氢气的关系式为: ,故1mol Na应对应生成0.5mol
H, 分子数目应为0.5 ,D错误;
2
故选A。5.【答案】C
【详解】
A. 的质子数为10,18g 的物质的量为 0.9mol, 则 重水( )中所含质子数为 ,
A错误;
B. 与 反应的化学方程式为:3NO +H O=2HNO +NO,该反应消耗3个NO 分子转移的电子数为
2 2 3 2
2个,则有3mol的NO 参与反应时,转移的电子数为 ,B错误;
2
C.一个 ( )分子中含有的 键数为8个,32gS 的物质的量为 mol,则含有的
8
键数为 ,C正确;
D.酸性 溶液中存在: ,含Cr元素微粒有 和 ,则
的 溶液中 离子数应小于 ,D错误;
故选C。