文档内容
考点 14 铁及其化合物
(好题冲关)
【基础过关】
1.(2023·河北省沧州市大数据应用调研联合测试评)磁石有纳气平喘的功能,《本草经集注》中有磁
石炮制用药的记载:能吸针者为上品,称净磁石,采集日久,为呆磁石;取上品武火煅至红透,醋淬,此
法后代一直沿用,下列有关磁石说法正确的是( )
A.上品净磁石为纯净物
B.净磁石采集日久变为呆磁石,是发生了分解反应的缘故
C.磁石的主要成分是Fe O
3 4
D.醋淬磁石涉及氧化还原反应
2.(2023·广东省茂名市高三联考)人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血。市场出售的
某种麦片中含有微量、颗粒细小的铁粉,这些铁粉在人体胃酸(胃酸的主要成分是HCl)作用下转化成亚铁
盐。下列叙述错误的是( )
A.铁粉具有还原性 B.铁是人体必需的微量元素
C.常温下,铁能与水发生置换反应 D.Fe2+用K[Fe(CN) ]溶液检验生成蓝色沉淀
3 6
3.(2023·江苏省徐州市三模)下列有关铁及其化合物的性质与用途具有对应关系的是( )
A.Fe O 能与盐酸反应,可用于制作红色颜料
2 3
B.FeCl 具有氧化性,可用于除去水中悬浮杂质
3
C.铁粉具有还原性,可用于食品袋中的抗氧化剂
D.FeS难溶于水,可用于除去废水中的Cu2+
4.草酸亚铁晶体是生产感光材料的原料[K (FeC O·2H O)= 3.0×10-7],制备流程如下:
sp 2 4 2
(NH )Fe(SO ) FeC O·2H O
4 2 4 2 2 4 2
下列说法错误的是( )
A.可用 溶液检验(NH )Fe(SO ) 是否变质
4 2 4 2
B.步骤①酸化的目的是抑制Fe2+的水解
C.步骤②反应为Fe2++H C O+2H O=FeC O·2H O↓+2H+
2 2 4 2 2 4 2
D.步骤③为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
5.铁元素是重要的金属元素,含有铁元素的物质,在人类的生产生活中有着重要的应用。Fe O(s)+
2 3
3CO(g) 2Fe(s)+3CO(g) ΔH<0是炼铁工业中的主反应。在指定条件下,下列选项所示的物质间转
2
化能实现的是( )
资料收集整理【淘宝店铺:向阳百分百】A. B. (胶体)
C. D.
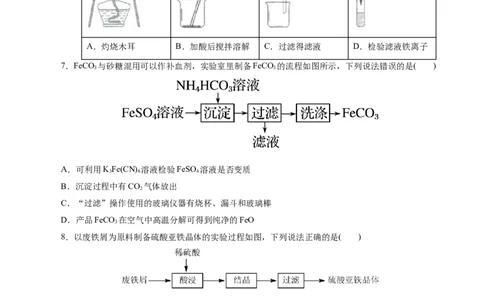
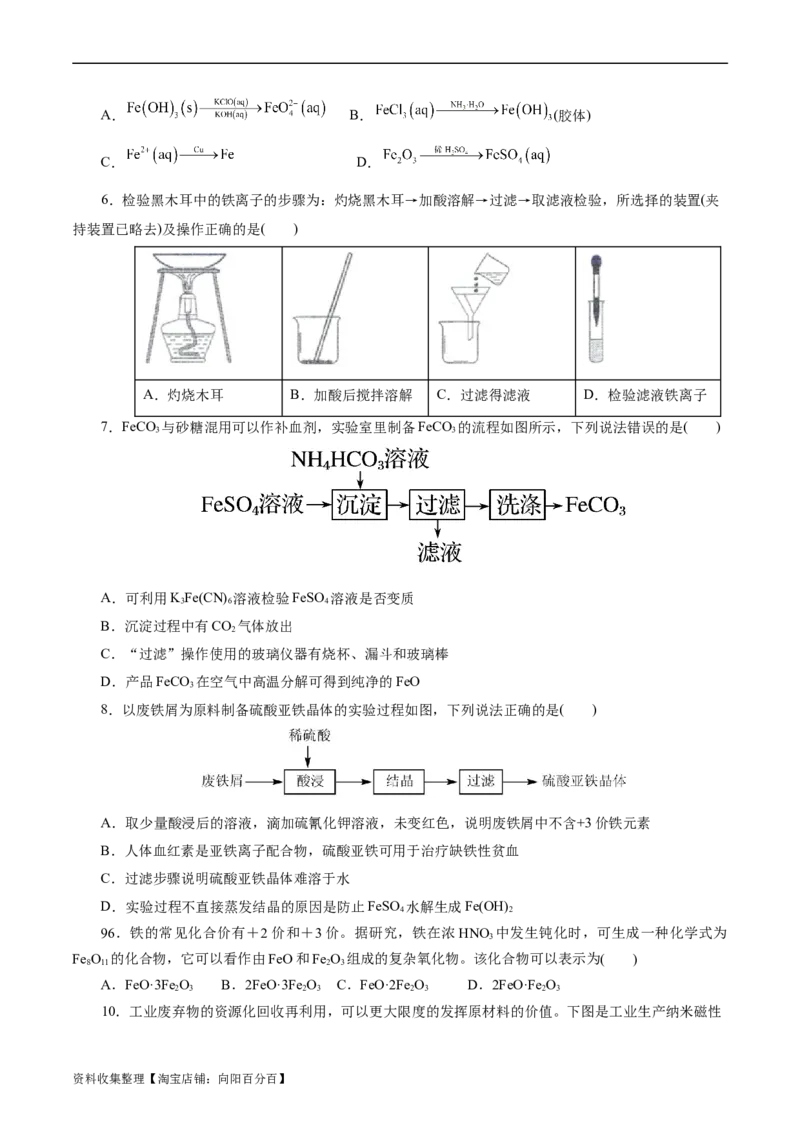
6.检验黑木耳中的铁离子的步骤为:灼烧黑木耳→加酸溶解→过滤→取滤液检验,所选择的装置(夹
持装置已略去)及操作正确的是( )
A.灼烧木耳 B.加酸后搅拌溶解 C.过滤得滤液 D.检验滤液铁离子
7.FeCO 与砂糖混用可以作补血剂,实验室里制备FeCO 的流程如图所示,下列说法错误的是( )
3 3
A.可利用KFe(CN) 溶液检验FeSO 溶液是否变质
3 6 4
B.沉淀过程中有CO 气体放出
2
C.“过滤”操作使用的玻璃仪器有烧杯、漏斗和玻璃棒
D.产品FeCO 在空气中高温分解可得到纯净的FeO
3
8.以废铁屑为原料制备硫酸亚铁晶体的实验过程如图,下列说法正确的是( )
A.取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明废铁屑中不含+3价铁元素
B.人体血红素是亚铁离子配合物,硫酸亚铁可用于治疗缺铁性贫血
C.过滤步骤说明硫酸亚铁晶体难溶于水
D.实验过程不直接蒸发结晶的原因是防止FeSO 水解生成Fe(OH)
4 2
96.铁的常见化合价有+2价和+3价。据研究,铁在浓HNO 中发生钝化时,可生成一种化学式为
3
Fe O 的化合物,它可以看作由FeO和Fe O 组成的复杂氧化物。该化合物可以表示为( )
8 11 2 3
A.FeO·3Fe O B.2FeO·3Fe O C.FeO·2Fe O D.2FeO·Fe O
2 3 2 3 2 3 2 3
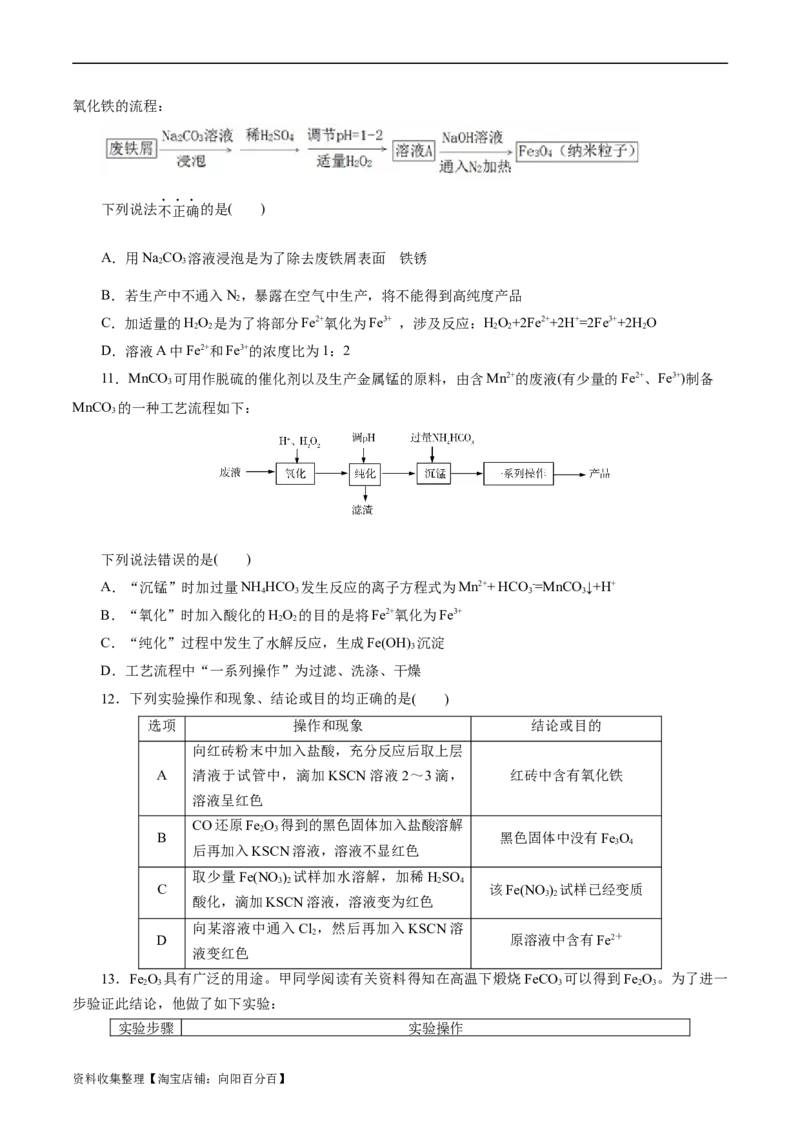
10.工业废弃物的资源化回收再利用,可以更大限度的发挥原材料的价值。下图是工业生产纳米磁性
资料收集整理【淘宝店铺:向阳百分百】氧化铁的流程:
下列说法不正确的是( )
的
A.用NaCO 溶液浸泡是为了除去废铁屑表面 铁锈
2 3
B.若生产中不通入N,暴露在空气中生产,将不能得到高纯度产品
2
C.加适量的HO 是为了将部分Fe2+氧化为Fe3+ ,涉及反应:HO+2Fe2++2H+=2Fe3++2H O
2 2 2 2 2
D.溶液A中Fe2+和Fe3+的浓度比为1:2
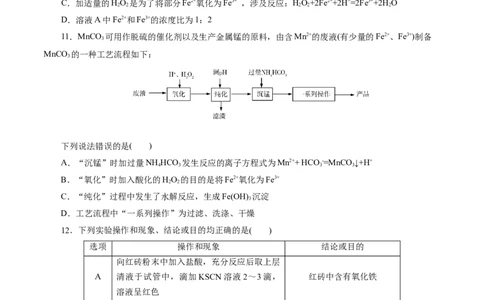
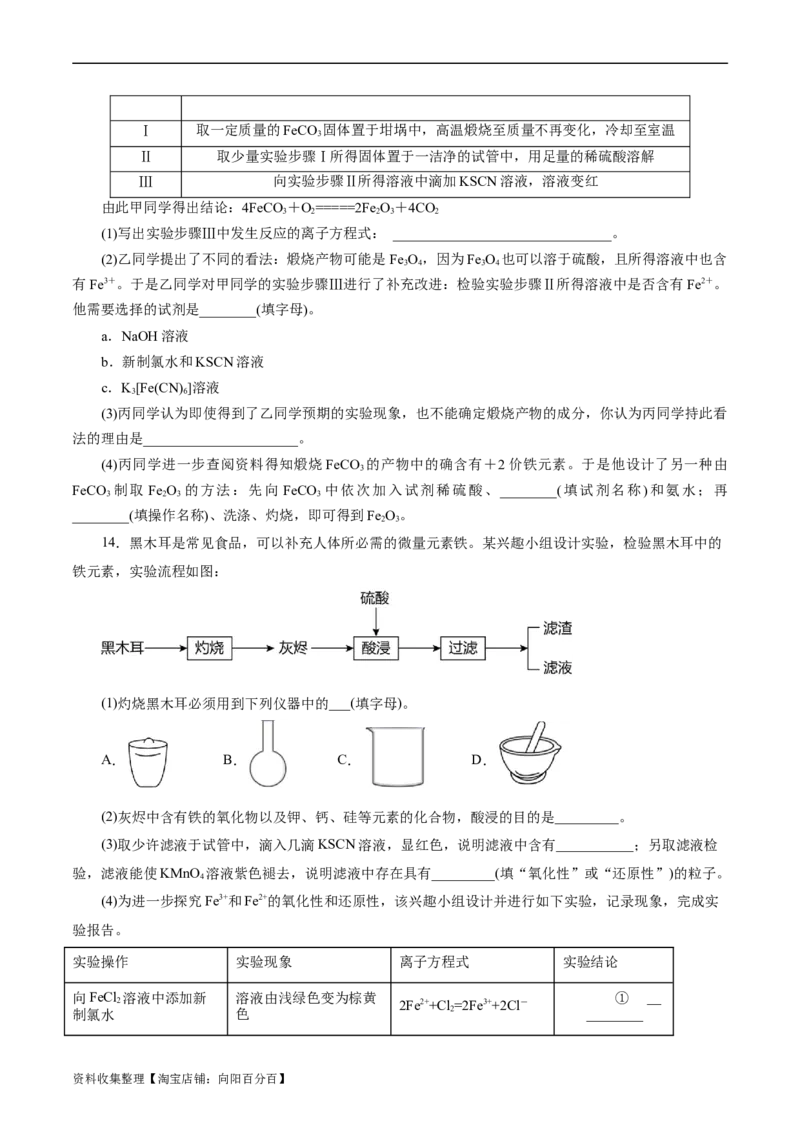
11.MnCO 可用作脱硫的催化剂以及生产金属锰的原料,由含Mn2+的废液(有少量的Fe2+、Fe3+)制备
3
MnCO 的一种工艺流程如下:
3
下列说法错误的是( )
A.“沉锰”时加过量NH HCO 发生反应的离子方程式为Mn2++ HCO -=MnCO↓+H+
4 3 3 3
B.“氧化”时加入酸化的HO 的目的是将Fe2+氧化为Fe3+
2 2
C.“纯化”过程中发生了水解反应,生成Fe(OH) 沉淀
3
D.工艺流程中“一系列操作”为过滤、洗涤、干燥
12.下列实验操作和现象、结论或目的均正确的是( )
选项 操作和现象 结论或目的
向红砖粉末中加入盐酸,充分反应后取上层
A 清液于试管中,滴加KSCN溶液2~3滴, 红砖中含有氧化铁
溶液呈红色
CO还原Fe O 得到的黑色固体加入盐酸溶解
2 3
B 黑色固体中没有Fe O
3 4
后再加入KSCN溶液,溶液不显红色
取少量Fe(NO ) 试样加水溶解,加稀HSO
3 2 2 4
C 该Fe(NO ) 试样已经变质
3 2
酸化,滴加KSCN溶液,溶液变为红色
向某溶液中通入Cl ,然后再加入KSCN溶
2
D 原溶液中含有Fe2+
液变红色
13.Fe O 具有广泛的用途。甲同学阅读有关资料得知在高温下煅烧FeCO 可以得到Fe O 。为了进一
2 3 3 2 3
步验证此结论,他做了如下实验:
实验步骤 实验操作
资料收集整理【淘宝店铺:向阳百分百】Ⅰ 取一定质量的FeCO 固体置于坩埚中,高温煅烧至质量不再变化,冷却至室温
3
Ⅱ 取少量实验步骤Ⅰ所得固体置于一洁净的试管中,用足量的稀硫酸溶解
Ⅲ 向实验步骤Ⅱ所得溶液中滴加KSCN溶液,溶液变红
由此甲同学得出结论:4FeCO+O=====2Fe O+4CO
3 2 2 3 2
(1)写出实验步骤Ⅲ中发生反应的离子方程式: _______________________________。
(2)乙同学提出了不同的看法:煅烧产物可能是Fe O,因为Fe O 也可以溶于硫酸,且所得溶液中也含
3 4 3 4
有Fe3+。于是乙同学对甲同学的实验步骤Ⅲ进行了补充改进:检验实验步骤Ⅱ所得溶液中是否含有Fe2+。
他需要选择的试剂是________(填字母)。
a.NaOH溶液
b.新制氯水和KSCN溶液
c.K[Fe(CN) ]溶液
3 6
(3)丙同学认为即使得到了乙同学预期的实验现象,也不能确定煅烧产物的成分,你认为丙同学持此看
法的理由是______________________。
(4)丙同学进一步查阅资料得知煅烧FeCO 的产物中的确含有+2价铁元素。于是他设计了另一种由
3
FeCO 制取 Fe O 的方法:先向 FeCO 中依次加入试剂稀硫酸、________(填试剂名称)和氨水;再
3 2 3 3
________(填操作名称)、洗涤、灼烧,即可得到Fe O。
2 3
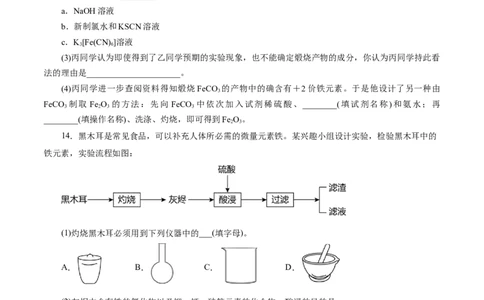
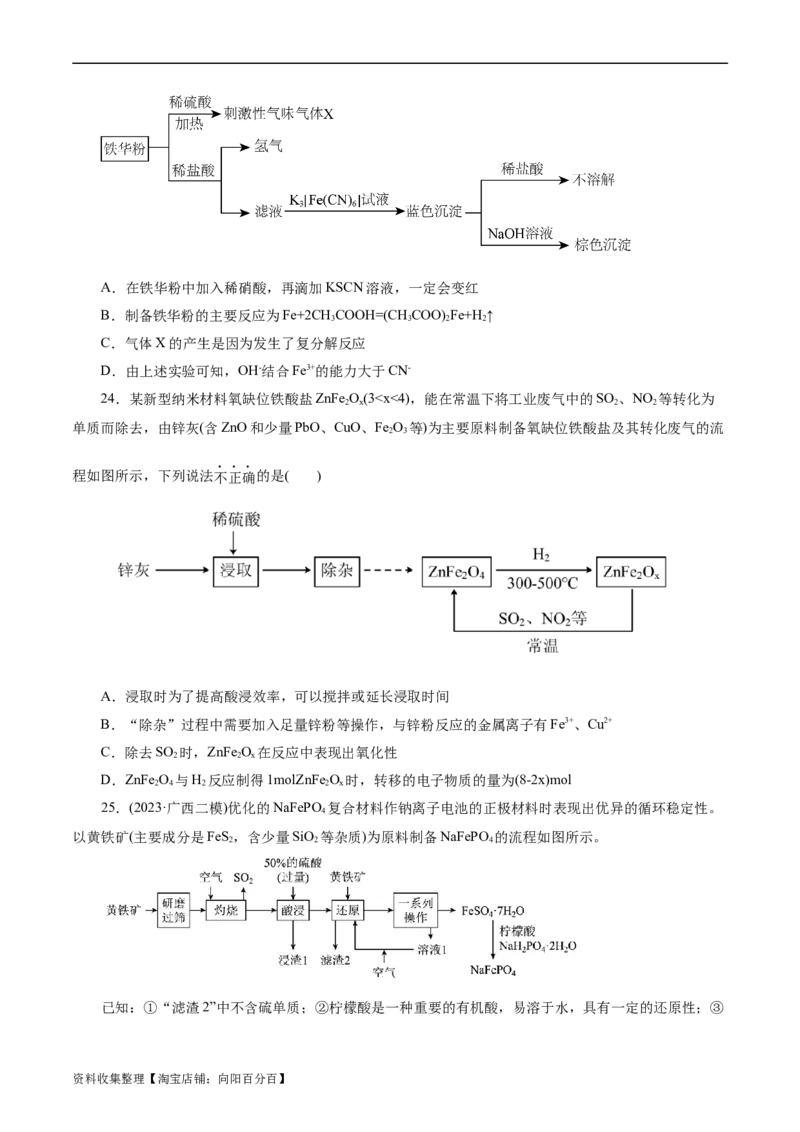
14.黑木耳是常见食品,可以补充人体所必需的微量元素铁。某兴趣小组设计实验,检验黑木耳中的
铁元素,实验流程如图:
(1)灼烧黑木耳必须用到下列仪器中的___(填字母)。
A. B. C. D.
(2)灰烬中含有铁的氧化物以及钾、钙、硅等元素的化合物,酸浸的目的是_________。
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有___________;另取滤液检
验,滤液能使KMnO 溶液紫色褪去,说明滤液中存在具有_________(填“氧化性”或“还原性”)的粒子。
4
(4)为进一步探究Fe3+和Fe2+的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实
验报告。
实验操作 实验现象 离子方程式 实验结论
向FeCl 溶液中添加新 溶液由浅绿色变为棕黄 ① __
2 2Fe2++Cl=2Fe3++2Cl-
制氯水 色 2 ________
资料收集整理【淘宝店铺:向阳百分百】向FeCl 溶液加入足量 铁粉逐渐溶解,溶液由
3 ②____________ Fe3+具有氧化性
的铁粉 棕黄色变为浅绿色
(5)实验结束,离开实验室之前,下列做法正确的是_________(填字母)。
A.废弃药品直接倒入水池冲走 B.药品仪器归放
C.清洁实验仪器,打扫实验室卫生 D.关闭水电、门窗
15.(2023·山东省高三联考)工业上利用硫铁矿烧渣(主要成分为Fe O、Fe O、FeO、SiO)为原料制备
3 4 2 3 2
高档颜料——铁红(Fe O),具体生产流程如下:
2 3
回答下列问题:
(1)为提高酸浸的效率,可采取的措施有___________(任写一种)。
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有___________、玻璃棒和烧杯等,该步骤是为
了除去___________(填相关物质的化学式)。
(3)检验步骤Ⅲ已经进行完全,可用的试剂是___________。
(4)步骤V的反应温度一般需控制在 以下,其目的是___________;该步骤中反应生成FeCO 的同
3
时有气泡产生,该反应的离子方程式为___________。
【能力提升】
16.(2023·河南省安阳市三模)某化学实验小组设计如下实验探究Zn与溶液中Fe3+发生反应的原理。
实验 试剂 现象
2 mL0.1 mol· L-1FeCl 溶 黄色溶液很快变浅,接着有无色气泡产生,固体中
I 3
液、过量锌粉 未检出铁单质
很快有大量气体产生,出现红褐色浑浊,30 min左
2 mL1 mol· L-1FeCl 溶
Ⅱ 3 右产生红褐色沉淀,溶液颜色变浅,产生少量铁单
液(pH≈0.70)、过量锌粉
质
下列说法错误的是( )
A.实验I说明Fe3+被还原为Fe2+
B.可用酸性高锰酸钾溶液检验实验I得到的溶液中含有Fe2+
C.实验Ⅱ发生了置换反应和复分解反应
D.实验说明Fe3+、H+与Zn的反应与离子浓度有关
17.NaFeO 是一种高效的水处理剂,下列用于解释事实的离子方程式中不正确的是( )
2 4
资料收集整理【淘宝店铺:向阳百分百】A.NaFeO 在酸性溶液中不稳定,与水反应生成Fe3+和O ,离子方程式为:4FeO2-+10HO+4Fe3+
2 4 2 4 2
===20OH-+3O↑
2
B.工业上可用FeCl 、NaOH、NaClO三种物质反应制得NaFeO 离子方程式为:2Fe3++10OH-+
3 2 4
3ClO-===2FeO2-+3Cl-+5HO
4 2
C.NaFeO 消毒杀菌时得到的 Fe3+可以净水,Fe3+能产生净水物质的原因是:Fe3++
2 4
3HO===Fe(OH) (胶体)+3H+
2 3
D.工业上可用铁做阳极,电解浓NaOH溶液的方法制NaFeO,阳极的电极反应为:Fe-6e-+8OH-
2 4
===FeO2-+4HO
4 2
18.硫酸亚铁晶体(FeSO •7H O)俗称绿矾,加热至高温会分解产生水、金属氧化物和非金属氧化 物,
4 2
某化学兴趣小组的同学对绿矾分解产物进行了探究,下列说法不正确的是( )
A.硫酸亚铁晶体高温分解产生的气体,用足量的BaCl 溶溶液吸收后有白色沉淀产生,说明非金属氧
2
化物中含有SO
3
B.硫酸亚铁晶体高温分解产生的气体,通入到紫色石蕊溶液中,若溶液变红,说明非金属氧化物中
含有SO
3
C.硫酸亚铁晶体分解产生的固体溶于稀硫酸后,向溶液中滴加 KSCN溶液,若变红说明固体中含有
三价铁
D.硫酸亚铁晶体分解产生的固体溶于稀硫酸后,向溶液中滴加酸性高锰酸钾,若紫色褪去,则发生
反应的离子方程式为:5Fe2++MnO-+8H+=Mn2++5Fe3++4H O
4 2
19.高铁酸钾(K FeO)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,微溶于浓
2 4
KOH溶液,且能与水反应放出氧气,并生成Fe(OH) 胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性
3
条件下,其氧化性强于Cl、KMnO 等。工业上湿法制备KFeO 的流程如下:
2 4 2 4
下列关于KFeO 的工业湿法制备工艺,说法正确的是( )
2 4
A.“反应”时,氧化剂和还原剂的物质的量之比为2:3
B.“过滤I”所得滤液中大量存在的离子有:Na+、Fe3+、Cl-、NO -、FeO2-
3 4
C.“转化”时,反应能进行的原因是该条件下KFeO 的溶解度比NaFeO 小
2 4 2 4
D.“过滤II”所得滤液在酒精灯外焰上灼烧,观察到火焰呈黄色,说明滤液为NaOH溶液
20.KFeO 是一种高效多功能的饮用水处理剂。已知:①一种干法制备KFeO 的反应为
2 4 2 4
2FeSO +6K O=2 K FeO+K O+2KSO +O ↑,②KFeO 处理水时发生反应FeO+10H O
4 2 2 2 4 2 2 4 2 2 4 4 2
4Fe(OH) +8OH-+3O 。下列说法错误的是( )
3 2
资料收集整理【淘宝店铺:向阳百分百】A.干法制备KFeO 的反应中,还原剂与氧化剂的物质的量之比为
2 4
B.干法制备KFeO 的反应中,每生成1mol KFeO,有5mol e-转移
2 4 2 4
C.KFeO 在强碱性溶液中能稳定存在
2 4
D.KFeO 处理水时,既能杀菌消毒,又能起絮凝作用除去水中悬浮杂质
2 4
21.将铁、氧化铁、氧化铜组成的混合物粉末mg放入盛 盐酸的烧杯中,充分反应后
产生2.24L H (标准状况),残留固体2.56g。过滤,滤液中无Cu2+。将滤液加水稀释到500mL,测得其中
2
c(H+)为 。下列说法正确的是( )
A.m=15.36
B.烧杯中转移电子的物质的量共为0.28mol
C.若将反应后的溶液倒入蒸发皿中直接蒸干可得到0.2mol FeCl
2
D.过滤时需要用到的玻璃仪器有烧杯、玻璃棒、漏斗、锥形瓶
22.由绿矾(FeSO ·7H O)制备三草酸合铁酸钾晶体{ K[Fe(C O) ]·3H O}的流程如图
4 2 3 2 4 3 2
下列说法正确的是( )
A.“溶解”时加硫酸的目的是抑制 水解
B.将“沉淀”所得的FeC O 加入酸性高锰酸钾溶液,观察到溶液褪色,说明产物中含C O2-
2 4 2 4
C.“氧化”过程中HO 被还原为O
2 2 2
D.隔绝空气加热K[Fe(C O) ]·3H O,分解产物为KCO、Fe O、CO、HO
3 2 4 3 2 2 3 2 3 2 2
23.《开宝本草》记载“取钢煅作叶如笏或团,平面磨错令光净,以盐水洒之,于醋瓮中阴处埋之一
百日,铁上衣生,铁华成矣”。铁华粉[主要成分为(CHCOO) Fe ·H O ]可用如下方法检测。下列相关说法
3 2 2
不正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A.在铁华粉中加入稀硝酸,再滴加KSCN溶液,一定会变红
B.制备铁华粉的主要反应为Fe+2CH COOH=(CH COO) Fe+H ↑
3 3 2 2
C.气体X的产生是因为发生了复分解反应
D.由上述实验可知,OH-结合Fe3+的能力大于CN-
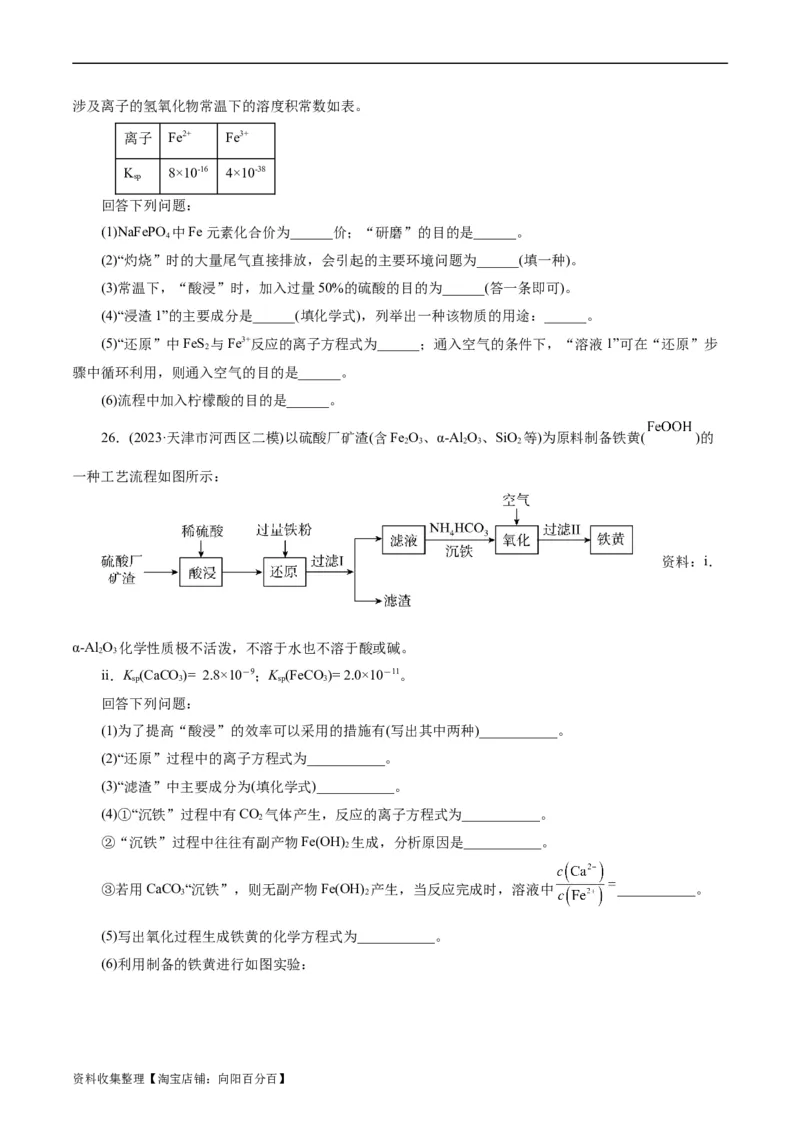
24.某新型纳米材料氧缺位铁酸盐ZnFe O(3